Voltar a: Física e Química
- Aula nº1
⇒ Teoria cinético-corpuscular ;
De que é feita a matéria
Demócrito (c.460-370a.C.) foi um filósofo que acreditava que a partícula mais pequena que podia existir era o átomo (que significa «indivisível»).
Demócrito afirmava que a divisão de uma maçã apenas é possível porque esta é constituída por átomos, pelo que não seria possível dividi-la indefinidamente.
As unidades estruturais da matéria
Se a matéria é constituída por corpúsculos, entre eles terão de existir espaços vazios.
Macroscopicamente vemos a matéria como um todo contínuo mas, na verdade, existem espaços vazios entre os corpúsculos.
Quando se comprime o ar de uma seringa, este passa a ocupar um volume menor,o que só se explica se existirem espaços vazios.
Todos os materiais são constituídos por corpúsculos, em constante movimento e separados uns dos outros por espaço vazio.
⇒ Toda a matéria é constituída por corpúsculos de dimensões muito reduzidas e em constante movimento, existindo entre eles espaço vazio.
⇒ Quanto maior a temperatura de um corpo, mais rapidamente se movem os corpúsculos que o constituem.
Evidências experimentais da existência de corpúsculos
-
Observação
Explicação
O cheiro a perfume é comunicado a todo o compartimento porque os corpúsculos, que estão em constante movimento, espalham-se por todo o espaço.
-
Observação
Explicação
A mesma porção de ar passa a ocupar um espaço menor porque os corpúsculos, que não se alteram, passam a ficar mais próximos uns dos outros.
-
Observação
Explicação
O sabor doce é comunicado a todo o chá porque os corpúsculos da substância doce – açúcar – espalharam-se entre os do líquido.
Teoria cinético-corpuscular:
⇒ a matéria é constituída por pequenos corpúsculos;
⇒ os corpúsculos estão em constante movimento;
⇒ entre os corpúsculos existem espaços vazios.
A temperatura e a agitação dos corpúsculos
⇒ Adição de igual porção de soluto na água quente e na água fria no mesmo instante.
Quanto maior é a temperatura de uma substância, maior é a agitação dos seus corpúsculos e por isso o soluto espalha-se mais facilmente na água quente.
Os corpúsculos e os estados físicos da matéria
Microscopicamente, os estados físicos da matéria, explicam-se em termos de agregação corpuscular.
As forças de ligação que se estabelecem condicionam a liberdade de movimento e organização dos corpúsculos.
Quanto maiores são as forças de ligação entre os corpúsculos, menor é a sua liberdade de movimento e maior é a sua organização.
Estado sólido – Num sólido as forças de interação entre as partículas são mais intensas do que no estado líquido, conferindo‑lhes uma certa «arrumação» e restringindo os movimentos a pequenas vibrações.
As partículas encontram‑se muito próximas e, por isso, os sólidos são praticamente incompressíveis e apresentam uma forma definida.
⇒ Forma e volume constantes
⇒ Liberdade de movimentos dos corpúsculos reduzida
⇒ Forças de interação são fortes
Estado líquido – Num líquido a agitação das partículas é menor que no estado gasoso, mas estas ainda possuem uma certa liberdade de movimentos.
As forças de interação existentes entre as partículas permitem que os líquidos se adaptem ao formato dos recipientes que os contêm, mas ocupando um volume praticamente constante.
⇒ Forma variável, volume constante
⇒ Liberdade de movimentos dos corpúsculos superior à dos sólidos
⇒ Forças de interação menos fortes que nos sólidos
Estado gasoso – Um gás ocupa sempre todo o espaço disponível, devido à grande agitação das partículas que o constituem.
As partículas de um gás encontram‑se muito afastadas umas das outras, podendo espalhar‑se livremente. Uma certa quantidade de gás não possui forma definida e o seu volume é variável, consoante o recipiente que o contém.
⇒ Forma e volume variáveis
⇒ Grande liberdade de movimentos dos corpúsculos
⇒ Forças de interação muito fracas
Conclusão: a agitação das partículas constituintes da matéria é maior quando a matéria se encontra no estado gasoso, sendo menor nos líquidos e menor ainda nos sólidos.
As forças de ligação entre as partículas são mais intensas nos sólidos, menos intensas nos líquidos e ainda menos intensas nos gases.
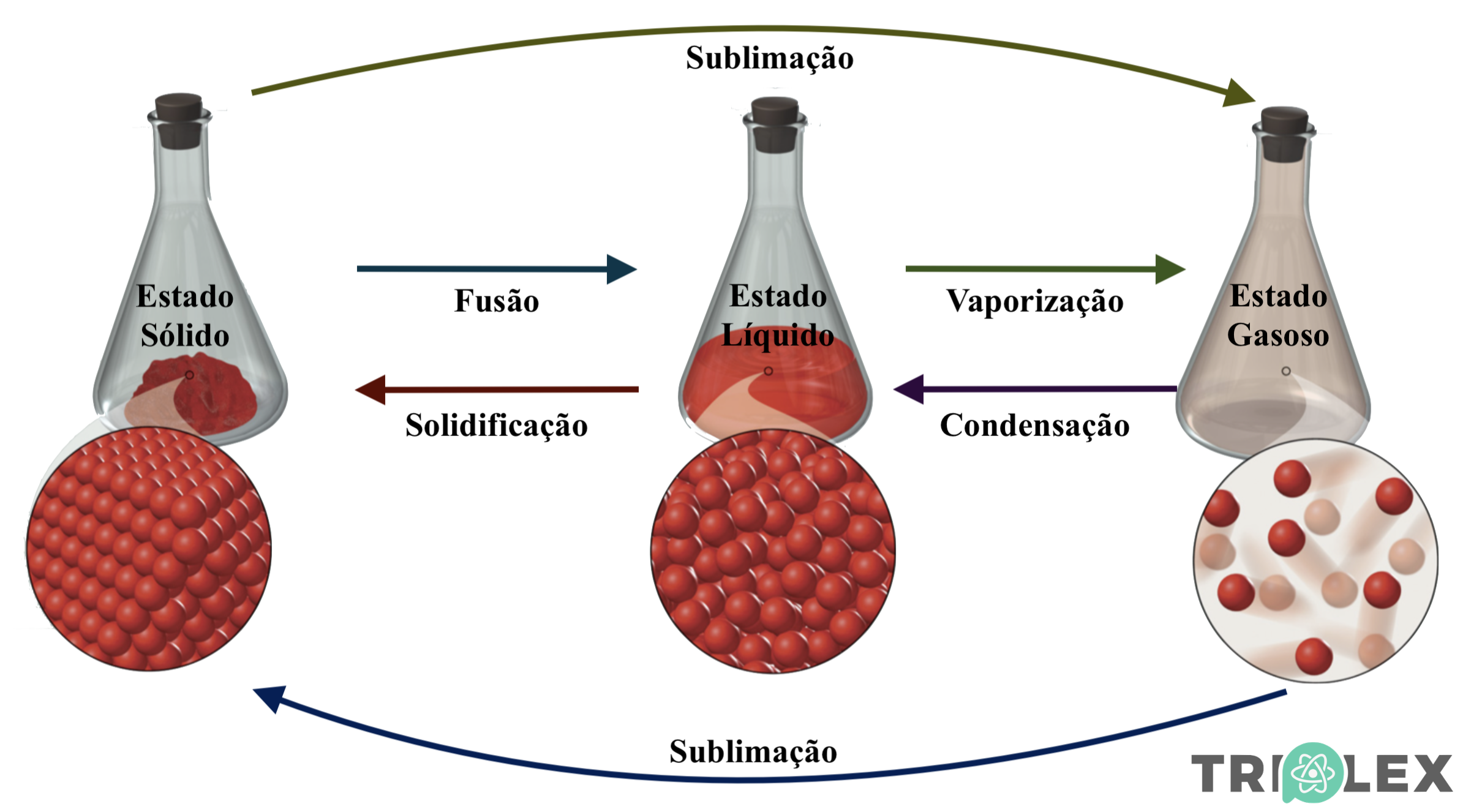
Mudanças de estado físico
Como vimos, a variação da temperatura interfere na agitação das partículas que constituem a matéria. Interpretemos agora as mudanças de estado físico que podem ser provocadas, por exemplo, por aquecimento ou arrefecimento da matéria.
Quando ocorrem mudanças de estado físico de um material, os seus corpúsculos não sofrem qualquer alteração.
Altera-se apenas a liberdade de movimentos dos corpúsculos e a proximidade entre eles.