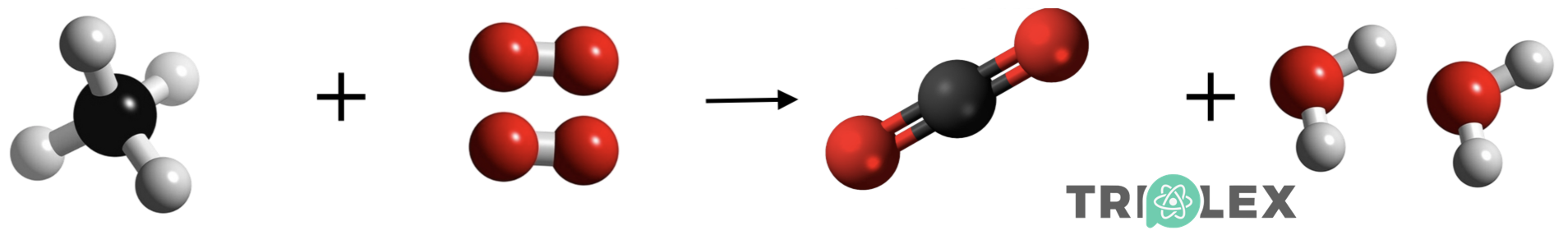Voltar a: Física e Química
- Aula nº6
⇒ Interpretação de reações químicas ;
Reações químicas e equações químicas
Reações químicas são transformações em que há formação de novas substâncias.
Quando ocorre uma reação química:
⇒ Há um rearranjo dos átomos;
⇒ Os átomos passam a ligar-se de forma diferente, formando-se novas substâncias;
⇒ Não há destruição de átomos nem formação de átomos novos.
As transformações químicas são vulgarmente designadas por reações químicas.
Uma reação química pode ser detetada através de manifestações muito diferentes, tais como:
⇒ mudança de cor
⇒ cheiro característico
⇒ variação de temperatura (aquecimento ou arrefecimento)
⇒ libertação de um gás a partir de reagentes sólidos ou líquidos
⇒ formação de um sólido a partir de reagentes líquidos
⇒ formação de chama
Numa reação química:
⇒ Substâncias iniciais – reagentes
⇒ Substâncias finais – produtos de reação
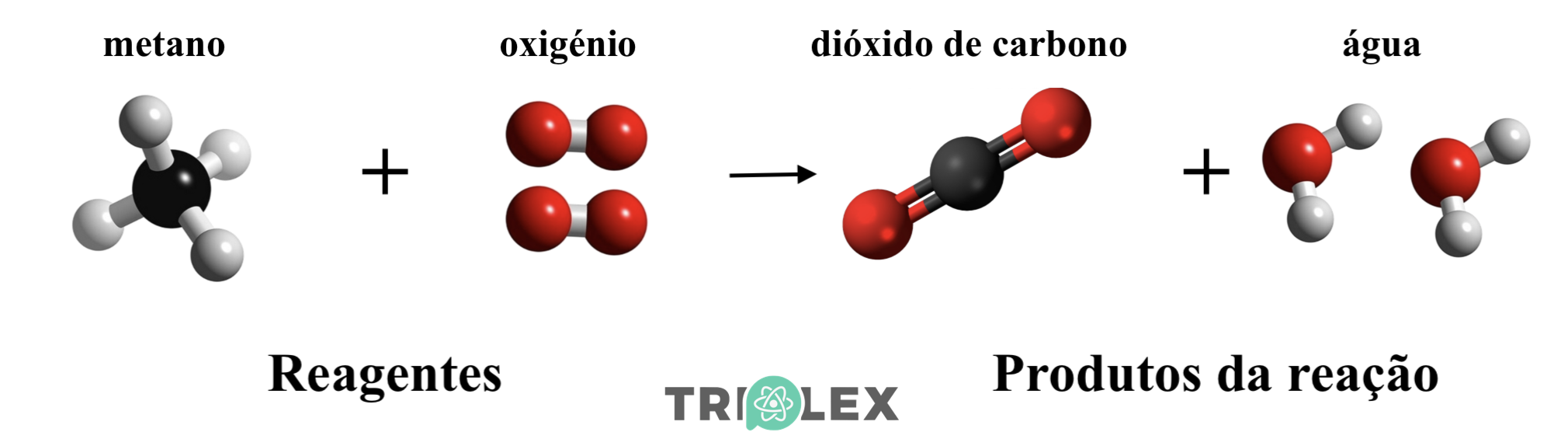
Reação de combustão do metano:
⇒ Nome dos reagentes separados por sinais: +
⇒ Uma seta, →, da esquerda para a direita que separa os reagentes dos produtos da reação.
⇒ Nome dos produtos separados por sinais: +
As reações químicas como rearranjos de átomos:
Ocorrem rearranjos dos átomos dos reagentes que conduzem à formação de novas substâncias, os produtos.
Indicam‑se também os estados físicos das diferentes substâncias usando abreviaturas:
⇒ (s) – sólido
⇒ (l) –líquido
⇒ (g) –gasoso
⇒ (aq) – solução aquosa (quando as substâncias estão dissolvidas em água)
As reações químicas podem ser representadas por esquemas de palavras, onde se indicam os nomes dos reagentes e dos produtos da reação.
Equação de palavras:
Metano (g) + Dioxigénio (g) → Dióxido de carbono (g) + Água (l)
- O número total de átomos de cada elemento conserva-se.
Durante a reação química os átomos não se destroem apenas se reorganizam
⇒ Como o nome de uma substância é diferente de língua para língua, os químicos utilizam equações químicas para representar as reações químicas, onde os reagentes e os produtos da reação são representados pelas respetivas fórmulas químicas.
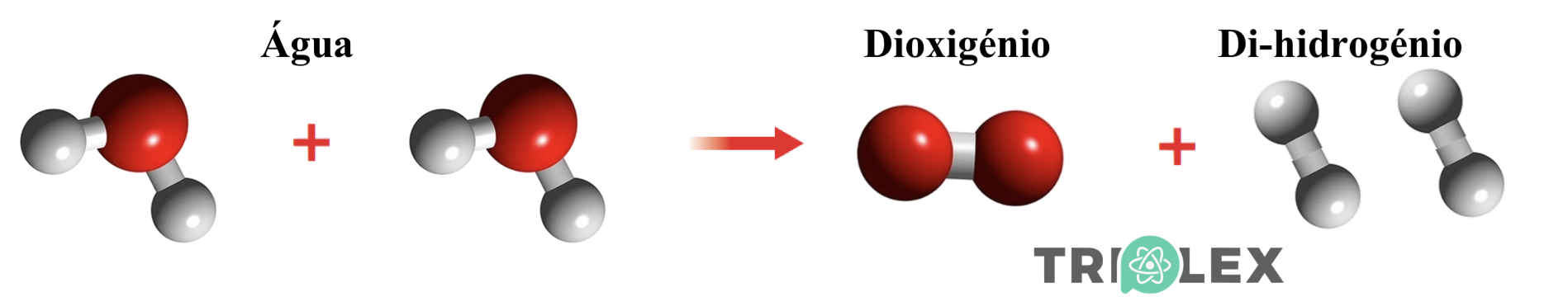
Na eletrólise da água
- Por ação da passagem de corrente elétrica …
⇒ duas moléculas de água chocam eficazmente e todos os átomos se separam.
⇒ dois átomos de oxigénio ligam-se e formam uma molécula de dioxigénio.
⇒ quatro átomos de hidrogénio ligam-se dois a dois, formando duas moléculas de di-hidrogénio.
Lavoisier e as reações químicas:
Antoine Laurent Lavoisier (1743-1794)
⇒ Durante as reações químicas, a matéria não se cria nem se destrói, mas antes se transforma
Se as substâncias que se misturam reagirem entre si, a massa das substâncias que tomam parte na reação variará?
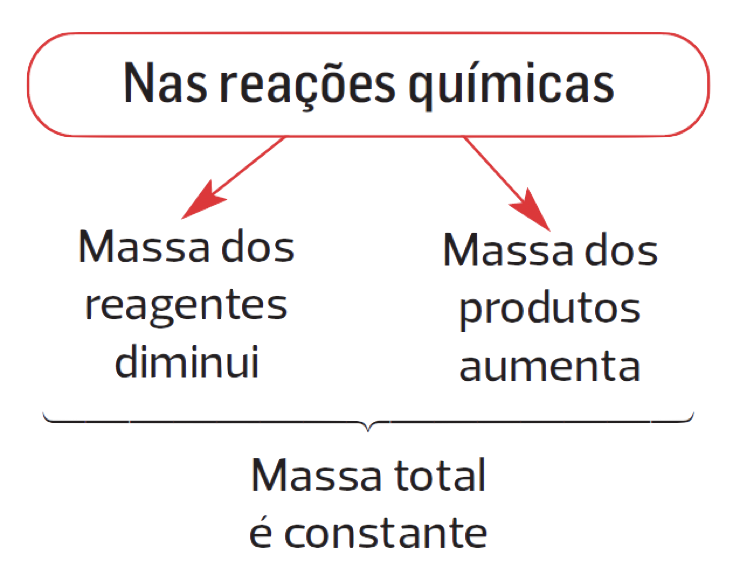
Durante uma reação química, é de esperar que:
⇒ A massa dos reagentes diminua;
⇒ A massa dos produtos da reação aumente.
No decurso da reação, verifica-se, experimentalmente, que:
⇒ A massa dos reagentes diminui à medida que são consumidos;
⇒ A massa dos produtos da reação aumenta à medida que se formam, permanecendo constante a massa total das substâncias envolvidas na reação;
Princípio da conservação da massa
⇒ Reação do bicarbonato de sódio com o vinagre
Numa reação química, a diminuição da massa total dos reagentes corresponde a um igual aumento da massa total dos produtos da reação, conservando-se a massa total das substâncias intervenientes na reação.
A conservação da massa nas reações químicas foi estabelecida por Lavoisier, com base em verificações experimentais.
⇒ Surgiu, assim, a Lei da Conservação da Massa, também designada por Lei de Lavoisier.
Lei de Lavoisier – Durante as reações químicas, a massa total da substâncias envolvidas permanece constante.
Representação das reações químicas – equações químicas
As reações químicas são representadas por equações químicas onde os átomos são representados por símbolos químicos e as moléculas por fórmulas químicas
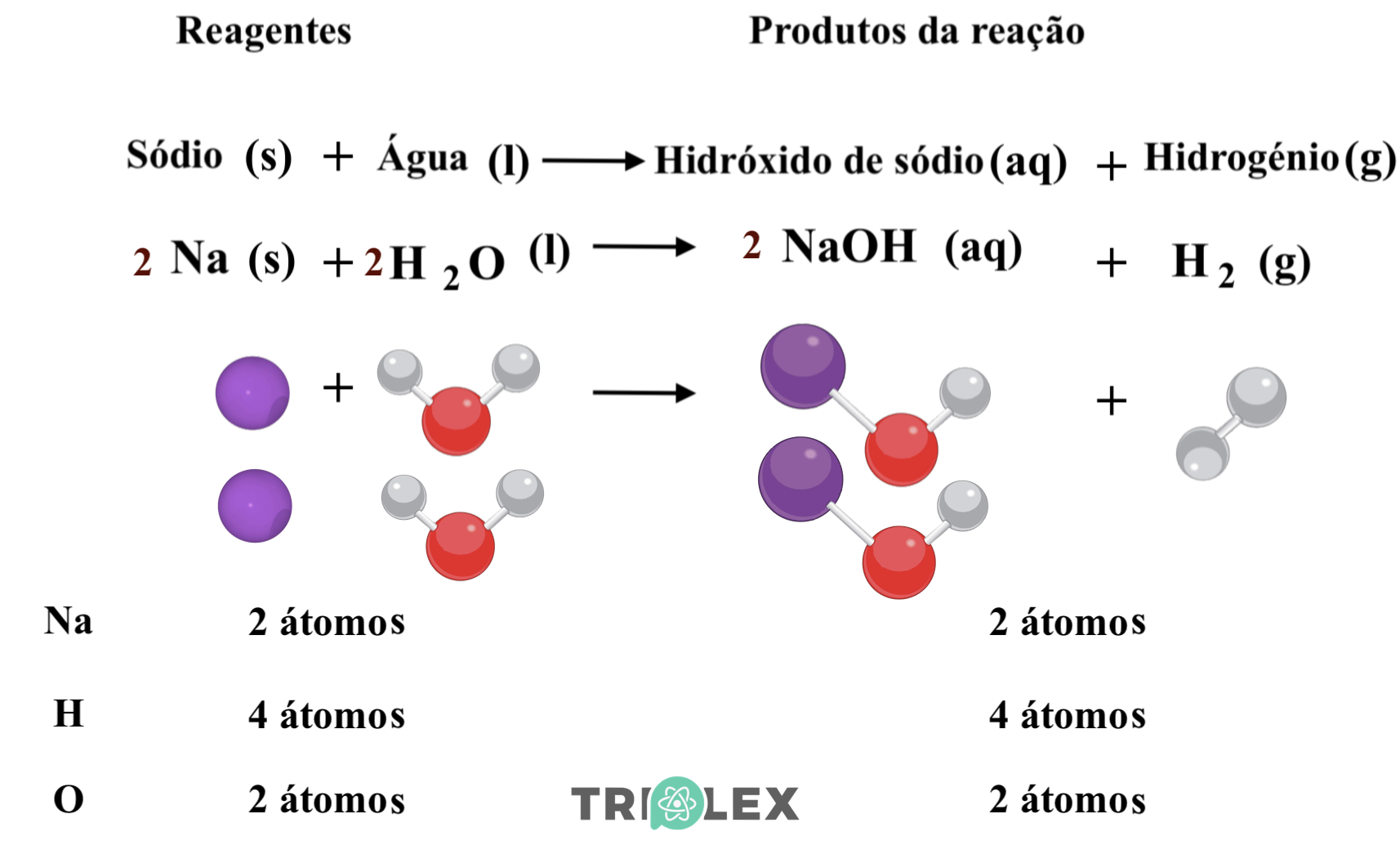
⇒ Reação do sódio com a água
- há conservação do número de átomos de cada elemento.
Leitura da reação química:
⇒ Dois átomos de sódio sólido reage com duas moléculas de água liquida originando duas moléculas de hidróxido de sódio aquoso e uma molécula de hidrogénio gasoso.
⇒ Na eletrólise da água:
H2O (ℓ) → O2 (g) + H2 (g)
Nas equações químicas, para além das fórmulas químicas dos reagentes e dos produtos da reação, surgem, muitas vezes, números antes das fórmulas químicas, para que o número de átomos de cada elemento nos reagentes e nos produtos da reação seja igual.
⇒ Para acertares uma equação química nunca deves alterar as fórmulas químicas.
Os coeficientes numéricos introduzidos para o acerto escrevem-se ao mesmo nível e antes das letras
2 H2O (ℓ) → O2 (g) + 2 H2 (g)
Leitura da reação química:
⇒ Duas moléculas de água líquida originam duas moléculas de hidrogénio gasoso e uma molécula de oxigénio gasoso.
Para escrever uma equação química é necessário:
⇒ Indicar as fórmulas químicas do(s) reagente(s) e do(s) produtos(s) da reação;
⇒ Separar o(s) reagente(s) do(s) produto(s) da reação por meio de uma seta que indica o sentido em que a reação se dá;
⇒ Separar as fórmulas químicas dos reagentes e dos produtos da reação por sinais +;
⇒ Indicar, dentro de parêntesis e à frente das respetivas fórmulas químicas, os estados físicos das substâncias ou se as mesmas se encontram dissolvidas em água;
⇒ Acertar o número de átomos dos elementos, nos reagentes e produtos da reação, colocando coeficientes numéricos antes das fórmulas químicas.