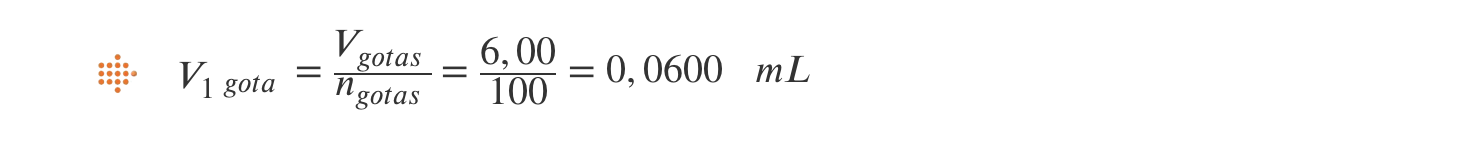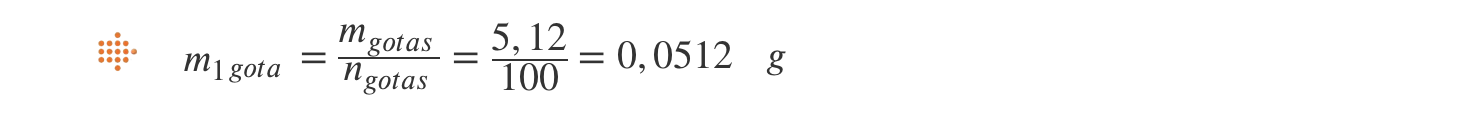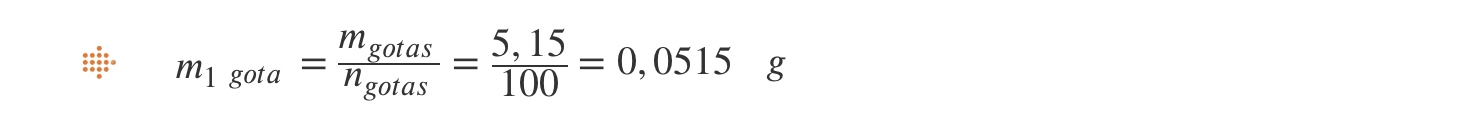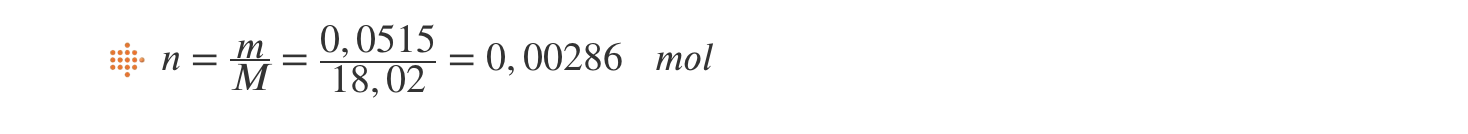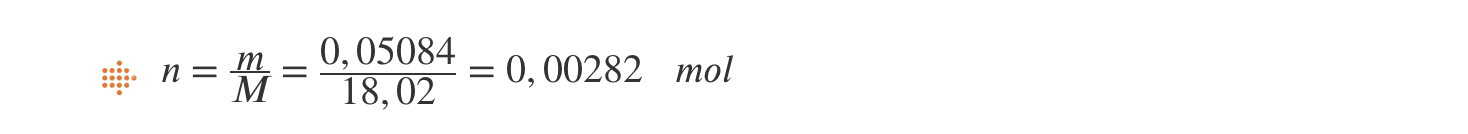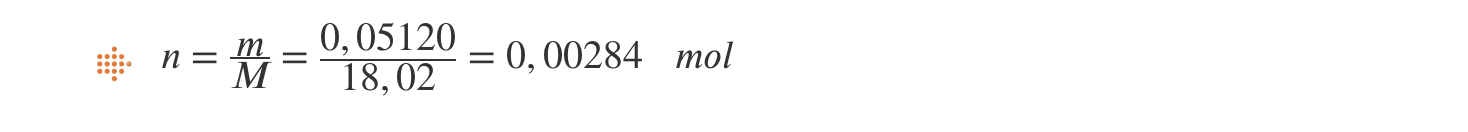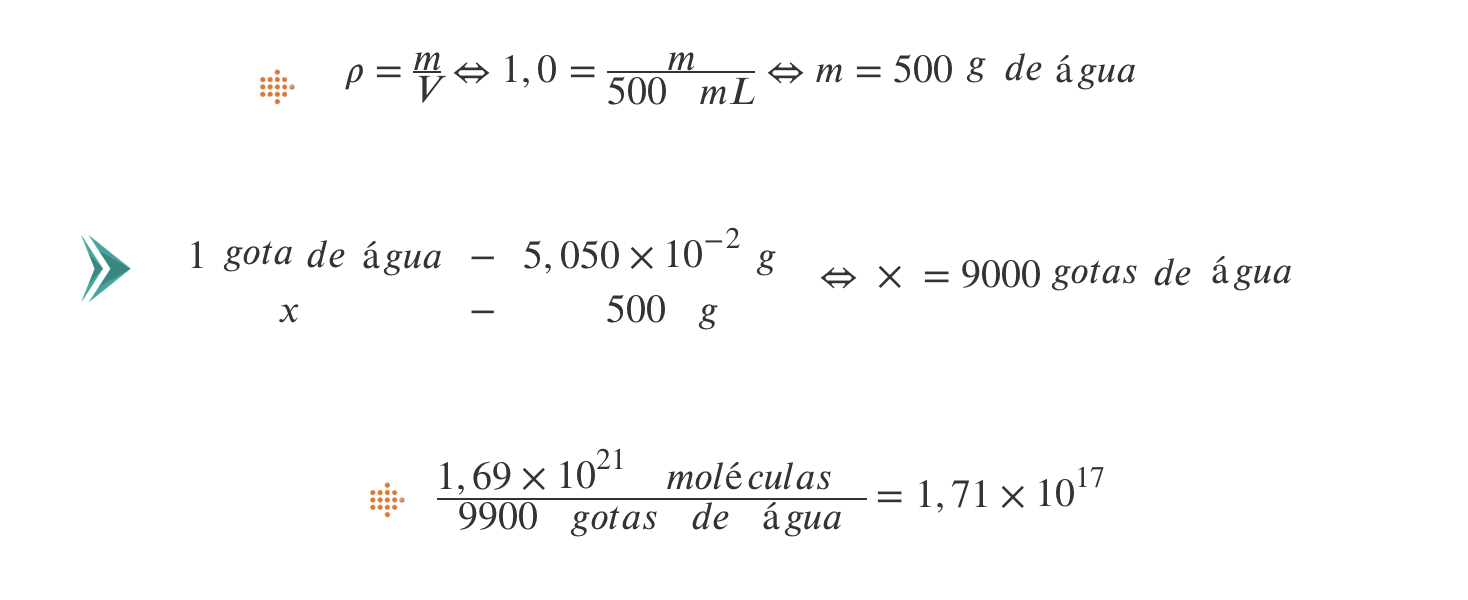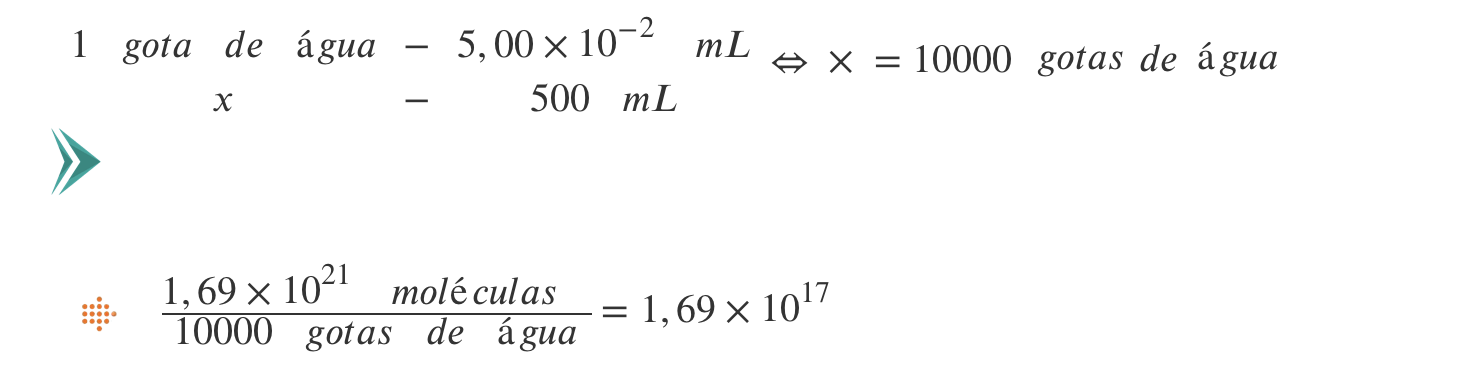Voltar a: Atividades Laboratoriais – 10ºAno
Questões práticas
- Al 1.1 – Volume e número de moléculas de uma gota de água
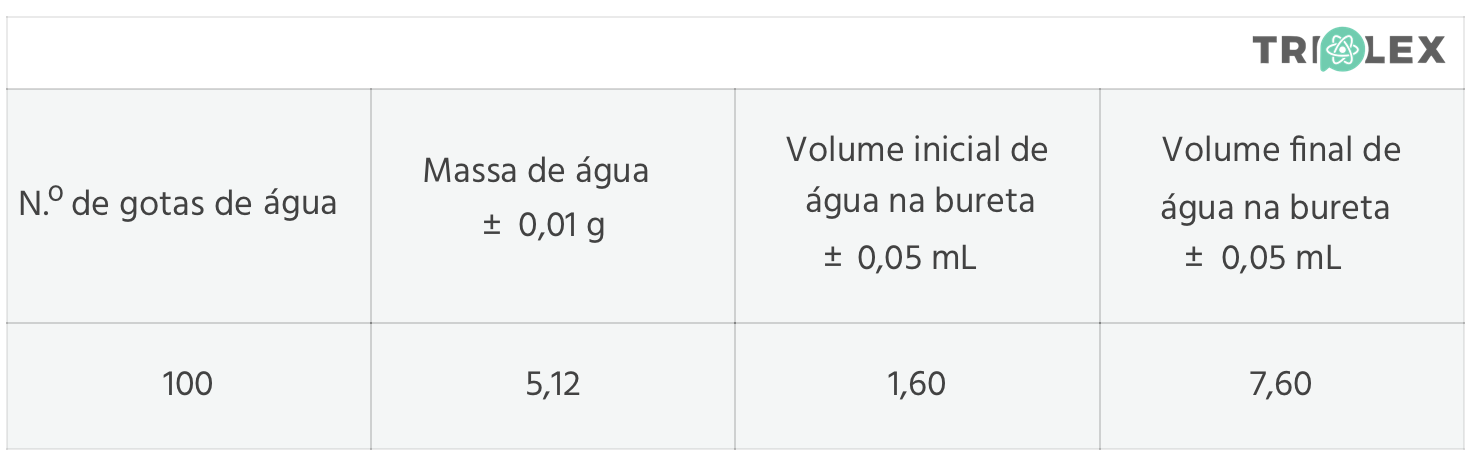
1. Com o objetivo de determinar experimentalmente o número de moléculas de uma gota de água, um grupo de alunos, obteve os seguintes resultados.
A massa das gotas de água foi medida com uma balança digital (a medida é indicada por um número), considerando-se a incerteza absoluta igual a uma unidade do último dígito de leitura.
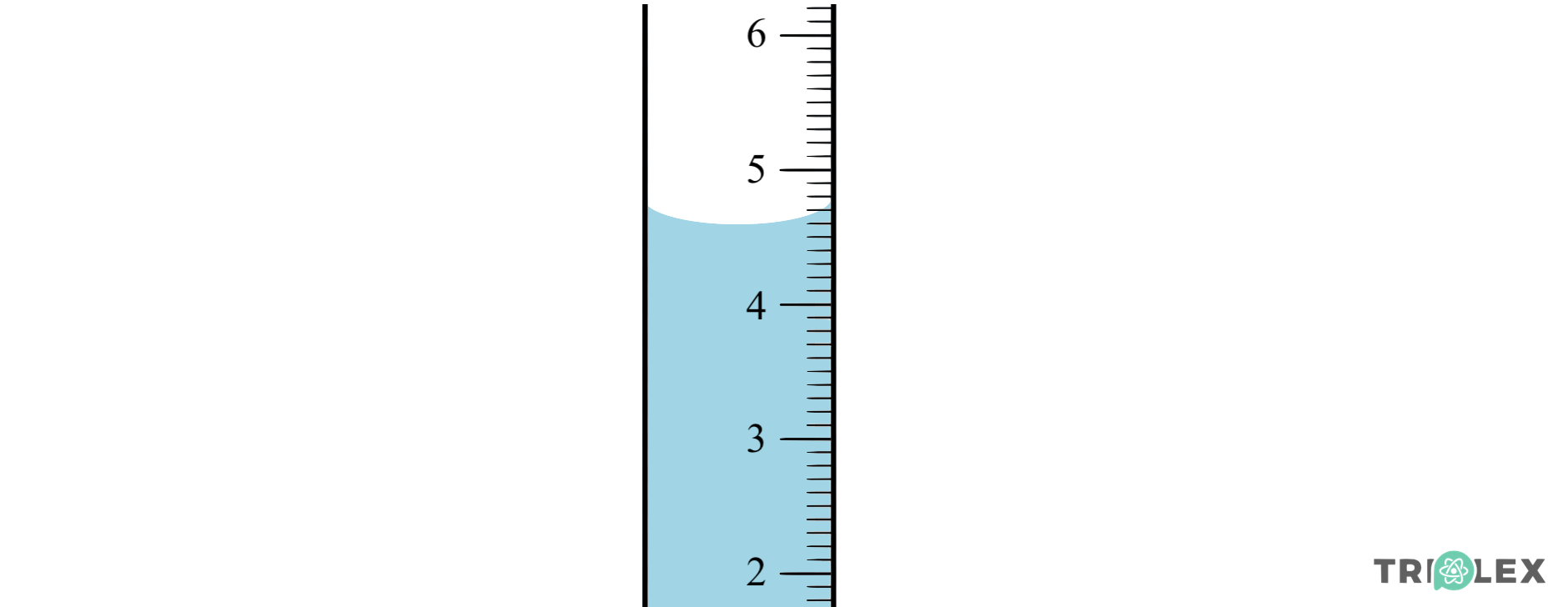
O volume das gotas de água foi medido com uma bureta, um instrumento analógico, logo, considera-se a incerteza absoluta igual a metade do valor da divisão menor da escala.
Assim, tanto o valor da massa como os valores de volume apresentam três algarismos significativos, sendo o último algarismo o algarismo estimado.
Note-se que, como o tamanho das gotas pode variar, podemos encontrar resultados diferentes com instrumentos diferentes, pelo que os dados apresentados são apenas uma sugestão de resolução.
1.1. O volume de água adicionado ao gobelé.
- Vgotas = Vfinal – Vinicial = 7,60 – 1,60 = 6,00 ml
Como o volume das gotas é obtido de uma diferença, o resultado deve apresentar o mesmo número de casas decimais que a parcela com o número mais reduzido de casas decimais, neste caso, duas.
1.2. o volume de uma gota de água.
1.3. A massa de uma gota de água.
1.4. O número de moléculas numa gota de água.
- M(H2O) = 18,02 g mol-1
Apesar do valor resultar de um quociente, como um dos fatores corresponde a um valor tabelado, o número de algarismos significativos do resultado deverá ser igual ao do valor obtido experimentalmente, ou seja, três.
- N = n NA = 0,00284 x 6,02 x 1023 = 1,71 x 1021 moléculas de água
1.5. Indica, justificando, quais as incertezas de leitura dos instrumentos de medida utilizados.
🔶 A massa das gotas de água no gobelé foi medida com uma balança digital cuja sensibilidade é 0,01 g e, sendo digital, a incerteza de leitura é igual, ou seja, ± 0,01 g.
🔶 O volume de água foi medido com uma bureta cuja menor divisão da escala era 0,1 mL pelo que a incerteza de leitura será metade, ou seja, ± 0,05 mL.
1.6. Qual é a relação entre a massa e o volume das gotas de água?
Procura encontrar uma justificação para essa relação.
🔶 O volume e a massa das gotas de água são semelhantes, uma vez que a densidade da água é aproximadamente 1 g cm–3 (varia ligeiramente com a temperatura).
2. Seleciona a opção que completa corretamente a afirmação.
O volume das 100 gotas de água resulta de um medição ______ e a massa de uma gota de água resulta de uma medição ______ .
(A) direta … direta
(B) direta … indireta
(C) indireta … indireta
(D) indireta … direta
- Opção (B)
3. Mediu-se a massa de um certo volume de água numa balança digital.
O valor obtido foi 12,060 g.
3.1. Com quantos algarismos significativos está escrito o valor desta massa?
(A) 3
(B) 2
(C) 5
(D) 4
- Opção (C)
3.2. Qual é a sensibilidade da balança?
(A) 0,01 g
(B) 0,001 g
(C) 1 g
(D) 1 mg
- Opção (D)
3.3. Como se deve apresentar o resultado desta medida?
(A) (12,060 ± 1) g
(B) (12,0600 ± 0,0005) g
(C) (12,060 ± 0,001) g
(D) (12,06 ± 0,001) g
- Opção (C)
4. Com o objetivo de determinar experimentalmente o número de moléculas de uma gota de água, um grupo de alunos, mediu a massa de uma proveta de 10 mL vazia, tendo registado 41,10.
Deixaram cair 100 gotas de água na proveta e, no final, voltaram a medir a massa do conjunto, tendo registado o valor de 46,25 g.
4.1. Indica a medida do volume registada pelos alunos com respetiva incerteza de leitura.
🔶 V = (4,60 ± 0,05 ) mL
4.2. Indica, justificando, a incerteza de leitura associada à medição de massa com a balança.
🔶 Como se trata de um instrumento digital, a incerteza absoluta de leitura corresponde ao valor mínimo que a balança é capaz de medir, ou seja, 0,01 g.
4.3. A partir da massa das gotas de água, determina o número de moléculas numa gota de água com o número adequado de algarismos significativos.
- M(H2O) = 18,02 g mol-1
🔶 Como a massa de uma gota é obtida de um quociente, o resultado deve apresentar o mesmo número de algarismos significativos do fator com o número mais reduzido de algarismos significativos, neste caso, três.
🔶 Apesar do valor resultar de um quociente, como um dos fatores corresponde a um valor tabelado, o número de algarismos significativos do resultado deverá ser igual ao do valor obtido experimentalmente, ou seja, três.
- N = n NA = 0,00286 x 6,02 x 1023 = 1,72 x 1021 moléculas de água
5. Para determinar o número de moléculas existentes numa gota de água, um grupo de alunos procedeu à medição da massa de 100 gotas de água numa balança digital com sensibilidade de 1 mg.
5.1. Por que razão os alunos não mediram diretamente a massa de uma gota de água?
🔶 Porque uma gota de água tem uma massa muito pequena que poderia ser menor que o menor valor que a balança permite ler.
🔶 Mesmo sendo possível medi-la diretamente numa balança, medida da massa de uma gota de água teria menos rigor (menor número de algarismos significativos) do que a medida da massa de 100 gotas de água.
5.2. Calcula o número de moléculas de água existentes numa gota e apresente o resultado com três algarismos significativos, sabendo que a medida efetuada pelos alunos foi 5,084 g.
- M(H2O) = 18,02 g mol-1
Como a massa de uma gota é obtida de um quociente, o resultado deve apresentar o mesmo número de algarismos significativos do fator com o número mais reduzido de algarismos significativos, neste caso, três.
Apesar do valor resultar de um quociente, como um dos fatores corresponde a um valor tabelado, o número de algarismos significativos do resultado deverá ser igual ao do valor obtido experimentalmente, ou seja, três.
- N = n NA = 0,00282 x 6,02 x 1023 = 1,70 x 1021 moléculas de água
6. O valor «100 gotas» tem um número infinito de algarismos significativos por ser um número inteiro:
(A) que resulta de uma definição.
(B) muito grande.
(C) que não resulta de uma medição.
(D) que resulta de uma contagem.
- Opção (D)
7. Com o objetivo de determinar o volume e o número de moléculas de uma gota de água, um grupo de alunos planeou uma atividade laboratorial, tendo obtido os seguintes valores:
- Massa / 100 gotas = 5,120 g ⇒ sensibilidade = 0,001 g
- Volume / 100 gotas = 5,10 mL ⇒ sensibilidade = 0,1 mL
7.1. Apresenta os resultados das medições da massa e do volume das 100 gotas de água indicando a incerteza associada a cada medição.
🔶 m = (5,120 ± 0,001) g;
🔶 V = (5,10 ± 0,05) ml
7.2. Determina o número de moléculas presentes numa gota de água.
7.3. Comprova que o valor da massa volúmica da água é de 1,0 g/ml.
7.4. Determina o número de átomos de hidrogénio e de oxigénio que fazem parte de uma gota de água.
Qual a sua ordem de grandeza?
Numa molécula de H2O existem 2 átomos de hidrogénio:
🔶 n(H) = 2 x 2,84 x 10-3 = 5,68 x 10-3 mol
🔶 N = n x NA ⇔ N = 5,68 x 10-3 x 6,022 x 1023 = 3,42 x 1021 átomos de hidrogénio
Numa molécula de H2O existem 2 átomos de oxigénio:
🔶 n(O) = 1 x 2,84 x 10-3 = 2,84 x 10-3 mol
🔶 N = n x NA ⇔ N = 2,84 x 10-3 x 6,022 x 1023 = 1,71 x 1021 átomos de oxigénio
- OG = 1021 átomos
8. Compara o número de moléculas contidas numa gota de água (1,69 x 1021) com o número de gotas de água contidas numa garrafa de 33 cl usando dois processos distintos:
Dados:
- m1 gota = 5,050 x 10-2 g ;
- V1 gota = 5,00 x 10-2 mL ;
- ρágua = 1,0 g/mL
8.1. a partir dos valores da massa volúmica da água, da massa de uma gota de água e do número de moléculas numa gota de água.
8.2. Utilizando os valores do volume de uma gota de água e do número de moléculas numa gota de água.
9. Para calcular a massa volúmica, ρ, de um líquido foi necessário medir os seguintes valores:
- Massa da amostra, m = 7,69 g
- Volume da amostra , V= 0,60 cm3
Com a massa da amostra e com o volume calculou-se a massa volúmica, e obteve-se 12,817 g/cm3
9.1. Indica o resultado final com o número correto de algarismos significativos.
- 13 g/cm3
9.2. Indica a incerteza associada à pipeta graduada usada para medir este volume, tendo em conta a menor divisão da sua escala.
- 0,05 cm3
9.3. Indica a incerteza associada à balança digital utilizada para medir esta massa.
- 0,01 g