Ficha nº12 – Diluição de soluções aquosas
1. Um concentrado de sumo um litro de concentrado, consegue fazer 10 litros de sumo.
Calcula o volume da garrafa concentrado de sumo se obtivermos 7,5 litros de sumo.
O fator de diluição do sumo concentrado é f =10.
Portanto, se uma garrafa 7,5 litros de sumo, o volume da garrafa de sumo concentrado é 10 vezes menor, ou seja, 0,75 litros.
2. O que distingue uma solução concentrada de uma solução diluída é:
(A) Uma solução concentrada contém mais solvente que igual volume de solução diluída.
(B) Uma solução concentrada contém mais soluto.
(C) Uma solução concentrada contém mais soluto que igual volume de solução diluída.
(D) Uma solução concentrada contém menos soluto que igual volume de solução diluída.
- Opção (C)
3. O rótulo de um frasco que contém uma solução aquosa de hidróxido de sódio.
3.1 Determina a concentração da solução de hidróxido de potássio que se encontra no frasco.
3.2 Determina o volume de solução que é necessário retirar para preparar 0,45 L de uma solução diluída de um fator 16.
3.1 Massa de 1 dm3 de solução: m = 2120 g.
Massa de soluto presente nesse volume:
30% x 2120 g = 636 g.
Quantidade de matéria de KOH correspondente a essa massa:
Logo 1 dm3 de solução tem 11,3 mol de soluto e portanto a concentração é c = 11,3 mol/dm3.
3.2 Concentracão final:
Em 0,45 dm3 dessa solução há 0,45 x 0,71 = 0,32 mol de soluto.
Volume da solução inicial com essa quantidade de matéria: 0,32/11,3 = 0,028 dm3
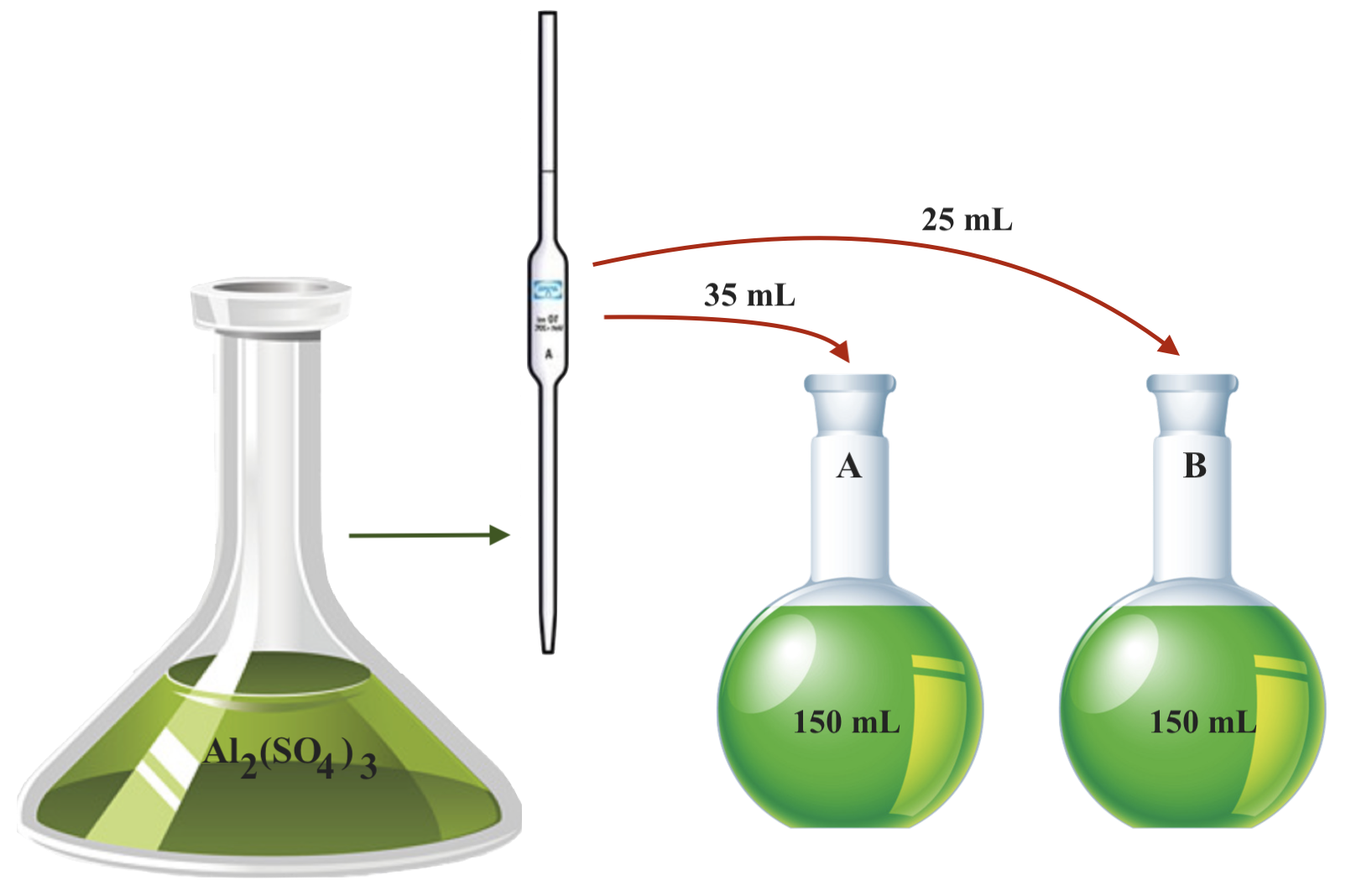
4. O Tomás pretendia obter duas soluções com diferentes concentrações, partindo de uma solução de sulfato de alumínio, Al2(SO4)3, com 0,20 mol dm-3.
Calcula a concentração molar em iões Al3+ das soluções preparadas.
Cálculo das novas concentrações nos balões volumétricos A e B, de 100 ml de capacidade cada.
Como 1 mol de Al2(SO4)3 contém 2 mol de iões Al3+,
[Al2(SO4)3] = 2 x [Al3+]
Balão A:
- ni=nf ⇒ ciVi = cfVf ⇒ 0,20 x 35 x 10-3 = cf x 150 x 10-3 ⇔ cf = 0,047 mol dm-3
[Al3+] = 2 x 0,47 = 0,093 mol dm-3
Balão B:
- ni=nf ⇒ ciVi = cfVf ⇒ 0,20 x 25 x 10-3 = cf x 150 x 10-3 ⇔ cf = 0,033 mol dm-3
[Al3+] = 2 x 0,47 = 0,067 mol dm-3
5. Diluíram-se 100 cm3 de uma solução 0,120 mol dm-3 em ácido nítrico, para a seguinte solução.
5.1. Calcula o valor do fator de diluição.
5.2. Seleciona a opção que permite calcular corretamente a concentração de ácido clorídrico na solução final.
(A)
(B)
(C)
(D)
5.1
5.2 Opção (D)
6. Dissolveram-se 21,2 g de sulfato de sódio, Na2SO4 em água até completar 200 cm3 de solução.
6.1 A concentração em massa da solução é:
(A) 5,3 g/dm3
(B) 21,2 g/dm3
(C) 106 g/dm3
(D) 212 g/dm3
6.2 A concentração da solução é:
(A) 0,20 mol/dm3
(B) 0,50 mol/dm3
(C) 0,75 mol/dm3
(D) 21,2 mol/dm3
6.3 Se fossem adicionados 600 cm3 de água à solução, a concentração da solução obtida seria:
(A) 3 vezes maior.
(B) 4 vezes menor.
(C) 3 vezes menor.
(D) 4 vezes maior.
6.1 Opção (C)
6.2 Opção (C)
6.3 Opção (B)
7. Para preparar uma solução de cloreto de magnésio, a partir do reagente sólido, pesaram-se 16,6 g deste reagente.
Sabendo que o volume de solução preparado foi de 350,0 cm3, calcule a concentração molar da solução.
M(MgCl2) = 95,2 g mol-1
8. Considera a seguinte mistura entre uma solução de ácido clorídrico e uma solução aquosa de cloreto de sódio.
Calcula a concentração de :
8.1 iões hidrogénio, H+;
8.2 iões cloreto, Cl–.
9. Calcula o volume de água que se deve adicionar a seguinte solução de carbonato de potássio, de forma a obter uma solução de concentração 0,096 mol dm-3 desse sal.
10. O Duarte pretende preparar um refresco a partir de um sumo concentrado.
Considera 200 ml de determinado sumo em que csoluto = 0,80 mol dm-3.
10.1 Seleciona a opção que traduz o volume de água, em cm3, que deverá ser acrescentado quando se faz uma diluição de um fator 10.
(A) 2000
(B) 1800
(C) 500
(D) 400
1.2 Indica a concentração da solução diluída.
1.1 Opção (B)
1.2
11. Para preparar um volume de 300,0 cm3 de uma solução diluída, a partir da solução de concentração 0,75 mol dm-3, usaram-se 30 cm3.
Calcula:
11.1. a concentração da solução diluída.
11.2. o fator de diluição.
11.1 ci x Vi = cf x Vf, logo
11.2
12. Considera a seguinte mistura: 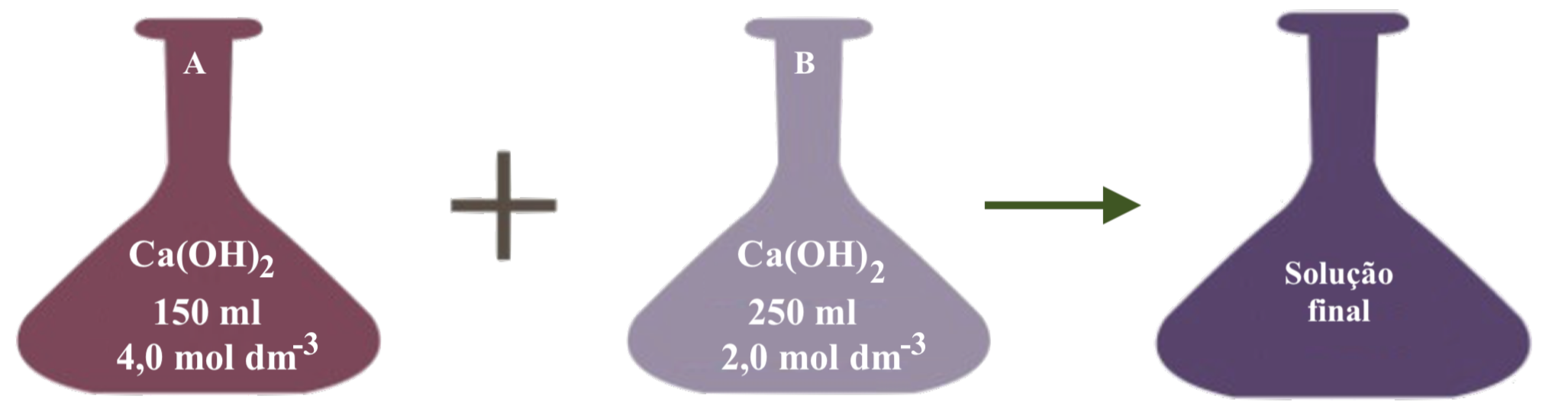
12.1 iões hidróxido, OH–;
12.2 iões cálcio, Ca2+.
12.1 Solução A:
Solução B:
Ca(OH)2 (aq) ➔ Ca2+ (aq) + 2 OH– (aq)
Verifica-se que [OH–] = 2 [Ca(OH)2] ➔ [OH–]= 2 x 2,75 ⇔ [OH–] = 5,5 mol dm-3
12.2 [Ca2+]= [ Ca(OH)2] ⇔ [Ca2+] = 2,75 mol dm-3
13. O Tomás pipetou 50,0 cm3 de uma solução aquosa de ácido sulfúrico, H2SO4, de concentração 0,40 mol dm-3 para um balão volumétrico de 250,0 cm3.
Determina a concentração de ácido sulfúrico, se adicionar água destilada até que o volume do balão atinja o traço de referência.
14. Adiciona-se 120 ml de água a 40 ml de uma solução 0,20 mol dm-3 de Cloreto de sódio.
14.1. Indique o fator de diluição utilizado.
14.2. Seleciona a opção a que corresponde à concentração da solução diluída, em mol dm-3.
(A) 0,10
(B) 0,20
(C) 0,25
(D) 0,40
14.1
14.2
Opção (A)
15. Uma dose de uma bebida tem o volume de 50 ml, se for adicionado 150 ml de água a esta dose.
A concentração desta solução passou para:
(A) 4 vezes mais;
(B) 4 vezes menos;
(C) 3,75 vezes mais;
(D) 3,75 vezes menos.
Opção (B)
fator de diluição 4.