Ficha nº13 – Química Verde e economia atómica
1. O titânio pode ser extraído por dois processos distintos.![]()
Um dos processos utiliza um metal mais reativo para provocar o deslocamento do titânio, de acordo com a seguinte equação química:
TiO2 (s) + 2 Mg (s) → Ti (s) + 2 MgO (s)
Outro processo consiste na eletrólise do TiO2, de acordo com a seguinte equação química:
TiO2 (l) → Ti (l) + O2 (g)
1.1 Calcula a economia atómica percentual para cada um dos processos.
1.2 De acordo com a alínea anterior, qual dos processos é mais “verde”?
1.1
1.2 O processo de eletrólise é mais “verde” uma vez que apresenta uma vez que apresenta uma maior economia atómica percentual.
2. Um dos princípios da «química verde» a nível de processos químicos de fabrico é:![]()
(A) dar prioridade à prevenção de resíduos e tornar os processos mais eficientes.
(B) aumentar a produção de resíduos e tornar os processos mais eficientes.
(C) dar prioridade ao tratamento de resíduos e tornar os processos mais eficientes.
(D) aumentar a produção de resíduos e tornar os processos menos eficientes.
- Opção (A)
3. Lê atentamente o seguinte texto:![]()
A Monsanto Company recebeu, em 1996, o prémio “Presidential Green Chemistry Challenge” por melhorar os métodos utilizados na produção do seu herbicida. Anteriormente, a síntese deste produto requeria o uso de amoníaco, formaldeído, cianeto de hidrogénio e ácido clorídrico. Todas estas substâncias representam um perigo para os trabalhadores que as utilizam e para o ambiente, mas o cianeto de hidrogénio, em particular, é extremamente tóxico. Outro problema era a quantidade produzida de resíduos.
A Monsanto desenvolveu um novo mecanismo de síntese capaz de eliminar o cianeto de hidrogénio e o formaldeído do processo de síntese e que não gera qualquer resíduo.
Adaptado de: Mark Bishop, An Introduction to Chemistry, p. 621
Identifique, pelo menos, dois princípios da Química Verde que são cumpridos com este novo mecanismo de síntese.
- prevenção. Deve-se evitar a produção de resíduos, investindo em técnicas de produção mais limpa.
- Sem a emissão de resíduos, não há necessidade de tratamento do mesmo, que muitas vezes envolve procedimentos de alto custo e não atinge os parâmetros estabelecidos pela legislação.
- Economia de átomos.
- Deve-se projetar metodologias que possam maximizar a incorporação de todos os compostos de partida no produto final, reduzindo a produção de subprodutos.
- Síntese de produtos menos perigosos. Sempre que possível, a síntese de um produto químico deve utilizar e gerar substâncias que possuam pouca ou nenhuma toxicidade à saúde humana e ao ambiente.
4. O método tradicional de produção da sertalina, um medicamento usado no tratamento da depressão, usava quatro solventes nocivos para o ambiente, o que originava resíduos apreciáveis a tratar no fim do processo.![]()
Esse método necessitava de 500 kg de solventes por cada quilograma de medicamento produzido.
Atualmente recorre-se a um único solvente, o etanol, vulgarmente designado por álcool etílico, sendo utilizados 50 kg de solvente por cada quilograma de sertalina produzido.
4.1 Quanto diminuiu a massa de solventes, do método tradicional para o método atual?
Apresenta o resultado em percentagem.
4.2 Compara os dois métodos do ponto de vista ambiental, justificando.
4.1 |Δm| = 500 – 50 = 450 kg, ou seja, houve uma diminuição de 450 kg na massa de solventes em relação aos 500 kg necessários no método tradicional. Tal corresponde a uma redução de solventes de a uma redução de solventes de (450/500) x 100% =
4.2 O método tradicional tem um maior impacto ambiental, devido à maior quantidade de resíduos a tratar e ao seu efeito nocivo para o ambiente, relativamente ao etanol usado no método atual.
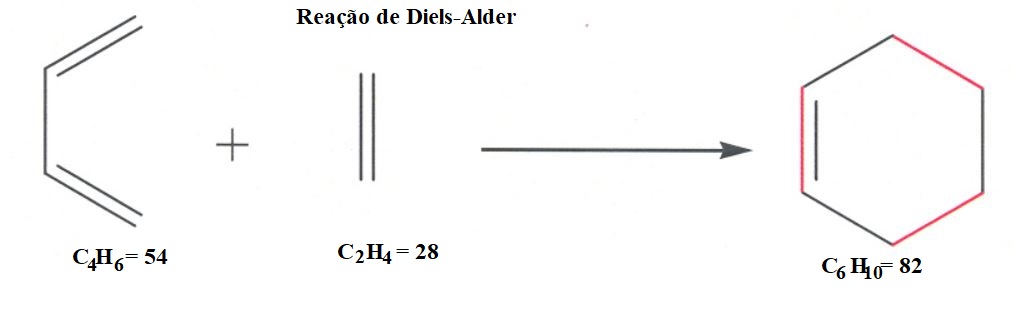
5. O conceito de economia atómica foi introduzido por Trost, em 1991, e mede a eficiência de uma reação.![]()
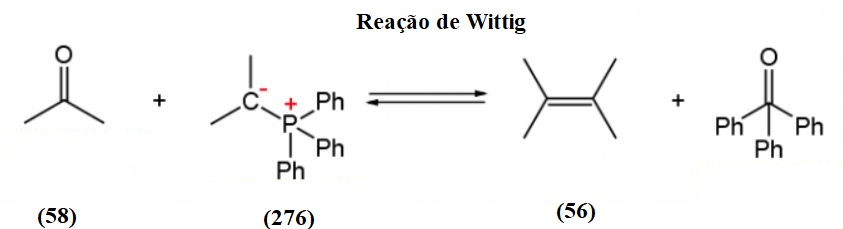
A adição de Diels-Alder é um excelente exemplo de uma reação com elevada economia atómica, o mesmo não acontecendo na reação de Wittig.
5.1 Calcula a economia atómica de cada uma das reações.
5.2 Indica uma outra razão, além da baixa economia atómica, por que a reação de Wittig não é considerada «verde».
5.1
%
%
5.2 É gerado um subproduto no processo.
6. A gasolina, essencialmente formada por octano, C8H18, o etanol, C2H5OH, e o hidrogénio, H2, podem ser usados como combustíveis.![]()
Na tabela apresentam-se informações sobre a variação de entalpia de cada reação de combustão (com oxigénio, O2), e sobre os produtos da reação.
| Combustível | ΔH / kcal mol-1 | Produtos da reação |
| H2 | -68,3 | H2O |
| C2H5OH | -326,7 | CO2 e H2O |
| C8H18 | -1222,5 | CO2 e H2O |
De acordo com a informação disponível, e comparando a reação de iguais quantidades de matéria de cada combustível, a combustão do:
(A) hidrogénio apresenta menor impacto ambiental e menor vantagem energética do que a do etanol.
(B) hidrogénio apresenta menor impacto ambiental e maior vantagem energética do que a do etanol.
(C) etanol apresenta maior impacto ambiental e menor vantagem energética do que a do octano.
(D) etanol apresenta maior impacto ambiental e maior vantagem energética do que a do octano.
- Opção (A)
7. O ibuprofeno é um fármaco do grupo dos anti-inflamatórios não esteroides, sendo também analgésico e antipirético.![]()
A sua síntese pode ser efetuada por dois mecanismos diferentes, cujas características se resumem na tabela seguinte:
| Mecanismo | Rendimento | Catalisador | Consumo energético | Quantidade de subprodutos |
| A | 77% | reutilizável | Baixo | Baixa |
| B | 40% | Não reutilizável | Elevado | Elevada |
Compara os mecanismos A e B tendo em conta os princípios da Química Verde.
O processo A é mais “verde” uma vez que apresenta maior rendimento, os seus catalisadores são reutilizável, apresenta menor consumo energético e menor quantidade de subprodutos o que se enquadra, respetivamente, nos princípios da química verde.
8. A economia atómica num processo químico de fabrico é tanto maior quanto:![]()
(A) maior for a produção de resíduos e menor for o número de átomos de reagentes incorporados no produto desejado.
(B) maior for a produção de resíduos e também maior for o número de átomos de reagentes incorporados no produto desejado.
(C) menor for a produção de resíduos e também menor for o número de átomos dos reagentes incorporados no produto desejado.
(D) menor for a produção de resíduos e maior for o número de átomos de reagentes incorporados no produto desejado.
- Opção (D)
9. A hidrazina (N2H4) é usada para combustível de foguetões.![]()
9.1 Calcula a economia atómica percentual da produção de hidrazina:
2 NH3 (g) + NaClO (aq) → N2H4 (l) + NaCl (aq) + H2O (l)
9.2 Sugere um processo para tornar maior a economia atómica percentual nesta reação.
9.1 e.a(%) = 29,5%
9.2 Fazer o aproveitamento de NaCl, visto ser um produto muito utilizado na industria, para reciclar a água, que é outro produto da reação.
Michael John Smith, catedrático do Departamento de Química da Universidade do Minho, considera que, pelo ”aumento da consciência ambiental de todos os cidadãos a química verde vai assumir um papel mais predominante nos próximos anos “. A verdade é que já há bastantes exemplos da aplicação dos seus tópicos principais. Tomemos o exemplo da prevenção de resíduos e da economia atómica. A maneira mais eficiente de diminuir o impacto ambiental de uma atividade industrial é desenvolver soluções que previnam a formação de resíduos. A partir do momento em que se investe em tecnologias de produção mais limpas, não há necessidade de aplicar recursos no tratamento de resíduos, que nem sempre resolve satisfatoriamente o problema.
in revista Super Interessante n.º 165, A Química Verde – Novo paradigma industrial, p. 70(2012)
10.1 Identifica os princípios da química verde referidos no texto.
10.2 Comenta a afirmação seguinte, extraída do texto:
“A partir do momento em que se investe em tecnologias de produção mais limpas, não há necessidade de aplicar recursos no tratamento de resíduos (… ).”
10.1 Prevenção de resíduos e economia atómica
10.2 O investimento em tecnologias mais limpas está na base da prevenção da poluição e corresponde à implementação de praticas, processos, técnicas ou tecnologias que evitem ou minimizem a geração de resíduos e de poluentes.
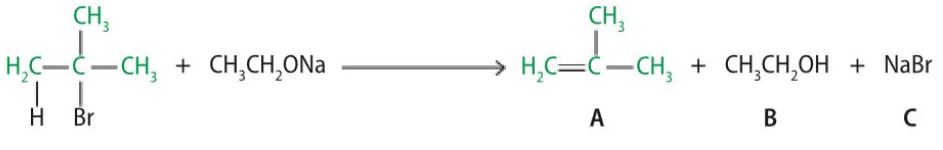
11. Considera a reação de produção do composto A, representado pela sua fórmula de estrutura.
11.1 Identifica pelos seus nomes os compostos A, B e C.![]()
11.2 Indica o significado dos átomos assinalados a verde e a negro.
11.3 Calcula a economia atómica percentual.
11.4 Discute se este seria o melhor processo para obter o composto A, sob o ponto de vista da Química.
11.1 A – metilpropreno ; B – etanol ; C – Brometo de sódio
11.2 A verde estão assinalados os átomos que fazem parte do produto pretendido. Os restantes serão desperdício da reação.
11.3 e.a.(%) = 27,3%
11.4 O valor da economia atómica percentual é muito baixo, porque os desperdícios (B e C) têm uma massa muito elevada. Daqui se conclui que este não será o melhor processo, a menos que se reutilizem os subprodutos.
12. A Química Verde baseia-se na noção que não basta pensar nos processos químicos do ponto de vista económico, é fundamental refletir sobre o seu impacto socioambiental.![]()
Das afirmações seguintes, seleciona a que corresponde a uma medida enquadrável na Química Verde:
(A) Avaliar os riscos ambientais apenas das matérias-primas.
(B) Selecionar processos que minimizem a economia atómica percentual.
(C) Utilizar matérias-primas de fontes não renováveis.
(D) Selecionar os processos de produção que minimize o consumo energético.
- Opção (D)
13. Elabora um pequeno texto sobre a necessidade/importância da Química Verde.
- Toda a massa dos reagentes está contida no produto.
- Melhor aproveitamento das matérias-primas.
- Não foram produzidos resíduos.
- Uso de catalisadores.
14. Determina a economia atómica percentual para a reação de produção de hidrogénio:
C(s) + 2 H2O (g) → CO2 (g) + 2 H2 (g)
e.a. (%) = 8,41%
15. Lê atentamente o seguinte texto:![]()
O processo tradicional de produção de um determinado medicamento para o colesterol implicava a utilização de reagentes perigosos e a produção de subprodutos tóxicos até ter sido desenvolvido um processo de síntese utilizando uma enzima sintética e matéria-prima de baixo custo. Este processo diminui a toxidade, quer das matérias-primas, quer dos subprodutos.
O texto reflete alterações efetuadas num processo industrial com vista à minimização dos seus impactos ambientais. Atendendo ao conceito de Química Verde identifique o princípio que é cumprido com este novo mecanismo de síntese.
As alterações enquadram-se no principio da química verde, nomeadamente, a síntese de produtos menos perigosos e a utilização de catalisadores altamente seletivos e efetivos.

Os exercícios foram muito bem escolhidos.