Ficha nº1 : Exames e TI (2006 – 2010)
Voltar a: 10ºAno – Química
Ficha nº1
Exercícios de exames e testes intermédios (2006 – 2010)
10ºano – Química – Domínio 2 – Subdomínio 1 (Ligação química)
1. (2006 – 1ªF) A configuração eletrónica de um átomo de azoto, no estado de menor energia, pode ser representada por [He] 2s2 2p3.
Selecione a alternativa que completa corretamente a frase:
A geometria de uma molécula de amoníaco é…
(A) … piramidal triangular, e o átomo central possui apenas três pares de eletrões.
(B) … piramidal triangular, e o átomo central possui três pares de eletrões ligantes e um não ligante.
(C) … triangular plana, e o átomo central possui apenas três pares de eletrões.
(D) … triangular plana, e o átomo central possui três pares de eletrões ligantes e um não ligante.
- Opção (B)
⇒ A geometria de uma molécula (distribuição espacial dos átomos que a constituem) é tal que seja mínima a intensidade das forças repulsivas, que se manifestam, essencialmente, entre os dupletos ligantes e entre estes e os não ligantes.
⇒ O átomo de azoto tem 5 eletrões de valência enquanto o de hidrogénio tem apenas 1 eletrão de valência. Na molécula de amoníaco, o átomo de azoto (átomo central) está ligado a três átomos de hidrogénio por três dupletos ligantes e possui um dupleto não ligante.
⇒ A geometria da molécula de amoníaco é piramidal triangular, pois estes dupletos, devido às forças repulsivas exercidas entre si, afastam-se o mais possível.
Os átomos de N e H localizam-se nos vértices de uma pirâmide triangular.
- Opção (B)…………. 7 pontos
2. (2007 – 1ªF) As moléculas de água, H2O, e de dióxido de carbono, CO2, têm estruturas bem definidas, a que correspondem propriedades físicas e químicas distintas.
Classifique como verdadeira (V) ou falsa (F) cada uma das afirmações seguintes.
(A) Na molécula de CO2, existem quatro pares de electrões não ligantes.
(B) Na molécula de H2O, existem dois pares de electrões partilhados.
(C) As duas moléculas (H2O e CO2) apresentam geometria linear.
(D) Na molécula de H2O, existe um par de electrões não ligantes.
(E) Na molécula de CO2, as ligações carbono-oxigénio têm diferentes comprimentos.
(F) O ângulo de ligação, na molécula de H2O, é superior ao ângulo de ligação, na molécula de CO2.
(G) Na molécula de H2O, existem quatro electrões ligantes e quatro não ligantes.
(H) Na molécula de CO2, nem todos os electrões de valência são ligantes.
- Verdadeiras – (A), (B), (G) e (H)
- Falsas – (C), (D), (E) e (F)
Por cada átomo de oxigénio existem dois pares de eletrões de valência não ligantes.
⇒ (B) Verdadeira.
Para cada ligação O–H contribui um par de eletrões partilhados. Como na molécula de água existem duas ligações O–H, existem dois pares de eletrões partilhados.
⇒ (C) Falsa.
A molécula de CO2 apresenta geometria linear, mas a molécula de H2O apresenta uma geometria angular.
⇒ (D) Falsa.
Na molécula de H2O existem dois pares de eletrões de valência não ligantes.
⇒ (E) Falsa.
Na molécula de CO2 as ligações carbono-oxigénio são equivalentes, pelo que têm o mesmo comprimento.
⇒ (F) Falsa.
O ângulo de ligação na molécula de CO2 é de 180° (molécula linear), enquanto que a molécula de H2O apresenta uma geometria angular, pelo que tem um ângulo inferior a 180°.
⇒ (G) Verdadeira.
Na molécula de H2O existem quatro eletrões de valência ligantes que formam as duas ligações O–H e existem dois pares de eletrões de valência não ligantes no O.
⇒ (H) Verdadeira.
Na molécula de CO2 há quatro pares de eletrões de valência não ligantes.
3. (TI – 13/02/2008) Actualmente, a troposfera é constituída por espécies maioritárias, como o azoto, N2, o oxigénio, O2, a água, H2O, e o dióxido de carbono, CO2, além de diversas espécies vestigiais, como o hidrogénio, H2, o metano, CH4, e o amoníaco, NH3.
3.1. Considerando as moléculas de N2 e de O2, seleccione a alternativa que corresponde à representação correcta de uma dessas moléculas.
- Opção (D)
⇒ O átomo de azoto tem 5 electrões de valência. A estrutura electrónica da molécula de azoto, N2, de acordo com a regra do octeto, implica uma ligação covalente tripla (partilha de três pares de electrões de valência) ente os átomos de azoto.
⇒ O átomo de oxigénio tem 6 electrões de valência. A estrutura electrónica da molécula de oxigénio, O2, de acordo com a regra do octeto, implica uma ligação covalente dupla (partilha de dois pares de electrões de valência) ente os átomos de oxigénio.
- Opção (D)…………. 8 pontos
(A) A molécula H2O tem geometria linear.
(B) A molécula NH3 tem geometria piramidal trigonal.
(C) A molécula CH4 tem geometria quadrangular plana.
(D) A molécula CO2 tem geometria angular.
- Opção (B)
⇒ A geometria de uma molécula é aquela que conduz à máxima estabilidade do sistema molecular.
⇒ Segundo o método da repulsão dos pares eletrónicos de valência, estes dispõem-se no espaço o mais afastados possível, de modo a conduzir às menores repulsões eletrónicas possíveis.
⇒ No caso da molécula NH3, os pares eletrónicos de valência que rodeiam o átomo central são três pares de eletrões ligantes, correspondentes às três ligações covalentes N–H e um par eletrónico não ligante localizado no azoto. O maior afastamento possível destes quatro pares obtém-se quando eles se dispõem no espaço de modo, aproximadamente, tetraédrico. Como um destes pares é não ligante, a molécula NH3 apresenta uma geometria piramidal trigonal.
Afirmações incorretas: ⇒ (A) A molécula de H2O tem geometria angular. ⇒ (C) A molécula de CH4 tem geometria tetraédrica. ⇒ (D) A molécula de CO2 tem geometria linear.- Opção (B)…………. 8 pontos
4. (TI – 13/02/2008) Os principais constituintes do petróleo bruto e do gás natural são compostos orgânicos pertencentes à família dos alcanos, também designados por hidrocarbonetos saturados.
Relativamente aos alcanos, classifique cada uma das seguintes afirmações como verdadeira (V) ou falsa (F).
(A) Os alcanos têm fórmula geral CnH2n+2 (com n = 1,2 3, …, sendo n o número de átomos de carbono).
(B) O alcano designado por heptano tem apenas seis átomos de carbono.
(C) Os alcanos podem ter ligações carbono-carbono simples e duplas.
(D) Um dos átomos de carbono do 2,2-dimetilpropano está ligado a quatro átomos de carbono.
(E) Os alcanos são hidrocarbonetos por só conterem átomos de carbono e de hidrogénio.
(F) Um alcano com apenas três átomos de carbono pode ser ramificado.
(G) O hexano tem mais átomos de carbono do que o 2,3-dimetilbutano.
(H) Os CFC podem ser considerados derivados halogenados dos alcanos.
- Verdadeiras – (A), (D), (E) e (H)
- Falsas – (B), (C), (F) e (G)
⇒ (C) Falsa.
Os alcanos só podem ter ligações carbono-carbono simples.
⇒ (F) Falsa.
Um alcano com apenas três átomos de carbono não pode ser ramificado.
⇒ (G) Falsa.
O hexano tem o mesmo número de átomos de carbono que o 2,3-dimetilbutano.
5. (TI – 30/05/2008) O monóxido de carbono, CO, e o dióxido de carbono, CO2, são gases que existem na atmosfera, provenientes de fontes naturais (fogos florestais, emissões vulcânicas) e de fontes antropogénicas (combustões domésticas e industriais, escapes de veículos motorizados).
As moléculas CO e CO2 podem ser representadas, respectivamente, por:Seleccione a alternativa que contém os termos que devem substituir as letras (a) e (b), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
A ligação carbono–oxigénio na molécula CO2 tem __(_a_)__ energia e __(_b_)__ comprimento do que a ligação carbono–oxigénio na molécula CO.
(A) … maior … maior …
(B) … menor … maior …
(C) … menor … menor …
(D) … maior … menor …
- Opção (B)
⇒ A formação de uma ligação química envolve libertação de energia – a energia de ligação.
⇒ Quanto mais forte for a ligação, mais energia será necessária para a quebrar. Quanto maior for o número de electrões partilhados numa ligação química menor será a distância média entre os núcleos dos átomos que estabelecem a ligação, e mais forte será a ligação.
⇒ Como os átomos envolvidos nas ligações das duas moléculas são os mesmos, o comprimento da ligação dupla é maior do que o comprimento da ligação tripla.
⇒ A um maior comprimento de ligação corresponde uma menor energia de ligação.
- Opção (B)…………. 8 pontos
6. (TI – 30/05/2008) Considere as configurações electrónicas dos átomos dos elementos P, Q, R, e S (as letras não correspondem aos símbolos químicos reais desses elementos), no estado fundamental.
P – [Ne] 3s1
Q – 1s2 2s2 2p5
R – 1s2 2s2 2p6 3s2
S – [Ar] 4s1
6.1. Seleccione a alternativa que contém, respectivamente, as configurações electrónicas dos iões Q– e R2+, no estado fundamental.
(A) 1s2 2s2 2p6 e 1s2 2s2 2p6
(B) 1s2 2s2 2p4 e 1s2 2s2 2p6 3s2 3p2
(C) 1s2 2s2 2p4 e 1s2 2s2 2p6
(D) 1s2 2s2 2p6 e 1s2 2s2 2p6 3s2 3p2
- Opção (A)
⇒ O elemento Q adquire maior estabilidade, recebendo um electrão que lhe irá completar o nível de valência.
⇒ Q transforma-se no anião Q–, ao qual corresponde a configuração electrónica 1s2 2s2 2p6.
⇒ O elemento R adquire máxima estabilidade perdendo os dois electrões de valência e transformando-se no catião R2+, ao qual corresponde a configuração 1s2 2s2 2p6.
- Opção (A)…………. 8 pontos
6.2. Seleccione a alternativa que corresponde é fórmula química do composto constituído pelos iões Q– e R2+.
(A) R2Q
(B) RQ2
(C) R2Q3
(D) R3Q2
- Opção (B)
⇒ Na escrita de fórmulas químicas de compostos iónicos, coloca-se primeiro o símbolo do catião e depois o do anião, de modo que a soma das cargas elétricas seja nula.
- Opção (B)…………. 8 pontos
7. (TI – 22/04/2008) Os átomos de carbono e de azoto podem ligar-se entre si de modos diferentes. Em alguns compostos a ligação carbono–azoto é tripla (C ≡ N), enquanto noutros compostos a ligação carbono–azoto é simples (C – N).
O valor da energia m.dia de uma dessas ligações é 276 kJ mol–1, enquanto o valor relativo à outra ligação é 891 kJ mol–1. Em relação ao comprimento médio dessas ligações, para uma o valor é 116 pm, enquanto para a outra é 143 pm.
Seleccione a alternativa que cont.m os valores que devem substituir as letras (a) e (b), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
O valor da energia média da ligação tripla carbono–azoto (C ≡ N) é __(_a_)__, e o valor do comprimento médio dessa ligação é __(_b_)__.
(A) … 276 kJ mol–1 … 116 pm.
(B) … 276 kJ mol–1 … 143 pm.
(C) … 891 kJ mol–1 … 116 pm.
(D) … 891 kJ mol–1 … 143 pm.
- Opção (C)
⇒ A ligação tripla carbono-azoto é mais forte e mais curta que a ligação simples carbono-azoto.
⇒ Assim, a energia média da ligação tripla é superior à da ligação simples e o comprimento médio da ligação tripla é menor que o da ligação simples.
⇒ A alternativa a que corresponde o maior valor da energia de ligação (891 kJ mol-1) e o menor valor de comprimento de ligação, (116 pm), correspondentes à ligação tripla carbono-azoto, é a (C).
- Opção (C)…………. 8 pontos
8. (TI – 22/04/2008) Considerando que a molécula de amoníaco, NH3, possui três pares de electrões de valência ligantes e um par de electrões de valência não ligante, seleccione a alternativa que completa correctamente a frase seguinte.
A geometria da molécula de amoníaco é piramidal trigonal, sendo os ângulos de ligação menores do que os ângulos de um tetraedro regular, porque…
(A) … apenas o par de electrões não ligante exerce repulsão sobre os pares de electrões ligantes.
(B) … as repulsões entre o par de electrões não ligante e os pares de electrões ligantes têm a mesma intensidade que as repulsões entre os pares ligantes.
(C) … as repulsões entre o par de electrões não ligante e os pares de electrões ligantes são mais fortes do que as repulsões entre os pares ligantes.
(D) … apenas os pares de electrões ligantes exercem repulsão sobre o par de electrões não ligante.
- Opção (C)
⇒ A geometria de uma molécula é aquela que conduz à máxima estabilidade do sistema molecular.
⇒ Segundo o método da repulsão dos pares eletrónicos de valência, estes dispõem-se no espaço o mais afastados possível, de modo a conduzir às menores repulsões eletrónicas possíveis.
⇒ No caso da molécula NH3, os pares eletrónicos de valência que rodeiam o átomo central são três pares de eletrões ligantes, correspondentes às três ligações covalentes N – H e o par eletrónico não ligante localizado no azoto.
⇒ O maior afastamento possível destes quatro pares obtém-se quando eles se dispõem no espaço de modo, aproximadamente, tetraédrico, conferindo ao conjunto NH3 uma geometria piramidal trigonal.
⇒ Os ângulos de ligação na molécula de amoníaco são menores que os ângulos de um tetraedro regular, devido ao facto de o efeito repulsivo entre os pares de eletrões não ligante-ligante ser superior ao efeito repulsivo entre os pares de eletrões ligante-ligante.
- Opção (C)…………. 8 pontos
9. (2008 – EE) Justifique o facto de a molécula de água apresentar uma geometria angular, e também o facto de o ângulo de ligação nesta molécula (104,5º) ser inferior ao ângulo correspondente a uma geometria tetraédrica regular (109,5º).
⇒ Na molécula da água, os átomos de oxigénio têm dois pares de eletrões de valência não ligantes, que repelem os pares de eletrões ligantes (existentes entre O e H), pelo que a molécula apresenta uma geometria angular.
⇒ Como a repulsão entre os dois pares não ligantes é superior à repulsão entre pares ligantes, os átomos de hidrogénio são forçados a aproximar-se mais do que o esperado numa disposição tetraédrica.
A resposta deve contemplar os seguintes elementos:
⇒ O átomo de oxigénio da molécula de água tem dois pares de electrões de valência não ligantes, que repelem os pares de electrões ligantes, pelo que a molécula apresenta uma geometria angular.
⇒ Como a repulsão entre pares não ligantes é superior à repulsão entre pares ligantes, os átomos de hidrogénio são forçados a aproximar-se mais do que o esperado numa disposição tetraédrica.
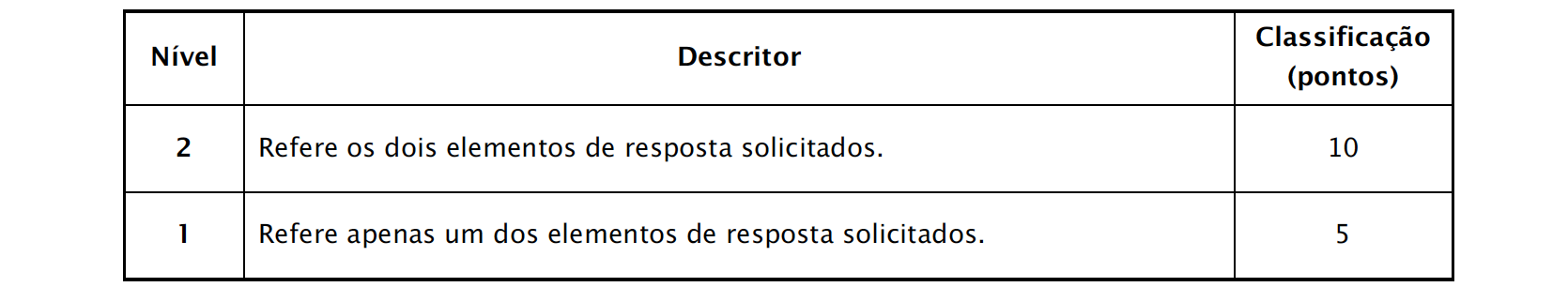
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
10. (TI – 17/03/2009) O dióxido de carbono, CO2 (g), é um dos principais gases que contribuem para o efeito de estufa, sendo conhecidas diversas acções conducentes à redução das suas emissões para a atmosfera.
No entanto, além do dióxido de carbono, o vapor de água, H2O (g), e o metano, CH4 (g), também contribuem para esse efeito.
10.1. Tanto a molécula H2O como a molécula CO2 têm um átomo central, respectivamente de oxigénio e de carbono.
Seleccione a alternativa que corresponde à geometria correcta dessas moléculas.
(A) A molécula H2O é linear, assim como a molécula CO2.
(B) A molécula H2O é linear, enquanto a molécula CO2 é angular.
(C) A molécula H2O é angular, assim como a molécula CO2.
(D) A molécula H2O é angular, enquanto a molécula CO2 é linear.
- Opção (D)
⇒ (A) Falsa.
- porque a molécula de água é angular;
⇒ (B) Falsa.
- pela razão anterior e por a molécula de CO2 ser linear;
⇒ (C) Falsa.
- porque a molécula de CO2 é linear.
- Opção (D)…………. 8 pontos
10.2. O metano, CH4, é o alcano mais simples, com apenas um átomo de carbono por molécula.
A cadeia carbonada dos alcanos pode ser ramificada ou não ramificada, ocorrendo a ramificação apenas a partir do butano, C4H10.
Considere o alcano de cadeia ramificada, cuja fórmula de estrutura está representada na figura 3.
Seleccione a alternativa que corresponde ao nome deste alcano, de acordo com as regras da IUPAC.
(A) 3 – metil-heptano.
(B) 2,4 – dimetil-hexano.
(C) 2 – etil – 4 – metilpentano.
(D) 3 – etil – 1,1 – dimetilbutano.
- Opção (B)
- Opção (B)…………. 8 pontos
11. (TI – 26/05/2009) Um átomo de oxigénio ligado a dois átomos de hidrogénio forma uma molécula de água.
Justifique a seguinte afirmação: «a molécula de água tem geometria angular».
⇒ Na molécula H2O, o átomo central (átomo de O) está rodeado por quatro pares eletrónicos – dois ligantes (ligações O–H) e dois não ligantes.
⇒ A molécula H2O tem geometria angular porque os quatro pares eletrónicos da molécula tendem a afastar-se o mais possível no espaço.
⇒ Como dois destes pares eletrónicos são não ligantes, o ângulo da ligação H–O–H é menor do que 180° (é um pouco superior a 90°).
- A resposta deve conter os elementos seguintes:
⇒ Existência de dois pares electrónicos não ligantes no átomo de oxigénio.
⇒ As repulsões entre os pares electrónicos não ligantes e os pares electrónicos ligantes forçam as ligações O — H a formarem um ângulo (menor do que 180º).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
12. (2009 – 1ªF) O metano é um hidrocarboneto saturado, a partir do qual se formam, por substituição, vários compostos halogenados.
Qual é o nome do composto a seguir representado, de acordo com a nomenclatura IUPAC?
- Diclorofluorometano
- Diclorofluorometano …………. 5 pontos
13. (2009 – EE) Muitos dos refrigerantes que contêm cafeína são gaseificados por adição de CO2 (g), sob pressão.
13.1. Seleccione a única alternativa que permite obter uma afirmação correcta.
Na molécula de CO2, existem…
(A) duas ligações covalentes duplas.
(B) apenas dois pares de electrões não ligantes.
(C) apenas dois pares de electrões ligantes.
(D) duas ligações covalentes simples.
- Opção (A)…………. 5 pontos
- Geometria linear
⇒ Geometria linear, pois é a que apresenta os dois “pares” eletrónicos em torno do carbono o mais afastados possível e este átomo não contém pares eletrónicos não ligantes.
- Geometria linear …………. 5 pontos
14. (TI – 30/04/2010) O amoníaco é um composto molecular que se encontra em fase gasosa à temperatura e pressão ambientes.
Atendendo apenas à estequiometria do composto, a molécula NH3 poderia assumir uma geometria triangular plana.
No entanto, aquela molécula apresenta uma geometria piramidal trigonal.
Apresente uma explicação para o facto de a molécula de amoníaco adoptar uma geometria piramidal trigonal.
⇒ A geometria de uma molécula é aquela que conduz à máxima estabilidade do sistema molecular.
⇒ Segundo o método da repulsão dos pares eletrónicos de valência estes dispõem-se no espaço o mais afastados possível, de modo a conduzir às menores repulsões eletrónicas possíveis.
⇒ No caso da molécula NH3, os pares eletrónicos de valência que rodeiam o átomo central são três pares de eletrões ligantes, correspondentes às três ligações covalentes N – H e o par eletrónico não ligante localizado no azoto.
⇒ O maior afastamento possível destes quatro pares obtém-se quando eles se dispõem no espaço de modo, aproximadamente, tetraédrico, conferindo à molécula NH3 uma geometria piramidal trigonal.
- A resposta deve abordar os seguintes tópicos:
⇒ Na molécula NH3 existe um par de electrões de valência não ligante no átomo de azoto.
⇒ As repulsões que se estabelecem entre este par de electrões e os restantes três pares de electrões de valência ligantes forçam a molécula a assumir uma geometria piramidal trigonal.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
15. (2010 – 1ªF) O azoto (N) é um elemento químico essencial à vida, uma vez que entra na constituição de muitas moléculas biologicamente importantes.
O azoto molecular (N2) é um gás à temperatura e pressão ambientes, sendo o componente largamente maioritário da atmosfera terrestre.
15.1. Considere que a energia média de ligação N – N é igual a 193 kJ mol–1 e que, na molécula de azoto (N2), a ligação que se estabelece entre os átomos é uma ligação covalente tripla.
Seleccione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
A quebra das ligações triplas em 1 mol de moléculas de azoto, no estado gasoso, envolve a _______ de uma energia ________ a 193 kJ.
(A) libertação … inferior
(B) libertação … superior
(C) absorção … superior
(D) absorção … inferior
- Opção (C)
⇒ Quando se quebram ligações é absorvida energia e quando se formam ligações ela é libertada.
⇒ A energia envolvida em ligações triplas é maior do que nas ligações simples.
- Opção (C)…………. 5 pontos
15.2. Represente a molécula de azoto (N2), utilizando a notação de Lewis.
- :N ≡ N:
⇒ Forma-se uma ligação tripla, a partir dos electrões das orbitais 2p de cada átomo, ficando um par de electrões (das orbitais 2s) para cada um dos átomos.
- :N ≡ N: …………. 5 pontos