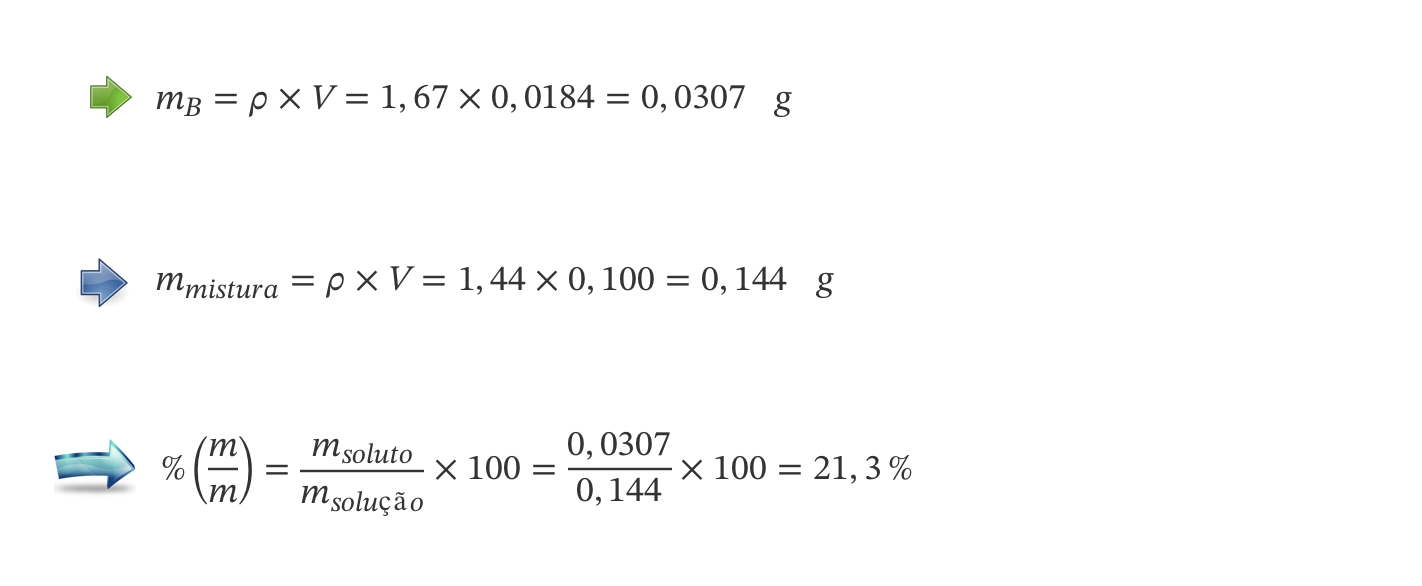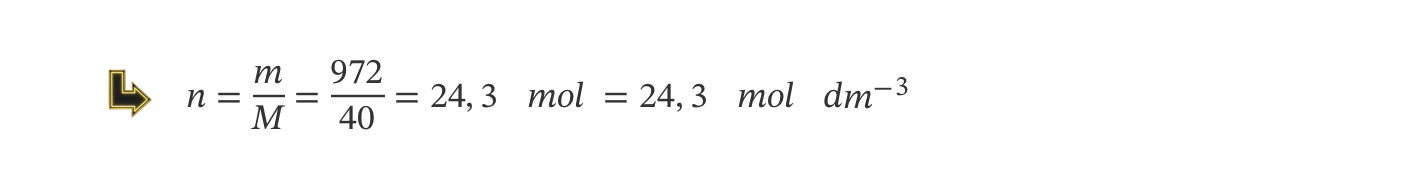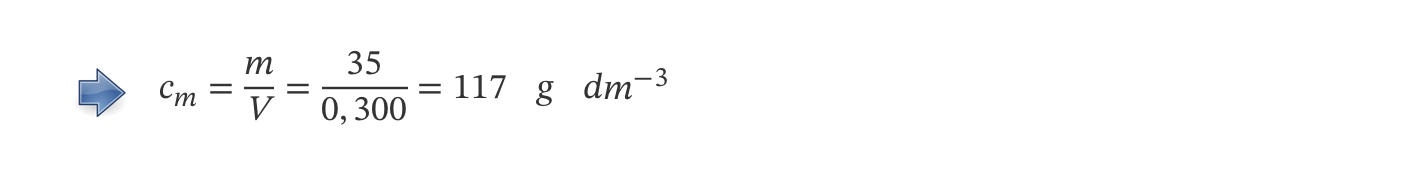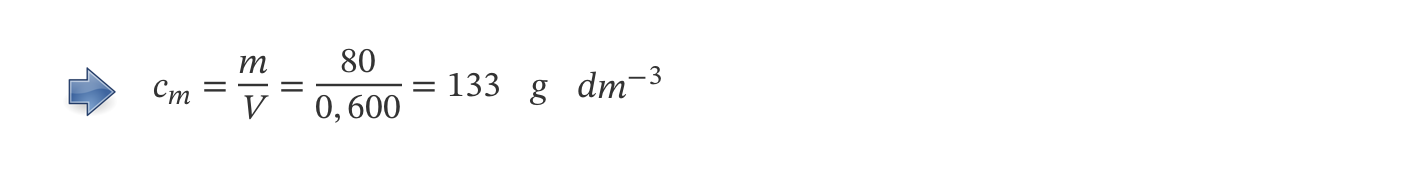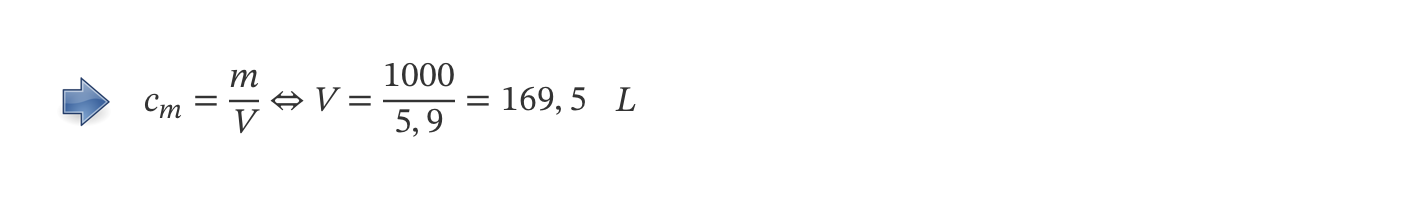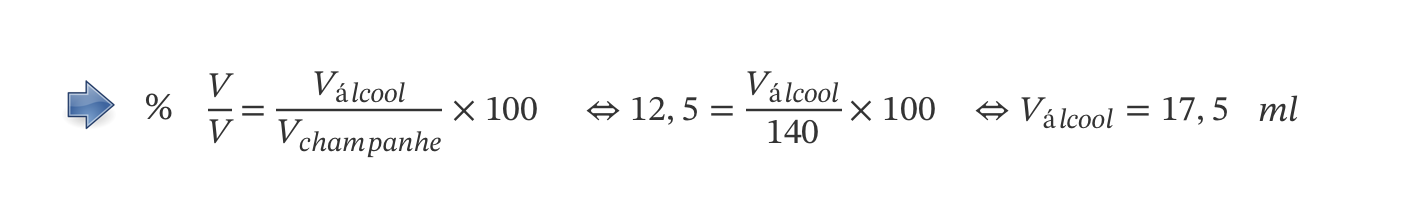Ficha nº6 – Composição quantitativa de soluções
Voltar a: 10ºAno – Química
Ficha nº6
Modos de exprimir a concentração de uma solução
1. Qual é a percentagem em massa de enxofre em 1 mole de moléculas de H2SO4?
2. Relativamente à informação contida no rótulo do vinho, podemos afirmar que …
(A) … existem 14,5 ml de álcool etílico por garrafa de 750 ml.
(B) … em cada litro de vinho existem 14,5 ml de álcool etílico.
(C) … nos 750 ml de vinho presente na garrafa existem 109 ml de álcool etílico.
(D) … em cada garrafa de vinho existem 100 ml de álcool etílico.
- Opção (C)
3. Destilou-se um volume de 650 ml de uma solução de KBr com concentração mássica de 48,0 g/L, recolhendo-se 250 ml de água.
Qual é a concentração mássica da solução que restou no balão de destilação, em unidades SI?
4*. Em termos médios a % V/V de CO2 na atmosfera é de 0,035 %.
Outra maneira de indicar essa concentração é em ppm (V) (partes por milhão em volume).
Selecione a alternativa que corresponde a essa concentração, expressa em ppm (V).
(A) 3,5 × 10-2
(B) 3,5 × 10-1
(C) 3,5 × 102
(D) 3,5 × 104
Teste Intermédio de Física e Química A do 10.º ano, 2008 (adaptado)
- Opção (C)
5. Calcula a concentração molar das seguintes soluções aquosas:
5.1 104,2 g de brometo de magnésio, MgBr2, em 650 ml de solução aquosa.
5.2 56,8 g de nitrato de cálcio, Ca(NO3)2, em 1,50 dm3 de solução aquosa.
5.3 68,5 g de sulfato de zinco, Zn2SO4, em 150 ml de solução aquosa.
6. Considera a tabela seguinte onde se indica a composição média dos principais componentes de uma mistura.
Considera que ρmistura = 1,44 g dm-3.
6.1. Calcula a percentagem em massa de B na mistura.
6.2. Determina o a quantidade de A na mistura.
7*. Indica a opção correta.
(A) A massa de uma solução é igual à soma da massa de soluto com a massa do solvente.
(B) O volume de uma solução é igual à soma do volume de soluto com o volume do solvente.
(C) O volume de uma solução é igual à soma da massa de soluto com o volume do solvente.
(D) A massa de uma solução é igual à soma da massa de soluto com o volume do solvente.
- Opção (A)
8. O nível máximo de chumbo permitido no sangue é de 180 mg dm-3.
Qual a opção equivalente à referida concentração.
(A) 180 ppm
(B) 0,75 mol L-1
(C) 4,2 x 10-7 mol L-1
(D) 4,2 x 10-4 mol L-1
- Opção (A)
9. Considera a informação contida na embalagem margarina.
9.1 O que significa a informação “70% (m/m) de lípidos” que consta no rótulo da embalagem de margarina?
9.2 Seleciona a opção que contém a expressão que permite calcular a massa de lípidos, em gramas, presente numa porção de 10 g de margarina.
9.1 Em cada 100 g de margarina existem 70 g de lípidos.
9.2 Opção (C)
10. 60 gramas de brometo de potássio (KBr) são dissolvidos em 54,0 g de água.
Calcula a fração molar deste composto em solução.
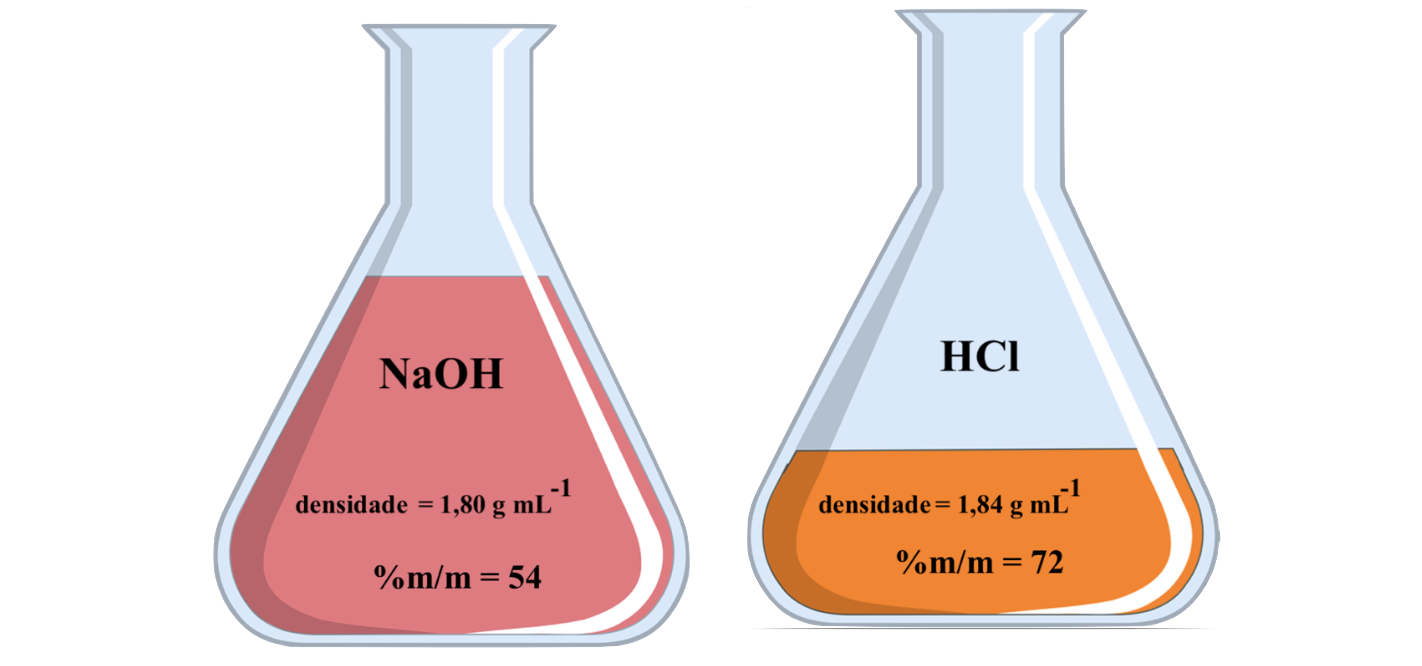
11. No laboratório de uma escola existem armazenados duas soluções, cujos rótulos têm as seguintes informações:
As concentrações destas soluções são, respetivamente, iguais a…
(A) … 12,5 e 14,4 mol dm-3
(B) … 14,3 e 12,5 mol dm-3
(C) … 2,43 e 3,63 mol dm-3
(D) … 24,3 e 36,3 mol dm-3
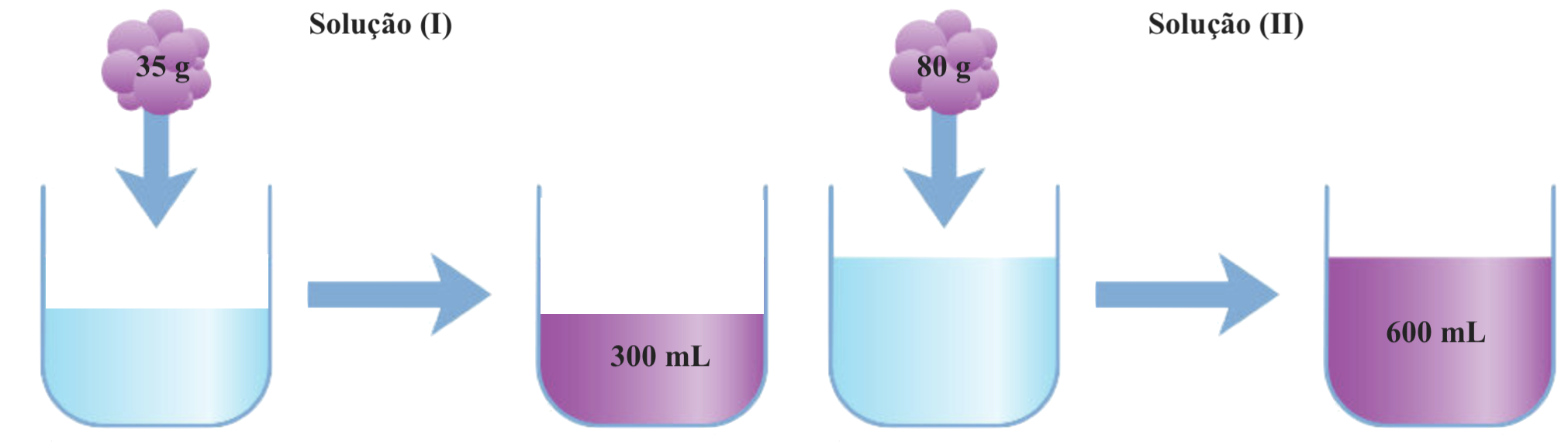
12. Preparam-se duas soluções, de dicromato de potássio, K2Cr2O7.
Qual destas soluções é a mais concentrada?
13. Considere um copo de leite em que o conteúdo de lactose C12H22O11 é 5,6% em volume e a densidade do leite é 1,040 g/mL.
13.1 Calcula a concentração molar da solução.
13.2 Determina a quantidade de matéria de lactose presente num copo de leite de 150 ml.
14. Uma amostra de água potável apresenta um teor em cálcio de 5,9 mg/dm3.
A ingestão oficial recomendada atualmente é de 1000 mg/dia para indivíduos entre os 19 e os 50 anos, 1200 mg/dia dos 50 anos em diante e 1300 mg/dia para gestantes e lactantes.
Determina o volume de água que é necessário beber para ingerir um indivíduo com 26 anos, para obter a dose recomendada de cálcio diária.
15. Sabendo-se que a concentração de NO, no sangue é de 0,050 mol/L, essa mesma concentração, em g L–1, é de:
(A) 1,67
(B) 1,67 x 10-3
(C) 2,0
(D) 1,5
- Opção (D)
16. Considera que uma pessoa ingere, durante a passagem de ano, um copo de champanhe de volume 140 ml.
16.1 Determina o volume de álcool etílico ingerido pela pessoa.
16.2 Sabendo que o álcool etílico possui uma massa volúmica, à temperatura ambiente, de 0,79 g/ml, determina a massa de álcool etílico presente no copo.
16.3 Calcula a percentagem, em massa, do álcool etílico no champanhe. Considera que a massa volúmica do champanhe é 0,97 g/ml.
17. Colocou-se uma solução aquosa de iodeto de magnésio, de concentração em massa 6 g dm-3, num frasco de 500 ml.
17.1 Relativamente à solução do frasco, indique qual das afirmações é a correta.
A. A solução tem 6 g de iodeto de magnésio.
B. A solução tem 3 g de iodeto de magnésio.
C. A solução tem 1 dm3 de iodeto de magnésio.
D. A solução tem 650 cm3 de iodeto de magnésio.
17.2 Retiraram-se 150 ml da solução do frasco e adicionou-se água até perfazer um volume de 500 ml, que se armazenou noutro frasco.
Indica, apresentando todos os cálculos, a concentração mássica da nova solução em g/dm3.
17.1 Opção (B)
Massa de iodeto de magnésio presente:
- m = Cm x V = 6 x 0,5 = 3 g
17.2
Massa de soluto em 150 ml (0,15 dm3):
- m = Cm x V= 6 x 0,15 = 0,90 g
O volume final é 0,5 dm3, logo a concentração mássica final é
- Cm = 0,90/0,5 = 1,8 g/dm3