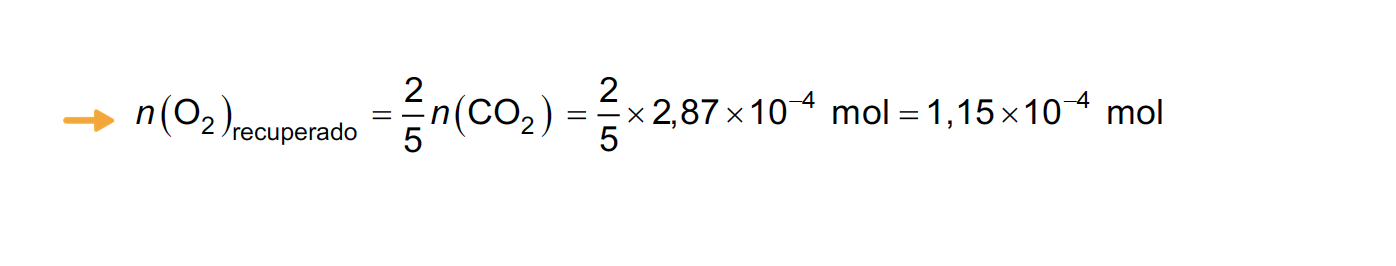Ficha nº7 : Exames e TI (2020 – 202*)
Voltar a: 10ºAno – Química
Ficha nº7
Exercícios de exames e testes intermédios (2020 – 202*)
10ºano – Química – Domínio 2 – Subdomínio 2 (Gases e dispersões)
1. (2021 – 1ªF) Dissolveu-se amoníaco, NH3 (g), em água, tendo-se obtido uma solução de concentração 2,27 mol dm-3 e de densidade 0,98 g cm-3 , a 25 ºC.
Determine o número de moléculas de água que existem em 250 cm3 de solução.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Como c = n/V , a quantidade de amoníaco existente em 250 cm3 da solução considerada é dada por:
- n = c x V = 2,27 mol dm−3 x 0,250 dm3 = 0,5675 mol
⇒ Como n = m/M, a massa de amoníaco em 250 cm3 da solução considerada será:
- m = n x M = 0,5675 mol x 17,04 g/mol = 9,670 g
⇒ Como ρsolução = m/V, a massa de 250 cm3 da solução considerada será:
- msolução = ρ x V = 0,98 x 250 cm3 = 245 g
⇒ A massa de água existente nos 250 cm3 da solução considerada será:
- m (H2O) = m (solução) − m (NH3) = 245 g − 9,670 g = 235,3 g
⇒ A quantidade de água existente nos 250 cm3 da solução é:
- n (H2O) = 235,3 /18,02 = 13,06 mol
⇒ Como o número de moléculas, N = n x NA , o número de moléculas de água nos 250 cm3 da solução considerada será:
- N = 13,06 x 6,02 x 1023 ⇔ N = 7,9 x 1024 moléculas
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a massa de amoníaco em 250 cm3 da solução considerada (9,670 g) ……. 2 pontos
⇒ Calcula a massa de água no volume da solução considerada (235,3 g) ……. 4 pontos
⇒ Calcula o número de moléculas de água que existem no volume da solução considerada (7,9 x 1024 moléculas) ……. 4 pontos
2. (2021 – 1ªF) Os componentes maioritários do ar são o nitrogénio, N2 (g), e o oxigénio, O2 (g).
Considere uma amostra de N2 (g) e uma amostra de O2 (g), com massas iguais.
Nas mesmas condições de pressão e de temperatura, pode concluir-se que os volumes das amostras são ______ e que o número de moléculas de cada uma das amostras é ______ .
(A) iguais … igual
(B) iguais … diferente
(C) diferentes … igual
(D) diferentes … diferente
- Opção (D)
⇒ Como as massas molares do nitrogénio, N2 (g) e do oxigénio, O2 (g) são diferentes e n = m/M, massas iguais das duas amostras contém quantidades de matéria diferentes.
⇒ Como, de acordo com a lei de Avogadro, nas mesmas condições de pressão e temperatura, os volumes são proporcionais as quantidades de matéria dos gases, sendo as quantidades de matéria diferentes, também os volumes das amostras são diferentes e o número de moléculas de cada uma das amostras é diferente.
- Opção (D) ……………. 10 pontos
3. (2021 – 2ªF) Considere que, na zona habitável da EEI, existem 4,1 x 10-2 mol de moléculas por cada dm3 de ar, sendo 7,0 x 10-3 a fração molar de CO2 .
Admita que se consegue recuperar uma quantidade de O2 igual a 2/5 da quantidade de CO2 .
Determine o volume de ar necessário para se conseguir recuperar 1,0 g de O2 .
Apresente todos os cálculos efetuados.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a quantidade de CO2 que existe por cada dm3 de ar (2,87 x 10-4 mol) …….. 3 pontos
⇒ Calcula a quantidade de O2 que se recupera por cada dm3 de ar (1,15 x 10-4 mol) …….. 3 pontos
⇒ Calcula o volume de ar necessário para se conseguir recuperar 1,0 g de O2 (2,7 x 102 dm3) …….. 4 pontos
ou
⇒ Calcula a quantidade de CO2 que permite recuperar 1,0 g de O2 (7,81 x 10-2 mol) …….. 3 pontos
⇒ Calcula a quantidade total de moléculas no ar necessária para se conseguir recuperar 1,0 g de O2 (11,2 mol) …….. 3 pontos
⇒ Calcula o volume de ar necessário para se conseguir recuperar 1,0 g de O2 (2,7 x 102 dm3) …….. 4 pontos
4. (2021 – EE) Os ácidos orgânicos apresentam um grupo funcional característico.
O ácido cítrico, C6H8O7 (M = 192,14 g mol-1), cuja fórmula de estrutura da molécula se representa na Figura 1, é uma substância presente nos citrinos.
Um sumo de limão, de massa volúmica 1,03 g cm-3, contém 4,71%, em massa, de ácido cítrico.
Determine a quantidade de ácido cítrico que existe em 75,0 cm3 desse sumo.
Apresente todos os cálculos efetuados.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a massa de ácido cítrico no sumo (3,638 g) …….. 6 pontos
⇒ Calcula a quantidade de ácido cítrico no sumo (1,89 x 10-2 mol) …….. 4 pontos
5. (2021 – EE) Em 1811, Amedeo Avogadro publicou um artigo em que admitia que volumes iguais de gases diferentes, nas mesmas condições de pressão e de temperatura, continham o mesmo número de moléculas.
Na Figura 8, representam-se quatro recipientes iguais (com o mesmo volume e a mesma massa).
Posteriormente, encheram-se estes recipientes com gases, identificados pelas respetivas fórmulas químicas, nas mesmas condições de pressão e de temperatura.
5.1. O número total de átomos contidos nos recipientes é igual em
(A) 1 e 2.
(B) 2 e 4.
(C) 2 e 3.
(D) 3 e 4.
- Opção (A)
⇒ De acordo com a Lei de Avogadro, se os quatro recipientes têm o mesmo volume (capacidade), nas mesmas condições de pressão e de temperatura, conterão igual número de moléculas dos gases com que foram enchidos, N.
Recipiente 4 : → Número de átomos de He (gás monoatómico) será N.
Recipiente 3 : → Número de átomos de CO2 (gás triatómico) será 3N.
Recipiente 2 : → Número de átomos de O2 (gás diatómico) será 2N.
Recipiente 1: → Número de átomos de N2 e O2 (gases diatómico) será 2N.
- Opção (A) ……………. 10 pontos
5.2. Selecione a opção que ordena os recipientes 1, 2 e 3, tendo em conta os respetivos gases, por ordem crescente das suas massas.
(A) 2 < 3 < 1
(B) 1 < 2 < 3
(C) 1 < 3 < 2
(D) 2 < 1 < 3
- Opção (B)
⇒ Se os quatro recipientes têm o mesmo volume (capacidade), nas mesmas condições de pressão e de temperatura, conterão quantidades iguais dos gases com que foram enchidos, n.
⇒ A massa de gás contido em cada um dos recipientes será:
- n = m/M
Recipiente 4 : (He) m4 = n x 4,00 = n x 4,0 g
Recipiente 3 : (CO2) m3 = n x 44,01 = n x 44,01 g
Recipiente 2 : (O2) m4 = n x 32,00 = n x 32,00 g
Recipiente 1: (N2 e O2) n x 28,02 < m1 < n x 32,00
⇒ Assim, m1 < m2 < m3
- Opção (B) ……………. 10 pontos
6. (2022 – 1ªF) Um navio transporta metano, CH4 (M = 16,05 g mol-1), acondicionado em tanques.
Um tanque na sua capacidade máxima contém 1,17 x 105 kg de CH4 liquefeito. O CH4 liquefeito tem massa volúmica de 0,4241 g cm-3.
Calcule a massa máxima de CH4 que seria possível transportar num tanque, caso esta substância se encontrasse no estado gasoso, em condições PTN.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Este item pode ser resolvido por, pelo menos, dois processos.
- 1.º Processo
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula o volume do tanque (2,759 x 105 dm3) …….. 4 pontos
⇒ Calcula a massa de CH4, em condições PTN, que será possível transportar no tanque (1,98 x 105 g) …….. 6 pontos
- 2.º Processo
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Deduz a expressão:
- (ou equivalente) …….. 6 pontos
⇒ Calcula a massa de CH4, em condições PTN, que será possível transportar no tanque (1,98 x 105 g) …….. 4 pontos
7. (2022 – EE) No âmbito da agricultura inteligente (ou smart farming), aposta-se na hidroponia, uma técnica de cultivo de espécies vegetais que não necessita de solo e em que se usam ferramentas tecnológicas.
Esta forma de cultivo mais sustentável pode ser implantada em meio urbano, permite economizar água e reforça a segurança alimentar.
Nesta técnica, utilizam-se estações hidropónicas constituídas por várias unidades.
Uma determinada unidade hidropónica beneficia de um enriquecimento do ar em dióxido de carbono, CO2 , para valores de 800 ppm (em volume). A percentagem de referência de CO2 no ar é 0,038% (em volume).
Admita que o volume de ar da unidade hidropónica é 3,0 dm3 e que, nas condições de pressão e temperatura desta unidade, o volume molar é 24,0 dm3 mol-1.
Calcule o aumento da quantidade de CO2 , na unidade hidropónica, caso se proceda ao referido enriquecimento do ar em CO2 , nas condições de pressão e temperatura indicadas.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Este item pode ser resolvido por, pelo menos, dois processos.
- 1.º Processo
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula o volume de CO2 nas condições de referência (3,80 x 10-4 dm3 em 1 dm3 de ar OU 1,14 x 10-3 dm3 em 3 dm3 de ar) (ver nota 1) …….. 3 pontos
⇒ Calcula a quantidade de CO2 no ar enriquecido (8,00 x 10-4 dm3 em 1 dm3 de ar OU 2,40 x 10-3 dm3 em 3 dm3 de ar) (ver nota 1) …….. 3 pontos
⇒ Calcula o aumento da quantidade de CO2 (5,3 x 10-5 mol) (ver nota 2) ……… 4 pontos
- 2.º Processo
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a quantidade de CO2 nas condições de referência (1,58 x 10-5 mol em 1 dm3 de ar OU 4,75 x 10-5 mol em 3 dm3 de ar) (ver notas 1 e 2) …….. 3 pontos
⇒ Calcula a quantidade de CO2 no ar enriquecido (3,33 x 10-5 mol em 1 dm3 de ar OU 1,00 x 10-4 mol em 3 dm3 de ar) (ver notas 1 e 2) …….. 3 pontos
⇒ Calcula o aumento da quantidade de CO2 (5,3 x 10-5 mol) (ver nota 2) ……… 4 pontos
Notas:
1. A ordem das duas primeiras etapas é arbitrária.
2. No caso de ser utilizado um volume molar em condições PTN, considera-se um erro de tipo 2.