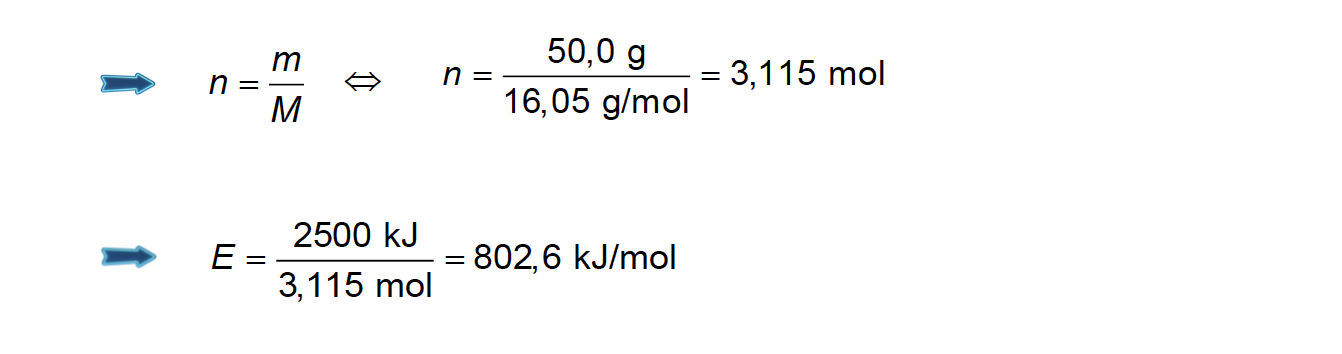Ficha nº2 : Exames e TI (2013 – 202*)
Voltar a: 10ºAno – Química
Ficha nº2
Exercícios de exames e testes intermédios (2013 – 202*)
10ºano – Química – Domínio 2 – Subdomínio 3 (Transformações químicas)
1. (2013 – EE) A combustão completa do metano pode ser representada por
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (g) ΔH = -802 kJ mol -1
Calcule a energia libertada quando, por combustão completa de metano, se consomem 2,0 m3 de oxigénio, em condições normais de pressão e de temperatura.
Apresente todas as etapas de resolução.
A equação química mostra que se consomem duas moles de dioxigénio quando se dá a combustão de uma mole de metano.
ΔH = – 802 kJ / mol de reação = – 802 kJ / mol de CH4 = – 802 kJ / 2 mol de O2
Por cada mole de O2 consumido libertam-se 401 kJ.
A quantidade de O2 existente em 2,0 m3 desse gás pode calcular-se a partir do volume molar, dado que n (O2) = V/Vm.
Como, em condições normais de pressão e temperatura Vm = 22,4 dm3 mol-1, vem:
A quantidade de calor libertado, Q, por reação desta quantidade de oxigénio calcula-se a partir da variação de entalpia:
- Q = n (O2) x ΔH = 89,3 mol x (- 401 kJ mol-1) = – 3,6 x 104 kJ
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Determinação da quantidade de oxigénio existente em 2,0 m3 desse gás, em condições normais de pressão e de temperatura (n = 89,3 mol).
B) Determinação da energia libertada por reação dessa quantidade de oxigénio (E = 3,6 x 104 kJ)
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
2. (2013 – EE) Os átomos de cloro são agentes destruidores da camada de ozono estratosférico.
Um mecanismo reacional que traduz a destruição do ozono pode ser representado pelas seguintes equações:
Cl + O3 → ClO + O2
ClO + O → Cl + O2
Escreva a equação que corresponde à soma destas duas equações.
- O (g) + O3 (g) → O2 (g)
- O (g) + O3 (g) → O2 (g) …………. 5 pontos
3. (2014 – 1ªF) A reação de síntese do amoníaco pode ser traduzida por
N2 (g) + 3 H2 (g) ⇋ 2 NH3 (g) ΔH = -92 kJ mol-1
Na reação de síntese do NH3 (g) considerada
(A) libertam-se 92 kJ por cada mole de NH3 (g) que se forma.
(B) libertam-se 92 kJ por cada duas moles de NH3 (g) que se formam.
(C) são absorvidos 92 kJ por cada mole de NH3 (g) que se forma.
(D) são absorvidos 92 kJ por cada duas moles de NH3 (g) que se formam.
- Opção (B)
⇒ A reação de síntese do amoníaco apresenta uma variação de entalpia negativa, o que significa haver libertação de energia.
⇒ O coeficiente estequiométrico do amoníaco, NH3, na equação química indica que é por cada duas moles de NH3 formadas.
- Opção (B) …………. 5 pontos
4. (2015 – EE) Na estratosfera, ocorrem, simultaneamente, reações que conduzem à formação do ozono e outras que conduzem à sua destruição.
Uma das reações que conduzem à formação do ozono ocorre entre as moléculas de oxigénio e os radicais livres de oxigénio.
4.1.Escreva a equação química que traduz essa reação.
- O2 (g) + O (g) → O3 (g)
- O2 (g) + O (g) → O3 (g) …………. 5 pontos
Notas:
A omissão da indicação do(s) estado(s) físico(s) de uma ou mais espécies não implica qualquer desvalorização.
A apresentação de ⇋ (em vez de →) não implica qualquer desvalorização.
4.2. Considere que por cada mole de O3 (g) que se forma se libertam cerca de 105 kJ.
A energia, em joule, que se liberta quando, através da reação referida, se forma uma molécula de ozono é
(A) 1,74 x 10-22 J
(B) 6,32 x 1028 J
(C) 1,74 x 10-19 J
(D) 6,32 x 1025 J
- Opção (C)…………. 5 pontos
4.3.Os radicais livres originados pela rutura de ligações nos CFC, por ação da radiação ultravioleta, catalisam algumas das reações que conduzem à destruição do ozono.
Conclua, justificando, qual das ligações, C – Cl ou C – F, sofrerá mais facilmente rutura.
⇒Os elementos flúor e cloro localizam-se no mesmo grupo da Tabela Periódica, grupo 17, e nos períodos 2 e 3, respetivamente, ou seja, o flúor antecede o cloro no mesmo grupo da TP.
⇒Como o raio atómico aumenta ao longo do grupo, o raio atómico do cloro é superior ao raio atómico do flúor.
⇒O comprimento de ligação C-Cl é maior do que o comprimento de ligação C-F.
⇒As diferenças nas energias de ligação resultam fundamentalmente dos diferentes comprimentos de ligação dos átomos ligados.
⇒ Menores comprimentos de ligação conduzem a ligações mais fortes, pelo que a energia de ligação C-Cl é menor que a energia de ligação C-F.
⇒Será necessário mais energia para romper a ligação C-F do que para romper a ligação C-Cl.
- A ligação C-Cl sofre mais facilmente rutura.
- A resposta integra os tópicos de referência seguintes ou outros de conteúdo equivalente:
A)O raio atómico do cloro é superior ao raio atómico do flúor, pelo que o comprimento da ligação C – Cl será maior do que o comprimento da ligação C – F.
B)Assim, será necessária mais energia para romper a ligação C – F do que para romper a ligação C – Cl, pelo que a ligação C – Cl sofrerá mais facilmente rutura.
5. (2017 – 2ªF) A energia, transferida como calor, necessária para dissociar 1 mol de moléculas de N2 (g), a pressão constante, é 945 kJ.
A variação de entalpia associada à obtenção de 4 mol de átomos de nitrogénio, em fase gasosa, a partir de 2 mol de N2 (g) é
(A) + (4 x 945) kJ
(B) – (4 x 945) kJ
(C) + (2 x 945) kJ
(D) – (2 x 945) kJ
- Opção (C)
⇒ Por convenção considera-se positiva a energia recebida.
⇒ Para a obtenção de 2 mol de átomos, por decomposição da molécula, tem-se
- N2 (g) → 2 N (g); ΔH = + 945 kJ
⇒ Para 4 mol de átomos são +2 × 945 kJ
- Opção (C) ……………. 5 pontos
6. (2017 – EE) O iodo, I2 (g), reage com o hidrogénio, H2 (g), em fase gasosa, formando-se iodeto de hidrogénio, HI (g).
A reação pode ser traduzida por
I2 (g) + H2 (g) ⇋ 2 HI (g)
Nesta reação, a variação de entalpia associada à formação de 2 mol de HI ( g ) é -9,2 kJ.A energia de ligação em H2 (H-H) é 436,4 kJ mol-1 e a energia de ligação em HI (H-I) é 298,3 kJ mol-1.
Qual é a energia que se liberta quando se forma 1 mol de ligações I-I em I2 ?
(A) 307,5 kJ
(B) 151,0 kJ
(C) 169,4 kJ
(D) 147,3 kJ
- Opção (B)
⇒ Na reação em causa, a variação de entalpia associada à formação de 2 mol de HI (g) é – 9,2 kJ.
⇒ Este valor é o “saldo energético” da energia absorvida para partir todas as ligações covalentes nas moléculas dos reagentes e da energia libertada na formação das ligações covalentes nas moléculas dos produtos da reação, ou seja:
- – 9,2 kJ = [+ Elig (H2) x 1 mol + Elig (I2) x 1 mol] – [ Elig (HI) x 2 mol ] ⇔
⇔ – 9,2 = [ + 436,4 x 1 + Elig (I2) x 1 ] – [ 298,3 x 2 ]
⇔ Elig (I2) = 151,0 kJ mol-1
⇒ A energia que se liberta quando se forma 1 mol de ligações I − I em I2 é 151,0 kJ
- Opção (B) ……………. 5 pontos
7. (2018 – EE) Um dos seis elementos mais abundantes, em massa, no corpo humano é o oxigénio (O), existindo cerca de 46 kg desse elemento numa pessoa de massa 70 kg.
Desses seis elementos mais abundantes, o fósforo (P) foi o único cuja descoberta resultou de experiências com um fluido fisiológico humano.
No corpo humano, os átomos de oxigénio estão maioritariamente ligados a átomos de hidrogénio, formando moléculas de água.
A água pode ser decomposta em hidrogénio e oxigénio, de acordo com
2 H2O (g) → 2 H2 (g) + O2 (g)
A variação de energia associada à decomposição de 2 mol de H2O (g), segundo a reação considerada, é 572 kJ.
As energias das ligações H-H e O=O são, respetivamente, 436 kJ mol-1 e 498 kJ mol-1.
Determine a energia que é necessário fornecer, em média, para quebrar uma mole de ligações O-H na molécula de água.
Apresente todas as etapas de resolução.
⇒ A energia necessária para quebrar as ligações O – H em duas mol de moléculas de H2O é
- Equebra = 4 x Eligação ( O – H)
⇒ A energia libertada na formação das ligações H – H e O = O é dada por
- Eformação = 2 x Eligação (H – H) + Eligação (O = O) ⇔ Eformação = 2 x 436 kJ + 1 x 498 = 1370 kJ
⇒ A variação de energia, ΔE, associada à decomposição de duas mol de H2O (g) é a diferença entre a energia absorvida, Equebra, e a energia libertada, Eformação:
- ΔE = Equebra – Eformação ⇔ 572 = 4 x Eligação (O – H) – 1370 ⇔ Eligação (O – H) = 486 kJ
⇒ É necessário fornecer , em média , a energia de 486 kJ para quebrar uma mole de ligações O – H na molécula de água.
- Etapas de resolução:
⇒ Determinação da energia libertada na formação de duas moles de ligações H-H e de uma mole de ligações O=O (E = 1370 kJ) (ver nota 1) …….. 4 pontos
⇒ Determinação da energia que é necessário fornecer, em média, para quebrar uma mole de ligações O-H na molécula de água (E = 486 kJ) (ver nota 2) …….. 6 pontos
Notas:
1. A consideração de uma estequiometria incorreta implica que a resposta seja classificada com zero pontos.
2. A utilização de sinais algébricos incorretos implica que a etapa seja pontuada com zero pontos.
8. (2020 – 2ªF) A água, presente nos estados sólido, líquido e gasoso na atmosfera terrestre, é uma substância peculiar, pois as propriedades que a caracterizam, como a variação de entalpia de vaporização e a capacidade térmica mássica, apresentam valores muito diferentes dos que seriam expectáveis.
A condensação de vapor de água envolve de energia, uma vez que ocorre com de ligações intermoleculares.(A) libertação … formação
(B) libertação … quebra
(C) absorção … formação
(D) absorção … quebra
- Opção (A)
⇒ Condensação é uma transformação física em que ocorre a passagem do estado físico gasoso para o estado físico líquido.
⇒ Como na passagem de vapor de água ao estado líquido ocorre a formação de ligações intermoleculares, particularmente ligações de hidrogénio, as opções B e D não são corretas.
- A formação de ligações envolve libertação de energia (ΔH < 0).
ou
⇒ A água condensa ao passar do estado gasoso ao estado líquido. Nessa transformação estabelecem-se ligações entre moléculas de água, por isso há libertação de energia.
- Opção (A) ……………. 10 pontos
9. (2020 – EE) A energia média da ligação C – C é 347 kJ mol-1.
No estabelecimento de uma ligação C – C é, em média,
(A) libertada uma energia de 5,76 x 10-19 J.
(B) absorvida uma energia de 5,76 x 10-19 J.
(C) absorvida uma energia de 5,76 x 10-22 J.
(D) libertada uma energia de 5,76 x 10-22 J.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (A)
⇒ A energia média de ligação é a energia que é absorvida, em média, por cada mole de ligações quebradas.
⇒ Como a energia libertada na formação de uma ligação é igual à energia absorvida na quebra dessa ligação, conclui-se que quando se forma uma ligação C-C é libertada, em média, uma energia de
- Opção (A) ……………. 10 pontos
10. (2021 – 1ªF) O pentacloreto de fósforo, PCl5, pode decompor-se, em fase gasosa, originando tricloreto de fósforo, PCl3 , e cloro, Cl2.
Esta reação pode ser traduzida por
PCl5 (g) ⇋ PCl3 (g) + Cl2 (g)
Considere que a variação de entalpia associada à decomposição de 1 mol de PCl5 (g) é 88 kJ.
A energia média da ligação P – Cl na molécula PCl5 é 257 kJ mol-1, e a energia média da ligação Cl – Cl na molécula Cl2 é 243 kJ mol-1 .
Conclua, a partir das energias fornecidas, se a ligação P – Cl é, em média, mais forte na molécula PCl5 ou na molécula PCl3 .
Mostre como chegou à conclusão solicitada, apresentando todos os cálculos.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Como é necessário fornecer energia para ocorrer a decomposição, em fase gasosa, do pentacloreto de fósforo, PCℓ5 , a reação é endotérmica. Por isso, ΔH > 0 .
Para calcular a energia da ligação P − Cℓ na molécula PCℓ3, pode fazer-se o balanço entre a energia posta em jogo na decomposição do PCℓ5 , ΔHr, a energia absorvida na rutura de ligações e a energia libertada na formação das novas ligações.
⇒ Energias envolvidas:
Seja x kJ/mol a energia de ligação P − Cℓ em PCℓ3
Variação de entalpia associada à reação de decomposição de
- 1 mol de PCℓ5 (g) : ΔHr = + 88 kJ/mol
Energia absorvida na dissociação de uma mol de ligações
- P − Cℓ em PCℓ5 = 257 kJ/mol
Energia libertada na formação de uma mol de ligações
- Cℓ − Cℓ = 243 kJ/mol
⇒ Nas ligações que se partem e que se formam, atendendo a que, por convenção, a energia absorvida pelo sistema é positiva e a energia libertada é negativa.
Energia absorvida para romper ligações nas moléculas reagentes:
- 5 x 257 = 1285 kJ/mol
Energia libertada ao formar ligações nas moléculas resultantes:
- − (3 x + 243) kJ/mol
⇒ Balanço energético:
- 1285 − (3 x + 243) = 88 ⇔ 1285 − 88 = 3 x + 243 ⇔ 954 = 3 x ⇔ x = 318 kJ/mol
Como 318 kJ/mol > 257 kJ/mol ⇔ Elig P − Cℓ em PCℓ3 > Elig P − Cℓ em PCℓ5 .
⇒ Como quanto maior for a energia de ligação mais forte é a ligação, a ligação P − Cℓ em PCℓ3 é mais forte do que em PCℓ5 .
- Elementos de resposta:
⇒ cálculo da energia da ligação P – Cl na molécula PCl3 com base na diferença entre a energia envolvida na rutura de ligações químicas e a energia envolvida na formação de ligações químicas (318 kJ mol-1);
⇒ identificação da ligação mais forte com base na associação entre uma maior energia de ligação e uma ligação mais forte (P – Cl na molécula PCl3).
11. (2021 – EE) A combustão do metano pode ser traduzida por
CH4 (g) + 2 O2 (g) → CO2 ( g ) + 2 H2O (g)
A energia libertada na combustão de 50,0 g de CH4 é 2500 kJ.
Considere as energias de ligação médias apresentadas na tabela.
Determine, em kJ mol-1, a energia média de dissociação da molécula de O2 .
Apresente todos os cálculos efetuados.
⇒ Calculo da variação de entalpia associada à reação de combustão do metano:
⇒ A energia libertada ou absorvida numa reação química resulta de um balanço entre a energia absorvida na rutura das ligações entre os átomos dos reagentes e a energia libertada na formação das novas ligações. Por convenção, a energia absorvida pelo sistema é positiva e a energia libertada é negativa.
⇒ Para determinar a energia de dissociação da molécula de O2, pode recorrer-se a este balanço energético:
- A energia de dissociação é numericamente igual à energia de ligação, Ediss (O = O) = 490 kJ/mol, ou seja, a energia necessária para dissociar de é 1 mol de O2 é 490 kJ.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a energia que se liberta na combustão de 1 mol de CH4 (802,6 kJ) …….. 4 pontos
⇒ Calcula a energia envolvida na formação das ligações de 1 mol de CO2 e de 2 mol de H2O (3438 kJ)…….. 3 pontos
⇒ Calcula a energia necessária para dissociar 1 mol de O2 (490 kJ) …….. 3 pontos
12. (2022 – 1ªF) A reação do CH4 com o dioxigénio, O2 , em fase gasosa, é traduzida por
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (g) ΔH = -890 kJ
Na reação completa do CH4 proveniente do tanque do navio de transporte, são
(A) libertados 6,49 x 1012 J de energia.
(B) libertados 8,90 x 105 J de energia.
(C) consumidos 8,90 x 105 J de energia.
(D) consumidos 6,49 x 1012 J de energia.
- Opção (A)
⇒ Determinação da quantidade de matéria de CH4:
⇒ Classificação da reação do ponto de vista energético:
- ΔH <0 ⇒ a reação é exotérmica. Logo, há libertação de energia.
⇒ Cálculo da energia libertada:
Nota: O calculo refere-se à reação completa da massa referente ao tanque do navio transportando o máximo volume possível, ou seja, na sua capacidade.
- Opção (A) ……………. 10 pontos