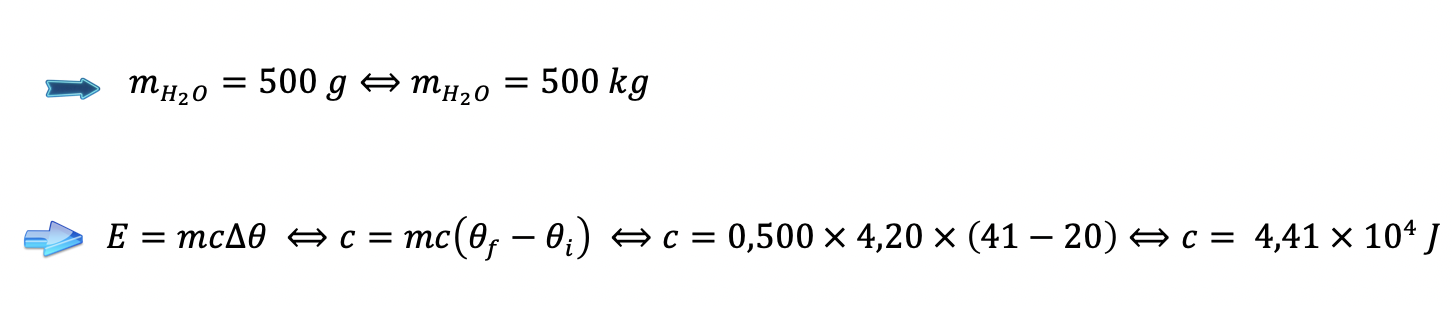Voltar a: 10ºAno – Física
Ficha nº4
Exercícios de exames e testes intermédios (2013 – 2015)
10ºano – Física – Subdomínio 3 (Energia, fenómenos térmicos e radiação)
1. (2013 – 2ªF) Nos finais do século XVIII, elevaram-se na atmosfera os primeiros balões, do tipo representado na Figura 1.
A história destes balões foi contada por Rómulo de Carvalho no livro História dos Balões (Atlântida, 1959).
Para fazer subir o primeiro balão, de volume aproximado 800 m3, «os inventores colocaram na boca do balão uma grelha de ferro, sobre a qual dispuseram palha e pedaços de lã, […] aos quais lançaram fogo», o que permitiu aquecer gradualmente o ar nele contido.
Identifique o principal processo de transferência de energia, como calor, que permite o aquecimento de todo o ar contido no balão e descreva o modo como essa transferência ocorre.
⇒ O principal mecanismo de transferência de energia, como calor, que permite o aquecimento de todo o ar é a convecção.
⇒ O ar que se encontra junto ao fogo aquece, tornando-se menos denso, o que dá origem a uma corrente quente ascendente.
⇒ Este ar, ao subir, arrefece, ao transferir energia para o ar que encontra, tornando-se assim mais denso, o que irá originar uma corrente descendente de ar mais frio.
⇒ As correntes quentes ascendentes e as correntes frias descendentes, repetindo-se, em simultâneo, ao longo do tempo, permitem o aquecimento de todo o ar.
- Na resposta, são apresentados os seguintes tópicos:
A) O principal processo de transferência de energia [, como calor, que permite o aquecimento de todo o ar contido no balão] é a convecção.
B) O ar que se encontra na base do balão aquece, tornando-se menos denso, o que dá origem a uma corrente quente ascendente. [Simultaneamente,] o ar mais frio no topo do balão desce por ser mais denso, o que dá origem a uma corrente fria descendente.
C) As correntes quentes ascendentes e as correntes frias descendentes, repetindo-se, [em simultâneo,] ao longo do tempo, permitem o aquecimento de todo o ar contido no balão.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
2. (2013 – EE) Qual é a relação entre a potência da radiação absorvida pelo planeta Terra e a potência da radiação emitida pelo planeta Terra para o espaço?
Como a Terra está em equilíbrio térmico, então a potência da radiação solar que absorve é igual à potência da radiação que emite para o Espaço.
- A potência da radiação absorvida [pelo planeta Terra] é igual à potência da radiação emitida [pelo planeta Terra para o espaço]. …………. 5 pontos
3. (2013 – EE) Na tabela seguinte, estão registadas as elevações de temperatura, Δϴ, do bloco de chumbo, de massa 3,2 kg, em função da energia, E, que lhe é fornecida.
Determine a capacidade térmica mássica do chumbo.
Comece por apresentar a equação da reta que melhor se ajusta ao conjunto de valores apresentados na tabela, referente ao gráfico da elevação de temperatura do bloco de chumbo, em função da energia que lhe é fornecida (utilize a calculadora gráfica).
Apresente todas as etapas de resolução.
- m = 3,2 kg
- c = ?
A expressão que relaciona a energia fornecida ao bloco de chumbo, em função da elevação da sua temperatura, é:
E = m c Δθ
então, a equação da reta que traduz Δθ = f (E) é:
o declive da reta:
Assim, recorrendo à calculadora gráfica, Δθ = f (E), é:
- Δθ = 2,46 x 10-3 E (SI)
Donde se conclui que:
A capacidade térmica mássica do chumbo é de cerca de 1,3 x 102 J kg-1 °C-1.
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Apresentação da equação da reta que melhor se ajusta ao conjunto de valores apresentados na tabela, referente ao gráfico da elevação da temperatura do bloco de chumbo, em função da energia que lhe é fornecida (Δθ = 2,46 x 10-3 E ou y = 2,46 x 10-3 x).
B) Cálculo da capacidade térmica mássica do chumbo, a partir do declive da reta obtida (c = 1,3 x 102 J kg-1 ºC-1).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
4. (TI – 12/02/2014) A água é uma substância vital para qualquer organismo vivo. Mas é também uma substância extraordinária, pois as propriedades que a caracterizam apresentam valores, em geral, muito diferentes dos que seriam de esperar.
Consideremos, por exemplo, o calor de vaporização da água. Verifica-se que é relativamente elevado, o que é bom, porque, assim, a água constitui um meio eficiente de arrefecimento do nosso corpo, por evaporação, quando transpiramos. Mas quão elevado é o calor de vaporização da água? Se aquecermos uma determinada massa de água, inicialmente a 0 ºC, poderá demorar, por exemplo, 5 minutos a atingir o ponto de ebulição. Se continuarmos a fornecer energia, à mesma taxa temporal, a essa mesma massa de água, demorará cerca de 20 minutos até que toda a água se vaporize completamente. Isto significa que vaporizar uma determinada massa de água consome cerca de quatro vezes mais energia do que aquecer a mesma massa de água de 0 ºC até 100 ºC, para o que apenas(!) são necessários 420 kJ por quilograma de água.
L. J. F. Hermans, Europhysics News, 43 (2), 13 (2012) (traduzido e adaptado)
4.1. Indique, com dois algarismos significativos, o calor (ou variação de entalpia) de vaporização da água, a partir da informação dada no texto.
- ΔHvap (H2O) = 420 × 4 = 1,69 × 103 = 1,7 × 103 kJ kg−1
⇒ Tendo em consideração a informação dada no texto o calor (ou variação de entalpia) de vaporização da água, é 1,7×103 kJ kg−1.
- 1,7 x 103 Kj kg-1 ou equivalente …………. 8 pontos
4.2. Utilizou-se uma resistência de aquecimento, com uma potência de 250W, para aquecer uma amostra de água de massa 500 g, inicialmente a 20 ºC. Verificou-se que, ao fim de 5,0 min de aquecimento, a temperatura da amostra era 41 ºC.
Determine o rendimento do processo de aquecimento da amostra de água.
Utilize o valor da capacidade térmica mássica da água que pode ser determinado a partir da informação dada no texto.
Apresente todas as etapas de resolução.
⇒ Determinar a capacidade térmica mássica da água a partir da informação do texto.
- Para aquecer um quilograma de água de 0 ºC até 100 ºC, são necessários 420 kJ.
⇒ Determinar a energia transferida para a amostra de água durante o aquecimento
⇒ Determinar energia utilizada para aquecer a amostra de água
⇒ Determinar o rendimento do processo de aquecimento da amostra de água
- O rendimento do processo de aquecimento da amostra de água foi de 58,8%.
- Na resposta, devem ser apresentadas as seguintes etapas:
A) Cálculo da energia transferida para a amostra de água durante o aquecimento (E = 7,50 × 104 J) …….. 6 pontos
B) Cálculo da energia utilizada para aquecer a amostra de água (E = 4,41 × 104 J) (ver nota) …….. 5 pontos
C) Cálculo do rendimento do processo de aquecimento da amostra de água (59%) …….. 5 pontos
Nota – A utilização de um valor de capacidade térmica mássica da água diferente de 4,20 × 103 J kg-1 ºC-1 implica que esta etapa seja pontuada com zero pontos.
5. (2014 – 1ªF) O alumínio é um metal que tem diversas aplicações tecnológicas.
Na tabela seguinte, estão registados os valores de algumas propriedades físicas do alumínio.
Considere que uma barra de alumínio, de massa 700 g e, inicialmente, a 25,0 °C, é aquecida.
5.1. Que energia é necessário fornecer à barra, para que a sua temperatura aumente de 25,0 °C para 27,0 °C?
- Opção (B)
⇒ Recorrer à expressão E = m c ΔT para calcular a energia que é necessário fornecer à barra de alumínio, para que a sua temperatura aumente de 25,0 ºC para 27,0 ºC.
- mbarra de Al = 700 g ⇔ mbarra de Al = 0,700 kg
⇒ Ao substituir o valor da massa da barra de alumínio na expressão, E = m c ΔT, esta deve expressa estar em kg devido às unidades da capacidade térmica mássica.
- E = m c ΔT ⇔ E = m c (Tfinal−Tinicial) ⇔ E = 0,700 × 897 × (27,0 – 25,0) ⇔ E = 0,700 × 897 × (2,0) ⇔ E = (1,4 × 897) J
- Opção (B) …………. 5 pontos
5.2. Admita que é transferida energia para a barra de alumínio considerada a uma taxa temporal constante de 1,1 kW.
Determine o tempo que a barra demora a fundir completamente, a partir do instante em que atinge a temperatura de 660 °C, admitindo que a totalidade da energia transferida contribui para o aumento da energia interna da barra.
Apresente todas as etapas de resolução.
- Etapas de resolução:
A) Cálculo da energia que é necessário transferir para a barra de alumínio, à temperatura de 660 ºC, para esta fundir completamente (E = 2,80 × 105 J) …….. 5 pontos
B) Cálculo do tempo que a barra demora a fundir completamente (Δt = 2,5 × 102 s) …….. 5 pontos
6. (2014 – 2ªF) Com o objetivo de estabelecer o balanço energético de um sistema gelo + água líquida, um grupo de alunos realizou uma experiência, na qual adicionou 30,0 g de gelo fragmentado, à temperatura de 0,0 ºC, a 260,0 g de água líquida, a 20,0 ºC.
Os alunos consultaram tabelas de constantes físicas e registaram os seguintes valores:
- cágua líquida (capacidade térmica mássica da água líquida) = 4,18 × 103 J kg-1 ºC-1
- ΔHfusão gelo (variação de entalpia (ou calor) de fusão do gelo) = 3,34 × 105 J kg-1
6.1. Identifique a fonte e o recetor, quando se inicia o processo de transferência de energia que ocorre no interior do sistema considerado.
⇒ Quando se inicia o processo de transferência de energia que ocorre no interior do sistema considerado, a fonte de energia será a água líquida que se encontra a 20,0 ºC e o recetor de energia será o gelo que se encontra a 0 ºC.
⇒ Quando dois corpos a temperaturas diferentes são colocados em contato, há energia a transferir-se como calor do corpo que se encontra a uma temperatura mais elevada, neste caso a água líquida que se encontra a 20,0 ºC, funcionando este como a fonte de energia, para aquele que se encontra a uma temperatura mais baixa, neste caso o gelo que se encontra a 0 ºC, funcionando este como recetor de energia, até que ambos atinjam a mesma temperatura.
Fonte: água líquida [, a 20,0 ºC].
Recetor: gelo [, a 0,0 ºC] …….. 5 pontos
6.2. Qual das expressões seguintes permite calcular a energia, em joules (J), necessária para fundir completamente o gelo?
- Opção (C)
⇒ Recorrer à expressão E = m ΔH para calcular a energia, expressa em joules, necessária para fundir 30,0 g de gelo que se encontra a 0 ºC
- E = m ΔH ⇔ E = (0,0300 × 3,34 × 105) J
⇒ O valor da massa de gelo deve estar expresso em quilogramas devido às unidades em que está indicada a variação da entalpia de fusão do gelo.
- Opção (C) …………. 5 pontos
6.3. Com base nos resultados obtidos experimentalmente, os alunos estabeleceram o balanço energético do sistema.
6.3.1. Em que lei se baseia o estabelecimento do balanço energético do sistema?
⇒ O estabelecimento do balanço energético do sistema baseia-se na Lei da Conservação da Energia ou 1ª Lei da Termodinâmica.
- Lei da conservação da energia ou 1.ª Lei da Termodinâmica …….. 5 pontos
6.3.2. Os alunos calcularam a energia recebida pelo gelo, desde que este foi adicionado à água líquida até toda a mistura ter ficado à mesma temperatura de 11,0 ºC, tendo obtido 1,140 × 104 J.
Calcularam também a energia cedida pela água líquida, inicialmente a 20,0 ºC, no mesmo intervalo de tempo. Com base nos resultados obtidos, concluíram que, naquele intervalo de tempo, tinha ocorrido transferência de energia entre o sistema considerado e o exterior.
Conclua, justificando, em que sentido terá ocorrido aquela transferência de energia.
Apresente todas as etapas de resolução.
⇒ Energia recebida pelo gelo:
- Er = 1,140 × 104 J
⇒ Energia cedida pela água:
- Ec = m c ΔT ⇔ E = m c (θf−θi) ⇔ E = 0,2600 × 4,18 × 104 × (11,0 – 20,0) ⇔ E = 0,2600 × 4,18 × 104× (– 9,0) ⇔ E = − 9,781 × 103 J
⇒ Energia cedida pela água:
- ΔU = Er + Ec ⇔ ΔU = + 1,140 × 104 J − 9,781 × 103 J ⇔ ΔU = + 0,181 × 104 J
A variação de energia interna do sistema é positiva, ΔU > 0, então o sistema recebeu energia do exterior.
⇒ Assim, houve energia que se transferiu do exterior (ambiente) para o sistema gelo + água.
- Etapas de resolução:
A) Cálculo da energia cedida pela água líquida, inicialmente a 20,0 ºC, no intervalo de tempo considerado (E = 9,781 × 103 J)
ou
- Cálculo da variação de energia da água líquida, inicialmente a 20,0 ºC, no intervalo de tempo considerado (ΔE = -9,781 × 103 J) …….. 5 pontos
B) Comparação da energia recebida pelo gelo com a energia cedida pela água líquida, inicialmente a 20,0 ºC, no intervalo de tempo considerado (1,140 × 104 J > 9,781 × 103 J )
ou
- Demonstração de que a energia interna do sistema aumentou, no intervalo de tempo considerado
ou
- Cálculo da energia necessária à fusão completa do gelo e comparação desta energia com a energia cedida pela água líquida, inicialmente a 20,0 ºC, no intervalo de tempo considerado (1,002 × 104 J > 9,781 × 103 J ) …….. 5 pontos
C) Conclusão sobre o sentido em que terá ocorrido a transferência de energia (do exterior para o sistema) …….. 5 pontos
ou
A) Cálculo da diminuição de temperatura que a água líquida, inicialmente a 20,0 ºC, sofreria se tivesse cedido toda a energia recebida pelo gelo (10,5 ºC) …….. 5 pontos
B) Comparação da diminuição de temperatura que a água líquida sofreria com a diminuição de temperatura real, no intervalo de tempo considerado (10,5 ºC > 9,0 ºC) …….. 5 pontos
C) Conclusão sobre o sentido em que terá ocorrido a transferência de energia (do exterior para o sistema) …….. 5 pontos
Nota – A apresentação de valores calculados com arredondamentos incorretos, ou com um número incorreto de algarismos significativos, não implica, por si só, qualquer desvalorização.
7. (2014 – EE) A construção de paredes duplas, separadas por um material que promova o isolamento térmico, contribui para melhorar o comportamento térmico dos edifícios.
Um material que promova um bom isolamento térmico terá
(A) baixa capacidade térmica mássica.
(B) elevada capacidade térmica mássica.
(C) baixa condutividade térmica.
(D) elevada condutividade térmica.
- Opção (C)
⇒ Um bom isolamento térmico implica uma baixa taxa temporal de transferência de energia como calor por condução, Q/Δt, que é traduzida pela expressão:
⇒ Da análise desta expressão verifica-se que um material mau condutor de calor, um bom isolante térmico, é aquele que apresenta um baixo valor de k, ou seja, uma baixa condutividade térmica.
- Opção (C) …………. 5 pontos
8. (2014 – EE) Através das janelas de vidro simples, há transferência de energia entre o exterior e o interior de uma habitação, sob a forma de calor, por condução.
Explique o facto de a condutividade térmica dos gases ser, geralmente, muito inferior à dos sólidos.
⇒ O processo de transferência de energia, como calor, por condução, dá-se através de interações entre as partículas constituintes do meio material.
⇒ Nos gases estas interações são muito menos frequentes do que nos sólidos, dado que as suas partículas estão, em média, muito mais afastadas umas das outras do que nos sólidos, pelo que, para as mesmas condições, a quantidade de energia transferida como calor por unidade de tempo, Q/Δt, é menor nos gases.
Da expressão
⇒ Verifica-se que a condutividade térmica, k, é diretamente proporcional a Q/Δt, o que, de acordo com o acima analisado, explica o facto da condutividade térmica dos gases ser, em geral, inferior à dos sólidos.
- Tópicos de referência:
A) [De acordo com a expressão
a condutividade térmica de um material será [, para as mesmas condições,] tanto maior quanto maior for a taxa temporal de transferência de energia, sob a forma de calor, por condução [, através desse material].
B) O mecanismo de transferência de energia, sob a forma de calor, por condução, envolve interações entre as partículas do meio (ou equivalente).
C) Nos gases, essas interações são mais difíceis (ou equivalente) uma vez que as partículas se encontram, em média, muito mais afastadas umas das outras do que nos sólidos (ou equivalente). [Assim, a condutividade térmica dos gases é, geralmente, muito inferior à dos sólidos].
9. (2014 – EE) Pretende-se instalar um sistema de coletores solares, com rendimento de 40%, para aquecimento de água, numa habitação que consome, em média, nesse aquecimento, 8,8 kW h por dia.
Determine a área de coletores a ser instalada, admitindo que estes vão ser colocados numa posição em que a energia da radiação incidente na sua superfície é, em média, 3,6 × 109 J, por ano e por m2 de área de coletores.
Apresente todas as etapas de resolução.
- Etapas de resolução:
A) Cálculo da energia da radiação incidente necessária para produzir diariamente 8,8 kW h (E = 22,0 kW h) …….. 5 pontos
B) Cálculo da área de coletores (A = 8,0 m2) (ver nota) …….. 5 pontos
Nota – A utilização de energias relativas a intervalos de tempo diferentes no cálculo da área de coletores implica a pontuação desta etapa com zero pontos.
10. (2015 – 1ªF) Nem o calor nem o trabalho são formas de energia.
O calor é a energia que se transfere entre corpos em contacto, como resultado de uma diferença de temperatura entre eles, fluindo a energia do corpo que se encontra a temperatura mais elevada para o corpo que se encontra a temperatura mais baixa. Antes dessa transferência, não existe calor armazenado na fonte, nem passa a existir calor acumulado no recetor após a transferência. Mas há energia armazenada na fonte antes da transferência, e a energia do recetor passa a ser mais elevada após a transferência – por exemplo, se o recetor for gelo, parte dele pode fundir-se.
Peter Atkins, O Dedo de Galileu, 1.ª ed., Lisboa, Gradiva, 2007, pp. 135-136 (adaptado)
O calor
A) é uma forma de energia interna.
B) é uma propriedade que depende da temperatura a que um corpo se encontra.
C) é um fluido que pode ser transferido de um corpo para outro.
D) é uma energia transferida.
- Opção (D)
⇒ O calor é uma medida da energia transferida entre corpos em contacto quando se encontram a temperaturas diferentes.
- Calor é energia transferida de forma espontânea entre dois sistemas.
- Opção (D) …………. 5 pontos
11. (2015 – 1ªF) Considere um sistema fechado que cedeu 400 J, como calor, tendo sido sobre ele realizado um trabalho de 300 J.
Qual foi a variação da energia interna do sistema?
⇒ Determinar a variação da energia interna do sistema recorrendo à expressão:
- ΔEinterna = Q + W + R ⇔ ΔEinterna = –400 + 300 + 0 ⇔ ΔEinterna = –100 J
⇒ A variação da energia interna do sistema foi de –100 J, isto é, a energia interna do sistema diminui 100 J.
- -100 J (ou equivalente) …………. 5 pontos
ou
- [A energia interna do sistema] diminuiu 100 J.
12. (2015 – 1ªF) Numa experiência, forneceu-se uma energia de 92,0 kJ a 400 g de gelo, inicialmente a -10,0 °C.
Admita que toda a energia fornecida contribuiu para o aumento da energia interna do gelo e que não houve outras trocas de energia entre o gelo e o exterior.
A energia necessária à fusão de 1,0 kg de gelo é 3,34 x 105 J e o ponto de fusão da água, nas condições da experiência, é 0,0 ºC.
Calcule a massa de gelo que não se fundiu. Apresente todas as etapas de resolução.
- cgelo (capacidade térmica mássica do gelo) = 2,11 x 103 J kg-1 °C-1
⇒ Energia utilizada para aumentar a temperatura de -10 ºC para 0 ºC:
- E = m c ΔT = 0,400 x 2,11 x 103 x [0 – (-10)] = 8,44 x 103 J
⇒ Energia disponível para a fusão do gelo:
- E = 92,0 x 103 – 8,44 x 103 = 8,356 x 104 J
⇒ Cálculo da massa de gelo que fundiu:
⇒ Cálculo da massa de gelo que não fundiu:
- m = 400 – 250 g = 150 g
ou
⇒ Determinar a energia necessária para elevar a temperatura das 400 g de gelo de –10,0 ºC para 0,0 ºC :
- E = m c ΔT ⇔ E = 0,400 x 2,11 x 103 x (0,0 –(–10,0)) ⇔ E = 8,44 x 103 J
⇒ Determinar a energia necessária para fundir 400 g de gelo.
- E = m ΔHf ⇔ E = 0,400 x 3,34 x 105 ⇔ E = 1,336 x 105 J
⇒ Determinar a energia total necessária para aumentar a temperatura e fundir 400 g de gelo
- Etotal = Eaquecer + Efundir ⇔ Etotal = 8,44 x 103 + 1,336 x 105 ⇔ Etotal = 1,420 x 105 J
⇒ Determinar a diferença, Efalta, entre a energia Etotal, necessária para aumentar a temperatura e fundir 400 g de gelo e a energia fornecida, Efornecida:
- Efalta = Etotal – Efornecida ⇔ Efalta = 1,420 x 105 – 9,20 x 104 ⇔ Etotal = 5,004 x 104 J
⇒ Determinar a massa de gelo que não fundiu (ms) a partir da energia em falta para fundir a totalidade do gelo recorrendo à expressão:
- Etotal = ms ΔHf ⇔ 5,004 x 104 = ms x 3,34 x 105 ⇔ ms = 0,150 kg
- Etapas de resolução:
A) Determinação da energia necessária para aumentar a temperatura da massa de gelo considerada de -10,0 ºC para 0,0 ºC (E = 8,440 × 103 J) …….. 5 pontos
B) Determinação da energia disponível para a fusão do gelo (E = 8,356 × 104 J) …….. 4 pontos
C) Determinação da massa de gelo que se fundiu (m = 0,2502 kg)
ou
- Determinação da energia que seria necessária para fundir 400 g de gelo (E = 1,336 × 105 J) e determinação da diferença entre esta energia e a energia disponível para a fusão do gelo (E = 5,00 × 104 J) …….. 4 pontos
D) Determinação da massa de gelo que não se fundiu (m = 0,150 kg) …….. 2 pontos
ou
A) Determinação da energia necessária para aumentar a temperatura da massa de gelo considerada de -10,0 ºC para 0,0 ºC (E = 8,440 × 103 J) …….. 5 pontos
B) Determinação da energia que seria necessária para fundir 400 g de gelo (E = 1,336 × 105 J) e determinação da energia (total) que seria necessária para aumentar a temperatura e para fundir 400 g de gelo (E = 1,420 × 105 J) ……..4 pontos
C) Determinação da diferença entre a energia (total) que seria necessária para aumentar a temperatura e para fundir 400 g de gelo e a energia fornecida (E = 5,00 × 104 J) …….. 4 pontos
D) Determinação da massa de gelo que não se fundiu (m = 0,150 kg) …….. 2 pontos
13. (2015 – 2ªF) Considere que uma barra de alumínio é aquecida.
Verificou-se que a energia interna da barra de alumínio aumentou 36 kJ quando lhe foi fornecida uma energia de 4,5 x 104 J.
Qual foi o rendimento deste processo de aquecimento?
- 80% ou 0,80 (ou equivalente) …………. 5 pontos
Nota – A apresentação do valor solicitado com um número incorreto de algarismos significativos não implica qualquer desvalorização.
14. (2015 – 2ªF) Para determinar a capacidade térmica mássica do alumínio, forneceu-se energia a um cilindro desse metal, de massa 1,010 kg, a uma taxa temporal de 3,0 J por segundo.
Na tabela seguinte, encontram-se registadas as variações de temperatura, Δɵ, do cilindro de alumínio em função do tempo de aquecimento, t.
Admita que toda a energia fornecida contribuiu para o aumento de temperatura do cilindro de alumínio.
Calcule a capacidade térmica mássica do alumínio.
Utilize as potencialidades gráficas da calculadora.
Apresente a equação da reta de ajuste obtida, identificando as grandezas físicas consideradas.
Apresente todas as etapas de resolução.
⇒ Determinar, para o gráfico de Δθ em função de t, a equação da reta que melhor se ajusta aos valores registados na tabela.
- Δθ = 3,28 x 10-3 t (SI)
⇒ Relação entre o declive da reta Δθ e a capacidade térmica mássica:
ou
⇒ Calcular, para cada tempo de aquecimento as energias fornecidas :
⇒ Determinar, para o gráfico de Δθ em função de t, a equação da reta que melhor se ajusta aos valores registados na tabela.
- Δθ = 1,09 x 10-3 E (SI)
⇒ Relação entre o declive da reta Δθ e a capacidade térmica mássica:
- Etapas de resolução:
A) Apresentação, para o gráfico de Δi em função de t, da equação da reta que melhor se ajusta ao conjunto dos valores registados na tabela (Δθ = 3,28 × 10-3 t (SI)) (ver notas 1 e 2) …….. 5 pontos
B) Determinação da capacidade térmica mássica do alumínio (c = 9,1 × 102 J kg-1ºC-1) (ver nota 3) …….. 5 pontos
OU
A) Apresentação, para o gráfico de Δθ em função de E, da equação da reta que melhor se ajusta ao conjunto dos valores considerados (Δθ = 1,09 × 10-3 E (SI)) (ver notas 1 e 2) …….. 5 pontos
B) Determinação da capacidade térmica mássica do alumínio (c = 9,1 × 102 J kg-1ºC-1) (ver nota 3) …….. 5 pontos
Notas:
1. A apresentação da equação da reta para o gráfico de t em função de Δi (t = 3,05 × 102 Δθ + 0,2) ou para o gráfico de E em função de Δθ (E = 9,14 × 102 Δθ + 0,7) será considerada um erro de tipo 2.
2. A não identificação ou a identificação incorreta de, pelo menos, uma das grandezas físicas consideradas implica a pontuação desta etapa com zero pontos.
3. A apresentação do valor solicitado com um número incorreto de algarismos significativos não implica qualquer desvalorização.
15. (2015 – EE) Os satélites estão geralmente equipados com painéis fotovoltaicos que se orientam segundo uma direção perpendicular à da radiação solar.
Considere que a potência média da radiação solar por unidade de área, ao nível da órbita de um satélite, é 1,3 x 103 W m-2 e que um conjunto de painéis fotovoltaicos, de área 12 m2, instalado no satélite, tem um rendimento médio de 20%.
Qual das expressões seguintes permite calcular, em kW h, a energia fornecida ao satélite por esse conjunto de painéis em 6 horas de funcionamento?
- Opção (A)
- A = 12 m2
- η = 20 %
- Δt = 6 h
- Er = 1,3 x 103 W m-2
Calcular a energia fornecida ao satélite, Eútil:
⇒ Er = P/A ⇔ Pradiação = Er x A = 1,3 x 103 x 12 W
⇒ Pútil = η x Pradiação = 0,20 x 1,3 x 103 x 12 W
⇒ Eútil = Pútil x Δt = 0,20 x 1,3 x 103 x 12 x 6 W = 0,20 x 1,3 x 103 x 12 x 6 x 10-3 kW = 0,20 x 1,3 x 12 x 6 kW
- Opção (A)…………. 5 pontos