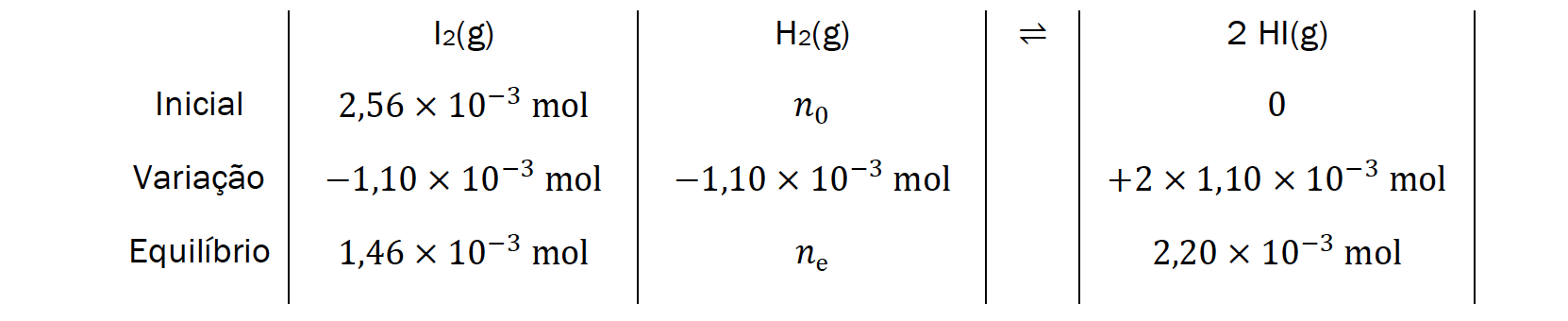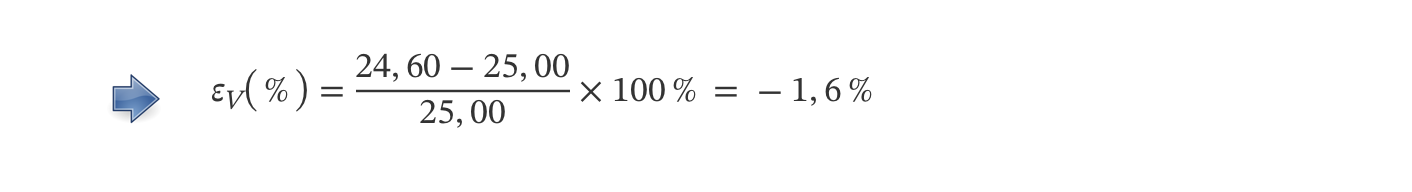2015 – 1ª Fase – Prova Escrita de Física e Química A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: 1.ª Fase – 2015
GRUPO I
Nem o calor nem o trabalho são formas de energia. O calor é a energia que se transfere entre corpos em contacto, como resultado de uma diferença de temperatura entre eles, fluindo a energia do corpo que se encontra a temperatura mais elevada para o corpo que se encontra a temperatura mais baixa. Antes dessa transferência, não existe calor armazenado na fonte, nem passa a existir calor acumulado no recetor após a transferência. Mas há energia armazenada na fonte antes da transferência, e a energia do recetor passa a ser mais elevada após a transferência – por exemplo, se o recetor for gelo, parte dele pode fundir-se.
Peter Atkins, O Dedo de Galileu, 1.ª ed., Lisboa, Gradiva, 2007, pp. 135-136 (adaptado)
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1. O calor
A) é uma forma de energia interna.
B) é uma propriedade que depende da temperatura a que um corpo se encontra.
C) é um fluido que pode ser transferido de um corpo para outro.
D) é uma energia transferida.
- Opção (D)
⇒ O calor é uma medida da energia transferida entre corpos em contacto quando se encontram a temperaturas diferentes.
- Calor é energia transferida de forma espontânea entre dois sistemas.
- Opção (D) …………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2. Considere um sistema fechado que cedeu 400 J, como calor, tendo sido sobre ele realizado um trabalho de 300 J.
Qual foi a variação da energia interna do sistema?
⇒ Determinar a variação da energia interna do sistema recorrendo à expressão:
- ΔEinterna = Q + W + R ⇔ ΔEinterna = –400 + 300 + 0 ⇔ ΔEinterna = –100 J
⇒ A variação da energia interna do sistema foi de –100 J, isto é, a energia interna do sistema diminui 100 J.
- -100 J (ou equivalente) …………. 5 pontos
ou
- [A energia interna do sistema] diminuiu 100 J.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3. Numa experiência, forneceu-se uma energia de 92,0 kJ a 400 g de gelo, inicialmente a -10,0 °C.
Admita que toda a energia fornecida contribuiu para o aumento da energia interna do gelo e que não houve outras trocas de energia entre o gelo e o exterior.
A energia necessária à fusão de 1,0 kg de gelo é 3,34 x 105 J e o ponto de fusão da água, nas condições da experiência, é 0,0 ºC.
Calcule a massa de gelo que não se fundiu. Apresente todas as etapas de resolução.
- cgelo (capacidade térmica mássica do gelo) = 2,11 x 103 J kg-1 °C-1
⇒ Energia utilizada para aumentar a temperatura de -10 ºC para 0 ºC:
- E = m c ΔT = 0,400 x 2,11 x 103 x [0 – (-10)] = 8,44 x 103 J
⇒ Energia disponível para a fusão do gelo:
- E = 92,0 x 103 – 8,44 x 103 = 8,356 x 104 J
⇒ Cálculo da massa de gelo que fundiu:
⇒ Cálculo da massa de gelo que não fundiu:
- m = 400 – 250 g = 150 g
ou
⇒ Determinar a energia necessária para elevar a temperatura das 400 g de gelo de –10,0 ºC para 0,0 ºC :
- E = m c ΔT ⇔ E = 0,400 x 2,11 x 103 x (0,0 –(–10,0)) ⇔ E = 8,44 x 103 J
⇒ Determinar a energia necessária para fundir 400 g de gelo.
- E = m ΔHf ⇔ E = 0,400 x 3,34 x 105 ⇔ E = 1,336 x 105 J
⇒ Determinar a energia total necessária para aumentar a temperatura e fundir 400 g de gelo
- Etotal = Eaquecer + Efundir ⇔ Etotal = 8,44 x 103 + 1,336 x 105 ⇔ Etotal = 1,420 x 105 J
⇒ Determinar a diferença, Efalta, entre a energia Etotal, necessária para aumentar a temperatura e fundir 400 g de gelo e a energia fornecida, Efornecida:
- Efalta = Etotal – Efornecida ⇔ Efalta = 1,420 x 105 – 9,20 x 104 ⇔ Etotal = 5,004 x 104 J
⇒ Determinar a massa de gelo que não fundiu (ms) a partir da energia em falta para fundir a totalidade do gelo recorrendo à expressão:
- Etotal = ms ΔHf ⇔ 5,004 x 104 = ms x 3,34 x 105 ⇔ ms = 0,150 kg
- Etapas de resolução:
A) Determinação da energia necessária para aumentar a temperatura da massa de gelo considerada de -10,0 ºC para 0,0 ºC (E = 8,440 × 103 J) …….. 5 pontos
B) Determinação da energia disponível para a fusão do gelo (E = 8,356 × 104 J) …….. 4 pontos
C) Determinação da massa de gelo que se fundiu (m = 0,2502 kg)
ou
- Determinação da energia que seria necessária para fundir 400 g de gelo (E = 1,336 × 105 J) e determinação da diferença entre esta energia e a energia disponível para a fusão do gelo (E = 5,00 × 104 J) …….. 4 pontos
D) Determinação da massa de gelo que não se fundiu (m = 0,150 kg) …….. 2 pontos
ou
A) Determinação da energia necessária para aumentar a temperatura da massa de gelo considerada de -10,0 ºC para 0,0 ºC (E = 8,440 × 103 J) …….. 5 pontos
B) Determinação da energia que seria necessária para fundir 400 g de gelo (E = 1,336 × 105 J) e determinação da energia (total) que seria necessária para aumentar a temperatura e para fundir 400 g de gelo (E = 1,420 × 105 J) ……..4 pontos
C) Determinação da diferença entre a energia (total) que seria necessária para aumentar a temperatura e para fundir 400 g de gelo e a energia fornecida (E = 5,00 × 104 J) …….. 4 pontos
D) Determinação da massa de gelo que não se fundiu (m = 0,150 kg) …….. 2 pontos
4. A energia pode ser transferida como radiação.
A taxa temporal de emissão de radiação pela superfície de um corpo é
A) diretamente proporcional à temperatura absoluta da superfície desse corpo.
B) inversamente proporcional à temperatura absoluta da superfície desse corpo.
C) diretamente proporcional à quarta potência da temperatura absoluta da superfície desse corpo.
D) inversamente proporcional à quarta potência da temperatura absoluta da superfície desse corpo.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
A taxa temporal de emissão de radiação pela superfície de um corpo é dada pela expressão P = eσAT4 , o que evidencia que a taxa temporal de emissão de radiação pela superfície de um corpo é …:
– … diretamente proporcional à quarta potência da temperatura absoluta da superfície desse corpo;
– … diretamente proporcional à área da superfície do corpo;
– … diretamente proporcional à emissividade da superfície do corpo.
- Opção (C) …………. 5 pontos
GRUPO II
1. Considere uma roda que, tendo apenas movimento de rotação em torno do seu eixo, efetua 50 rotações, em cada minuto, durante um determinado intervalo de tempo.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.1. O módulo da velocidade angular da roda, em radianos por segundo, no intervalo de tempo considerado, pode ser calculado pela expressão

- Opção (A) …………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
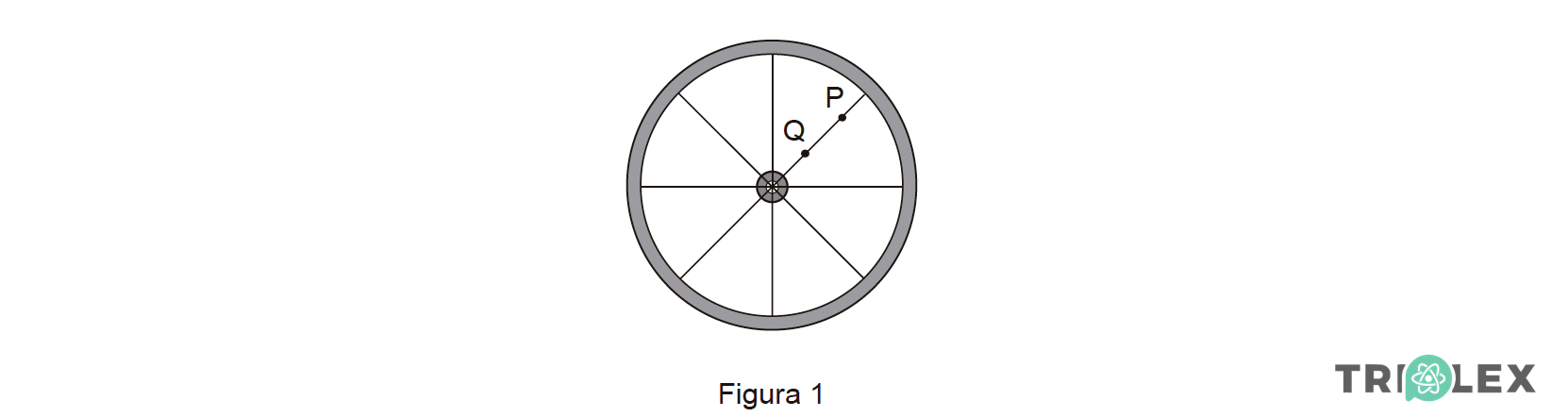
1.2. Na Figura 1, estão representados essa roda e dois pontos, P e Q, de um dos seus raios.
O módulo da aceleração do ponto P, no intervalo de tempo considerado, é
A) superior ao módulo da aceleração do ponto Q.
B) inferior ao módulo da aceleração do ponto Q.
C) igual ao módulo da aceleração do ponto Q, sendo ambos nulos.
D) igual ao módulo da aceleração do ponto Q, sendo ambos diferentes de zero.
- Opção (A)
⇒ A velocidade angular é constante2, todos os pontos da roda executam um movimento circular e uniforme, e, por isso, a aceleração de qualquer desses pontos é centrípeta:
- 𝑎 = 𝑎n
⇒ O módulo da componente normal da aceleração (ou aceleração centrípeta), 𝑎n, de um ponto qualquer a uma distância 𝑟 do eixo da roda é
- 𝑎n = 𝑣2/𝑟 = (𝜔𝑟)2/𝑟 = 𝜔2𝑟2/r = 𝜔2 𝑟
⇒ Num certo instante, todos os pontos da roda têm a mesma velocidade angular, portanto, quanto mais afastados estiverem do eixo da roda, maior 𝑟, maior será a aceleração centrípeta.
⇒ Encontrando-se o ponto P mais afastado do eixo, maior 𝑟, a sua aceleração é maior do que a de Q.
→ 2 Se a velocidade angular não for constante, a aceleração de um ponto da roda tem uma componente centrípeta e uma componente tangencial. O módulo da aceleração, 𝑎, de um ponto aumenta com a distância 𝑟 ao eixo. Mostra-se que são diretamente proporcionais: 𝑎/𝑟 é, num certo instante, o mesmo para todos os pontos da roda.
- Opção (A)…………. 5 pontos
2. Na Figura 2 (que não está à escala), estão representados dois conjuntos ciclista + bicicleta, CI e CII, que se movem ao longo de uma estrada retilínea e horizontal, coincidente com o eixo Ox de um referencial unidimensional.
Considere que cada um dos conjuntos pode ser representado pelo seu centro de massa (modelo da partícula material).

Considere que no instante t = 0 s o conjunto CII inicia o seu movimento e que, nesse instante, o conjunto CI passa na origem do referencial.
Admita que, a partir desse instante, e durante um determinado intervalo de tempo, as componentes escalares, segundo o eixo Ox, das posições, xCI e xCII , dos conjuntos CI e CII, respetivamente, variam com o tempo, t, de acordo com as equações
XCI = 7,0 t (SI)
XCII = 800 – 0,030 t2 (SI)
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
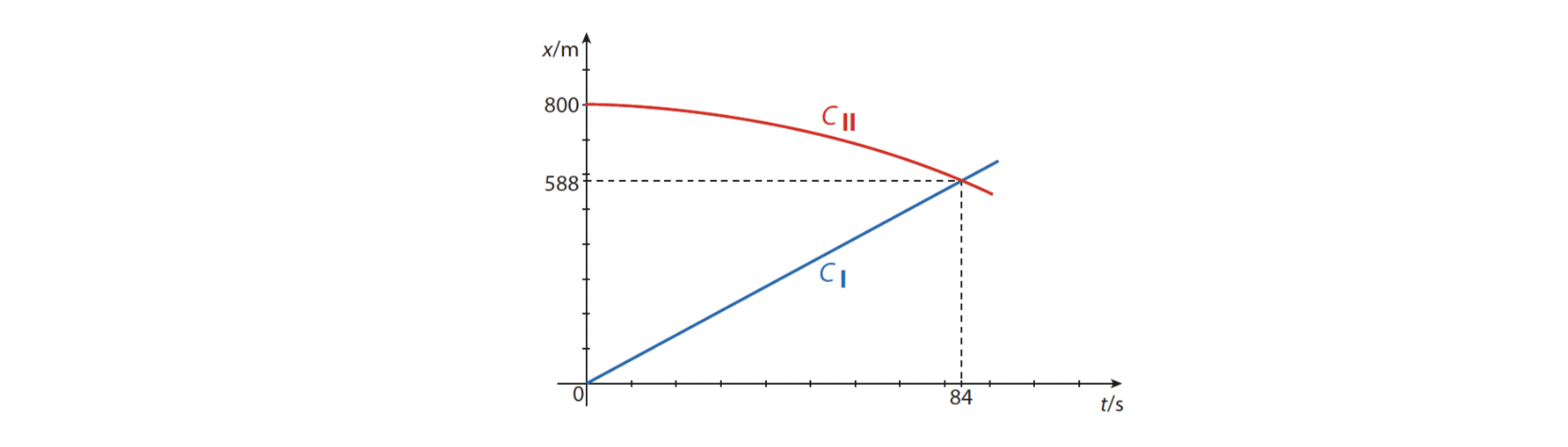
2.1. Apresente, num mesmo sistema de eixos, os esboços dos gráficos que traduzem, no intervalo de tempo considerado, as componentes escalares das posições, xCI e xCII , em função do tempo, desde o instante t = 0 s até, pelo menos, ao instante em que os conjuntos se cruzam.
Determine o instante em que os conjuntos CI e CII se cruzam e a componente escalar da posição daqueles conjuntos nesse instante.
Utilize as potencialidades gráficas da calculadora.
- Etapas de resolução:
A)Apresentação dos esboços dos gráficos que traduzem as componentes escalares das posições, xCI e xCII , dos conjuntos CI e CII, respetivamente, em função do tempo, desde o instante t = 0 s até, pelo menos, ao instante em que os conjuntos se cruzam (ver notas 1, 2 e 3) …….. 4 pontos
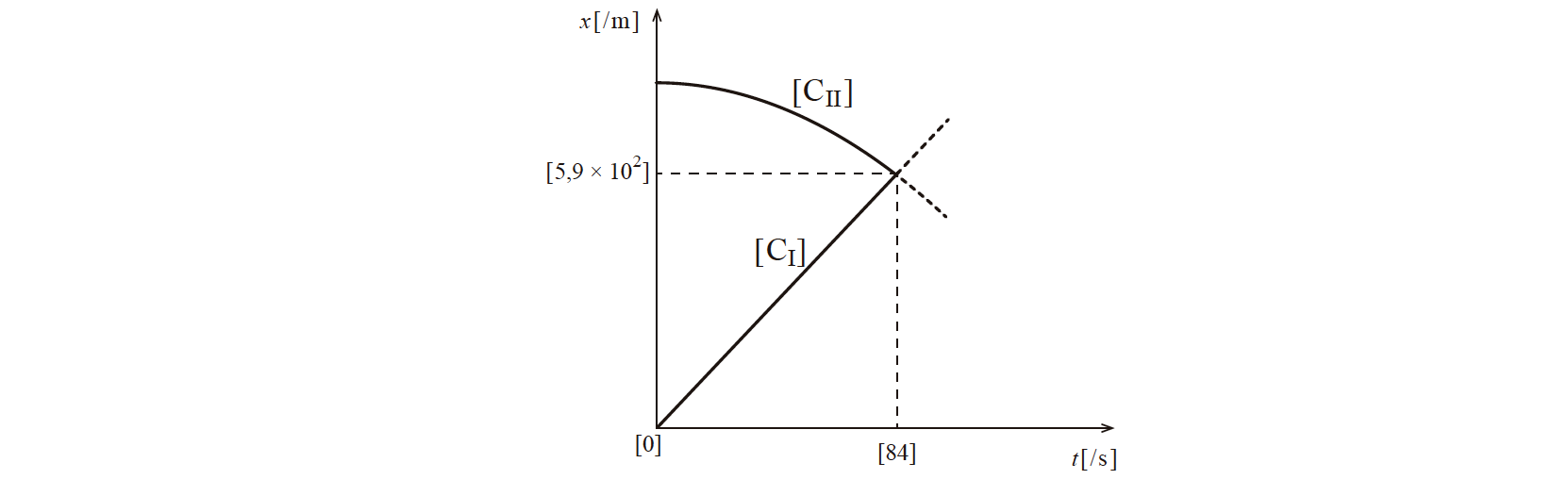
B) Determinação do instante em que os conjuntos CI e CII se cruzam (t = 84 s) (ver notas 4, 5 e 6) …….. 3 pontos
C)Determinação da componente escalar da posição dos conjuntos no instante em que se cruzam (x = 5,9 × 102 m) (ver notas 4, 5 e 6) …….. 3 pontos
Notas:
1. A não apresentação ou a apresentação incorreta de, pelo menos, um dos esboços dos gráficos solicitados implica a pontuação desta etapa com zero pontos.
2. A apresentação de, pelo menos, um esboço de gráfico que não respeite o intervalo de tempo solicitado implica a pontuação desta etapa com zero pontos.
3. A não indicação ou a indicação incorreta de uma das grandezas representadas implica uma desvalorização de 2 pontos. A não indicação ou a indicação incorreta das duas grandezas representadas implica a pontuação desta etapa com zero pontos.
4. O valor da grandeza a determinar poderá ser indicado no esboço do gráfico ou separadamente.
5.A ausência de unidade ou a apresentação de uma unidade incorreta no resultado obtido implica uma desvalorização de 1 ponto.
6. A apresentação do resultado obtido com um número incorreto de algarismos significativos não implica qualquer desvalorização.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.2. Em qual dos esquemas seguintes se encontram corretamente representadas, num dado instante do intervalo de tempo considerado, a velocidade, V, e a aceleração, a, do conjunto CII?
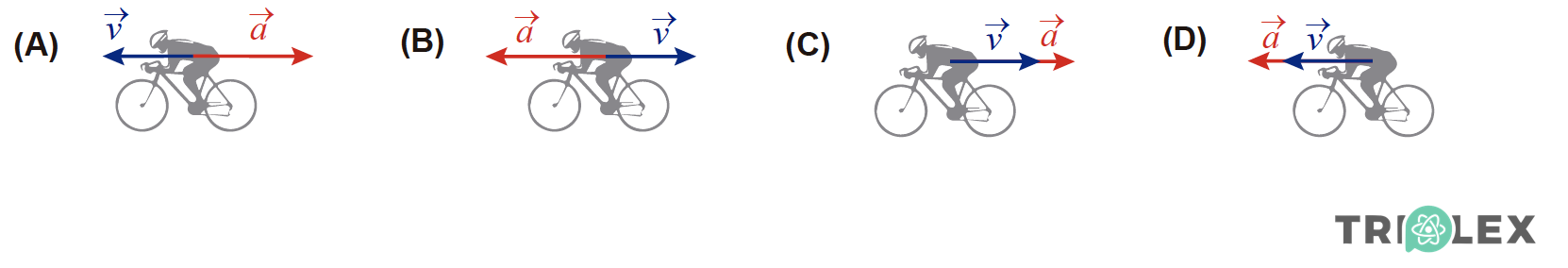
- Opção (D)
⇒ O ciclista CII partindo do repouso passa a mover-se no sentido negativo do eixo.
- 𝑥CII = xo + v0t + ½ at2 = 800 − 0,030 𝑡2 (SI)
- 𝑎CII = −0,060 m s−2
- 𝑣CII = v0 + at = −0,060𝑡 (SI)
⇒ Então, a velocidade é um vetor com o sentido negativo do eixo dos xx e o movimento é acelerado com aceleração também no sentido negativo do eixo dos xx.
- Ambos os vetores apontam no mesmo sentido.
⇒ As componentes escalares da aceleração e da velocidade são negativas, por isso os vetores apontam no sentido convencionado negativo.
- Opção (D) …………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2.3. A soma dos trabalhos realizados pelas forças que atuam no conjunto CI, num deslocamento desse conjunto no intervalo de tempo considerado, é
A) nula, uma vez que atuam no conjunto forças não conservativas.
B) negativa, uma vez que a energia cinética do conjunto diminui.
C) nula, uma vez que a energia cinética do conjunto se mantém constante.
D) negativa, uma vez que atuam no conjunto forças não conservativas.
- Opção (C)
⇒ Para o ciclista CI o declive da reta no gráfico x(t) é constante, logo, ele tem um movimento retilíneo e uniforme, movendo-se assim com velocidade constante.
⇒ No contexto do modelo da partícula material, o trabalho da resultante das forças é igual à variação de energia cinética e igual à soma dos trabalhos de todas as forças.
Sendo constante a velocidade também o é a energia cinética e a sua variação é nula.
- A soma dos trabalhos de todas as forças é nula.
- Opção (C) …………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
3. Na Figura 3 (que não está à escala), está representado um conjunto ciclista + bicicleta que iniciou a subida de uma rampa com uma energia cinética de 2,0 x 103 J.
Após percorrer 68 m sobre a rampa, atinge uma altura de 3,0 m, com uma velocidade de módulo 3,5 m s-1.
A massa do conjunto ciclista + bicicleta é 80 kg.
Considere que o conjunto pode ser representado pelo seu centro de massa (modelo da partícula material) e considere a base da rampa como nível de referência da energia potencial gravítica.
Calcule, no percurso considerado, a intensidade da resultante das forças não conservativas que atuam no conjunto ciclista + bicicleta, na direção do deslocamento. Admita que essa resultante se mantém constante.
Apresente todas as etapas de resolução.
⇒ Cálculo da variação de energia cinética entre a base e o topo do plano:
- ΔEc = ½ m v2 – Ec(inicial) = ½ × 80 kg × 3,52 m2 s–2 − 2,0 × 103 J = −1,51 × 103 J
⇒ Cálculo da variação de energia potencial entre a base e o topo do plano:
- ΔEc = m gh − 0 = 80 kg × 10 m s–2 × 3,0 m = 2,40 × 103 J
⇒ Na subida existem forças conservativas (fc) e forças não conservativas (fnc), sendo o trabalho das forças conservativas simétrico da variação de energia potencial:
- Wfc = −ΔEp = −2,40 × 103 J
⇒ Aplicação da lei do trabalho energia:
- W = ΔEc ⇔ Wfc + Wfnc = ΔEc ⇔−2,40 × 103 + Wfnc = −1,51 × 103 J ⇔ Wfnc = 2400 − 1510 = 8,90 × 102 J
⇒ Cálculo da intensidade das forças não conservativas:
- Wfnc = F d cos 0º ⇔ 8,90 × 102 = F × 68 × 1 ⇒ F = = 13 N
O ângulo entre a resultante das forças não conservativas e o deslocamento é 0 porque o trabalho é positivo.
- Etapas de resolução:
A) Determinação da energia mecânica do sistema quando o conjunto ciclista + bicicleta atinge a altura de 3,0 m (Em = 2,89 × 103 J)
OU
- Determinação da variação da energia cinética do conjunto ciclista + bicicleta e da variação da energia potencial gravítica do sistema, no percurso considerado (ΔEc = –1,51 × 103 J e ΔEp = 2,40 × 103 J) …….. 5 pontos
B) Determinação da variação da energia mecânica do sistema, no percurso considerado (ΔEm = 8,90 × 102 J) …….. 4 pontos
C) Determinação da intensidade da resultante das forças não conservativas que atuam no conjunto ciclista + bicicleta, na direção do deslocamento (F = 13 N) (ver nota 1) …….. 6 pontos
OU
A) Determinação da variação da energia cinética do conjunto ciclista + bicicleta (ΔEc = –1,51 × 103 J) e identificação desta variação com a soma dos trabalhos realizados pelas forças que atuam no conjunto, no percurso considerado …….. 5 pontos
B) Determinação da intensidade da resultante das forças que atuam no conjunto ciclista + bicicleta (F = 22,2 N) (ver nota 2) …….. 4 pontos
C) Determinação da intensidade da componente tangencial da força gravítica que atua no conjunto (Fgt = 35,3 N ) e determinação da intensidade da resultante das forças não conservativas que atuam no conjunto ciclista + bicicleta, na direção do deslocamento (F = 13 N) …….. 6 pontos
OU
A) Determinação do módulo da aceleração do conjunto, no percurso considerado (a = 0,277 m s-2) …….. 5 pontos
B) Determinação da intensidade da resultante das forças que atuam no conjunto ciclista + bicicleta (F = 22,2 N) …….. 4 pontos
C) Determinação da intensidade da componente tangencial da força gravítica que atua no conjunto (Fgt = 35,3 N ) e determinação da intensidade da resultante das forças não conservativas que atuam no conjunto ciclista + bicicleta, na direção do deslocamento (F = 13 N) …….. 6 pontos
Notas:
1. A explicitação do ângulo considerado na determinação da intensidade da resultante das forças não conservativas que atuam no conjunto é obrigatória: se, na etapa B, tiver sido calculada uma variação de energia mecânica do sistema positiva, a = 0º; se, na etapa B, tiver sido calculada incorretamente uma variação de energia mecânica do sistema negativa, a = 180º.
Em qualquer dos casos, se os ângulos acima referidos não forem explicitados, a etapa é pontuada com 0 pontos.
2. A explicitação do ângulo considerado na determinação da intensidade da resultante das forças que atuam no conjunto é obrigatória: se, na etapa A, tiver sido calculada uma variação de energia cinética do conjunto negativa, a = 180º; se, na etapa A, tiver sido calculada incorretamente uma variação de energia cinética do conjunto positiva, a = 0º.
Em qualquer dos casos, se os ângulos acima referidos não forem explicitados, a etapa é pontuada com 0 pontos.
GRUPO III
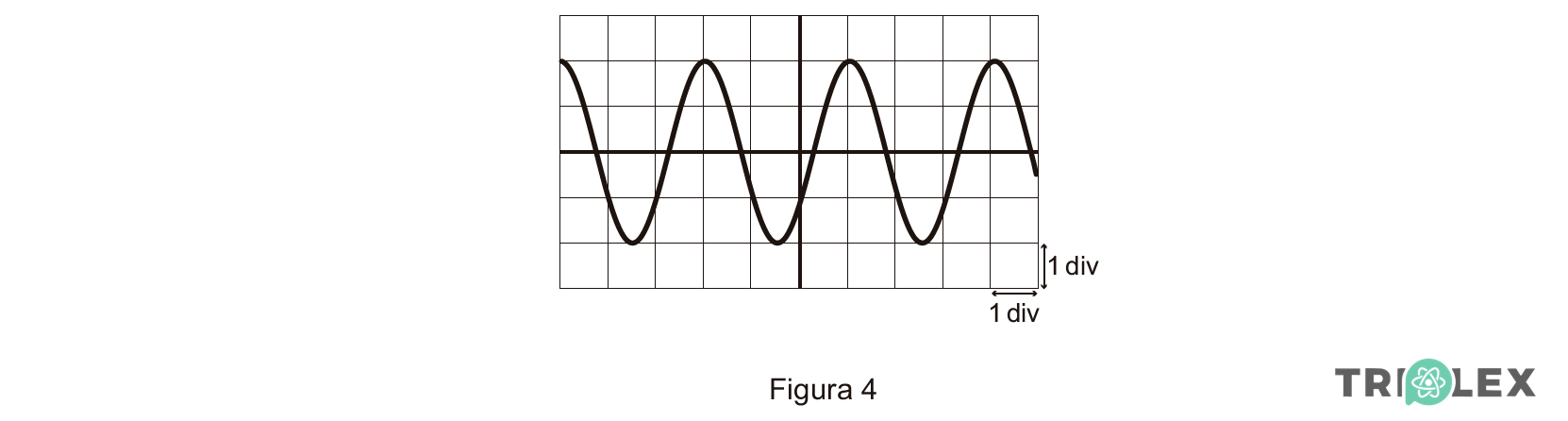
1. A Figura 4 representa o ecrã de um osciloscópio, no qual está registado o sinal elétrico resultante da conversão de um sinal sonoro, de frequência 330 Hz, emitido por um diapasão.
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
1.1. A base de tempo do osciloscópio estava regulada para
(A) 0,1 ms/div
(B) 1 ms/div
(C) 0,3 ms/div
(D) 3 ms/div
- Opção (B)
O período é o inverso da frequência:
- T = 1/f = 1/330 = 3,0 × 10–s = 3,0 ms
⇒ Como no gráfico um período corresponde a 3 divisões, e as 3 divisões correspondem a 3,0 ms, cada divisão vale 1,0 ms, que é a base de tempo para a qual o osciloscópio estava regulado 1 ms/div.
- Opção (B) …………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
1.2. Se o diapasão for percutido com uma força de maior intensidade, o sinal elétrico registado no ecrã do osciloscópio terá
(A) menor período e maior amplitude.
(B) menor período e a mesma amplitude.
(C) o mesmo período e a mesma amplitude.
(D) o mesmo período e maior amplitude.
- Opção (D)
⇒ Percutir o diapasão com maior intensidade significa fornecer, inicialmente, mais energia ao diapasão, aumentando a amplitude de vibração das suas hastes e, em consequência, a amplitude de pressão do sinal sonoro que se propaga e a amplitude do correspondente sinal elétrico, detetado no osciloscópio.
⇒ Ao vibrar origina um som puro com maior ou menor amplitude, dependendo da intensidade com que é percutido.
⇒ Para maior intensidade da pancada ele vibra com maior amplitude e produz um som mais intenso, com maior amplitude de pressão e de maior amplitude no ecrã do osciloscópio.
⇒ A frequência não é alterada, uma vez que é característica do diapasão que está a ser percutido (cada diapasão emite um som de uma frequência bem característica, dito som puro, descrito por uma função sinusoidal).
- Opção (D) …………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
2. Considere um sinal elétrico cuja tensão, U, varia com o tempo, t, de acordo com a expressão
U = 5,0 sin (8,80 x 102 πt ) (SI)
Esse sinal tem
(A) uma frequência angular de 8,80 x 102 rad s-1.
(B) um período de 7,14 x 10 -3 s.
(C) uma frequência angular de 4,40 x 102 rad s-1.
(D) um período de 2,27 x 10 -3 s.
- Opção (D)
⇒ U = Umáx sin(ωt) = 5,0 sin (8,80 x 102 πt) (SI) ⇒ ω = 8,80 x 102 π = 2,764 x 103 rad s-1
⇒ ω = 2π/T ⇒ T = 2π/ω = 2,27 x 10-3 s
- Opção (D)…………. 5 pontos
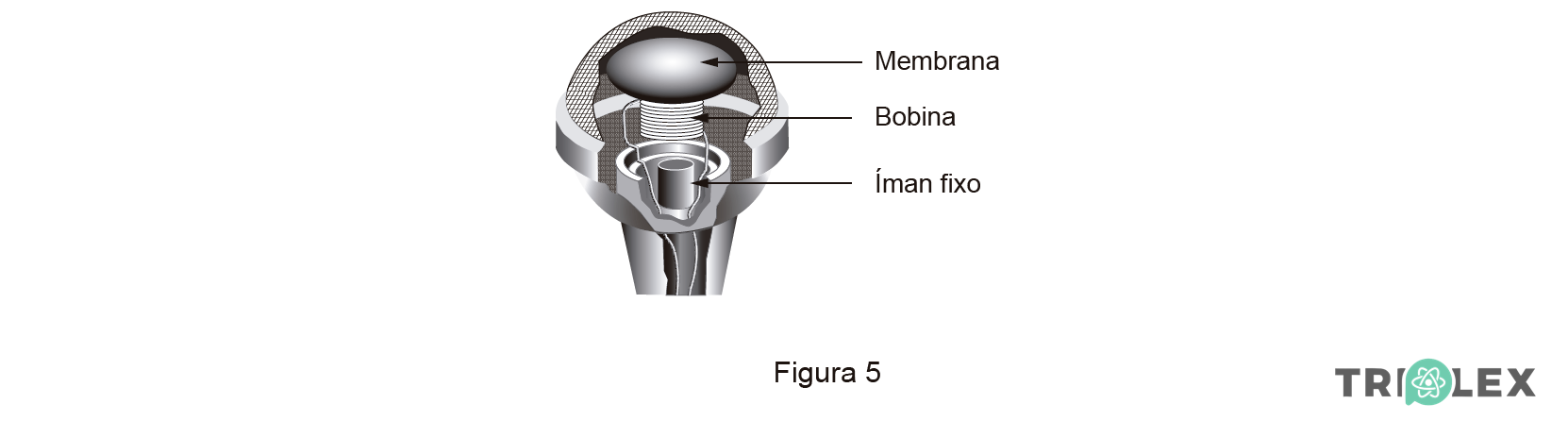
3. Descreva como é que um sinal sonoro é convertido num sinal elétrico, num microfone de indução semelhante ao representado na Figura 5.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ O sinal sonoro, onda de pressão, origina uma vibração da membrana.
⇒ Esta vibração transmite-se à bobina que se move em relação ao íman.
⇒ Este movimento relativo faz variar o fluxo magnético que atravessa a bobina, Δ𝛷 ≠ 0, criando uma força eletromotriz, |𝜀i| = |Δ𝛷|/Δ𝑡|, dita, por isso, induzida.
⇒ Esta força eletromotriz é a responsável pelo sinal elétrico detetado (corrente elétrica).
- A resposta integra os tópicos de referência seguintes ou outros de conteúdo equivalente:
A) Quando um sinal sonoro atinge a membrana do microfone, esta vibra, provocando uma oscilação da bobina em relação ao íman [fixo].
B) Esta oscilação provoca uma variação do fluxo magnético [que atravessa a bobina], induzindo na bobina uma força eletromotriz [que é responsável pelo aparecimento de um sinal elétrico].

GRUPO IV
1. O flúor e o cloro são dois halogéneos.
- 10ºano – Química – Domínio 1 – subdomínio 1 (Massa e tamanho dos átomos)
1.1 O cloro apresenta dois isótopos estáveis, o cloro-35 e o cloro-37.
Os átomos destes isótopos têm
(A) número atómico diferente.
(B) igual número de nucleões.
(C) igual número de protões.
(D) número de eletrões diferente.
- Opção (C)
⇒ Isótopos são átomos do mesmo elemento, têm o mesmo número de protões, 𝑍 (número atómico), e diferente número de neutrões, 𝑁.
⇒ O número de nucleões, 𝐴 = 𝑍 + 𝑁 (protões e neutrões), de dois isótopos é diferente, por diferirem no número de neutrões.
⇒ Neste caso o átomo de cloro-35 tem 35 nucleões e o de cloro-37 tem 37 nucleões. Ambos têm o mesmo número de protões que é a propriedade que identifica o elemento cloro.
- Opção (C) …………. 5 pontos
1.2. A orbital de valência menos energética de um átomo de cloro, no estado fundamental, pode ser caracterizada pelo conjunto de números quânticos
(A) (3, 1, 0)
(B) (3, 0, -1)
(C) (3, 1, -1)
(D) (3, 0, 0)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (D)
⇒ Consultando a tabela periódica constata-se que o número atómico, 𝑍, do cloro é 17. Um átomo de cloro tem um núcleo com 17 protões, logo, também, 17 eletrões.
⇒ A configuração eletrónica do cloro, 17Cl = (1s)2 (2s)2 (2p)6 (3s)2 (3p)5 . As orbitais de valência são as do último nível, 𝑛 = 3: a orbital 3s e as orbitais 3p. Destas, a menos energética é a orbital 3s.
⇒ O número quântico principal da orbital 3s é 3 (𝑛 = 3), o de momento angular (ou secundário) é 0 por se tratar de uma orbital s (𝑙 = 0) e, sendo 𝑙 = 0, necessariamente o número quântico magnético também é nulo (𝑚𝑙 = 0): (𝑛, 𝑙, 𝑚𝑙 ) = (3, 0, 0).
- Opção (D) …………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
1.3. Um átomo de flúor e um átomo de cloro, no estado fundamental, apresentam
(A) o mesmo número de orbitais p completamente preenchidas.
(B) ambos uma orbital p semipreenchida.
(C) o mesmo número de orbitais s completamente preenchidas.
(D) ambos uma orbital s semipreenchida.
- Opção (B)
⇒ O flúor e o cloro pertencem ao grupo 17, apresentando ambos, por isso, 7 eletrões de valência.
⇒ A configuração eletrónica de valência destes elementos, no estado fundamental, é (𝑛s)2 (𝑛p)5, sendo 𝑛 o número quântico principal de valência: 𝑛 = 2 para o flúor, por se encontrar no 2.º período, e 𝑛 = 3 para o cloro, por se encontrar no 3.º período.
⇒ Existindo três orbitais p em cada nível 𝑛 > 1, a configuração eletrónica de valência pode ser escrita como (𝑛s)2 (𝑛p𝑥)2 (𝑛p𝑦)2 (𝑛p𝑧 )1, existindo para ambos os átomos uma orbital com 1 eletrão (semipreenchida).
⇒ Quanto às orbitais completamente preenchidas, com 2 eletrões, o cloro tem mais uma orbital s preenchida (a orbital 3s) e mais três orbitais p preenchidas (uma orbital 2p e duas orbitais 3p) do que o flúor, o que está de acordo com o facto de o cloro (17Cl) ter mais 8 eletrões do que o flúor (9F).
- Opção (B) .…………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
1.4. A energia de ionização do átomo de cloro, isolado e em fase gasosa, é a energia de remoção mínima necessária para, a partir do átomo no estado fundamental, se formar um determinado ião.
Escreva a fórmula química desse ião.
- Cl+ (g)
A energia de ionização é a energia mínima necessária para remover um eletrão de um átomo de cloro, em fase gasosa, no estado fundamental: é a energia mínima que o átomo de cloro, no estado fundamental, tem de absorver para que ocorra o processo.
- Cl (g) ⟶ Cl+(g) + e−
- Cl+ …………. 5 pontos
Nota – A escrita de uma equação química que traduza a formação do ião Cl+ a partir do respetivo átomo não implica qualquer desvalorização.
2. Considere uma mistura gasosa constituída por 5,00 x 10-2 mol de F2(g) e 8,00 x 10-2 mol de Cl2(g), nas condições normais de pressão e de temperatura.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2.1. Quantos átomos de flúor existem na mistura gasosa?
Uma molécula de flúor, F2, tem 2 átomos.
O número de moléculas :
- N = n × NA
O número total de átomos é
- 2N = 2 × n × NA = 2 × 5,00 × 10–2 mol × 6,02 × 1023 mol–1 = 6,02 × 1022 átomos F
- 6,02 × 1022 átomos (ou equivalente) ………….. 5 pontos
Notas:
– A omissão da palavra «átomos» não implica, por si só, qualquer desvalorização.
– A apresentação do valor solicitado com um número incorreto de algarismos significativos não implica qualquer desvalorização.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2.2. Determine a densidade da mistura gasosa, nas condições de pressão e de temperatura referidas.
Apresente todas as etapas de resolução.
Massa molares do F2 e do Cl2:
- M(F2) = 19,0 x 2 = 38,0 g/mol
- M(Cl2) = 35,45 x 2 = 70,9 g/mol
⇒ Massa total:
- m = m(F2) + m(Cl2) = 5,00 x 10-2 x 38 + 8,00 x 10-2 x 70,9 = 7,572 g
⇒ Volume dos gases:
- V = V(F2) + V(Cl2) = n x Vm = (5,00 x 10-2 x 38 + 8,00 x 10-2 ) x 22,4 = 2,912 dm3
⇒ Cálculo da massa volúmica:
- ρ = m/V = 7,572 /2,912 = 2,60 g/dm3
- Etapas de resolução:
A) Cálculo da massa da mistura gasosa (m = 7,572 g) …….. 4 pontos
B)Cálculo do volume da mistura gasosa, nas condições de pressão e de temperatura consideradas (V = 2,912 dm3) …….. 3 pontos
C) Cálculo da densidade da mistura gasosa, nas condições de pressão e de temperatura consideradas ( ρ = 2,60 g dm-3 ) …….. 3 pontos
OU
A)Cálculo da densidade do F2 (g), nas condições de pressão e de temperatura consideradas (ρ = 1,696 g dm-3 ) ……..3 pontos
B) Cálculo da densidade do Cl2 (g), nas condições de pressão e de temperatura consideradas (ρ = 3,165 g dm-3 ) ……..3 pontos
C) Cálculo da densidade da mistura gasosa, nas condições de pressão e de temperatura consideradas, a partir da média ponderada das densidades dos gases constituintes da mistura ( ρ = 2,60 g dm-3) ……..4 pontos
3. Os átomos dos halogéneos podem ligar-se a átomos de hidrogénio, originando compostos designados por halogenetos de hidrogénio, como, por exemplo, o cloreto de hidrogénio, HCl, e o iodeto de hidrogénio, HI.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
3.1. Quantos eletrões de valência existem, no total, na molécula de HCl?
- Oito
⇒ O átomo de cloro, Cl, sendo do grupo 17 tem 7 eletrões de valência, e o de hidrogénio, H, do grupo 1, tem 1.
⇒ A molécula de HCl terá 8 eletrões de valência.
- Oito [eletrões] ou quatro pares [de eletrões] …………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
3.2. O cloro antecede o iodo no mesmo _____ da tabela periódica, o que permite prever que o comprimento da ligação H – Cl deverá ser ____ do que o comprimento da ligação H – I.
(A) grupo … maior
(B) grupo … menor
(C) período … menor
(D) período … maior
- Opção (B)
⇒ O cloro, Cl, antecede o iodo, I, no grupo 17 da Tabela Periódica, apresentando menor raio dado que no grupo quando o número atómico diminui, o raio atómico também diminui.
⇒ Como o raio do átomo Cl é menor do que o do átomo I, o comprimento da ligação H— Cl é também menor do que o comprimento da ligação H— I.
- Opção (B) …………. 5 pontos
GRUPO V
O iodo, I2, reage com o hidrogénio, H2, em fase gasosa, formando-se iodeto de hidrogénio, HI(g). A reação pode ser traduzida por
I2 (g) + H2 (g) ⇋ 2 HI (g)
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
1. Na reação de formação do HI considerada, a variação do número de oxidação do iodo é ____ , sendo a espécie I2 o agente _____ .
(A) +1 … oxidante
(B) -1 … oxidante
(C) +1 … redutor
(D) -1 … redutor
- Opção (B)
⇒ O número de oxidação do iodo na espécie I2 é 0 e em HI é −1, logo, a variação do número de oxidação do iodo é −1 − 0 = −1.
⇒ Como o número de oxidação do iodo diminui, significa que a espécie I2 é reduzida, logo a outra espécie, H2, será oxidada ao reagir com I2.
Portanto, I2 atua como oxidante.
- Opção (B)…………. 5 pontos
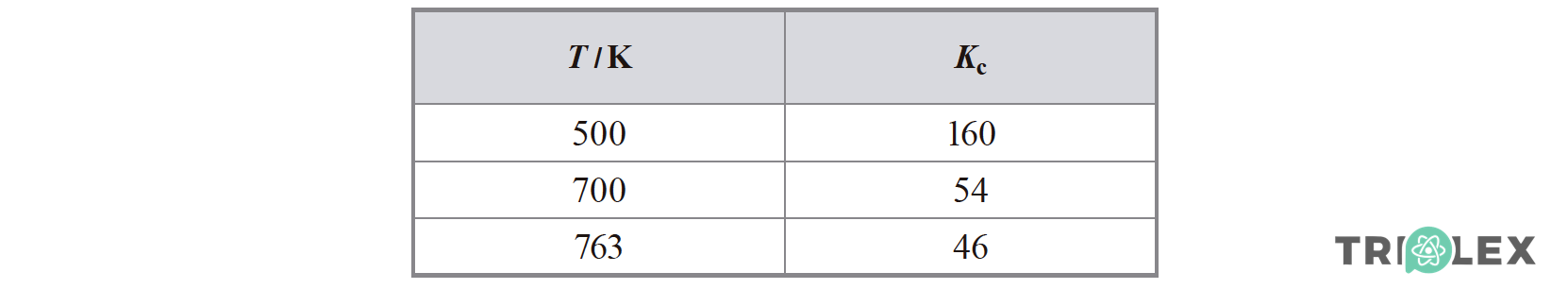
2. Na tabela seguinte, estão registados os valores da constante de equilíbrio, Kc, da reação de formação do HI(g) considerada, a três temperaturas diferentes.
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
2.1. Considere que, num reator com a capacidade de 1,00 L, foram inicialmente introduzidas 2,56 x 10-3 mol de I2(g) e uma certa quantidade de H2(g). Considere ainda que, no início, não existia HI(g) no reator.
Quando, a 763 K, o sistema atingiu um estado de equilíbrio, a quantidade de I2(g) que existia no reator era 1,46 x 10-3 mol.
Calcule a quantidade, em mol, de H2(g) que deverá existir no reator quando o sistema está em equilíbrio àquela temperatura.
Apresente todas as etapas de resolução.
- Etapas de resolução:
A) Determinação da quantidade de I2(g) que reagiu (n = 1,100 × 10-3 mol ) …….. 3 pontos
B) Determinação da quantidade de HI(g) que se terá formado (n = 2,200 × 10-3 mol) …….. 2 pontos
C)Determinação da concentração de equilíbrio de H2(g) , a 763K ([H2] = 7,21 × 10-5 mol dm-3) …….. 3 pontos
D) Determinação da quantidade de H2(g) que deverá existir no reator (n = 7,2 × 10-5 mol) …….. 2 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
2.2. Compare a energia absorvida na quebra das ligações com a energia libertada no estabelecimento das ligações, na reação química considerada.
Fundamente a sua resposta com base na variação da constante de equilíbrio da reação com a temperatura.
⇒ A constante de equilíbrio, Kc diminui com o aumento da temperatura T, o que significa que com o aumento de temperatura a reação inversa é favorecida.
⇒ De acordo com o Princípio de Le Châtelier, o aumento da temperatura favorece a reação endotérmica.
⇒ Sendo a reação inversa endotérmica, a direta, a da formação de HI, é exotérmica. Na reação direta há libertação de energia.
⇒ A energia libertada na formação das ligações nas moléculas de HI é superior à energia absorvida na quebra das ligações nas moléculas de H2 e de I2.
- A resposta integra os tópicos de referência seguintes ou outros de conteúdo equivalente:
A)A constante de equilíbrio da reação diminui à medida que a temperatura aumenta, o que significa que o aumento de temperatura favorece a reação inversa.
B) Como [, de acordo com o Princípio de Le Châtelier,] um aumento de temperatura favorece a reação endotérmica, conclui-se que a reação direta é exotérmica.
C)Assim, [para a reação considerada,] a energia absorvida [na quebra das ligações] será menor do que a energia libertada [no estabelecimento das ligações].

GRUPO VI
Com o objetivo de determinar a concentração de uma solução de ácido clorídrico, HCl(aq), um grupo de alunos titulou 50,00 cm3 dessa solução com uma solução padrão de hidróxido de sódio, NaOH(aq), de concentração 1,00 x 10-1 mol dm-3.
A reação que ocorre pode ser traduzida por
NaOH (aq) + HCl (aq) → NaCl (aq) + H2O (l)
Os alunos gastaram 24,60 cm3 da solução padrão de NaOH até ao ponto final da titulação.
- 11ºano – Física – A.l. – Medições
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- 11ºano – Química – A.l. – 2.1 – Titulação ácido-base
1. Qual é o instrumento que deve ser utilizado para, de forma regular e controlada, adicionar ao titulado pequenos volumes da solução padrão de NaOH?
(A) Bureta.
(B) Pipeta.
(C) Balão de erlenmeyer.
(D) Proveta.
- Opção (A)
⇒ A bureta contém uma escala graduada rigorosa, geralmente em cm3, possuindo na extremidade inferior uma torneira de precisão que permite adicionar pequenos volumes de titulante na vizinhança do ponto final da titulação.
- Opção (A) …………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- 11ºano – Química – A.l. – 2.1 – Titulação ácido-base
2. Calcule a concentração, em mol dm-3, da solução de HCl.
Comece por calcular a quantidade de NaOH adicionada até ao ponto final da titulação.
Apresente todas as etapas de resolução.
⇒ Cálculo da quantidade de NaOH adicionada até ao ponto final da titulação:
- nNaOH = [NaOH]/VNaOH = 1,00 × 10–1 mol dm–3 × 24,60 × 10–3 dm3 = 2,46 × 10–3 mol
⇒ O excesso, ou defeito, da quantidade de HCl que possa existir no ponto final da titulação relativamente ao ponto de equivalência é desprezável, dado que a variação de pH é brusca no ponto final da titulação, mudando o indicador de cor com um incremento de volume de titulante desprezável face ao volume total de titulante.
⇒ No ponto de equivalência, como a estequiométrica é de 1 mol de NaOH para 1 mol de HCl, pode tomar-se a quantidade de NaOH como sendo aproximadamente igual à de HCl.
⇒ No ponto de equivalência, nHCl = 2,46 × 10–3 mol.
⇒ Cálculo da concentração de HCl:
- nHCl = [HCl] x VHCl ⇒ 2,46 × 10–3 mol = [HCl] × 50,00 × 10–3 dm3 ⇒ [HCl] = = 4,92 × 10–2 mol dm–3
- Etapas de resolução:
A) Determinação da quantidade de NaOH adicionada até ao ponto final da titulação (n = 2,460 × 10-3 mol) …….. 5 pontos
B)Determinação da concentração da solução de HCl (c = 4,92 × 10-2 mol dm-3) …….. 5 pontos
Nota – A apresentação dos valores solicitados com um número incorreto de algarismos significativos não implica qualquer desvalorização.
3. Depois de terem realizado a titulação e determinado a concentração da solução de ácido clorídrico, o professor disse aos alunos que a solução de HCl que tinham utilizado era uma solução padrão.
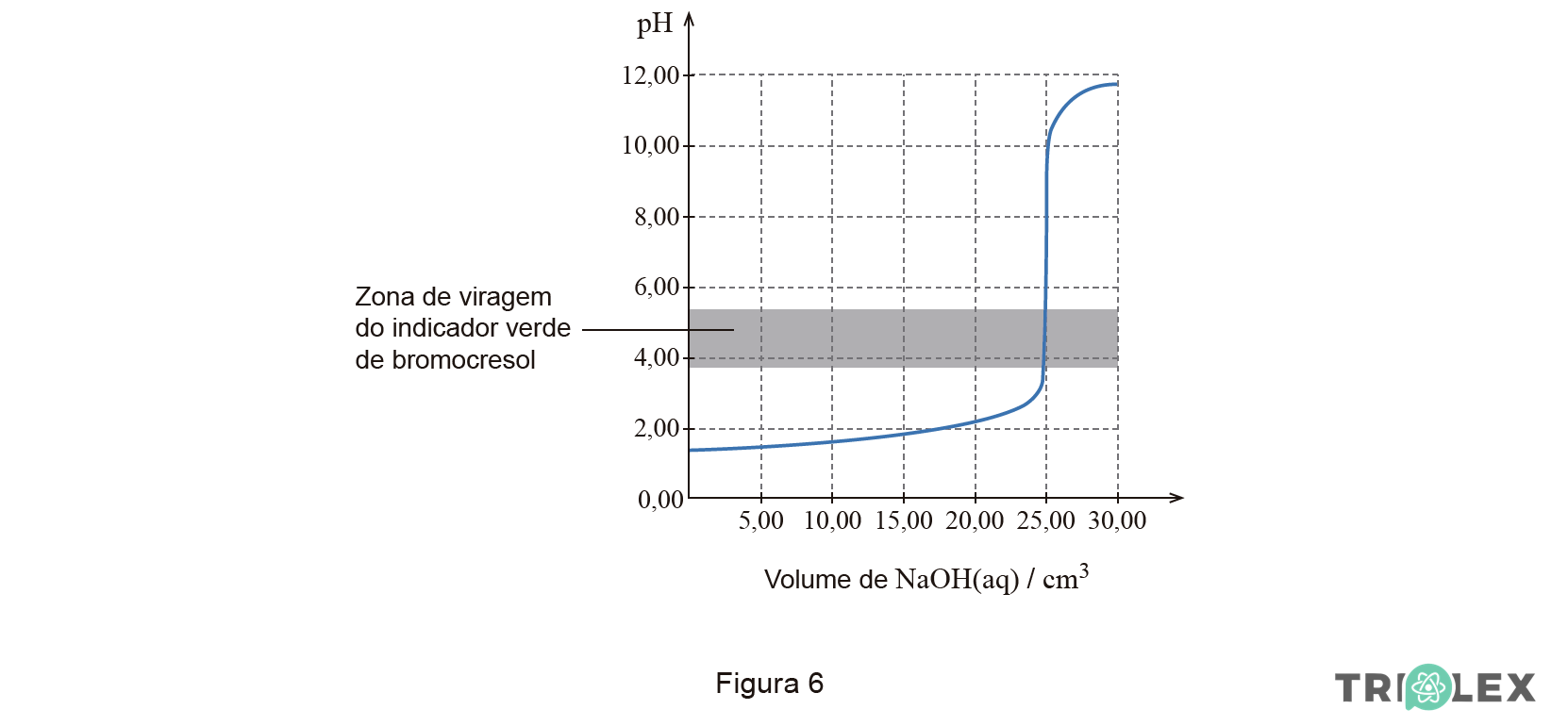
Na Figura 6, está representada a curva teórica da titulação de 50,00 cm3 dessa solução padrão de HCl com uma solução padrão de NaOH 1,00 x 10-1 mol dm-3.
Na curva, está assinalada a zona de viragem do indicador de ácido-base verde de bromocresol.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- 11ºano – Química – A.l. – 2.1 – Titulação ácido-base
3.1. Apresente uma expressão numérica que permita calcular o erro relativo, em percentagem, cometido pelos alunos na medição do volume de titulante gasto até ao ponto final da titulação.
- …………………………………………… 5 pontos

- Ou

- Ou

- Ou

Notas:
– A apresentação de uma expressão numérica que conduza a um erro relativo, em percentagem, simétrico do erro relativo cometido na medição não implica qualquer desvalorização.
– A apresentação de uma expressão numérica que conduza a um erro relativo que não esteja expresso em percentagem implica uma desvalorização de 2 pontos.
– O cálculo do erro relativo, em percentagem, não implica, por si só, qualquer desvalorização desde que a expressão numérica solicitada seja apresentada.
– A apresentação de valores numéricos com um número incorreto de algarismos significativos não implica qualquer desvalorização, desde que essas incorreções decorram apenas da supressão de zeros nos valores numéricos apresentados.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- 11ºano – Química – A.l. – 2.1 – Titulação ácido-base
3.2. Com base na informação fornecida na Figura 6, justifique a seguinte afirmação.
O indicador verde de bromocresol pode ser utilizado para assinalar o ponto de equivalência da titulação em causa.
⇒ pH no ponto de equivalência está incluído na região de variação brusca de pH.
⇒ Como a zona de viragem do verde de bromocresol (pH=3,8 a pH=5,5) está contida na região de variação brusca de pH (pH=3,5 a pH=10,0), [3,8; 5,5] ⊂ [3,5; 10,5], este indicador pode ser utilizado para assinalar o ponto de equivalência da titulação.
- A resposta integra os tópicos de referência seguintes ou outros de conteúdo equivalente:
A) [A figura mostra que na titulação em causa,] ocorre uma variação acentuada de pH na vizinhança do ponto de equivalência.
B)[Como] a zona de viragem do indicador [verde de bromocresol] está contida no intervalo de pH que corresponde àquela variação [, este indicador pode ser utilizado para assinalar o ponto de equivalência da titulação em causa].

FIM