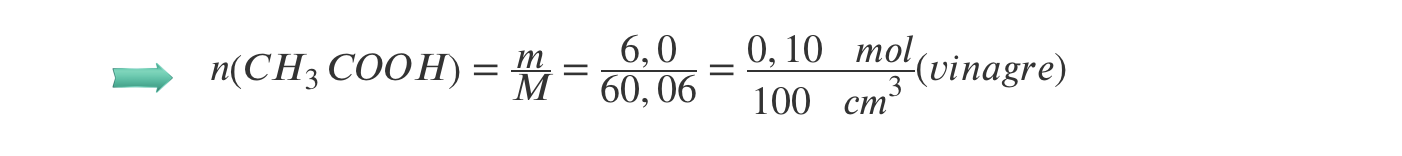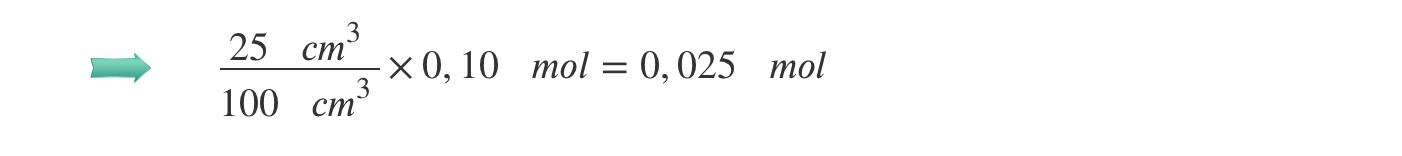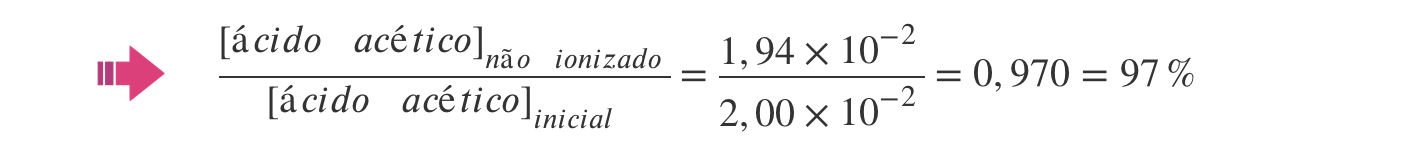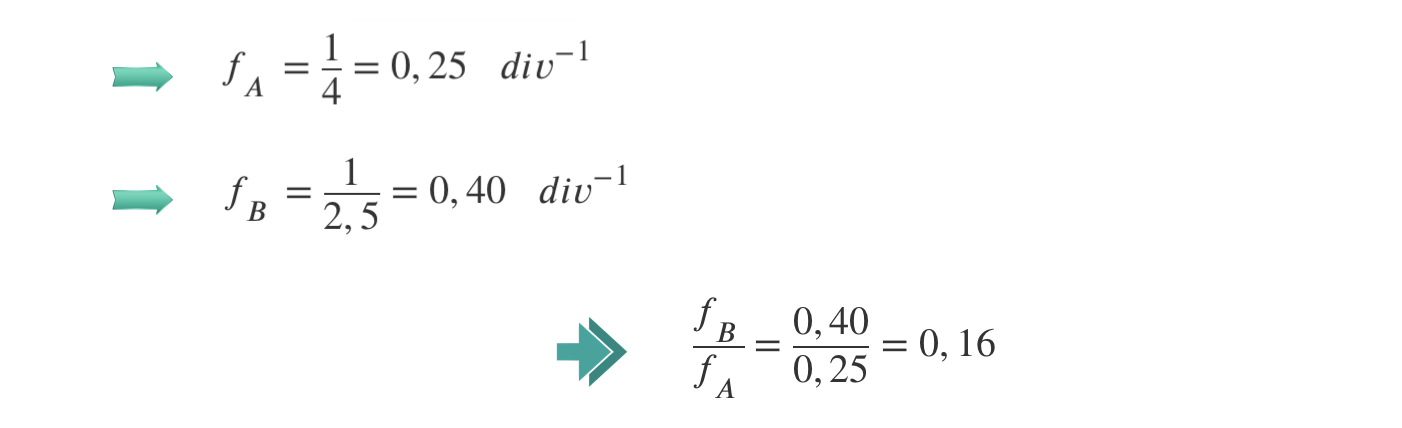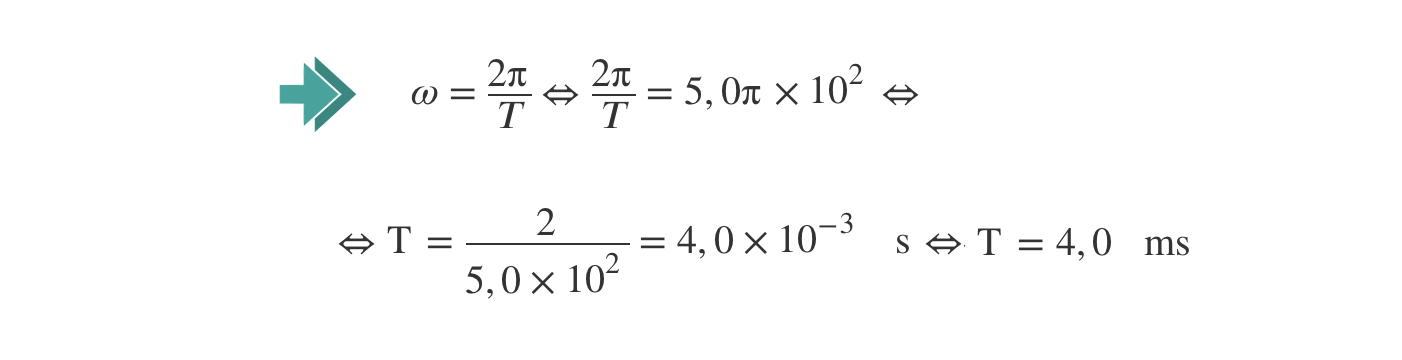2013 – Época Especial – Prova Escrita de Física e Química A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: Época especial – 2013
GRUPO I
Na sua obra Princípios Matemáticos de Filosofia Natural, editada pela primeira vez em 1687, Newton estabeleceu as três leis da Dinâmica e mostrou que tanto a queda de um corpo à superfície da Terra (por exemplo, a queda de um fruto da árvore para o solo) como o movimento da Lua na sua órbita podem ser explicados pela existência de uma força, resultante da interação entre cada um desses corpos e a Terra.
Essa força depende das massas dos dois corpos que interatuam e da distância entre os seus centros de massa.
Assim, um fruto cai da árvore porque é atraído para a Terra. Mas, embora tendo uma massa muito inferior à da Terra, também o fruto atrai a Terra.
M. Ferreira, G. Almeida, Introdução à Astronomia e às Observações Astronómicas, Plátano Edições Técnicas, 6.ª ed., 2001 (adaptado)
- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
1. Considere que m representa a massa de um fruto que se encontra acima da superfície da Terra e que d representa a distância entre o centro de massa do fruto e o centro de massa da Terra.
A intensidade da força com que a Terra atrai esse fruto é
(A) inversamente proporcional a m.
(B) diretamente proporcional a d.
(C) diretamente proporcional a m2.
(D) inversamente proporcional a d2.
- Opção (D)
A intensidade da força com que a Terra atrai o fruto, a intensidade da força gravítica, é:
Da análise desta expressão conclui-se que a intensidade da força com que a Terra atrai o fruto é diretamente proporcional à sua massa, m, e inversamente proporcional ao quadrado da distância que o separa do centro da Terra.
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
2. A força com que a Terra atrai um fruto e a força com que esse fruto atrai a Terra têm intensidades
(A) iguais e determinam acelerações de módulos diferentes em cada um desses corpos.
(B) iguais e determinam acelerações de módulos iguais em cada um desses corpos.
(C) diferentes e determinam acelerações de módulos diferentes em cada um desses corpos.
(D) diferentes e determinam acelerações de módulos iguais em cada um desses corpos.
- Opção (A)
A força exercida pela Terra sobre o fruto e a exercida por este sobre a Terra são um par ação-reação, pelo que têm a mesma intensidade.
Da 2ª lei de Newton, FR = m a, conclui-se que o módulo da aceleração adquirida pelo fruto é muito superior ao módulo da aceleração adquirida pela Terra, dado que a massa desta é muito superior à do fruto.
- Opção (A)…………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
3. Conclua, justificando, se o trabalho realizado pelo peso de um fruto que cai da árvore para o solo depende da forma da trajetória descrita pelo fruto.
⇒ O peso é uma força conservativa e o trabalho realizado por uma força conservativa é independente da trajetória, depende apenas das posições final e inicial.
⇒ Quando o fruto cai da árvore para o chão, o trabalho que realiza depende apenas da diferença de altura entre a sua posição inicial, na árvore, e a sua posição final, no chão, pelo que é independente da trajetória que descreve durante a queda.
- Na resposta, são apresentados os seguintes tópicos:
A) O trabalho realizado pelo peso do fruto é simétrico da variação da energia potencial do sistema fruto + Terra.
B) Como esta variação da energia potencial depende apenas da diferença de altura entre as posições inicial e final do fruto, conclui-se que o trabalho realizado pelo peso de um fruto, quando este cai da árvore para o solo, é independente da forma da trajetória descrita pelo fruto.
ou
A) O peso é uma força conservativa.
B) Assim, o trabalho realizado pelo peso do fruto depende apenas da diferença de altura entre as posições inicial e final do fruto, pelo que se conclui que o trabalho realizado pelo peso de um fruto, quando este cai da árvore para o solo, é independente da forma da trajetória descrita pelo fruto.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
4. Considere um fruto que cai de uma árvore, abandonado de uma posição situada a 1,60 m acima do solo.
Admita que a resistência do ar é desprezável e que o fruto pode ser representado pelo seu centro de massa (modelo da partícula material).
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
4.1 Qual é o esboço do gráfico que pode representar o modo como varia a energia cinética, Ec, do fruto em função do tempo, t, durante a queda?
- Opção (B)
Durante a queda, a energia cinética do fruto é, em cada instante:
e o módulo da sua velocidade é:
v = g t
Substituindo esta expressão na da energia cinética, tem-se:
Da análise de Ec = f (t), conclui-se que o gráfico que melhor traduz a variação da energia cinética durante a queda do fruto, em função do tempo, é o representado pelo ramo de uma parábola.
- Opção (B)…………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
4.2 Qual é o módulo da velocidade com que o fruto passa na posição situada a 0,70 m do solo?
(A) v = 5,6 m s−1
(B) v = 4,2 m s−1
(C) v = 3,7 m s−1
(D) v = 2,6 m s−1
- Opção (B)…………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
4.3 Admita que, no seu movimento de translação em torno da Terra, a Lua descreve uma órbita circular, de raio 3,84 × 105 km.
Determine o quociente entre o módulo da aceleração da Lua, no movimento de translação referido, e o módulo da aceleração do fruto, no movimento de queda considerado.
Apresente todas as etapas de resolução.
Massa da Lua = 7,35 × 1022 kg
Massa da Terra = 5,98 × 1024 kg
- R = 3,84 x 105 km;
- mLua = 7,35 x 1022 kg;
- mTerra = 5,98 x 1024 kg
- G = 6,67 x 10-11 N m2 kg-2;
- g = 10 m s–2
A aceleração do fruto, afruto, durante o movimento de queda é igual à aceleração gravítica, g.
A resultante das forças que atuam sobre a Lua, no seu movimento de translação em torno da Terra, é igual à força gravítica.
- A razão entre os módulos da aceleração da Lua e da aceleração do fruto é igual a 2,7 x 10-4.
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Cálculo da intensidade da força gravítica exercida pela Terra sobre a Lua (Fg = 1,988 x 1020 N).
B) Cálculo do módulo da aceleração da Lua, no movimento de translação referido (a = 2,70 x 10-3 m s-2).
C) Determinação do quociente entre o módulo da aceleração da Lua, no movimento de translação referido, e o módulo da aceleração do fruto, no movimento de queda considerado (aLua /afruto = 2,7 x 10-4)
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
GRUPO II
O planeta Terra é um sistema que recebe energia quase exclusivamente do Sol. Dessa energia, recebida sob a forma de radiação, cerca de 50% é absorvida pela superfície da Terra, cerca de 20% é absorvida pela sua atmosfera e cerca de 30% é refletida para o espaço.
1. O albedo médio da Terra é, assim, cerca de
(A) 70%
(B) 50%
(C) 30%
(D) 20%
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
O albedo é a refletividade média da Terra, ou seja, a fração da radiação solar incidente que é refletida pela Terra.
De acordo com o texto, da radiação solar incidente a Terra reflete 30%, isto é o albedo é de 30%,
- Opção (C)…………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2. Qual é a relação entre a potência da radiação absorvida pelo planeta Terra e a potência da radiação emitida pelo planeta Terra para o espaço?
Como a Terra está em equilíbrio térmico, então a potência da radiação solar que absorve é igual à potência da radiação que emite para o Espaço.
- A potência da radiação absorvida [pelo planeta Terra] é igual à potência da radiação emitida [pelo planeta Terra para o espaço]. …………. 5 pontos
3. Justifique a afirmação seguinte.
O comprimento de onda da radiação de máxima intensidade emitida pelo Sol é muito inferior ao comprimento de onda da radiação de máxima intensidade emitida pela Terra.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
Segundo a lei de Wien, λT = b, o comprimento de onda da radiação de máxima intensidade emitida por um corpo, em equilíbrio térmico, é inversamente proporcional à sua temperatura absoluta.
Assim, como a temperatura média da superfície solar (cerca de 5800 K) é muito superior à temperatura média da superfície terrestre (cerca de 257 K), então o comprimento de onda da radiação de máxima intensidade emitida pelo Sol é muito inferior (banda do visível) ao comprimento de onda da radiação de máxima intensidade emitida pela Terra (banda do infravermelho).
- Na resposta, são apresentados os seguintes tópicos:
A) [De acordo com a lei de Wien,] o comprimento de onda da radiação de máxima intensidade emitida por um corpo é inversamente proporcional à temperatura absoluta desse corpo.
B) A temperatura média da superfície do Sol é muito superior à temperatura média da superfície da Terra. [Assim, o comprimento de onda da radiação de máxima intensidade emitida pelo Sol é muito inferior ao comprimento de onda da radiação de máxima intensidade emitida pela Terra].
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
GRUPO III
1. O metano, CH4, principal constituinte do gás natural, é um combustível muito usado.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
1.1 Represente a molécula de metano, utilizando a notação de Lewis. Refira o número total de eletrões de valência ligantes dessa molécula.
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
1.2. A combustão completa do metano pode ser representada por
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (g) ΔH = -802 kJ mol -1
Calcule a energia libertada quando, por combustão completa de metano, se consomem 2,0 m3 de oxigénio, em condições normais de pressão e de temperatura.
Apresente todas as etapas de resolução.
A equação química mostra que se consomem duas moles de dioxigénio quando se dá a combustão de uma mole de metano.
ΔH = – 802 kJ / mol de reação = – 802 kJ / mol de CH4 = – 802 kJ / 2 mol de O2
Por cada mole de O2 consumido libertam-se 401 kJ.
A quantidade de O2 existente em 2,0 m3 desse gás pode calcular-se a partir do volume molar, dado que n (O2) = V/Vm.
Como, em condições normais de pressão e temperatura Vm = 22,4 dm3 mol-1, vem:
A quantidade de calor libertado, Q, por reação desta quantidade de oxigénio calcula-se a partir da variação de entalpia:
- Q = n (O2) x ΔH = 89,3 mol x (- 401 kJ mol-1) = – 3,6 x 104 kJ
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Determinação da quantidade de oxigénio existente em 2,0 m3 desse gás, em condições normais de pressão e de temperatura (n = 89,3 mol).
B) Determinação da energia libertada por reação dessa quantidade de oxigénio (E = 3,6 x 104 kJ)
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
2. O metano pode ser usado como combustível no aquecimento de um bloco de chumbo.
2.1. Admita que o bloco de chumbo se encontra inicialmente à temperatura de 0 °C.
A essa temperatura, o bloco
(A) emite um conjunto de radiações que constitui um espectro descontínuo.
(B) emite radiação de uma única frequência.
(C) não emite qualquer radiação.
(D) emite um conjunto de radiações que constitui um espectro contínuo.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (D)
Qualquer corpo, em equilíbrio térmico, emite radiação – radiação térmica –, que depende da sua temperatura, cujo espetro é contínuo.
- Opção (D)…………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2.2. Na tabela seguinte, estão registadas as elevações de temperatura, Δϴ, do bloco de chumbo, de massa 3,2 kg, em função da energia, E, que lhe é fornecida.
Determine a capacidade térmica mássica do chumbo.
Comece por apresentar a equação da reta que melhor se ajusta ao conjunto de valores apresentados na tabela, referente ao gráfico da elevação de temperatura do bloco de chumbo, em função da energia que lhe é fornecida (utilize a calculadora gráfica).
Apresente todas as etapas de resolução.
- m = 3,2 kg
- c = ?
A expressão que relaciona a energia fornecida ao bloco de chumbo, em função da elevação da sua temperatura, é:
E = m c Δθ
então, a equação da reta que traduz Δθ = f (E) é:
o declive da reta:
Assim, recorrendo à calculadora gráfica, Δθ = f (E), é:
- Δθ = 2,46 x 10-3 E (SI)
Donde se conclui que:
A capacidade térmica mássica do chumbo é de cerca de 1,3 x 102 J kg-1 °C-1.
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Apresentação da equação da reta que melhor se ajusta ao conjunto de valores apresentados na tabela, referente ao gráfico da elevação da temperatura do bloco de chumbo, em função da energia que lhe é fornecida (Δθ = 2,46 x 10-3 E ou y = 2,46 x 10-3 x).
B) Cálculo da capacidade térmica mássica do chumbo, a partir do declive da reta obtida (c = 1,3 x 102 J kg-1 ºC-1).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
GRUPO IV
O vinho é uma mistura líquida essencialmente constituída por água e etanol, embora nela existam também outras substâncias dissolvidas. A oxidação do etanol pode dar origem à formação do ácido acético, um dos constituintes dos vinagres.
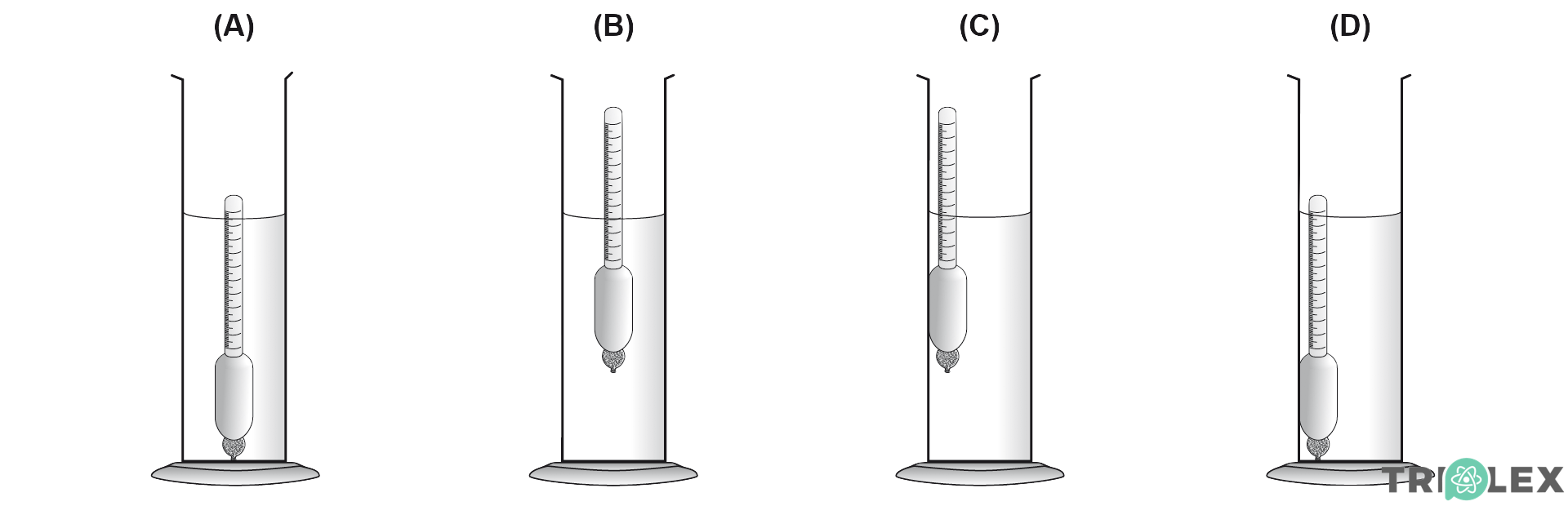
1. Pretende-se medir a densidade (ou massa volúmica) de um vinho, utilizando um densímetro.
Em qual dos esquemas seguintes se encontra corretamente representada a posição do densímetro quando se pretende efetuar aquela medição?
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B)
- As restantes opções são incorretas pelas seguintes razões:
(A) e (D) utilizam um densímetro inadequado, próprio para um líquido de maior densidade que o vinho; (C) apresenta o densímetro encostado à parede da proveta, o que, por questões de tensão superficial, pode acarretar erros na densidade lida pelo instrumento.
- Opção (B)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2. O grau de acidez de um vinagre é expresso em termos da massa de ácido acético, CH3COOH (M = 60,06 g mol-1), em gramas, dissolvida em 100 cm3 desse vinagre.
Um vinagre comercial de grau de acidez 6,0% é diluído 20 vezes, preparando-se um volume total de 500,0 cm3 de solução diluída.
Determine a quantidade de ácido acético dissolvida na solução diluída de vinagre.
Apresente todas as etapas de resolução.
Grau de acidez do vinagre = 6,0% = 6,0 g (CH3COOH) / 100 cm3 (vinagre)
A quantidade de ácido acético dissolvida em 100 cm3 de vinagre é:
Por diluição de 20 vezes a mesma quantidade de vinagre, passou a existir num volume 20 vezes maior, ou seja, o fator de diluição, f, é igual a 20.
Como se pretende preparar 500,0 cm3 de solução diluída, e f = Vdil / Vcon, deveríamos ter partido de 500/20 cm3 de vinagre concentrado, ou seja, 25,0 cm3.
A quantidade de ácido acético contida em 25,0 cm3 deste vinagre comercial é, assim:
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Cálculo da massa de ácido acético dissolvida em 500,0 cm3 da solução diluída de vinagre (m = 1,50 g).
B) Cálculo da quantidade de ácido acético dissolvida na solução diluída de vinagre (n = 2,5 x 10-2 mol).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
3. O ácido acético é um ácido monoprótico fraco, cuja reação de ionização em água pode ser traduzida por
CH3COOH (aq) + H2O (l) ⇋ CH3COO– (aq) + H3O+ (aq)
Considere uma solução 0,0200 mol dm-3 de ácido acético, CH3COOH (aq), cujo pH, a 25 ºC, é 3,23.
Determine a percentagem de ácido acético não ionizado na solução.
Apresente todas as etapas de resolução.
- pH (CH3COOH (aq)) = 3,23 a 25 °C
De acordo com a definição de pH, pH = – log [H3O+], podemos calcular a concentração hidrogeniónica da solução:
- [H3O+] = 10-pH = 10-3,23 = 5,89 x 10-4 mol dm-3
Desprezando a quantidade de H3O+ proveniente da autoionização da água, e de acordo com a equação que traduz a reação de ionização em água do ácido acético, podemos supor que:
- [CH3COO–]e = [H3O+ ]e = 5,89 x 10-4 mol dm-3
- [CH3COOH]ionizado = [CH3COO– ]e
Como [CH3COOH]não ionizado = [CH3COOH]inicial – [CH3COOH]ionizado , vem:
[CH3COOH]não ionizado = (0,0200 – 5,89 x 10-4) mol dm-3 = 1,94 x 10-2 mol dm-3
A percentagem de ácido acético não ionizado na solução é, então:
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Cálculo da concentração de ácido acético ionizado na solução (c = 5,888 x 10-4 mol dm-3).
B) Cálculo da percentagem de ácido acético não ionizado na solução (97,0%).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
GRUPO V
Na titulação de uma solução de ácido acético, CH3COOH (aq), com uma solução de hidróxido de sódio, NaOH(aq), uma base forte, a reação que ocorre pode ser traduzida por
CH3COOH (aq) + NaOH (aq) → NaCH3COO (aq) + H2O (l)
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1. Considere que o volume de solução de ácido acético a titular é 25,0 cm3 e que se adicionou 50,0 cm3 de NaOH(aq) de concentração 0,100 moldm-3 até ser atingido o ponto de equivalência da titulação.
Determine a concentração da solução de ácido acético.
Comece por calcular a quantidade de NaOH adicionada até ter sido atingido o ponto de equivalência da titulação.
Apresente todas as etapas de resolução.
Quantidade de solução de NaHO (aq) adicionada até se atingir o ponto de equivalência da titulação:
- n (NaHO) = V x c = 0,0500 dm3 x 0,100 mol dm-3 = 5,00 x 10-3 mol
Como a proporção estequiométrica entre os reagentes da reação ácido-base referente à titulação ocorrida é de 1:1, a quantidade estequiometricamente equivalente de ácido é também igual a 5,00 x 10-3 mol, que existiam inicialmente em 25,0 cm3 de solução de ácido acético.
Como c = n/V, a concentração inicial desta solução de ácido acético é, então:
- Na resposta, são apresentados as seguintes etapas de resolução:
A) Cálculo da quantidade de NaOH adicionada até ter sido atingido o ponto de equivalência da titulação (n = 5,000 x 10-3 mol).
B) Cálculo da concentração da solução de ácido acético (c = 2,00 x 10-1 mol dm-3).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
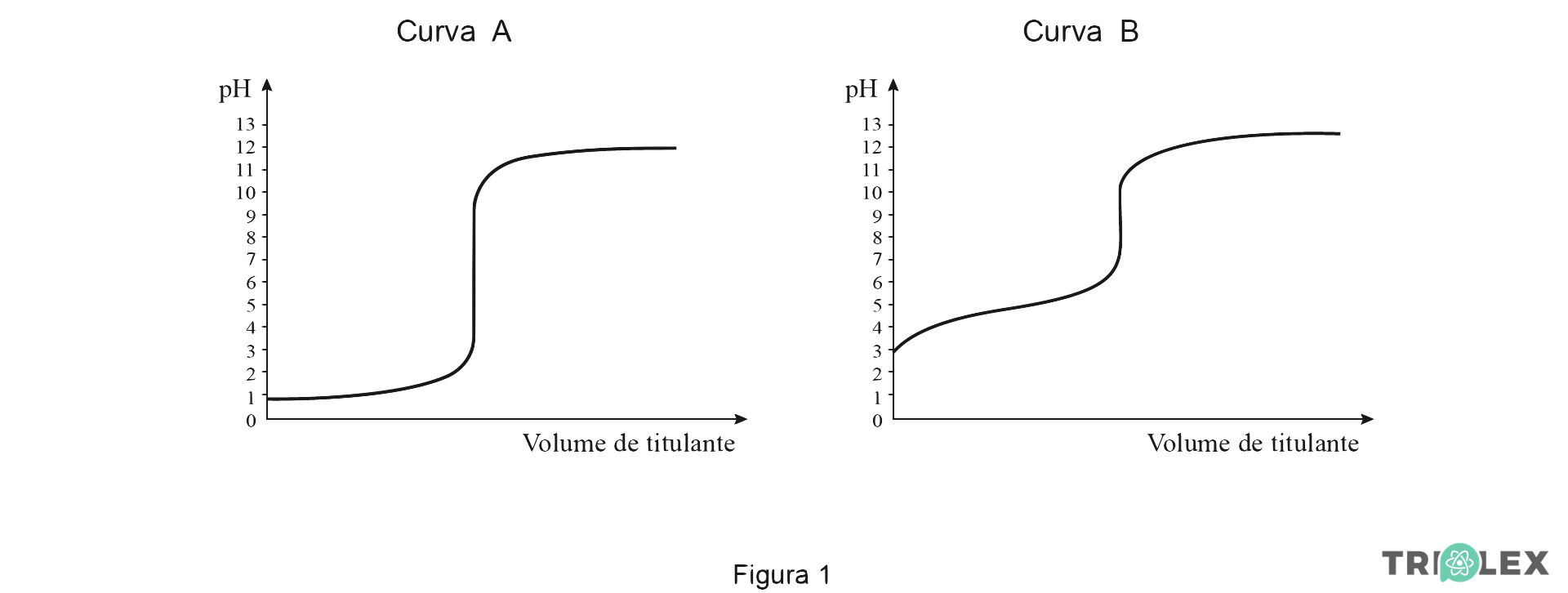
2. Na Figura 1, estão representadas uma curva de titulação de um ácido forte com uma base forte (Curva A) e uma curva de titulação de um ácido fraco com uma base forte (Curva B).
Conclua, justificando, a partir das curvas de titulação apresentadas, em qual das situações o número de indicadores ácido-base suscetíveis de serem utilizados será mais reduzido.
Comece por referir qual a função de um indicador ácido-base, numa titulação.
Numa titulação, a função de um indicador é detetar o ponto de equivalência da respetiva titulação.
Como a zona de viragem de um indicador utilizado numa titulação deve estar totalmente contida na zona de variação brusca de pH, a titulação correspondente à curva A, em que a variação brusca de pH na vizinhança do ponto de equivalência é maior, poderá incluir mais zonas de viragem (ou seja, mais indicadores suscetíveis de serem utilizados) do que a titulação a que corresponde a curva B.
- A resposta deve apresentar os seguintes tópicos:
A) A função de um indicador ácido-base, numa titulação, é assinalar o ponto de equivalência [da titulação].
B) A curva A apresenta [, na vizinhança do ponto de equivalência,] uma variação de pH mais acentuada do que a curva B.
C) Como os indicadores ácido-base suscetíveis de serem utilizados devem ter a sua zona de viragem contida no intervalo correspondente à variação acentuada de pH, conclui-se que na titulação de um ácido fraco com uma base forte, o número de indicadores ácido-base suscetíveis de serem utilizados será mais reduzido.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
GRUPO VI
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
1. Considere a reação química, em fase gasosa, traduzida por
2 NO (g) + Cl2 (g) ⇋ 2 NOCl (g)
Preveja, justificando, como variará a concentração de Cl2 (g) se ocorrer um aumento de pressão, por diminuição do volume, no sistema químico, inicialmente em equilíbrio, à temperatura T.
De acordo com o Princípio de Le Châtelier, se ocorrer um aumento de pressão por diminuição de volume, num sistema em equilíbrio a uma dada temperatura, T, o equilíbrio desloca-se de modo a contrariar o aumento de pressão, isto é, no sentido que conduz à formação de um menor número de moléculas gasosas.
Como todos os intervenientes desta reação química estão no estado gasoso e a reação que conduz a uma diminuição do número de moléculas ocorre no sentido direto, se ocorrer aumento da pressão do sistema por diminuição do volume, o equilíbrio desloca-se neste sentido, diminuindo assim a concentração de Cl2 (e de NO).
- Na resposta, são apresentados os seguintes tópicos:
A) De acordo com o Princípio de Le Châtelier, um aumento de pressão favorece a reação que conduz a uma diminuição da pressão ou a reação que conduz a uma diminuição da quantidade total de gases.
B) Neste caso, a reação que conduz a uma diminuição da pressão ou a reação que conduz a uma diminuição da quantidade total de gases é a reação direta.
C) Prevê-se, assim, que a concentração de Cl2 (g) diminua.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
2. A molécula de Cl2 é constituída por átomos de cloro.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
2.1 Num átomo de cloro, no estado fundamental, o número de orbitais ocupadas é
(A) 3
(B) 5
(C) 8
(D) 9
- Opção (D)
O cloro tem número atómico 17 e localiza-se no grupo 17 e no 3.° período da Tabela Periódica.
A sua configuração eletrónica no estado fundamental é 1s2 2s2 2p6 3s2 3p5, tendo ocupadas 3 orbitais s (1s, 2s e 3s) e 6 orbitais p (2px, 2py, 2pz, 3px, 3py e 3pz), ou seja, um total de 9 orbitais atómicas (uma das orbitais 3p está semipreenchida)
- Opção (D)…………. 5 pontos
2.2 Um dos eletrões de valência menos energéticos de um átomo de cloro, no estado fundamental, pode ser caracterizado pelo conjunto de números quânticos
(A) (3,1, 0, -1/2)
(B) (3,1,1,+1/2)
(C) (3, 0, 0, -1/2)
(D) (3, 0,1, +1/2)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
De acordo com a configuração eletrónica no estado fundamental do elemento cloro, 1s2 2s2 2p6 3s2 3p5, os eletrões de valência do átomo de cloro, ou seja, os eletrões no último nível, ocupam orbitais 3s e 3p.
Se é um dos eletrões de valência menos energéticos, ocupa a orbital 3s (n = 3, l = 0). Como l = 0, o valor de m terá de ser 0 e o valor de s pode ser + 1/2 ou – 1/2, o que está de acordo com a opção (C).
A opção (D) é incorreta porque sendo l = 0, m não pode ser 1.
As opções (A) e (B) também são incorretas porque correspondem a orbitais 3p, que são as orbitais de valência mais energéticas.
- Opção (C)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
2.3 Os átomos de cloro são agentes destruidores da camada de ozono estratosférico.
Um mecanismo reacional que traduz a destruição do ozono pode ser representado pelas seguintes equações:
Cl + O3 → ClO + O2
ClO + O → Cl + O2
Escreva a equação que corresponde à soma destas duas equações.
- O (g) + O3 (g) → O2 (g)
- O (g) + O3 (g) → O2 (g) …………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2.4 Os átomos de cloro podem substituir átomos de hidrogénio nas moléculas dos alcanos, como na molécula a seguir representada.
Qual é o nome do composto acima representado, de acordo com a nomenclatura IUPAC?
(A) 2,3-dicloro-2-metilbutano
(B) 2-cloro-2-metil-3-clorobutano
(C) 2,3-dicloro-3-metilbutano
(D) 2-cloro-3,3-clorometilbutano
- Opção (A)
Deve-se salientar que a cadeia fundamental foi numerada da esquerda para a direita porque assim se atribuem números mais baixos aos substituintes. Os substituintes (cloro e metilo) são indicados por ordem alfabética.
- Opção (A)…………. 5 pontos
GRUPO VII
1. Na Figura 2, estão representados dois sinais elétricos, A e B, visualizados simultaneamente no ecrã de um osciloscópio, com a mesma base de tempo selecionada nos dois canais.
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
1.1 A frequência do sinal B é
(A) 4 vezes superior à frequência do sinal A.
(B) 1,6 vezes inferior à frequência do sinal A.
(C) 1,6 vezes superior à frequência do sinal A.
(D) 4 vezes inferior à frequência do sinal A.
- Opção (C)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
1.2 Verificou-se que o sinal A pode ser descrito pela equação
U = 2,0 sin (5,0 π × 102 t ) (SI)
A base de tempo do osciloscópio estava, assim, regulada para
(A) 0,5 ms / div
(B) 1 ms / div
(C) 2 ms / div
(D) 5 ms / div
- Opção (B)
U = 2,0 sin (5,0 π x 102 t) (SI)
Comparando esta equação com:
- y = A sin (ω t)
verifica-se que:
ω = 5,0 π x 102 rad s-1
O segundo algarismo significativo deste valor é não exato.
Como a base de tempo corresponde a uma divisão que, por sua vez, contempla 5 menores divisões, a base de tempo deve ser 1 ms, pois o menor valor será de 0,2 ms e a incerteza associada à leitura será de 0,1 ms.
- Opção (B)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 2 (Eletromagnetismo)
2. Os microfones de indução permitem converter sinais sonoros em sinais elétricos.
Neste tipo de microfones, a vibração da membrana provoca a oscilação de uma bobina imersa num campo magnético.
Quanto mais rapidamente se movimentar a bobina, maior será
(A) o fluxo magnético através da bobina e menor será a força eletromotriz induzida na bobina.
(B) a taxa de variação temporal do fluxo magnético através da bobina e menor será a força eletromotriz induzida na bobina.
(C) o fluxo magnético através da bobina e maior será a força eletromotriz induzida na bobina.
(D) a taxa de variação temporal do fluxo magnético através da bobina e maior será a força eletromotriz induzida na bobina.
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 2 (Eletromagnetismo)
3. Um campo magnético pode ser criado por um íman, como o representado na Figura 3.
Qual dos seguintes vetores pode representar o campo magnético criado no ponto P pelo íman representado na figura?
- Opção (D)
Como o campo magnético criado entre os ramos de um íman em U é uniforme, com direção perpendicular a estes e sentido do polo norte para o polo sul.
- Opção (D)…………. 5 pontos
FIM