2013 – 2ª Fase – Prova Escrita de Física e Química A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: 2.ª Fase – 2013
GRUPO I
Em 1945, Arthur C. Clarke, numa revista de eletrónica amadora, avançou com uma das maiores ideias das ciências espaciais: o satélite geoestacionário. O artigo especulava sobre a possibilidade de uma rede de satélites fornecer uma cobertura radiofónica à escala mundial.
Um satélite geoestacionário devia situar-se numa órbita especial, a chamada órbita de Clarke. Essa órbita, sobre o equador da Terra e a cerca de 3,6 ×104 km de altitude, está hoje povoada de satélites, não só de comunicações, como de meteorologia. Porquê 3,6 ×104 km? É só fazer as contas, usando a segunda lei de Newton e a lei da gravitação universal. Aprende-se na Física do 11º ano que um satélite a essa altitude demora um dia a dar a volta à Terra. Como a Terra também dá uma volta completa em torno do seu eixo nesse intervalo de tempo, um satélite geoestacionário é visto do equador da Terra como estando permanentemente parado.
Carlos Fiolhais, «Arthur C. Clarke: da órbita ao elevador espacial», Gazeta de Física, vol. 30, n.o 3/4, 2007 (adaptado)
- 11ºano – Física – Domínio 1 – subdomínio 1 (Tempo, posição e velocidade)
1. Considere um local à superfície da Terra situado a 3,6 × 104 km de um satélite geoestacionário.
Qual das expressões seguintes permite calcular o tempo, em segundos (s), que um sinal eletromagnético enviado por esse satélite demora a chegar àquele local?
- Opção (B) …………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2. Verifique, partindo da segunda lei de Newton e da lei da gravitação universal, que um satélite a 3,6 × 104 km de altitude demora um dia a dar a volta à Terra.
Apresente todas as etapas de resolução.
raio da Terra = 6,4 × 106 m
massa da Terra = 5,98 × 1024 kg
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Determinação, a partir da expressão
- do módulo da aceleração do satélite (a = 0,222 m s-2).
B) Determinação do módulo da velocidade do satélite (v = 3,07 × 103 m s-1)
ou
- do módulo da velocidade angular do satélite (ω = 7,23 × 10-5 rad s-1).
C) Determinação do período do movimento de um satélite a 3,6 × 104 km de altitude (T = 8,7 × 104 s = 24 h) (ver nota).
ou
A) Substituição adequada de a por v2/r OU por ω2 r , na expressão
B) Substituição adequada, na expressão obtida,
⇒ de v por
ou
⇒ de ω por
C) Determinação do período do movimento de um satélite a 3,6 × 104 km de altitude (T = 8,7 × 104 s = 24 h) (ver nota).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
Nota – A ausência de conversão de unidades do período do movimento (de segundos a horas ou a dias), ou a ausência de um procedimento equivalente, será considerada um erro de tipo 2.
3. Os satélites estão, geralmente, equipados com painéis fotovoltaicos, que produzem energia elétrica para o funcionamento dos sistemas de bordo.
Considere que a intensidade média da radiação solar, ao nível da órbita de um satélite geoestacionário, é 1,3 × 103 W m-2.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.1 Para que a intensidade média da radiação solar incidente num painel colocado num satélite geoestacionário seja 1,3 × 103 W m-2, esse painel terá de estar orientado segundo um plano
(A) perpendicular à direção da radiação incidente, e poderá ter uma área diferente de 1 m2.
(B) perpendicular à direção da radiação incidente, e terá que ter uma área de 1 m2.
(C) paralelo à direção da radiação incidente, e terá que ter uma área de 1 m2.
(D) paralelo à direção da radiação incidente, e poderá ter uma área diferente de 1 m2.
- Opção (A)
⇒ Para que a intensidade média da radiação solar seja 1,3 x 103 W m-2 é necessário que o painel seja perpendicular à direção da radiação incidente.
⇒ Estando com essa orientação, a área do painel pode ser qualquer dado que para a mesma distância ao Sol a intensidade da radiação incidente no painel é constante.
⇒ A potência média da radiação e a área do painel são, no mesmo local e para a mesma orientação, diretamente proporcionais:
- Opção (A) …………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.2 Admita que um satélite geoestacionário está equipado com um conjunto de painéis fotovoltaicos, adequadamente orientados, de rendimento médio 20% e de área total 12 m2.
Determine a energia elétrica média, em quilowatt-hora (kWh), produzida por aquele conjunto de painéis fotovoltaicos durante um dia.
Apresente todas as etapas de resolução.
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo da potência elétrica média produzida pelo conjunto de painéis fotovoltaicos (P = 3,12 × 103 W).
ou
Cálculo da energia elétrica média que seria produzida pelo conjunto de painéis fotovoltaicos, durante um dia, se o rendimento desse conjunto fosse 100% (E = 1,35 × 109 J ou E = 374 kWh).
B) Cálculo da energia elétrica média, em quilowatt-hora, produzida pelo conjunto de painéis fotovoltaicos durante um dia (E = 75 kW h).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
4. As comunicações via satélite utilizam, geralmente, radiações na gama das micro-ondas.
Indique duas características dessas radiações que as tornam adequadas às comunicações via satélite.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Duas das seguintes características: não se difratam significativamente (propagam-se em linha reta), não se refletem significativamente na ionosfera, não são absorvidas (são pouco absorvidas) pela atmosfera.
- Na resposta, são apresentados dois dos seguintes tópicos:
A) [As radiações micro-ondas] são pouco absorvidas pela atmosfera.
B) [As radiações micro-ondas] não se difratam apreciavelmente na atmosfera.
C) [As radiações micro-ondas] não se refletem apreciavelmente na atmosfera.
ou
- Na resposta, são apresentados os seguintes tópicos:
D) [As radiações micro-ondas] são pouco absorvidas pela atmosfera.
E) [As radiações micro-ondas] propagam-se em linha reta na atmosfera.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
GRUPO II
Nos finais do século XVIII, elevaram-se na atmosfera os primeiros balões, do tipo representado na Figura 1.
A história destes balões foi contada por Rómulo de Carvalho no livro História dos Balões (Atlântida, 1959).
1. Para fazer subir o primeiro balão, de volume aproximado 800 m3, «os inventores colocaram na boca do balão uma grelha de ferro, sobre a qual dispuseram palha e pedaços de lã, […] aos quais lançaram fogo», o que permitiu aquecer gradualmente o ar nele contido.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1.1 Identifique o principal processo de transferência de energia, como calor, que permite o aquecimento de todo o ar contido no balão e descreva o modo como essa transferência ocorre.
⇒ O principal mecanismo de transferência de energia, como calor, que permite o aquecimento de todo o ar é a convecção.
⇒ O ar que se encontra junto ao fogo aquece, tornando-se menos denso, o que dá origem a uma corrente quente ascendente.
⇒ Este ar, ao subir, arrefece, ao transferir energia para o ar que encontra, tornando-se assim mais denso, o que irá originar uma corrente descendente de ar mais frio.
⇒ As correntes quentes ascendentes e as correntes frias descendentes, repetindo-se, em simultâneo, ao longo do tempo, permitem o aquecimento de todo o ar.
- Na resposta, são apresentados os seguintes tópicos:
A) O principal processo de transferência de energia [, como calor, que permite o aquecimento de todo o ar contido no balão] é a convecção.
B) O ar que se encontra na base do balão aquece, tornando-se menos denso, o que dá origem a uma corrente quente ascendente. [Simultaneamente,] o ar mais frio no topo do balão desce por ser mais denso, o que dá origem a uma corrente fria descendente.
C) As correntes quentes ascendentes e as correntes frias descendentes, repetindo-se, [em simultâneo,] ao longo do tempo, permitem o aquecimento de todo o ar contido no balão.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.2 Considere que o ar contém cerca de 21%, em volume, de oxigénio e que Vm representa o volume molar de um gás, em dm3 mol-1, em quaisquer condições de pressão e de temperatura.
Qual das expressões seguintes permite calcular a quantidade aproximada de oxigénio que existia no balão?
- Opção (C) …………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2. Jacques Charles (1746-1823), pioneiro do estudo dos gases, conseguiu estimar a variação da altitude de um balão, admitindo que a pressão atmosférica diminuía cerca de 1,32 × 10-3 atm por cada 10 m subidos.
Assim, um balão que tivesse sido largado de um local onde a pressão atmosférica fosse 1,00 atm e que se encontrasse num local onde a pressão atmosférica fosse 0,60 atm, teria subido cerca de
(A) 1,0 × 103 m
(B) 3,0 × 103 m
(C) 4,5 × 103 m
(D) 7,5 × 103 m
- Opção (B) …………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
3. A Figura 2 representa um balão, de massa m, que subiu 2,0 × 103 m na vertical e que foi depois desviado pelo vento, deslocando-se 1,0 × 103 m na horizontal.
Qual das expressões seguintes, onde g representa o módulo da aceleração gravítica, permite calcular o trabalho realizado, no deslocamento considerado, pela força gravítica, Fg, que atua no balão?
(A) WFg = -2,0 × 103 m g
(B) WFg = -1,0 × 103 m g
(C) WFg = -3,0 × 103 m g
(D) WFg = -2,2 × 103 m g
- Opção (A) …………. 5 pontos
4. Qual é o esboço do gráfico que pode representar, globalmente, a temperatura do ar na troposfera, em função da altitude?
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
⇒ Na troposfera a temperatura diminui com a altitude.
- Opção (C) …………. 5 pontos
GRUPO III
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1. Considere uma bola que, tendo sido abandonada, no instante t = 0,0 s, de uma determinada altura em relação ao solo, cai em queda livre.
Em qual dos seguintes diagramas se encontram corretamente marcadas as posições da bola nos instantes t = 0,0 s, t = 0,2 s e t = 0,4 s, em relação ao referencial unidimensional representado?
- Opção (D) …………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2. Considere agora uma bola, de massa 4,0 g, que cai verticalmente, acabando por atingir uma velocidade terminal.
Admita que a bola pode ser representada pelo seu centro de massa (modelo da partícula material).
Calcule a energia dissipada pelo sistema bola + Terra quando a bola percorre 50,0 cm com velocidade terminal.
Apresente todas as etapas de resolução.
⇒ A energia dissipada traduz-se numa diminuição de energia mecânica do sistema bola + Terra.
⇒ A velocidade terminal é constante logo a variação de energia cinética da bola é nula.
⇒ Variação de energia potencial gravítica do sistema bola + Terra:
Como a variação de energia mecânica é igual à soma da variação de energia cinética com a variação de energia potencial, conclui-se que a variação de energia mecânica é igual à variação de energia potencial:
⇒ Assim a energia dissipada é, 2,0 x 10-2 J
ou
A energia dissipada corresponde ao simétrico do trabalho das forças dissipativas.
⇒ Como o movimento é uniforme a resultante das forças é nula.
⇒ Assim a resultante das forças dissipativas (resistência do ar) é simétrica do peso e o seu trabalho é:
⇒ Conclui-se que a energia dissipada é 2,0 x 10-2 J
ou
Como a velocidade terminal é constante, a variação de energia cinética é nula e, consequentemente, o trabalho da resultante das forças é também nulo.
⇒ Assim o trabalho da resistência do ar (força dissipativa) é simétrico do trabalho do peso:
⇒ O módulo do trabalho da resistência do ar é igual à energia dissipada: 2,0 x 10-2 J
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Determinação da variação da energia potencial gravítica do sistema bola + Terra, no percurso considerado (ΔEp = -2,00 x 10-2 J).
ou
- Determinação do trabalho realizado pela força gravítica que atua na bola, no percurso considerado (WFg = 2,00 x 10-2 J).
B) Determinação da variação da energia cinética da bola, no percurso considerado (ΔEc = 0 J).
ou
- Determinação do trabalho realizado pela força de resistência do ar que atua na bola, no percurso considerado (WFresistência do ar = -2,00 x 10-2 J).
C) Determinação da energia dissipada pelo sistema bola + Terra, no percurso considerado (Ed = 2,0 x 10-2 J).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
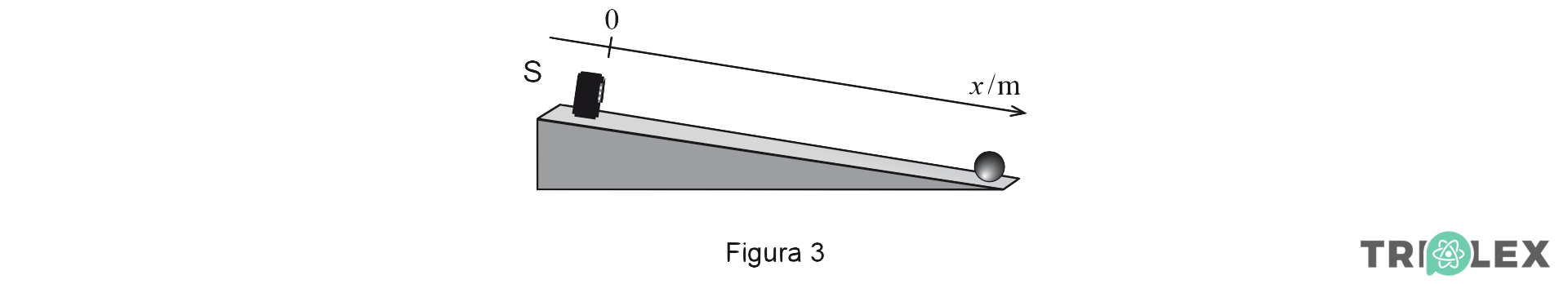
3. A Figura 3 representa um plano inclinado, no topo do qual se colocou um sensor de movimento, S.
Uma pequena bola foi lançada de modo a subir o plano, segundo uma trajetória retilínea com a direção do eixo Ox do referencial unidimensional representado na figura.
Admita que a bola pode ser representada pelo seu centro de massa (modelo da partícula material).
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
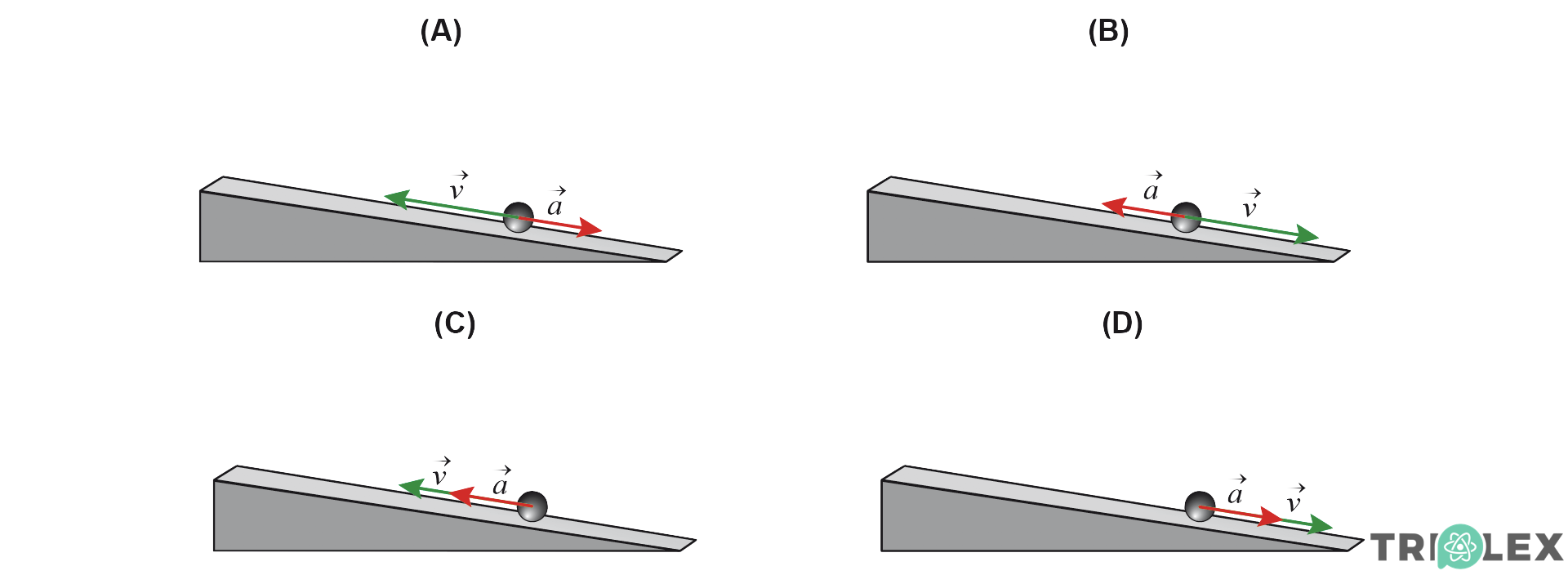
3.1 Em qual dos seguintes esquemas se encontram corretamente representados os vetores velocidade, v , e aceleração, a, num instante em que a bola se encontra a subir o plano?
- Opção (A)
⇒ A velocidade da bola tem a direção e o sentido do movimento, ou seja, direção paralela ao plano e sentido negativo do eixo dos xx (subida).
⇒ Como o movimento de subida é retardado, a aceleração tem sentido oposto à velocidade (sentido positivo do eixo dos xx).
- Opção (A) …………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
3.2 Se as forças dissipativas forem desprezáveis, a altura máxima atingida pela bola sobre o plano será
(A) diretamente proporcional ao módulo da velocidade de lançamento.
(B) inversamente proporcional ao quadrado do módulo da velocidade de lançamento.
(C) inversamente proporcional ao módulo da velocidade de lançamento.
(D) diretamente proporcional ao quadrado do módulo da velocidade de lançamento.
- Opção (D)
⇒ Na ausência de forças dissipativas a energia mecânica do sistema bola + Terra permanece constante.
⇒ Tomando como referência para medição da energia potencial a posição inicial:
A altura máxima atingida pela bola, hmáx, é diretamente proporcional ao quadrado da velocidade de lançamento, v02.
ou
⇒ O trabalho da resultante das forças é igual à variação de energia cinética.
⇒ Como a resultante das forças e a massa são contantes, e o módulo do deslocamento máximo é proporcional à altura máxima, conclui-se que a altura máxima é diretamente proporcional ao quadrado da velocidade.
- Opção (D) …………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
3.3 A partir dos dados adquiridos com o sensor de movimento, concluiu-se que, durante a subida, a componente escalar, segundo o eixo Ox, da posição, x, da bola sobre o plano variava com o tempo, t, de acordo com a equação
x = 1,5t2 − 2,4 t + 2,0 (SI)
Apresente o gráfico da componente escalar da posição, x, da bola em função do tempo, t, desde o instante em que a bola foi lançada (t = 0 s) até ao instante em que, sobre o plano, a bola inverteu o sentido do movimento.
Utilize a calculadora gráfica.
Na sua resposta, deve reproduzir o gráfico obtido com a calculadora, no intervalo de tempo considerado, indicando no gráfico:
• as grandezas representadas e as respetivas unidades;
• as coordenadas dos pontos que correspondem ao instante em que a bola foi lançada e ao instante em que, sobre o plano, a bola inverteu o sentido do movimento.
Na resposta, é reproduzido o gráfico obtido com a calculadora, com indicação, no gráfico, das:
⇒ grandezas representadas (ver notas 1 e 2) ………….. 4 pontos
⇒ unidades em que estão expressas as grandezas representadas …. (1 + 1) ….. 2 pontos
⇒ coordenadas do ponto que corresponde ao instante em que a bola foi lançada ……… 2 pontos
⇒ coordenadas do ponto que corresponde ao instante em que, sobre o plano, a bola inverteu o sentido do movimento ……….. 2 pontos
Notas:
1. Se o examinando não indicar corretamente as grandezas representadas, esta etapa não é considerada para efeito de classificação.
2. Se o examinando apresentar um gráfico que não corresponda ao intervalo de tempo considerado, ou se apresentar um gráfico no qual esse intervalo de tempo não se encontre definido, a pontuação a atribuir nesta etapa deverá ser desvalorizada em dois pontos.
GRUPO IV
1. O trióxido de enxofre, SO3, pode decompor-se, em fase gasosa, originando dióxido de enxofre, SO2, e oxigénio, O2 .
A reação pode ser traduzida por
2 SO3 (g) ⇋ 2 SO2 (g) + O2 (g)
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
1.1 Considere que num recipiente de 2,0 dm3 se introduziram 4,0 mol de SO3 (g), à temperatura T .
Depois de o sistema químico atingir o equilíbrio, verificou-se que apenas 40% da quantidade inicial de SO3 (g) tinha reagido.
Determine a constante de equilíbrio, Kc , da reação considerada, à temperatura T .
Apresente todas as etapas de resolução.
⇒ Variação da quantidade de SO3 até ser atingido o equilíbrio:
⇒ A proporção estequiométrica entre SO2 e SO3 é 1:1 (a quantidade de SO2 que se forma é igual à quantidade de SO3 que reage), assim:
⇒ A proporção estequiométrica entre O2 e SO3 é 1:2 (a quantidade de O2 que se forma é metade da quantidade de SO3 que reage), assim:
⇒ As concentrações de equilíbrio são:
⇒ Assim a constante de equilíbrio é:
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo das quantidades de SO3 (g), de SO2 (g) e de O2 (g), no equilíbrio (nSO3 = 2,40 mol; nSO2 = 1,60 mol; nO2 = 0,800 mol).
B) Cálculo da constante de equilíbrio da reação considerada, à temperatura T (Kc = 1,8 x 10-1).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
1.2 A reação de decomposição do SO3 (g) é uma reação endotérmica, em que o sistema químico absorve 9,82 × 104 J por cada mole de SO3 que se decompõe.
A variação de energia, em joule (J), associada à decomposição de duas moles de SO3 (g) será
- Opção (C)
⇒ Na decomposição há absorção de energia: 9,82 x 104 J mol-1
⇒ Assim para duas moles a energia interna do sistema aumentará de
⇒ 9,82 x 104 J mol-1 x 2 mol = + 9,82 x 104 x 2 J
- Opção (C) …………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2. Quantas vezes é que a densidade do SO3 (g) é maior do que a densidade do SO2 (g), nas mesmas condições de pressão e de temperatura?
Apresente o resultado com três algarismos significativos.
- 1,25 (vezes) …………. 5 pontos
Nota – O resultado pode ser apresentado numa forma matemática equivalente, desde que com três algarismos significativos.
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
3. O SO3 (g) é usado na preparação do ácido sulfúrico comercial, por reação com vapor de água.
A reação que ocorre pode ser traduzida por
SO3 (g) + H2O (g) ⇋ H2SO4 (aq)
Considere que se obtém uma solução concentrada de ácido sulfúrico, de densidade 1,84 g cm-3, que contém 98%, em massa, de H2SO4.
Determine a massa de H2SO4 que existe em 100 cm3 da solução.
Apresente todas as etapas de resolução.
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo da massa de solução correspondente a 100 cm3 (m = 184 g).
ou
Cálculo do volume de solução correspondente a 100 g (V = 54,4 cm3).
B) Cálculo da massa de H2SO4 que existe em 100 cm3 da solução (m = 1,8 × 102 g).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
GRUPO V
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
1. Considere que se representa a molécula de O2 utilizando a notação de Lewis.
Quantos pares de eletrões de valência não ligantes devem ser representados em cada um dos átomos de oxigénio?
(A) Um par.
(B) Dois pares.
(C) Três pares.
(D) Quatro pares.
- Opção (B) …………. 5 pontos
2. Um dos eletrões de valência menos energéticos de um átomo de oxigénio, no estado fundamental, pode ser caracterizado pelo conjunto de números quânticos
(A) (2 , 1 , 0 , +½)
(B) (2 , 0 , 0 , -½)
(C) (2 , 1 , 2 , +½)
(D) (2 , 0 , 1 , -½)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B) …………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
3. A energia de ionização do átomo de oxigénio, isolado e em fase gasosa, é a energia mínima necessária para que, a partir do átomo no estado fundamental, se forme o ião
(A) O– (g)
(B) O2- (g)
(C) O+ (g)
(D) O2+ (g)
- Opção (C)
⇒ A energia de ionização do átomo de oxigénio é a energia mínima necessária para formar o ião monopositivo de oxigénio a partir do átomo, ambos no seu estado fundamental.
- Opção (C) …………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
4. O lítio é um elemento químico que, na tabela periódica, está situado no mesmo período do oxigénio, mas que pertence ao grupo 1.
Na Figura 4, está representado, a preto e branco, o espectro de emissão atómico do lítio, na região do visível.
Represente, utilizando a mesma escala, o espectro de absorção atómico do lítio, na região do visível.
GRUPO VI
O nitrato de potássio, KNO3, é um sal inorgânico muito solúvel em água.
O equilíbrio que se estabelece entre o sal sólido e os iões resultantes da dissolução do sal em água pode ser traduzido por
KNO3 (s) ⇋ K+ (aq) + NO3– (aq)
1. Considere que se prepara uma solução aquosa de KNO3 por dissolução do soluto sólido.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.1 O intervalo de tempo necessário à dissolução completa do KNO3 (s)
(A) não depende do estado de divisão do sólido, nem da agitação da solução.
(B) não depende do estado de divisão do sólido, mas depende da agitação da solução.
(C) depende do estado de divisão do sólido e da agitação da solução.
(D) depende do estado de divisão do sólido, mas não depende da agitação da solução.
- Opção (C)
⇒ O intervalo de tempo necessário para a dissolução completa diminui com o aumento do estado de divisão do sólido e com o aumento da agitação da mistura, dependendo, portanto, desses dois fatores.
- Opção (C) …………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
1.2 Admita que a solução aquosa de KNO3 preparada é uma solução saturada e que s é a solubilidade do KNO3 em água, expressa em mol dm-3, à temperatura a que se encontra a solução.
Qual é a relação entre a solubilidade, s, e as concentrações dos iões K+ (aq) e NO–3 (aq), também expressas em mol dm– 3, nessa solução?
- Opção (D)
A solubilidade de um sal em água é a concentração do sal dissolvido numa solução saturada.
⇒ Para o nitrato de potássio a proporção entre os iões é 1:1. Logo as concentrações dos iões potássio e nitrato são iguais à concentração do nitrato de potássio que se dissolveu e, portanto, à solubilidade.
- Opção (D) …………. 5 pontos
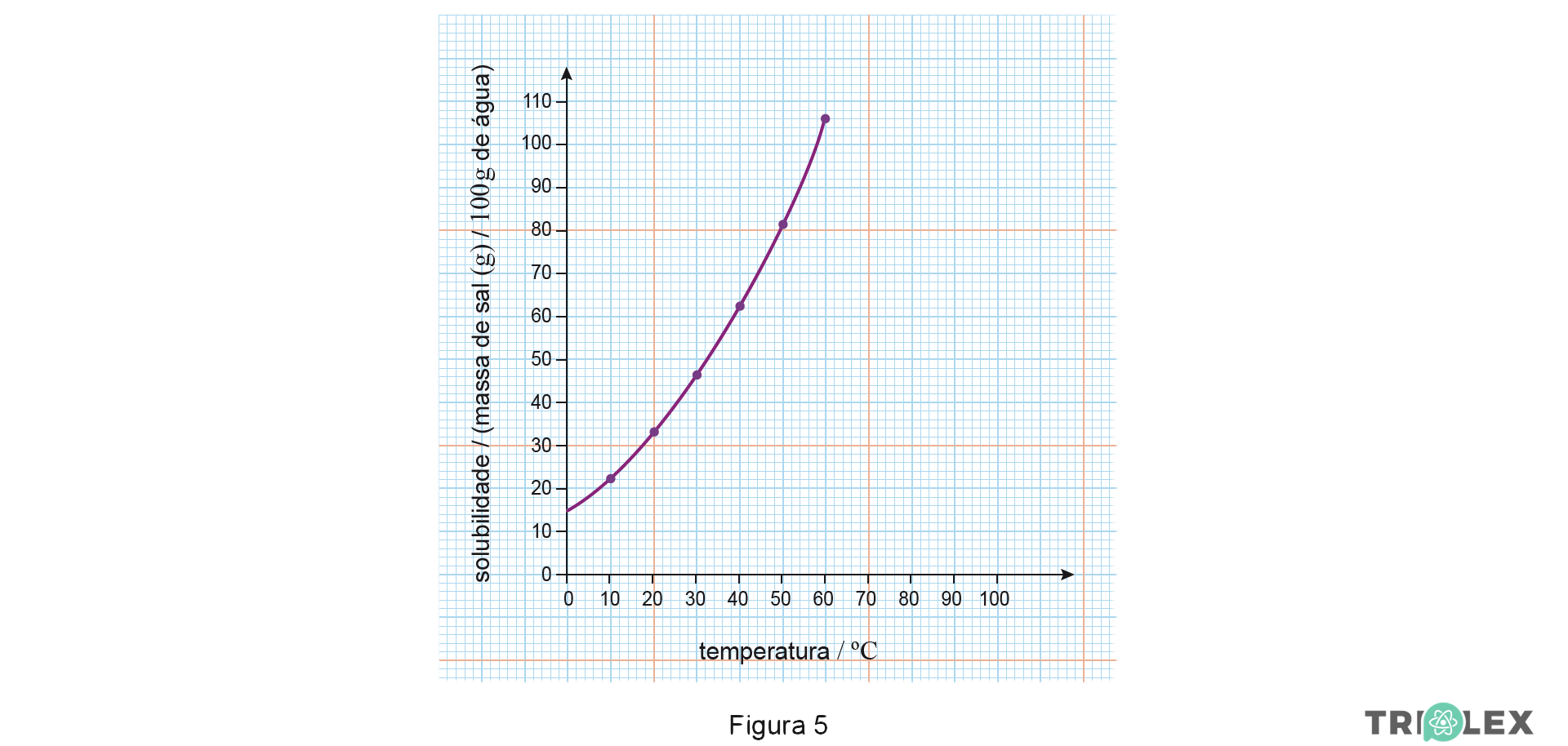
2. Na Figura 5, está representada a curva que traduz a solubilidade do KNO3 em água, expressa em massa de sal, em gramas (g), por 100 g de água, em função da temperatura.
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
2.1 Que massa, em gramas (g), de KNO3 é possível dissolver em 50 g de água à temperatura de 40 oC?
- 31 g …………. 5 pontos
Nota – Deve ser também aceite como correta a resposta 32 g.
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
2.2 Considere que, ao fazer o estudo experimental da solubilidade do KNO3 em água em função da temperatura, um grupo de alunos obteve o valor de 55 g de KNO3 por 100 g de água à temperatura de 30 oC.
Determine o erro relativo, em percentagem, deste valor experimental.
Apresente todas as etapas de resolução.
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Determinação do valor da solubilidade do KNO3 em água, à temperatura de 30 ºC (s = 46 g de sal / 100 g de água) (ver notas 1 e 2).
B) Cálculo do erro relativo, em percentagem, do valor experimental de solubilidade (20%) (ver nota 3).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos*.
* Descritores e desvalorizações apresentados no primeiro quadro da página C/4 dos Critérios Gerais de Classificação.
Notas:
1. Deve ser também aceite como correto s = 47 g de sal / 100 g de água.
2. A apresentação de um número incorreto de algarismos significativos implica que esta etapa não seja considerada para efeito de classificação.
3. A apresentação de um resultado final com um arredondamento incorreto e/ou com um número incorreto de algarismos significativos não implica qualquer penalização.
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
2.3 Conclua, justificando, se a dissolução do KNO3 (s) em água é um processo endotérmico ou um processo exotérmico.
⇒ A solubilidade do KNO3 aumenta com a temperatura, o que significa que um aumento de temperatura favorece a dissolução do sal.
⇒ De acordo com o Princípio de Le Châtelier, o aumento de temperatura favorece a transformação que ocorre com absorção de energia (reação endotérmica) isto é, o sentido em que se retira energia do meio.
- Conclui-se que a dissolução do KNO3 é um processo endotérmico.
Na resposta, são apresentados os seguintes tópicos:
A) Verifica-se [, a partir do gráfico,] que a solubilidade do KNO3 (s) em água aumenta à medida que a temperatura aumenta.
ou
- Verifica-se [, a partir do gráfico,] que a dissolução do KNO3(s) em água é favorecida pelo aumento da temperatura.
B) De acordo com o Princípio de Le Châtelier, um aumento de temperatura favorece o processo endotérmico.
C) Conclui-se, assim, que a dissolução do KNO3 (s) em água é um processo endotérmico.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
FIM



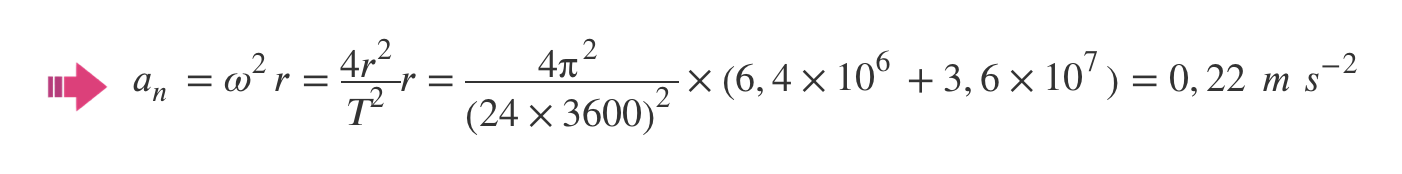
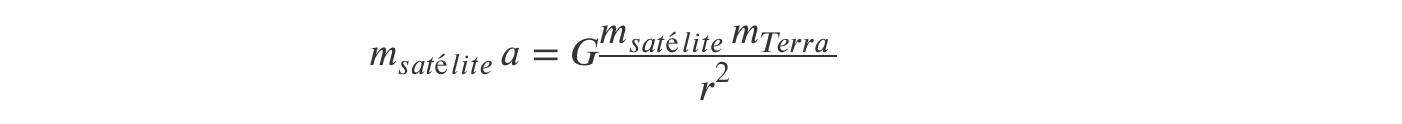
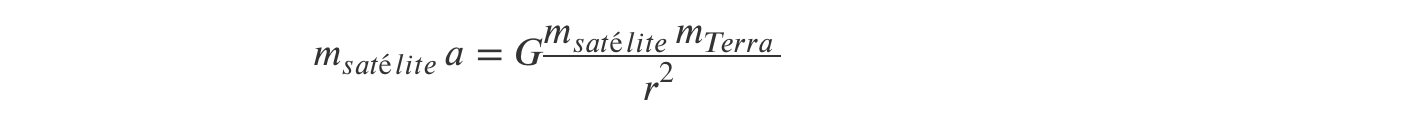











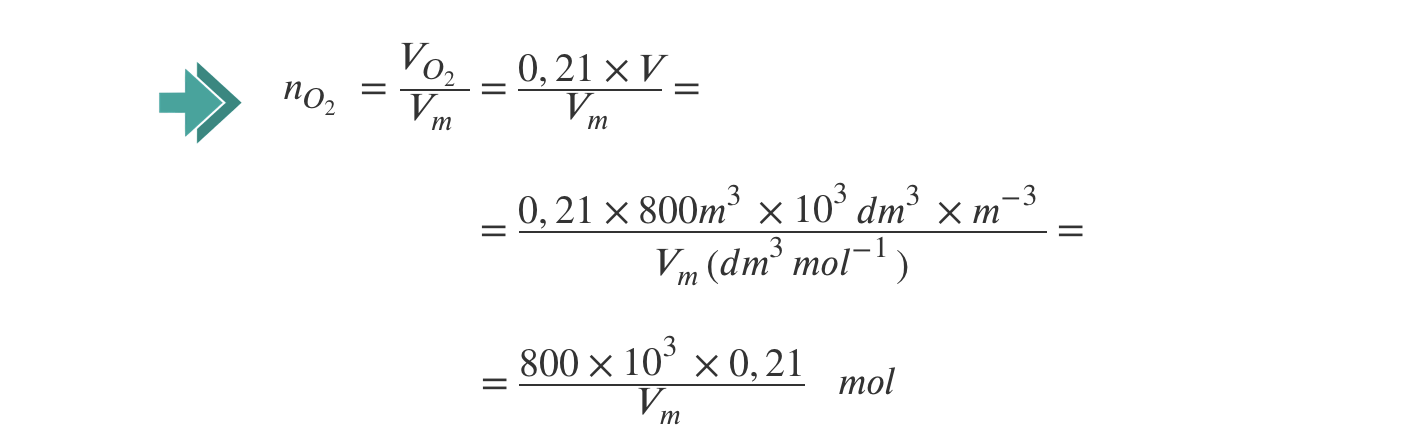





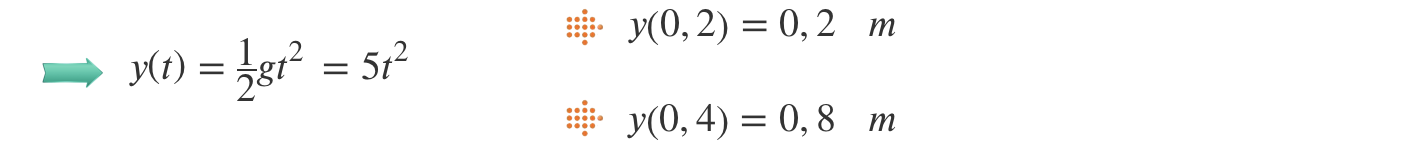

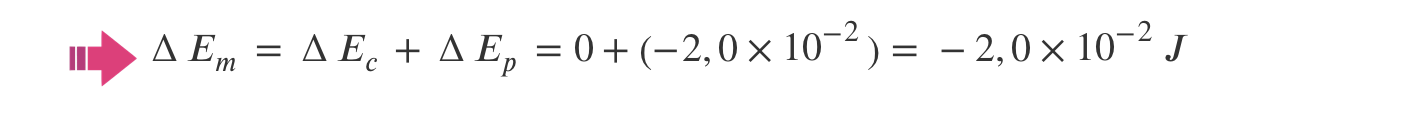

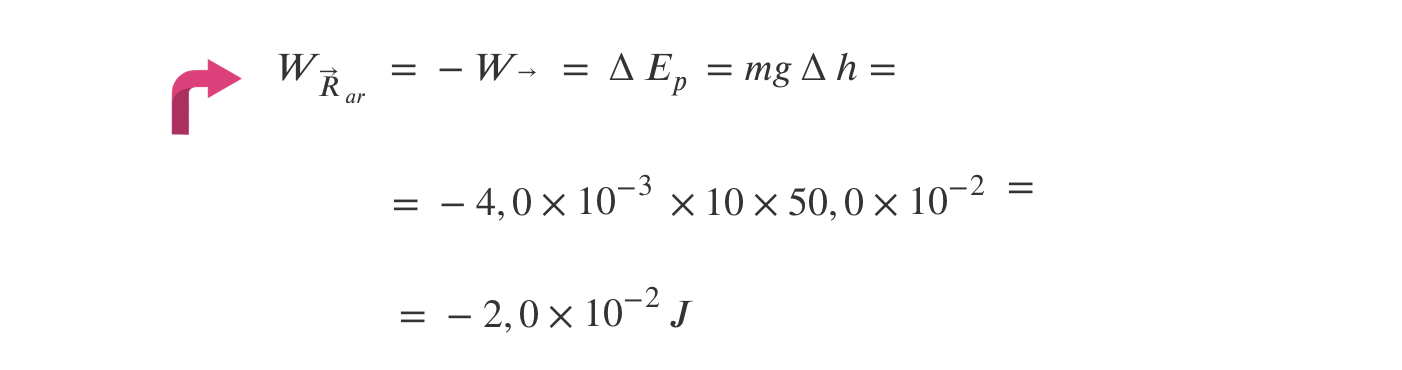








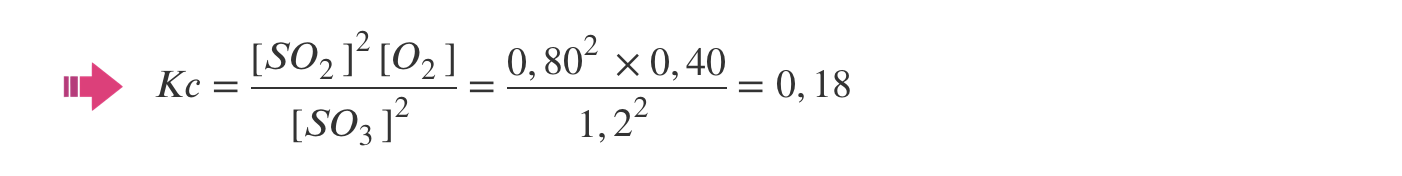


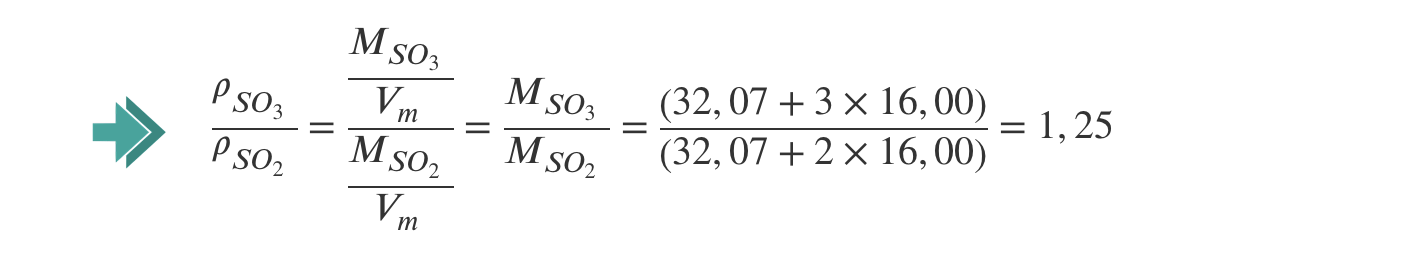



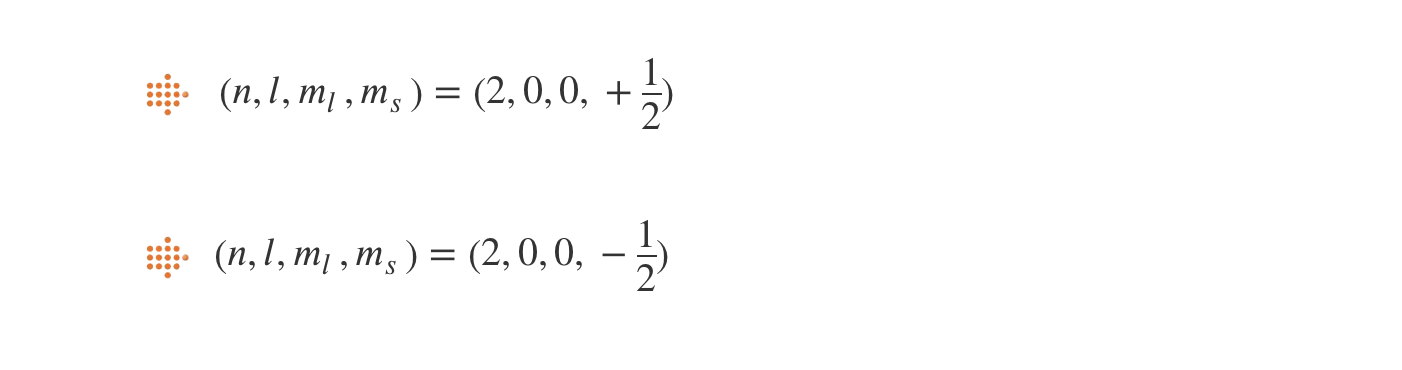







verygood the website i like it so much
gostei muito do seu site parabéns