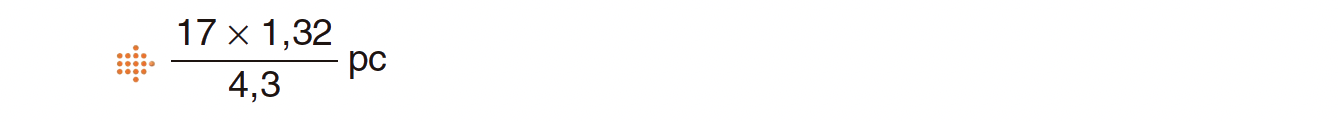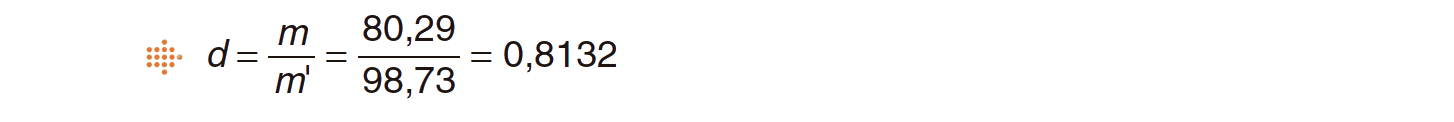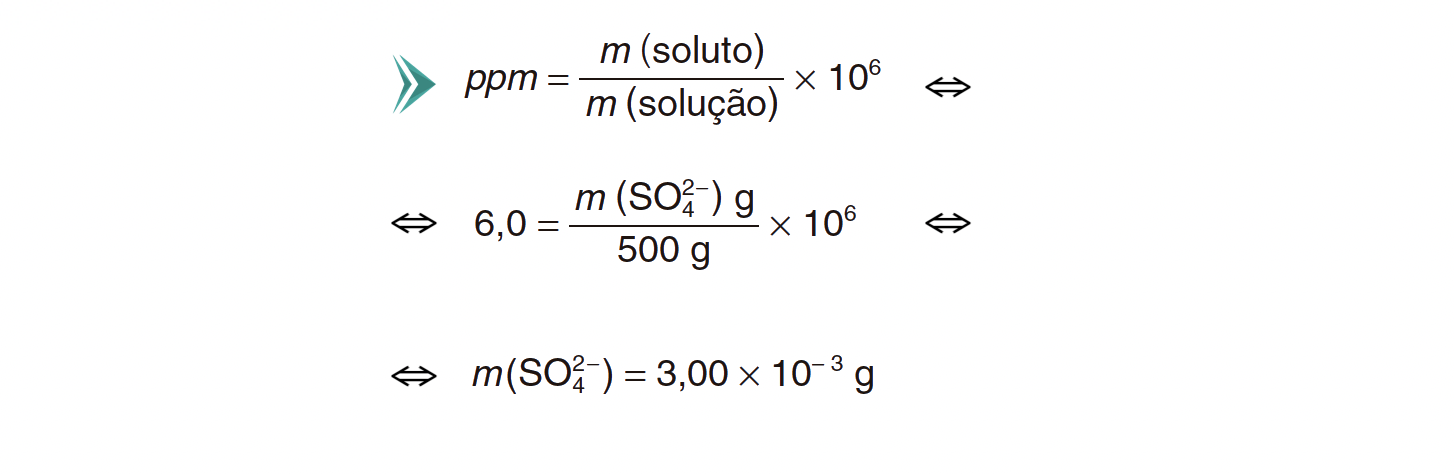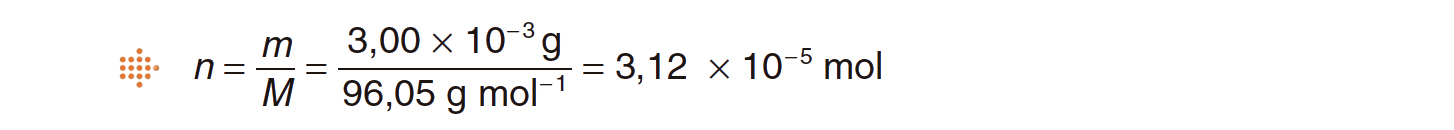2010 – Teste Intermédio – 10ºAno – março
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 10ºAno – 2010
- Duração do Teste: 90 minutos | 10.03.2010
Pensa-se que a atmosfera primordial da Terra tenha sido substancialmente diferente da atmosfera actual, contendo muito pouco, ou nenhum, oxigénio, O2. Este terá sido libertado para a atmosfera por organismos unicelulares, como produto secundário da fotossíntese.
O oxigénio terá, assim, começado a surgir na atmosfera há, pelo menos, 3,5 x 109 anos, embora os registos geoquímicos indiquem que a concentração de oxigénio na atmosfera só tenha começado a aumentar de modo significativo há 2,3 x 109 anos.
O aumento da concentração de oxigénio na atmosfera terrestre permitiu iniciar a forma..o da camada de ozono estratosférico, o que, por sua vez, permitiu a conquista da terra firme pelos organismos vivos. Nessa camada, moléculas de oxigénio dissociam-se, por acção da radiação ultravioleta (UV) solar.
Os átomos resultantes dessa dissociação combinam-se com oxigénio molecular para formar ozono, O3.
Este, por sua vez, ao ser dissociado pela radiação UV, produz oxigénio atómico e molecular, que acaba por se recombinar de novo.
F. D. Santos, Que Futuro? Ciência, Tecnologia, Desenvolvimento e Ambiente, Gradiva, 2007 (adaptado)
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
1.1. Seleccione, tendo em conta a informação dada no texto, o único gráfico que pode descrever a evolução da percentagem de oxigénio (%O2) na atmosfera terrestre, ao longo do tempo, t, desde a formação da atmosfera primordial da Terra até à actualidade.
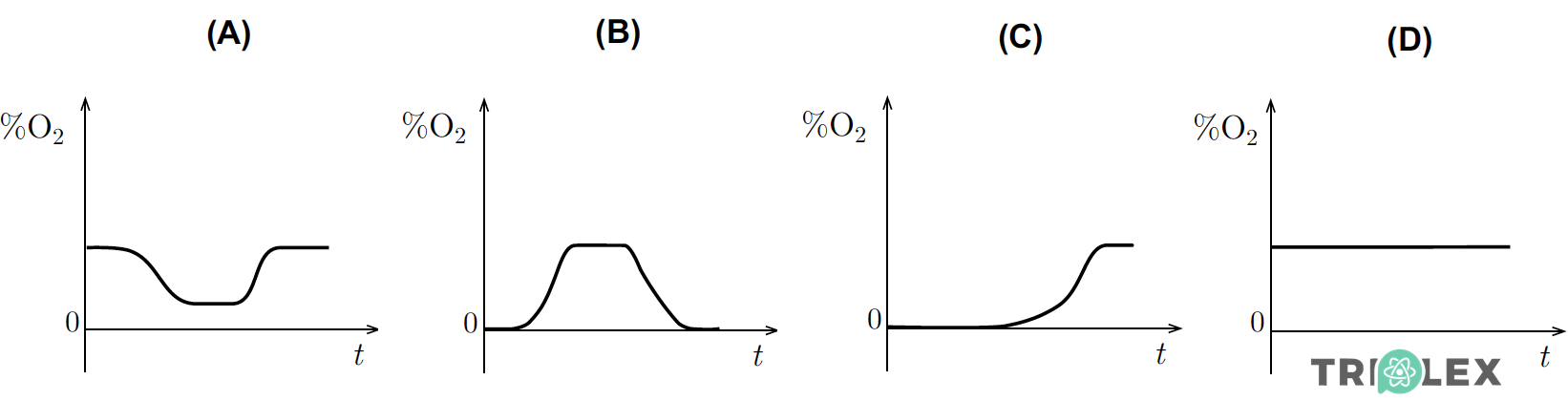
- Opção (C)
⇒ De acordo com a informação apresentada no texto, a atmosfera primordial da Terra continha muito pouco ou nenhum oxigénio.
⇒ Este terá começado a surgir na atmosfera há, pelo menos, 3,5 x 109 anos e o aumento da sua concentração na atmosfera terrestre permitiu iniciar a formação da camada de ozono estratosférico.
- Opção (C)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
1.2. Identifique o fenómeno, fundamental para a vida na Terra, que ocorre na camada de ozono estratosférico.
- Na camada de ozono estratosférico ocorre absorção de radiação ultravioleta.
⇒ A presença de ozono estratosférico constitui um filtro para estas radiações, absorvendo cerca de 95% das radiações UV mais perigosas (UVB) que atingem a troposfera, protegendo os seres vivos da sua ação nefasta.
- Absorção de radiação ultravioleta …………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
1.3. Escreva as duas equações químicas que traduzem o mecanismo reaccional de produção do ozono estratosférico, com base na informação dada no texto.
⇒ O2 (g) → O (g) + O (g)
⇒ O (g) + O2 (g) → O3 (g)
⇒ O2 (g) → O (g) + O (g) …………. 8 pontos
⇒ O (g) + O2 (g) → O3 (g)
- 10ºano – Química – Domínio 1 – subdomínio 1 (Massa e tamanho dos átomos)
1.4. Calcule o número de átomos que existe numa amostra de 48 g de oxigénio, O2 (g).
Apresente todas as etapas de resolução.
- m (O2) = 48 g
⇒ Cálculo da quantidade de O2 existente na amostra:
⇒ Cálculo do número de moléculas de oxigénio existentes na amostra:
- N (O2) = n x NA = 1,50 x 6,02 x 1023 = 9,03 x 1023 moléculas
⇒ Cálculo do número de átomos de oxigénio existentes na amostra:
- N (O) = 2 x 9,03 x 1023 = 1,8 x 1023 átomos
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Determina a quantidade de moléculas de oxigénio existentes na amostra (n = 1,50 mol).
⇒ Determina o número de moléculas de oxigénio existentes na amostra (N = 9,03 x 1023).
⇒ Determina o número de átomos de oxigénio existentes na amostra (N = 1,8 x 1024).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.5. Seleccione a única opção que permite obter uma afirmação correcta.
Nas mesmas condições de pressão e temperatura, o volume ocupado por 0,5 mol de oxigénio, O2 (g), é aproximadamente …
(A) um quarto do volume ocupado por 32 g desse mesmo gás.
(B) um meio do volume ocupado por 32 g desse mesmo gás.
(C) o dobro do volume ocupado por 32 g desse mesmo gás.
(D) o quádruplo do volume ocupado por 32 g desse mesmo gás.
- Opção (B)
⇒ Como a quantidade de oxigénio existente em 32 g deste gás é 1,0 mol (M(O2) = 32 g mol-1), nas mesmas condições de pressão e temperatura, 0,5 mol de oxigénio ocupam metade do volume ocupado por 32 g deste gás.
- Opção (B)…………. 8 pontos
2. Apesar das enormes distâncias que nos separam das estrelas, os astrónomos conseguem obter uma grande quantidade de informação a partir da luz que nos chega desses astros.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
2.1. A composição química da atmosfera das estrelas pode ser determinada por comparação dos espectros da radiação por elas emitida com os espectros dos elementos químicos conhecidos.
A Figura 1 representa, à mesma escala, parte de um espectro atómico de emissão e parte de um espectro atómico de absorção.
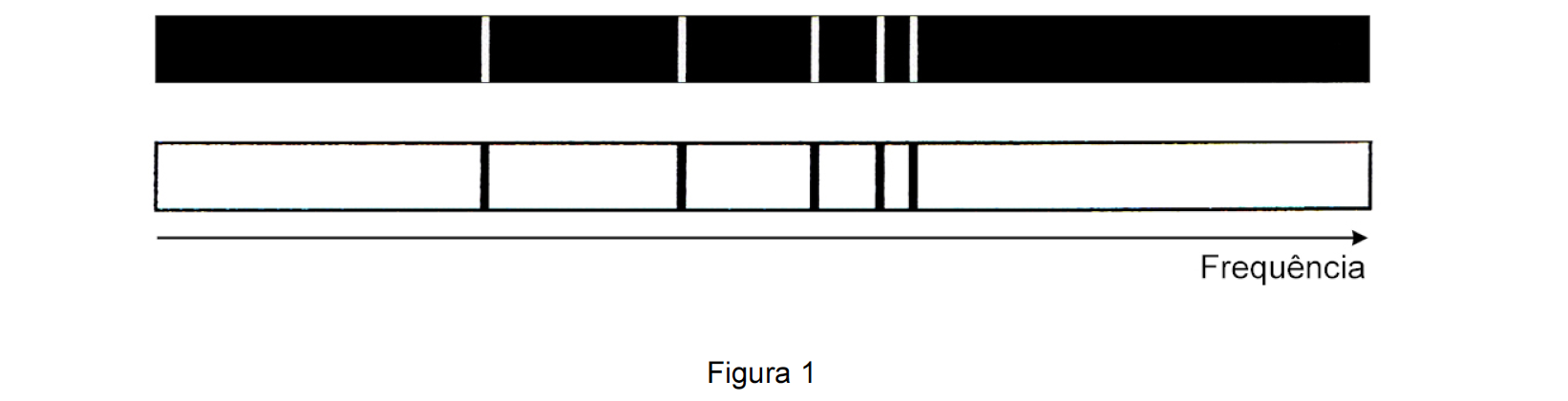
Por que motivo se pode concluir que os dois espectros apresentados se referem a um mesmo elemento químico?
⇒ Cada elemento tem um espetro de emissão próprio.
⇒ No espetro de absorção representado na Figura 1 as riscas negras localizam-se na mesma posição das riscas do espetro de emissão, correspondendo, portanto, aos mesmos valores de frequência.
⇒ Pode, assim, concluir-se que os dois espetros apresentados se referem a um mesmo elemento químico.
⇒ As riscas aparecem aos mesmos valores de frequência em ambos os espectros ———– 8 pontos
- 11ºano – Física – Domínio 1 – subdomínio 1 (Tempo, posição e velocidade)
2.2. A estrela Alfa A da constelação do Centauro encontra-se a uma distância de 1,32 parsec da Terra, ou seja, a 4,3 anos-luz do nosso planeta. A estrela Altair, da constelação da Águia, encontra-se a 17 anos-luz da Terra.
Seleccione a única opção que permite calcular correctamente a distância da estrela Altair à Terra, em parsec (pc).

- Opção (A)…………. 8 pontos
2.3. No núcleo das estrelas ocorre um tipo de reacções responsáveis pela energia por elas irradiada.
Identifique esse tipo de reacções.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Reação nuclear de fusão
- Reação nuclear de fusão …………. 8 pontos
3. Os hidrocarbonetos são compostos químicos constituídos por átomos de carbono (um dos elementos mais abundantes no espaço interestelar) e de hidrogénio (o elemento mais abundante no Universo).
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3.1. A Figura 2 representa um diagrama de níveis de energia do átomo de hidrogénio.
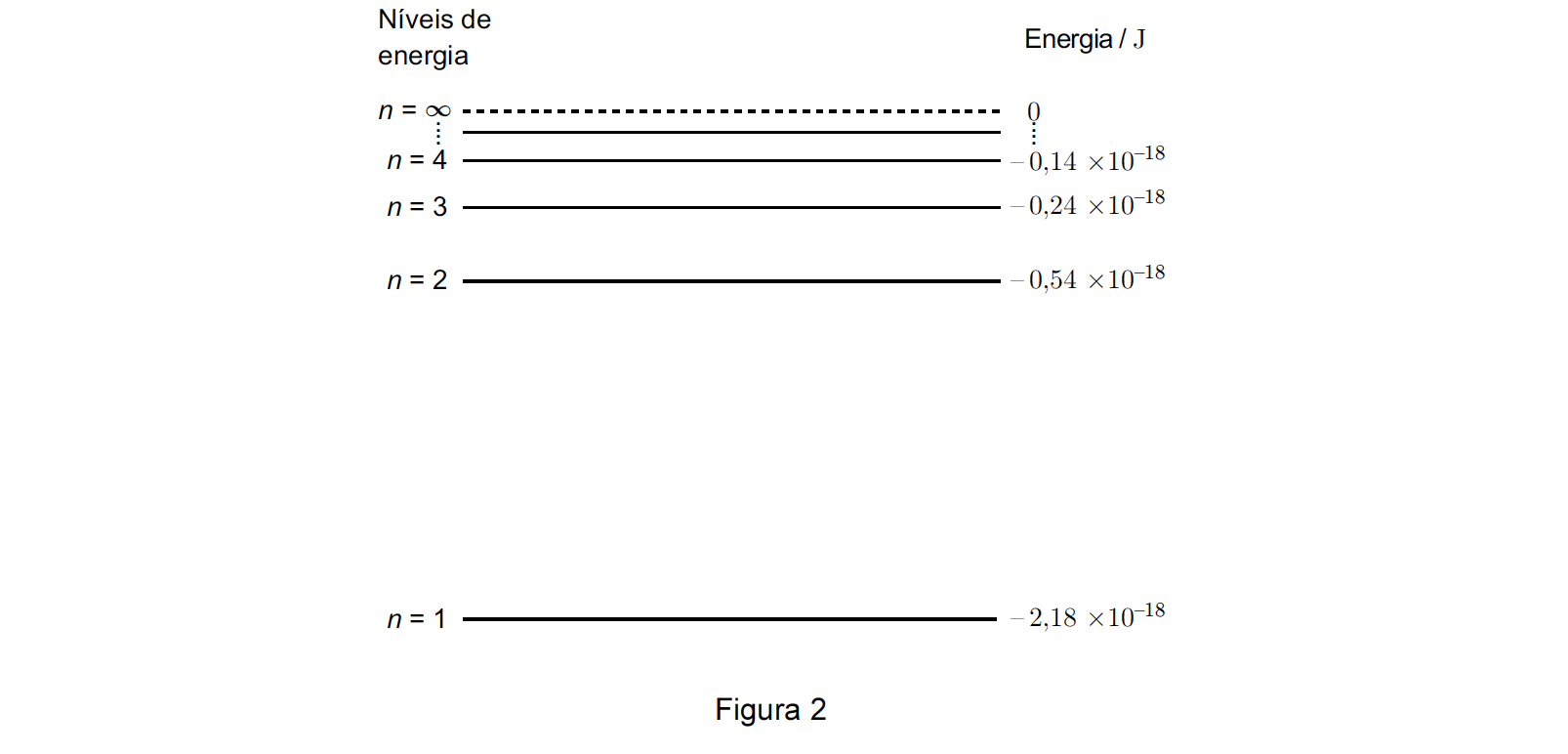
Seleccione a única opção que apresenta o valor da energia da radiação envolvida na transição do electrão, do nível energético correspondente ao primeiro estado excitado do átomo de hidrogénio, para o nível energético correspondente ao estado fundamental do mesmo átomo.
(A) 0,30 x 10–18 J
(B) 2,18 x 10–18 J
(C) 0,14 x 10–18 J
(D) 1,64 x 10–18 J
- Opção (D)
⇒ O primeiro estado excitado corresponde ao nível energético n = 2 e o estado fundamental corresponde ao nível n = 1.
- ΔE = E2 – E1 = – 0,54 x 10-18 – (- 2,18 x 10-18) = 1,64 x 10-18 J
⇒ A energia da radiação envolvida numa transição é igual ao módulo de variação de energia, ΔE.
- Opção (D)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3.2. Seleccione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
Os átomos de carbono (C), no estado fundamental, apresentam _______ electrões de valência, distribuídos por _________ .
(A) dois … uma orbital
(B) dois … duas orbitais
(C) quatro … duas orbitais
(D) quatro … três orbitais
- Opção (D)
⇒ 6C – 1s2 2s2 2p2
⇒ Os átomos de carbono, no estado fundamental, apresentam quatro eletrões de valência (dois eletrões 2s e dois eletrões 2p), distribuídos por três orbitais (uma orbital 2s e duas orbitais 2p, que podem ser 2px e 2py, 2px e 2pz ou 2py e 2pz ).
- Opção (D)…………. 8 pontos
3.3. O etino, C2H2, é um hidrocarboneto, de fórmula de estrutura
H – C ≡ C – H
Classifique, justificando, a ligação que se estabelece entre os átomos de carbono, na molécula considerada.
⇒ No etino, entre os átomos de carbono estabelece-se uma ligação covalente tripla, porque estes átomos de carbono partilham entre si três pares de eletrões.
- A resposta deve abordar os seguintes tópicos:
⇒ Entre os átomos de carbono estabelece-se uma ligação covalente tripla.
⇒ Os átomos de carbono partilham entre si três pares de electrões.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

4. Considere que na sua bancada de laboratório se encontrava um frasco contendo uma solução aquosa de etanol e que o trabalho que lhe foi proposto consistia na determinação da densidade relativa daquela solução, utilizando o método do picnómetro.
4.1. Seleccione a única opção que apresenta a imagem de um picnómetro de líquidos.
(As imagens não estão representadas à mesma escala.)

*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (D)
⇒ Opção (A) → balão volumétrico
⇒ Opção (B) → proveta graduada
⇒ Opção (C) → matraz
- Opção (D)…………. 8 pontos
4.2. Para realizar o trabalho que lhe foi proposto, a primeira determinação que teve que efectuar foi a massa do picnómetro vazio.
Em seguida, teve que determinar a massa do picnómetro cheio com a solução aquosa de etanol e a massa do picnómetro cheio com água. Estas pesagens foram realizadas . temperatura aproximada de 20 ºC.
Calcule a densidade relativa da solução aquosa de etanol, com base nos valores experimentais registados na tabela seguinte.
Apresente todas as etapas de resolução.

*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
⇒ m – massa da solução aquosa de etanol = 111,84 – 31,55 = 80,29 g
⇒ mA – massa de igual volume de água = 130,28 – 31,55 = 98,73 g
⇒ A densidade relativa da solução aquosa de etanol, à temperatura da experiência, é a razão das massas de igual volume de solução de etanol e água.
⇒ A densidade relativa da solução de etanol é 0,8132.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Determina a massa da solução de etanol (80,29 g) e a massa de água (98,73 g).
⇒ Determina o valor da densidade relativa da solução aquosa de etanol (d = 0,813).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

4.3. Seleccione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
No trabalho laboratorial realizado, a densidade relativa foi determinada ______ e as massas foram determinadas ______ .
(A) indirectamente … directamente
(B) directamente … indirectamente
(C) indirectamente … indirectamente
(D) directamente … directamente
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (A)
⇒ As massas foram medidas diretamente (numa balança) enquanto a densidade relativa foi determinada a partir de uma expressão matemática.
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
- 10ºano – Química – A.l. – 2.3 – Diluição de soluções
4.4. Considere que, em seguida, lhe foi pedido que preparasse, com rigor, 500,0 mL de uma solução aquosa de etanol mais diluída, a partir da solução aquosa de etanol que encontrou na sua bancada de laboratório.
Descreva o procedimento seguido na preparação da solução diluída de etanol, considerando, por ordem cronológica, as três principais etapas que devem ser realizadas nesse procedimento.
⇒ Para preparar 500,0 mL de uma solução aquosa diluída a partir de outra solução mais concentrada, mede-se, rigorosamente, com uma pipeta volumétrica, um certo volume de solução concentrada e transfere-se essa solução para um balão volumétrico de 500,0 mL.
⇒ Seguidamente, perfaz-se o volume do balão com água destilada até ao traço de referência.
- A resposta deve abordar os seguintes tópicos:
⇒ A primeira etapa é a medição do volume da solução inicial de etanol, utilizando uma pipeta (graduada ou volumétrica).
⇒ A segunda etapa é a transferência desse volume de solução inicial para um balão volumétrico de 500,0 mL .
⇒ A terceira etapa é perfazer o volume de 500,0 mL com água destilada, adicionando água destilada até ao traço de referência do balão volumétrico.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
5. Numa análise efectuada a uma amostra de 500 g de água de um poço, destinada a ser utilizada para fins agrícolas, determinou-se um teor em ião sulfato, SO42–, de 6,0 ppm (m/m).
Calcule a quantidade de ião SO42– que existia naquela amostra de solução.
Apresente todas as etapas de resolução.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Determina a massa de ião sulfato que existia na amostra de solução (m = 3,00 x 10–3 g).
⇒ Determina a quantidade de ião sulfato correspondente àquela massa (n = 3,1 x 10–5 mol).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

6. Um dos sulfatos industrialmente mais importantes é o sulfato de sódio (Na2SO4), muito usado na produção de pasta de papel e na indústria de detergentes, entre outras.
O sulfato de sódio é constituído por sódio (Na), enxofre (S) e oxigénio (O).
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
6.1. Seleccione a única opção que corresponde a uma configuração electrónica possível de um átomo de enxofre num estado excitado.
(A) 1s2 2s2 2p7 3s2 3p3
(B) 1s2 2s2 2p5 3s2 3p5
(C) 1s2 2s1 2p6 3s3 3p4
(D) 1s2 2s2 2p6 3s2 3p4
- Opção (B)
⇒ Opção (A) → o subnível 2p comporta, no máximo, 6 eletrões
⇒ Opção (C) → a orbital 2s comporta, no máximo, 2 eletrões
⇒ Opção (D) → corresponde à configuração eletrónica do átomo de enxofre no estado fundamental
- Opção (B)…………. 8 pontos
6.2. Seleccione a única opção que contém o conjunto de números quânticos que pode caracterizar um dos electrões mais energéticos do átomo de enxofre, no estado fundamental.
(A) (3 , 2 , 0 , +½)
(B) (3 , 1 , 1 , +½)
(C) (3 , 1 , 2 , +½)
(D) (3 , 2 , 1 , +½)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B)
Os eletrões mais energéticos do átomo de enxofre são eletrões 3p (n = 3 e l = 1), que podem ser caracterizados pelo conjunto de números quânticos (3, 1, 1, +½)
⇒ Opção (A) → A configuração eletrónica corresponde a orbitais 3d.
⇒ Opção (C) → A configuração eletrónica é impossível porque, para l = 1, ml só pode tomar os valores de – 1, 0, + 1.
⇒ Opção (D) → A configuração eletrónica corresponde a orbitais 3d.
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
6.3. Justifique a afirmação seguinte, com base nas posições relativas dos elementos sódio e enxofre na Tabela Periódica.
O raio atómico do sódio é superior ao raio atómico do enxofre.
⇒ Os elementos sódio e enxofre estão localizados no 3.º período da Tabela Periódica e nos grupos 1 e 16, respetivamente.
⇒ Como o sódio precede o enxofre no mesmo período e o raio atómico tem tendência a diminuir ao longo de um período, o sódio tem maior raio do que o enxofre.
⇒ Embora o número de eletrões do enxofre, (16), seja superior ao número de eletrões do sódio, (11), o número de camadas eletrónicas mantém-se.
⇒ No entanto, a carga nuclear do átomo de enxofre, (+ 16), é superior à carga nuclear do átomo de sódio, (+ 11), o que provoca um aumento da força atrativa núcleo-eletrões.
⇒ Embora as repulsões entre os eletrões sejam maiores no átomo de enxofre (por conter maior número de eletrões), não são suficientes para vencer as maiores atrações nucleares, e, por isso, o raio atómico do sódio é superior ao raio atómico do enxofre.
- A resposta deve abordar os seguintes tópicos:
⇒ O sódio precede o enxofre no mesmo período da Tabela Periódica.
⇒ Como o raio atómico apresenta tendência para diminuir ao longo de um período, o sódio apresentará maior raio atómico do que o enxofre.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

FIM