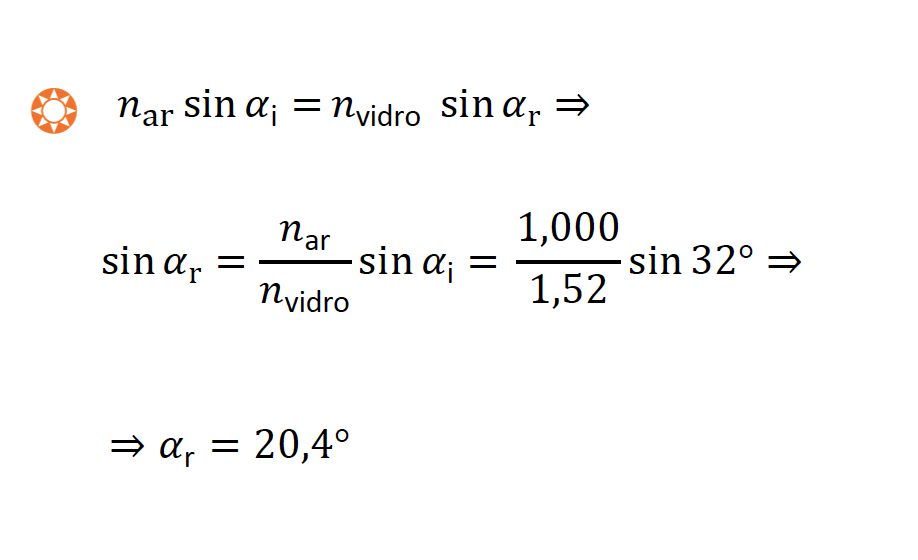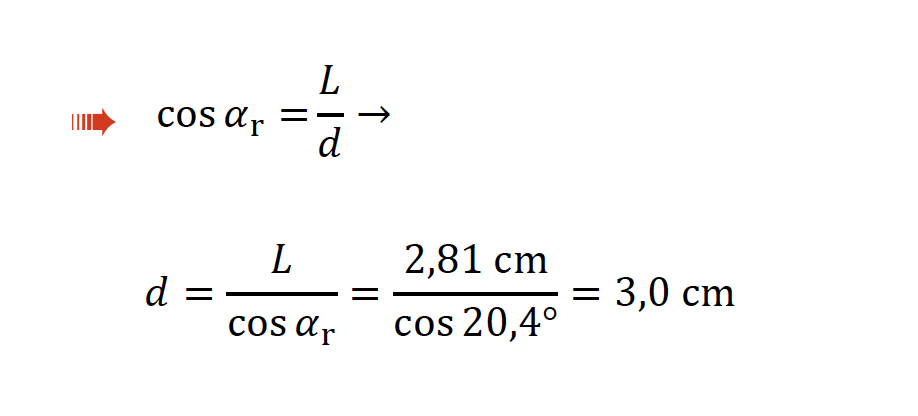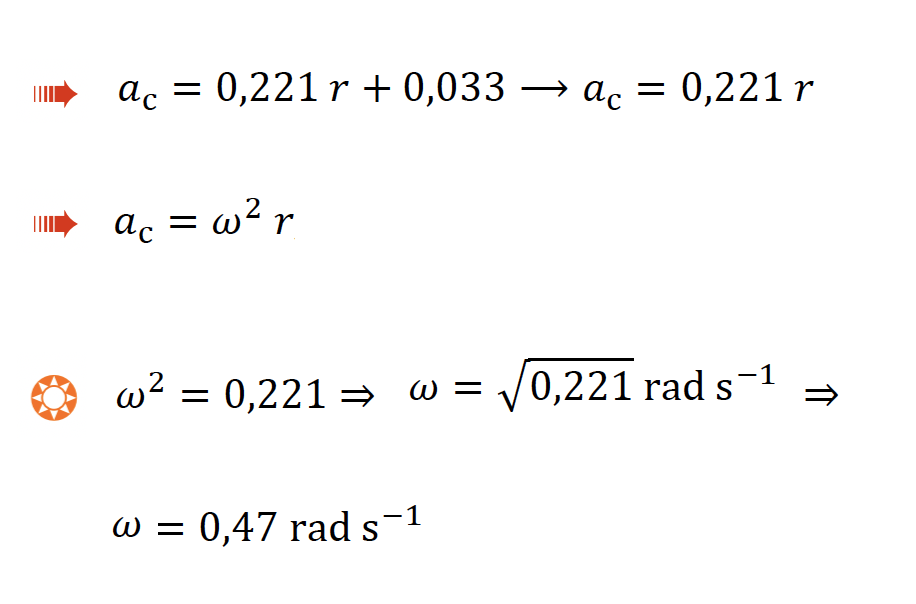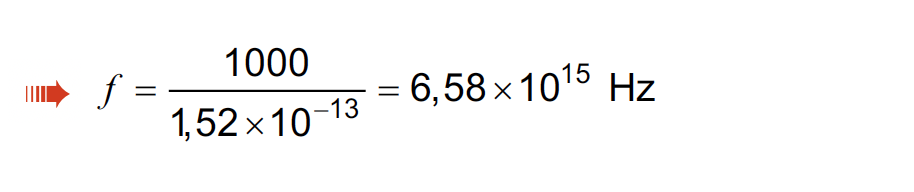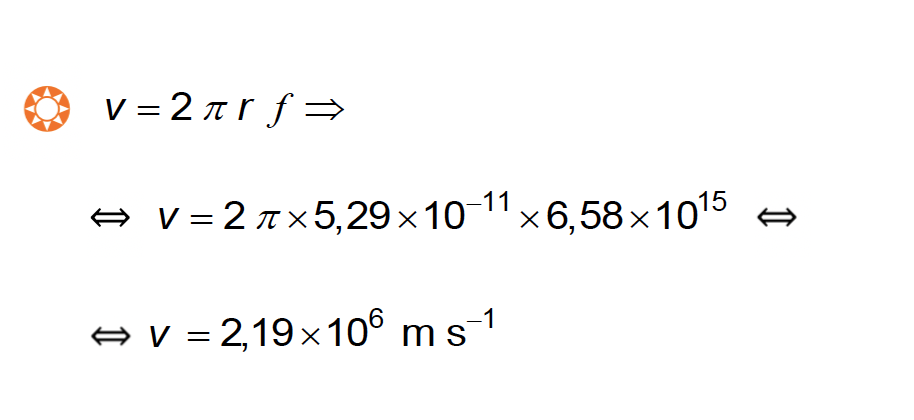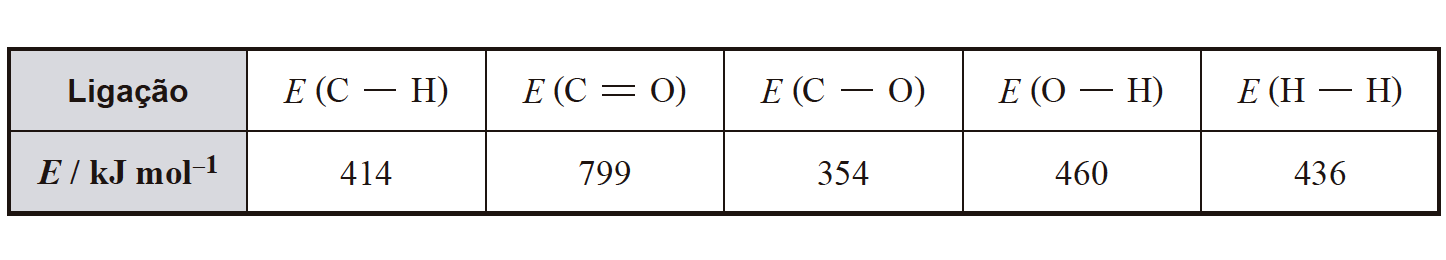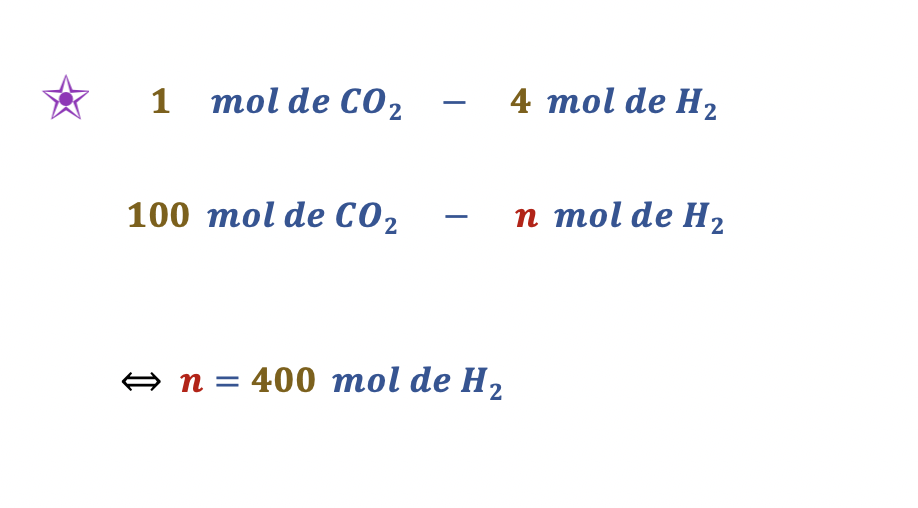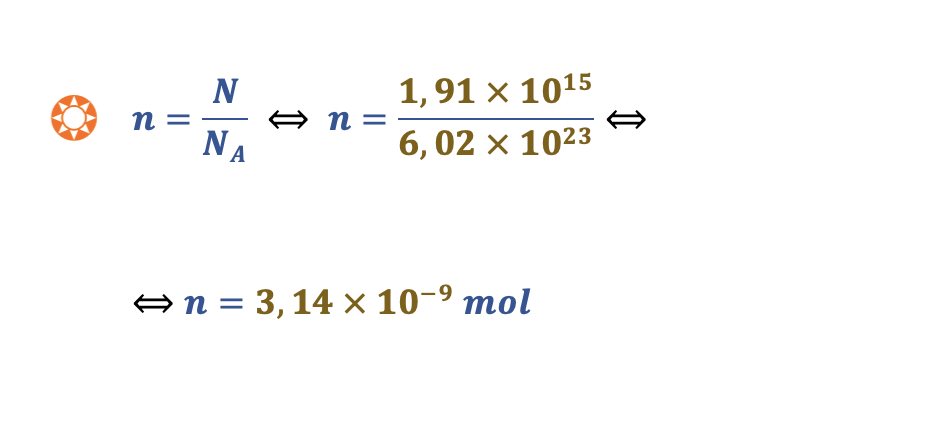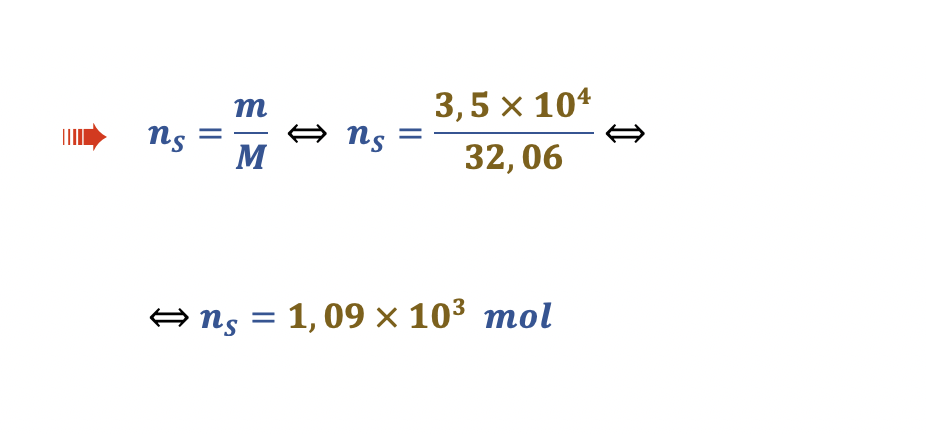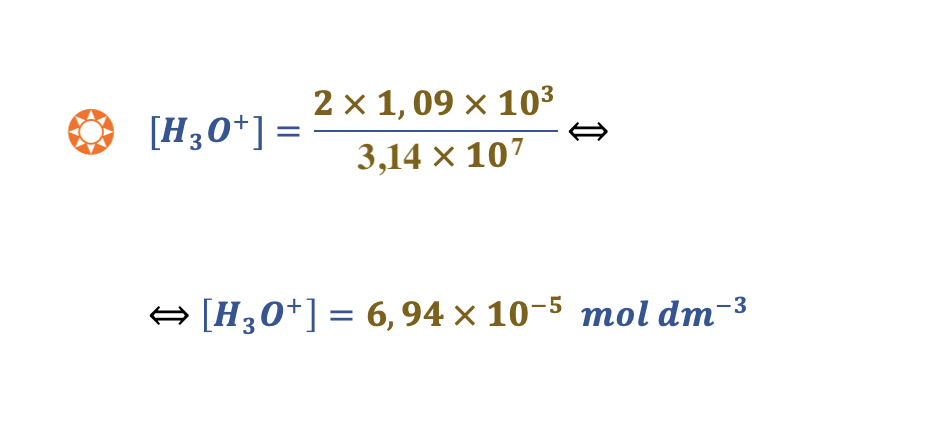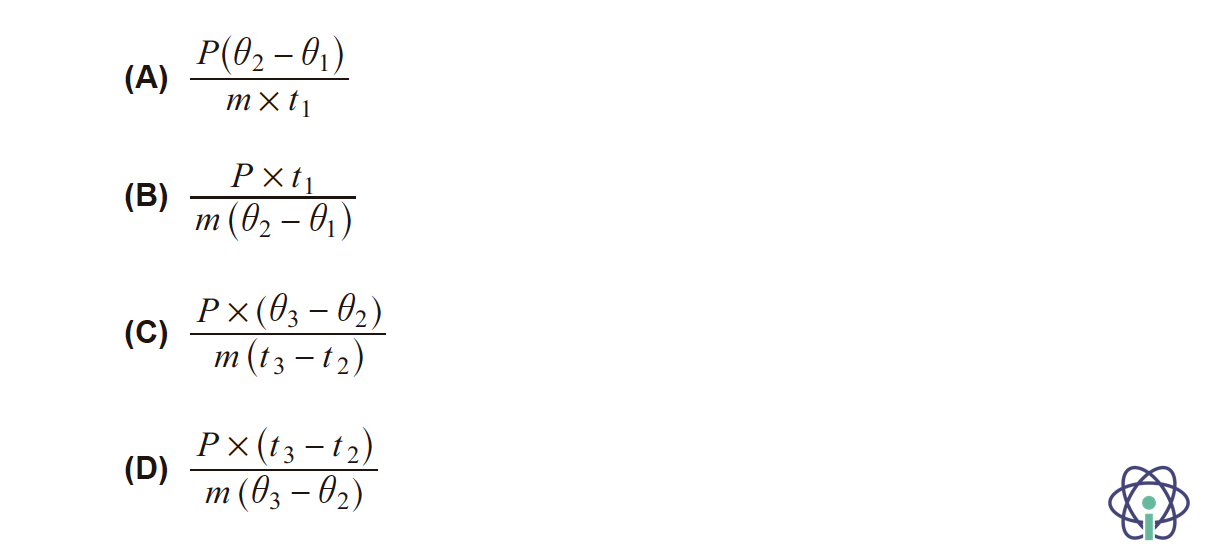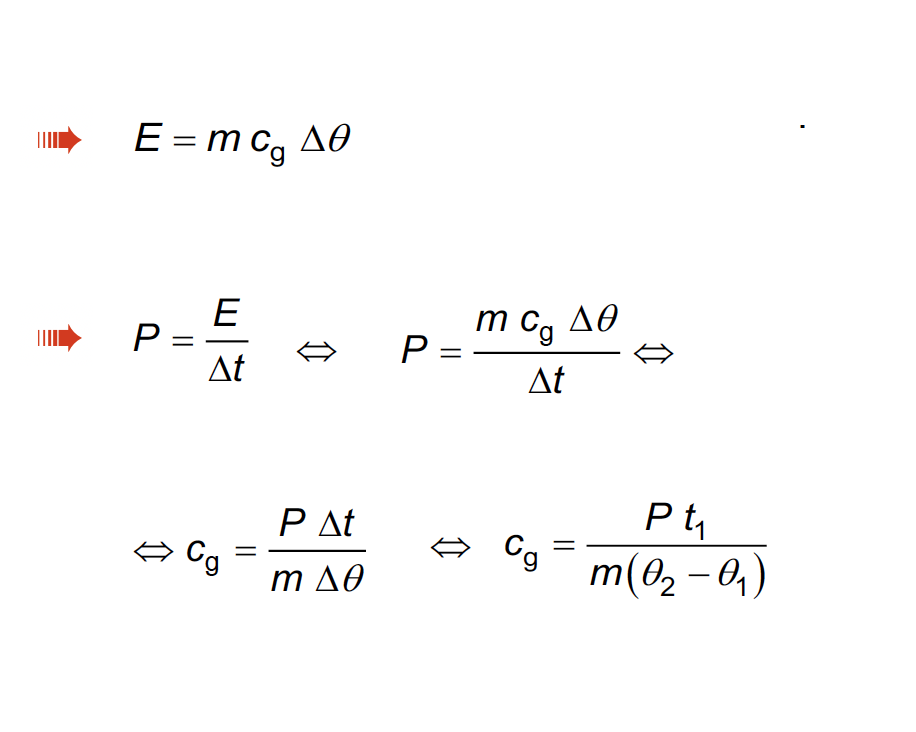Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: 2.ª Fase – 2023
A prova inclui 16 itens, devidamente identificados no enunciado, cujas respostas contribuem obrigatoriamente para a classificação final.
Dos restantes 8 itens da prova, apenas contribuem para a classificação final os 4 itens cujas respostas obtenham melhor pontuação.
1. O «papel salgado» foi um dos primeiros processos de impressão fotográfica, tendo sido utilizado comercialmente com muito sucesso entre 1840 e 1860.
Nesta técnica, um papel era impregnado com duas soluções:
- uma solução aquosa de cloreto de sódio, NaCl (M = 58,44 g mol-1);
- uma solução aquosa de nitrato de prata, AgNO3 (M = 169,88 g mol-1).
A Figura 1 apresenta o gráfico da solubilidade do AgNO3, e do NaCI em função da temperatura.
1.1. O sal mais solúvel em água, no intervalo de temperaturas considerado no gráfico, é o
(A) NaCl, e a sua solubilidade aumenta com o aumento da temperatura.
(B) NaCl, e a sua solubilidade não é afetada pela temperatura.
(C) AgNO3, e a sua solubilidade aumenta com o aumento da temperatura.
(D) AgNO3, e a sua solubilidade não é afetada pela temperatura.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (C)
🛑 O gráfico apresenta a solubilidade expressa em gramas de sal por 100 mL de água.
🛑 Para uma dada temperatura, se a massa de sal dissolvida numa mesma massa de água for maior (maior solubilidade), esse sal é mais solúvel a essa temperatura.
🛑 Verifica-se que para um dada massa de água, no intervalo de temperaturas considerado, é maior a massa dissolvida do nitrato de prata, AgNO3, e também se verifica que a massa dissolvida desse sal aumenta com o aumento de temperatura.
- Opção (C) ……………. 10 pontos
1.2. Numa reprodução deste processo, as soluções foram preparadas a 24 °C, de acordo com o procedimento seguinte:
- dissolver 12,0 g de AgNO3 em 100 mL de água destilada;
- dissolver 5,0 g de NaCI em 100 mL de água destilada.
Admita que o volume de cada solução corresponde ao volume do solvente.
1.2.1. Qual é a massa de AgNO3 que ainda seria possível adicionar à solução inicialmente preparada desse sal, para obter uma solução saturada, à temperatura de 24 °C?
(A) 245 g
(B) 238 g
(C) 250 g
(D) 210 g
- Opção (B)
🛑 De acordo com a definição de solubilidade e a partir dos dados fornecidos no gráfico da Figura 1, a massa máxima de nitrato de prata que, a 24ºC, poderá existir dissolvida em 100 mL de solução saturada é 250 g
🛑 Como a massa de nitrato de prata já dissolvida, a 24ºC, em 100 mL de água destilada é 12,0 g, a massa de nitrato de prata que ainda seria possível adicionar é:
- 250 g – 12,0 g = 238 g
- Opção (B) ……………. 10 pontos
1.2.2. O cloreto de prata, AgCl, é um sal pouco solúvel em água, sendo o seu equilíbrio de solubilidade expresso por
AgCl (s) ⇌ Ag+ (aq) + CI– (aq)
O produto de solubilidade do AgCI, Ks, é 1,6 x 10-10, à temperatura de 24 °C.
Verifique que ocorreu formação de precipitado de AgCl (s) quando se juntaram as soluções de AgNO3 e de NaCl previamente preparadas.
Mostre como chegou à verificação solicitada, apresentando todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
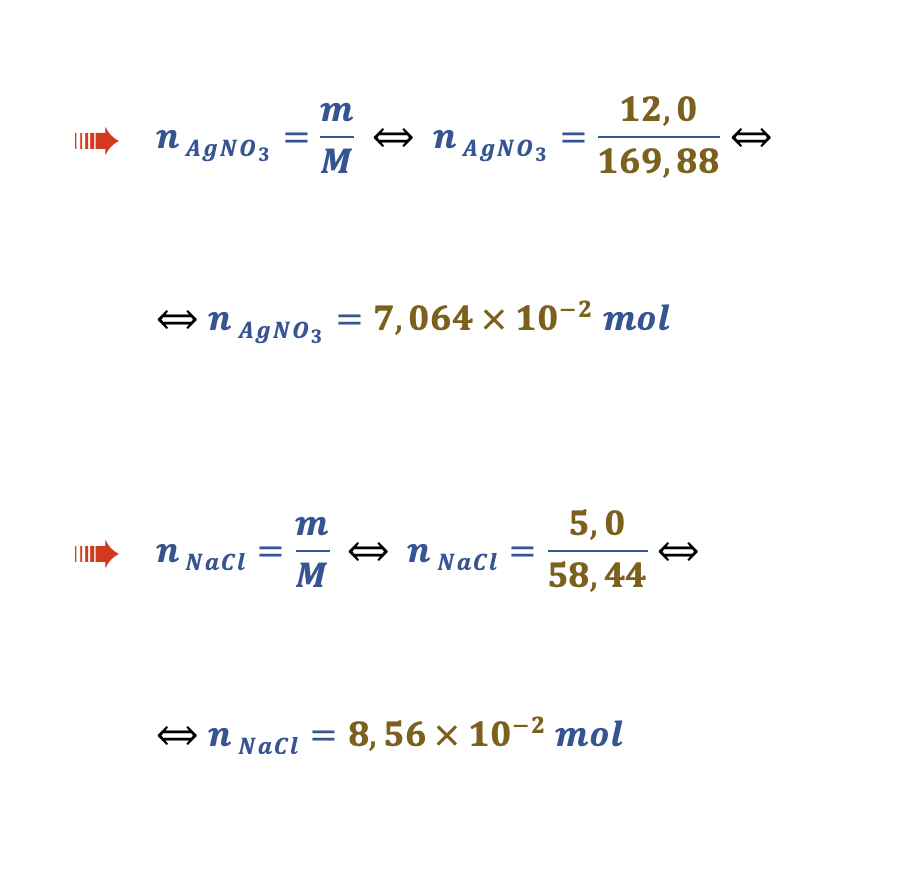
🛑 Cálculo das quantidades de matéria correspondente a 12,0 g de AgNO3 e a 5,0 g de NaCℓ:
🛑 Como se admite que o volume de cada solução é o volume do solvente (considera-se que não há variação de volume após dissolução do sal), o volume da solução resultante é:
- 𝑉 = (100 + 100) mL = 0,200 L = 0,200 dm3
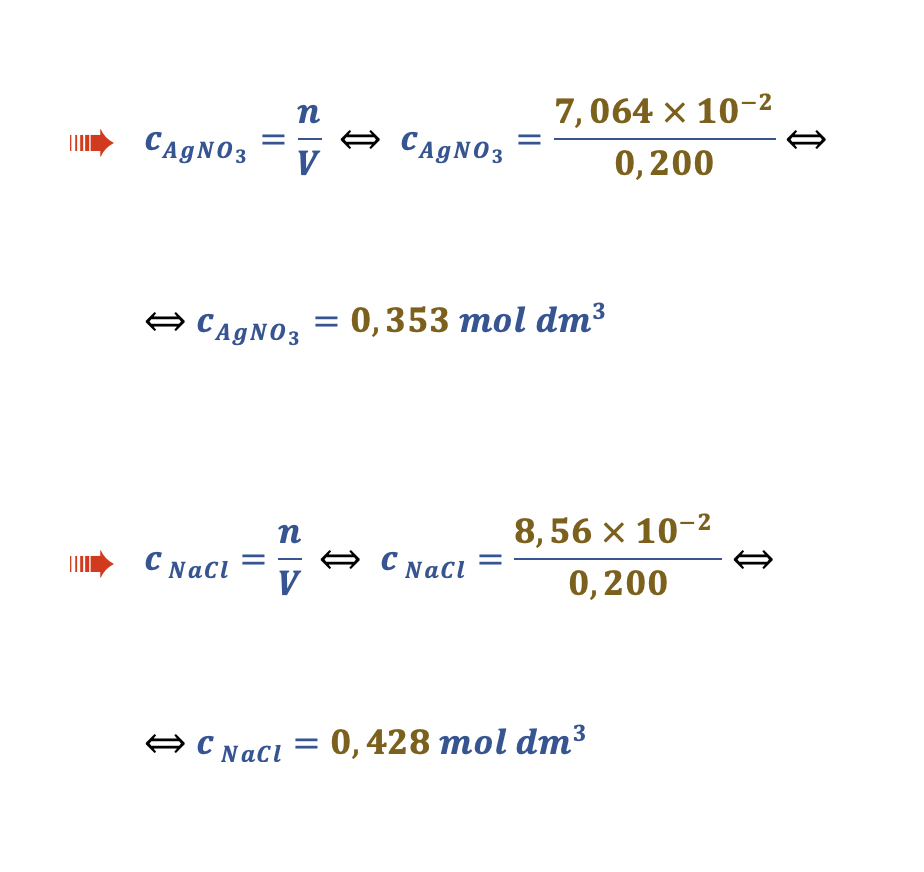
🛑 Cálculo das concentrações de AgNO3 e de NaCℓ na solução resultante da adição das duas soluções preparadas:
🛑 Como ao se dissociarem 1 mol de AgNO3 e 1 mol de NaCℓ originam, respetivamente, 1 mol de Ag+ e 1 mol de Cℓ−, na solução resultante da adição das soluções preparadas as concentrações são :
- [Ag+] = 0,353 mol dm−3
- [Cℓ−] = 0,428 mol dm−3
O quociente e reação é:
- 𝑄s = |Ag+||Cℓ−| = 0,353 × 0,428 = 0,15
Para uma solução saturada:
- |Ag+||Cℓ−| = 𝐾s = 1,6 × 10−10
🛑 Como se verifica 𝑄s > 𝐾s, houve formação de precipitado, diminuindo progressivamente o 𝑄s até se atingir a condição 𝑄s = 𝐾s, com o consequente equilíbrio químico.
2. O cloreto de prata, AgCI, é um sal branco que, ao ser exposto a uma luz suficientemente energética, sofre uma reação fotoquímica, observando-se um escurecimento.
Para investigar experimentalmente o efeito de algumas radiações do espectro visível na reação fotoquímica do AgCl, um grupo de alunos preparou cinco tubos de ensaio da forma seguinte:
Tubo de ensaio A – Sem revestimento
Tubo de ensaio B – Revestimento transparente vermelho
Tubo de ensaio C – Revestimento transparente verde
Tubo de ensaio D – Revestimento transparente azul
Tubo de ensaio E – Revestimento opaco prateado
Em cada tubo de ensaio, os alunos colocaram 1,0 mL de solução aquosa de nitrato de prata, AgNO3 (aq), e 1,0 mL de solução aquosa de cloreto de sódio,
NaCl (aq), para formar o precipitado de AgCl (s).
Após o mesmo tempo de exposição à luz visível, os alunos removeram os revestimentos dos tubos de ensaio B, C, D e E.
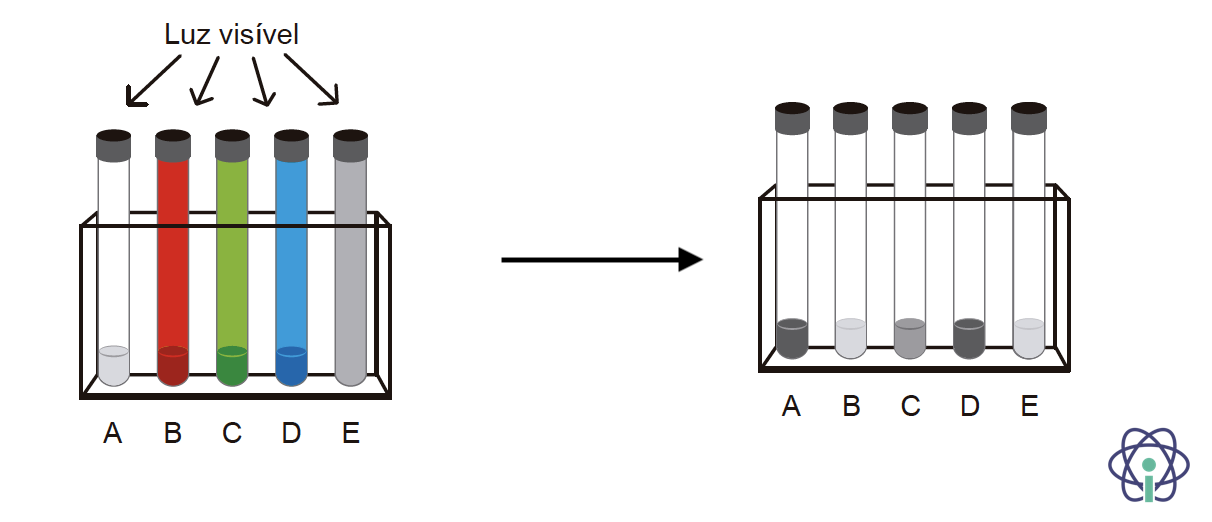
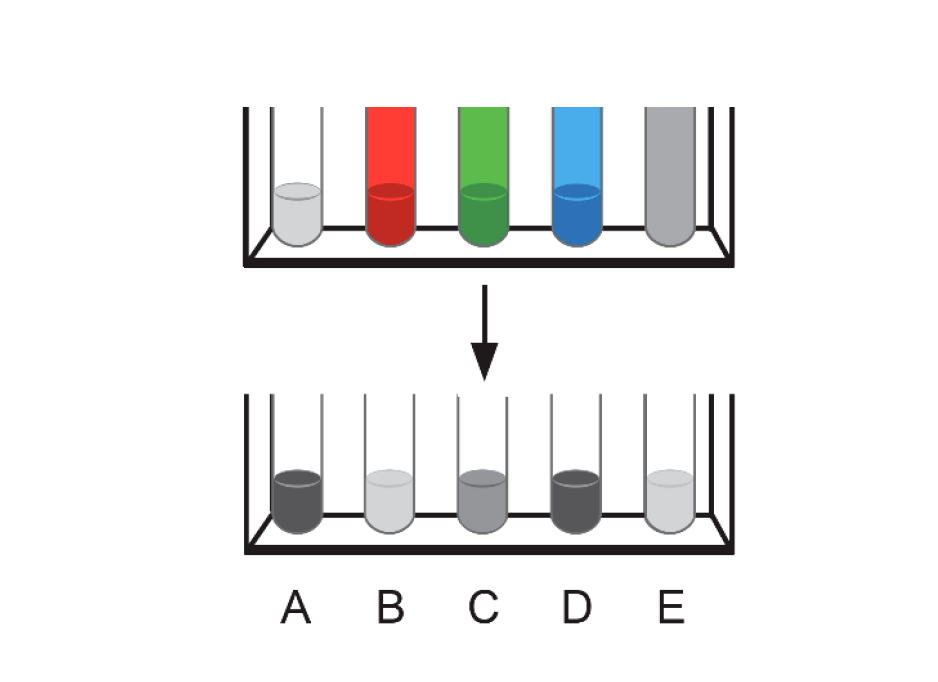
A Figura 2 esquematiza os tubos de ensaio, antes e após a remoção dos revestimentos.
Figura 2
2.1. Analisados os resultados da experiência, conclui-se que as amostras de AgCl escurecem quando são expostas a _______ das radiações da luz visível e que, no tubo de ensaio E, sendo a luz visível ________ pelo revestimento, a amostra não escurece.
(A) algumas … refletida
(B) algumas … transmitida
(C) qualquer uma … refletida
(D) qualquer uma … transmitida
- Opção (A)
🛑 Ficaram escurecidas as amostras nos tubos A, C e D: no tubo A exposto diretamente à luz ambiente, no tubo D após exposição a luz azul, predominantemente, e um pouco escurecida no tubo C após exposição a luz verde, predominantemente.
🛑 No tubo E, por ser revestido com material opaco, a luz não chegou à amostra (prevê-se que não haja transmissão de luz visível para o interior do tubo); não podendo existir nenhuma reação fotoquímica, este tubo constitui um controlo sobre como estava a solução inicialmente. Uma superfície opaca prateada é refletora da luz.
🛑 O tubo B apresenta um aspeto semelhante ao tubo E, portanto, a luz que chegou à solução não terá produzido reação no tubo B.
- Verifica-se que o AgCℓ não escurece quando exposto a luz vermelha, mas escurece com luz azul e verde.
- Opção (A) ……………. 10 pontos
2.2. Qual é a opção em que se apresentam as radiações testadas por ordem crescente de energia?
(A) Azul, vermelha e verde.
(C) Vermelha, verde e azul.
(B) Azul, verde e vermelha.
(D) Vermelha, azul e verde.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (C)
🛑 As radiações que incidiram nas amostras têm fotões tanto mais energéticos quanto mais escuras ficarem as amostras (indicando que mais AgCℓ sofreu reação) e a cor que apresentam os revestimentos correspondem às radiações que predominantemente os atravessam.
🛑 O vermelho é a cor visível mais “fria” (radiação com menor frequência) e, das radiações testadas, o azul é a cor visível mais “quente” (com maior frequência).
🛑 A sequência crescente de escurecimento das amostras é a dos tubos B, C e D (vermelho, verde e azul), correspondendo esta sequência a uma energia crescente dos fotões das radiações que atravessaram os revestimentos.
- Opção (C) ……………. 10 pontos
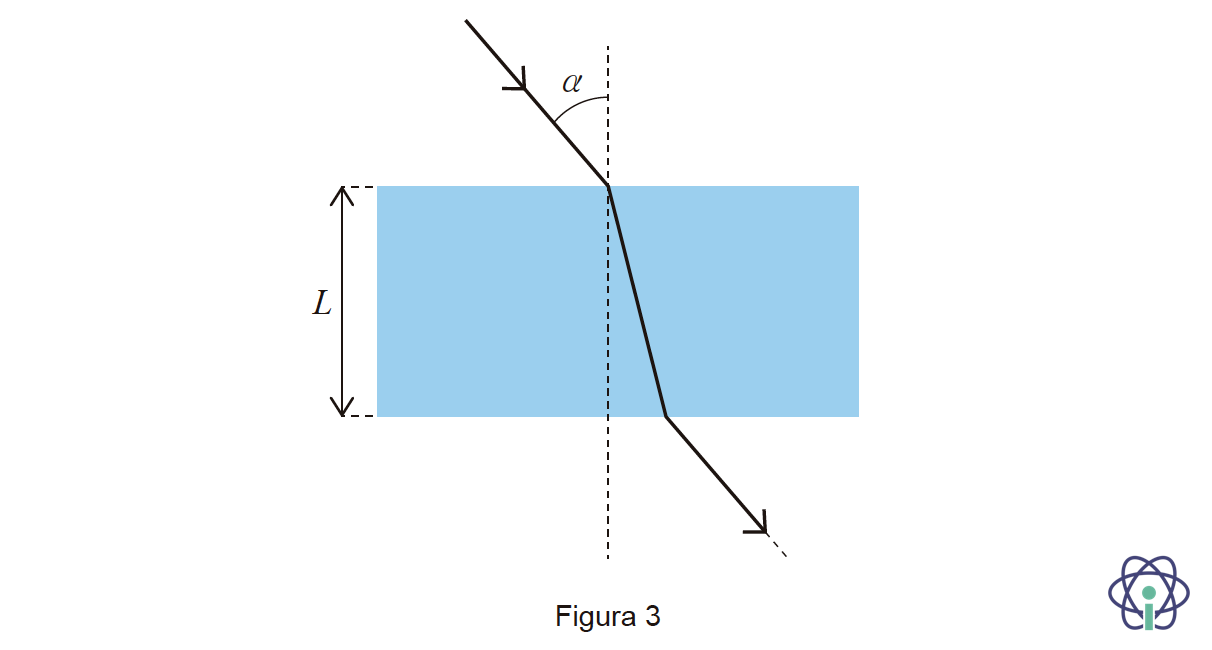
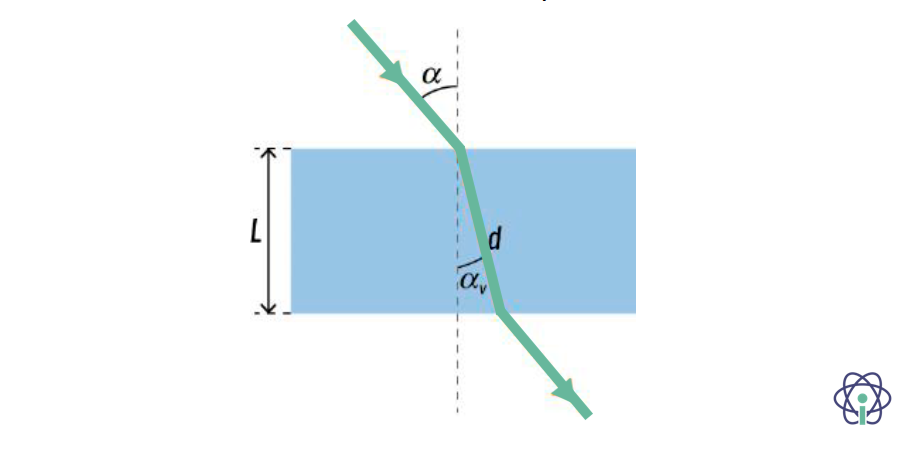
3. Um feixe de radiação monocromática, que se propaga inicialmente no ar, incide numa das faces paralelas de uma lâmina de vidro, com um ângulo de incidência α.
Ao atravessar a lâmina de vidro, de largura L, o feixe sofre um desvio na sua direção de propagação, como mostra a Figura 3.
3.1. A lâmina de vidro tem um índice de refração 1,52 para o feixe de luz considerado.
Considere que α = 32° e que L = 2,81 cm.
Determine a distância que a luz percorre ao atravessar a lâmina de vidro.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula o ângulo de refração de acordo com a lei de Snell-Descartes (20,4º) ……….. 5 pontos
🛑 Calcula a distância que a luz percorre ao atravessar a lâmina de vidro (3,0 x 10-2 m) ………… 5 pontos
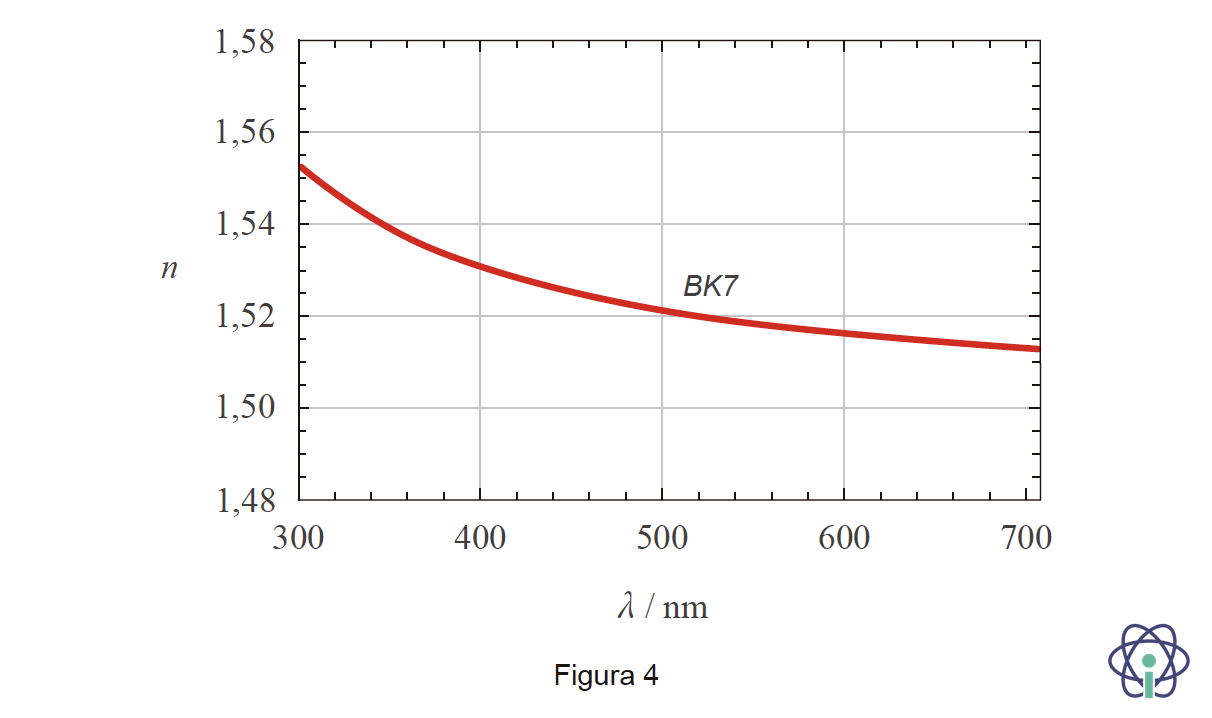
3.2. A Figura 4 apresenta o gráfico do índice de refração, n, de um vidro BK7, em função do comprimento de onda, λ, da radiação eletromagnética visível (no vácuo).
Explique, considerando a informação do gráfico, como varia a velocidade de propagação da radiação eletromagnética no vidro BK7, à medida que o comprimento de onda da radiação diminui.
Escreva um texto estruturado, utilizando linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
🛑 De acordo com a informação do gráfico da Figura 4, à medida que o comprimento de onda, λ, da radiação diminui, o índice de refração, n, do vidro aumenta.
🛑 Como c = n v, sendo c a velocidade de propagação de qualquer radiação no vazio constante, pode concluir-se que, com o aumento de n, a velocidade de propagação da radiação no vidro diminui.
🛑 De acordo com o referido, pode afirmar-se que a velocidade de propagação da radiação eletromagnética no vidro diminui com a diminuição do comprimento de onda desta.
Elementos de resposta:
🛑 refere que [de acordo com o gráfico] a um menor comprimento de onda de radiação corresponde um maior índice de refração do vidro;
🛑 refere que o índice de refração [do vidro] e a velocidade de propagação [da radiação eletromagnética no vidro] são inversamente proporcionais (ou equivalente);
🛑 conclui que para um menor comprimento de onda da radiação, a velocidade de propagação [da radiação eletromagnética] diminui.
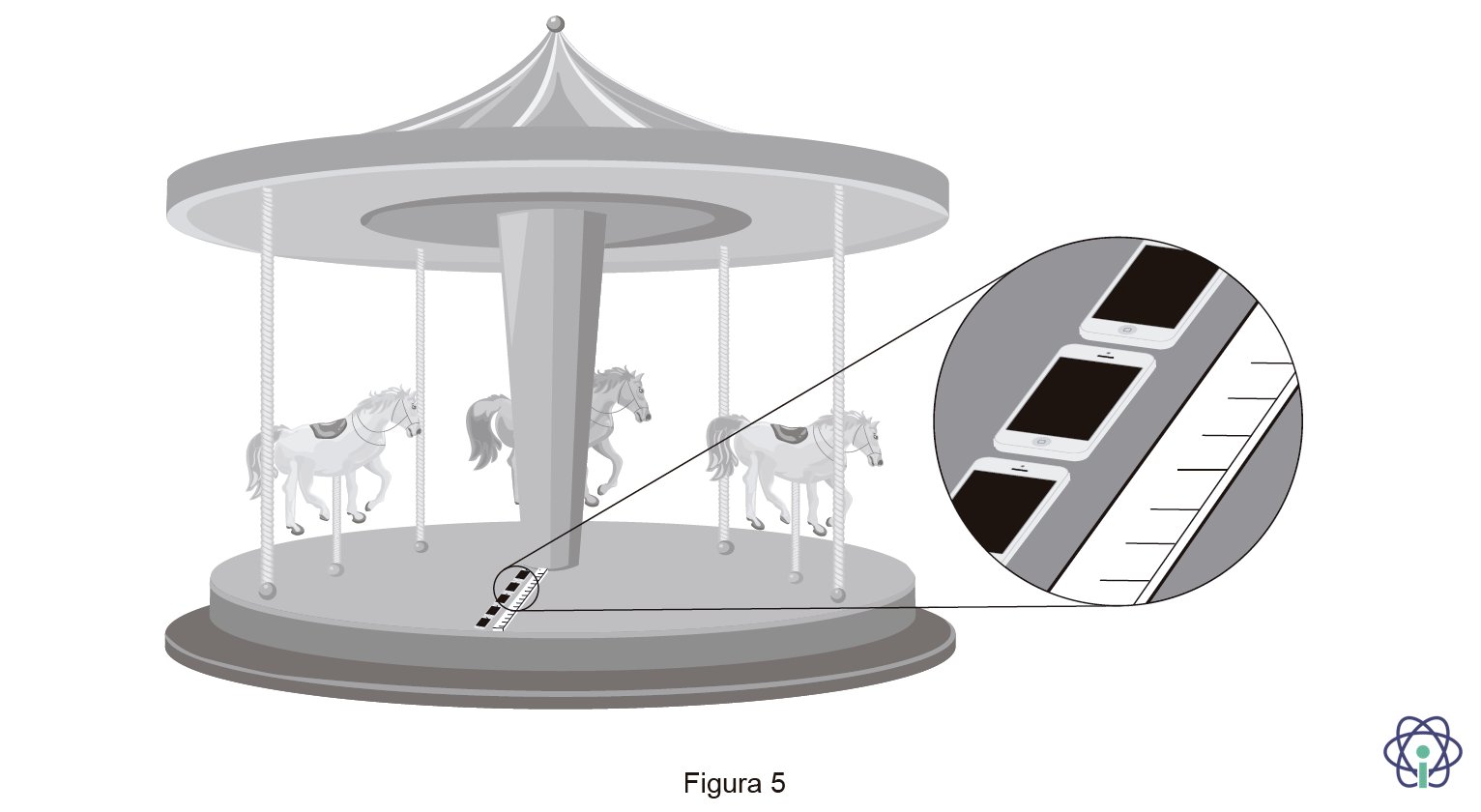
4. Para o estudo das características de um movimento circular uniforme, realizaram-se, em contexto real, num carrossel, medições do módulo da aceleração em função do raio, utilizando sensores de aceleração em telemóveis (smartphones).
Tal como é ilustrado na Figura 5, num carrossel circular, fixaram-se cinco telemóveis em posições diferentes, numa direção radial.
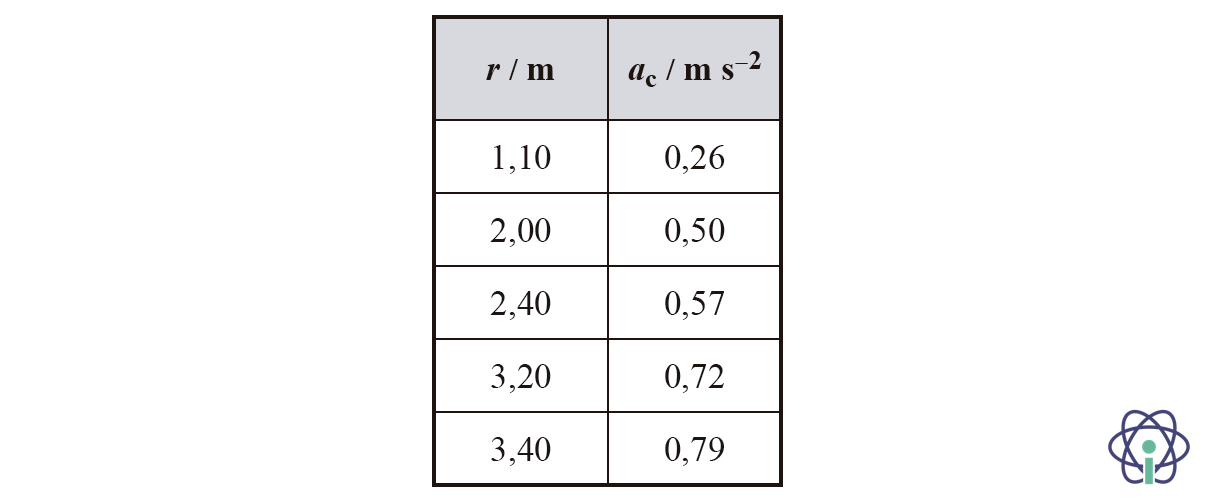
Na tabela seguinte, estão registados os raios, r, e os módulos da aceleração centrípeta, ac, medidos.
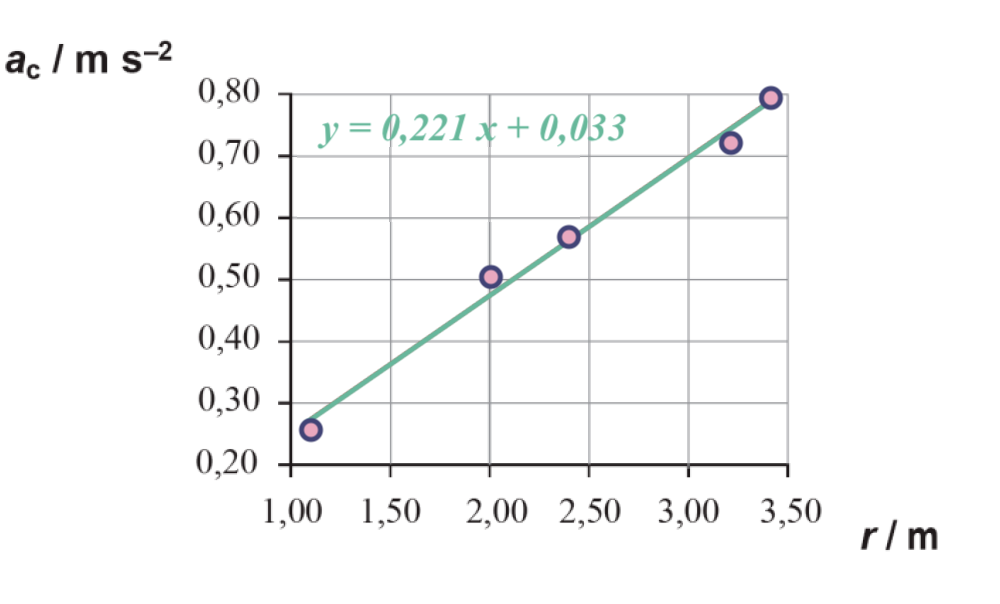
Determine o módulo da velocidade angular, nas condições em que decorre a experiência, a partir da equação da reta de ajuste a um gráfico adequado.
Na sua resposta:
- identifique as variáveis independente e dependente a considerar nos eixos do gráfico;
- apresente a equação da reta de ajuste ao gráfico;
- apresente o valor solicitado com dois algarismos significativos.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
🛑 O carrossel roda com velocidade angular constante. Como se colocam os telemóveis em diferentes posições radiais, a variável independente é o raio, 𝑟, de cada uma das trajetórias circulares descritas pelos telemóveis.
🛑 Em função da posição dos telemóveis são medidas as respetivas acelerações centrípetas, por isso, a variável dependente é a aceleração centrípeta, 𝑎c.
🛑 A aceleração centrípeta e o raio da trajetória relacionam-se por 𝑎c = 𝜔2 𝑟, sendo 𝜔 o módulo da velocidade angular.
🛑 Elaborando o gráfico 𝑎c =𝑓(𝑟) encontra-se uma relação linear, com uma reta de regressão de declive igual ao quadrado do módulo da velocidade angular.
A abcissa na origem, 0,033, resulta de erros de medida, mas é próxima de zero.
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Relaciona os raios medidos com os módulos das acelerações centrípetas medidas, através da expressão ac = ω2 x r …………. 5 pontos
🛑 Calcula o módulo da velocidade angular a partir da reta de ajuste (0,47 rad s-1) (ver nota) ………… 5 pontos
Nota ‒ A apresentação do resultado final com um número de algarismos significativos diferente do solicitado no enunciado do item implica a desvalorização de dois pontos.
5. O modelo de Bohr do átomo de hidrogénio, proposto em 1913, baseando-se em órbitas estacionárias circulares, permite o cálculo da energia dos eletrões nos diferentes níveis de energia.
A cada nível de energia do eletrão corresponde uma única órbita em torno do protão.
5.1. Admita que, no estado fundamental, o eletrão se move numa órbita circular de raio 5,29 x 10-11 m (raio de Bohr) e realiza 1000 voltas em 1,52 × 10-13 s.
Considere que o movimento do eletrão é circular e uniforme.
Qual é o módulo da velocidade do eletrão nesta órbita?
(A) 6,96 × 105 m s-1
(B) 1,09 x 106 m s-1
(C) 4,13 × 1016 m s-1
(D) 2,19 x 106 m s-1
- Opção (D) ……………. 10 pontos
5.2. Submetendo um tubo de descarga com gás di-hidrogénio rarefeito a uma descarga elétrica de alta tensão, é possível, através de um espectroscópio, observar o espectro de emissão daquele elemento.
5.2.1. A diferença de potencial entre os elétrodos nas extremidades do tubo de descarga corresponde à
(A) energia transferida para o gás rarefeito por unidade de carga que o atravessa.
(B) energia transferida para o gás rarefeito por unidade de tempo.
(C) carga transferida para o gás rarefeito por unidade de energia que é absorvida.
(D) carga transferida para o gás rarefeito por unidade de tempo.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (A) ……………. 10 pontos
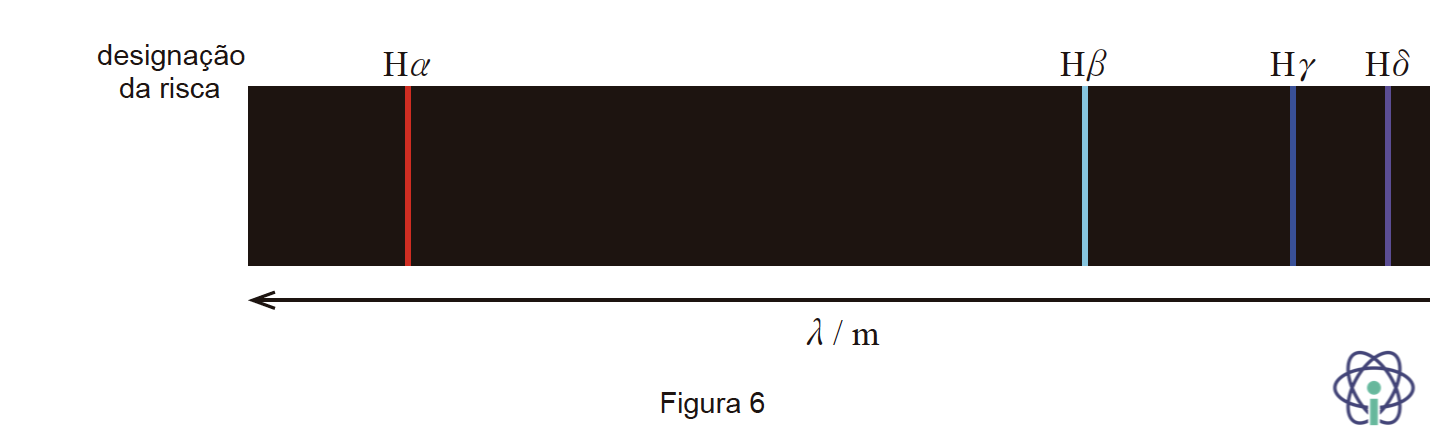
5.2.2. A Figura 6 representa as quatro primeiras riscas do espectro de emissão, na zona do visível, do átomo de hidrogénio em função do comprimento de onda, λ, da radiação.
Qual é a risca correspondente à transição eletrónica com origem no nível 4?
(A) Hα
(B) Hβ
(C) Hγ
(D) Hδ
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (B)
🛑 Um átomo, quando excitado, emite radiação por transições eletrónicas de níveis de energia superiores para níveis de energia inferiores. A energia dos fotões da radiação emitida é igual à diferença entre a energia do nível superior e a do nível inferior.
🛑 Para o átomo de hidrogénio, as radiações situam-se na zona do espetro visível quando o eletrão transita de um nível 𝑛 de energia superior (𝑛 > 2) para o nível 2. Assim, as quatro primeiras riscas no visível resultam das transições dos níveis 3, 4, 5 e 6 para o nível 2.
🛑 A transição do eletrão do nível 𝑛 = 3 para o nível 𝑛 = 2 corresponde à risca de menor energia na região do visível, a transição do eletrão do nível 𝑛 = 4 para o nível 𝑛 = 2 corresponde ao segundo menor valor de energia. Como a energia dos fotões é inversamente proporcional ao comprimento de onda, a transição eletrónica 4→2 corresponde ao segundo maior valor do comprimento de onda das riscas apresentadas, portanto, à risca H𝛽.
- Opção (B) ……………. 10 pontos
6. O di-hidrogénio, H2 (g), pode ser obtido a partir de uma reação do monóxido de carbono, CO (g), com água.
Esta reação pode ser traduzida por
CO (g) + H2O (g) ⇌ CO2 (g) + H2 (g) Н < 0
Admita que o sistema se encontra inicialmente em equilíbrio, num reservatório fechado.
Pretende-se maximizar a produção de H2.
Preveja, justificando, se cada um dos procedimentos seguintes assegura o cumprimento do objetivo pretendido:
- diminuir o volume do reservatório, mantendo a temperatura do sistema constante;
- diminuir a temperatura do sistema, mantendo o volume do reservatório constante.
Escreva um texto estruturado, utilizando linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
🛑 Uma diminuição do volume produz igual aumento, em percentagem, das concentrações de cada uma das espécies. Como a soma dos coeficientes estequiométricos dos reagentes é igual à soma dos coeficientes estequiométricos dos produtos (essas somas são iguais a 2) e as concentrações de reagentes e de produtos variam na mesma proporção, o quociente da reação, por diminuição de volume, manter-se-ia igual à constante de equilíbrio. Como a constante de equilíbrio é constante a uma mesma temperatura, diminuir o volume mantendo a temperatura, não altera o equilíbrio químico.
🛑 Pelo contrário, se o volume for constante não se alteram as concentrações, mas a diminuição de temperatura altera o valor da constante de equilíbrio. Como a reação é exotérmica no sentido direto (dado que a variação de entalpia é negativa), uma diminuição de temperatura, de acordo com o princípio de Le Châtelier, favorece o sentido direto, o da libertação de energia, aumentando, assim, a produção de di-hidrogénio.
🛑 Prevê-se que apenas com o segundo procedimento se assegure o cumprimento do objetivo pretendido, a maximização da produção de H2 (g).
Elementos de resposta:
🛑 refere que [,de acordo com o princípio de Le Châtelier,] a diminuição do volume do reservatório corresponde a um aumento da pressão que não tem influência na quantidade de H2 produzido, porque a quantidade de gases nos reagentes e nos produtos da reação é igual;
🛑 refere que [,de acordo com o princípio de Le Châtelier,] pelo facto de se tratar de uma reação exotérmica, a diminuição da temperatura do sistema [favorece a reação no sentido direto, o que] irá aumentar a quantidade de H2 produzido.
7. As indústrias cimenteiras são grandes emissoras de dióxido de carbono, CO2.
Uma das estratégias para a redução e valorização do CO2 (g) consiste em fazê-lo reagir com di-hidrogénio, H2 (g), formando metano, CH4 (g), e água, H2O (g), o que permite armazenar energia na forma de CH4 (gás natural sintético).
A reação pode ser traduzida por
CO2 (g) + 4 H2 (g) → CH4 (g) + 2 H2O (g)
7.1. Determine a variação de entalpia da reação.
Considere as energias de ligação médias apresentadas na tabela.
Apresente todos os cálculos etetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Cálculo da energia libertada na formação das ligações covalentes nas moléculas dos produtos da reação:
- 1 mol de CH4 = 4 mol de ligações C – H = 4 x 414 = 1656 kJ
- 2 mol de H2O = 2 x 2 mol de ligações O – H = 2 x 2 x 460 = 1840 kJ
🛑 Total = 3496 kJ
Cálculo da energia absorvida na rutura das ligações covalentes nas moléculas dos reagentes:
- 1 mol de CO2 = 2 mol de ligações C = O = 2 x 799 = 1598 kJ
- 4 mol de H2 = 4 mol de ligações H – H = 4 x 436 = 1744 kJ
🛑 Total = 3342 kJ
Por convenção, a energia absorvida é positiva e a energia libertada é negativa.
Determinação da variação de entalpia da reação:
- ΔH = – 3496 + 3342 = – 154 kJ
Esta reação é exotérmica, pois o valor da energia total envolvida na rutura das ligações nos reagentes é inferior ao valor da energia total envolvida na formação das ligações nos produtos.
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula a energia absorvida na quebra das ligações de 1 mol de CO2 e 4 mol de H2 (3342 kJ) (ver nota) ……….. 3 pontos
🛑 Calcula a energia libertada na formação de 1 mol de CH4 e 2 mol de H2O (3496 kJ) (ver nota) ………… 3 pontos
🛑 Calcula a variação de entalpia da reação (– 154 kJ) …………. 4 pontos
Nota ‒ A ordem das duas primeiras etapas é arbitrária.
7.2. Uma indústria cimenteira avalia a produção de gás natural sintético num teste-piloto.
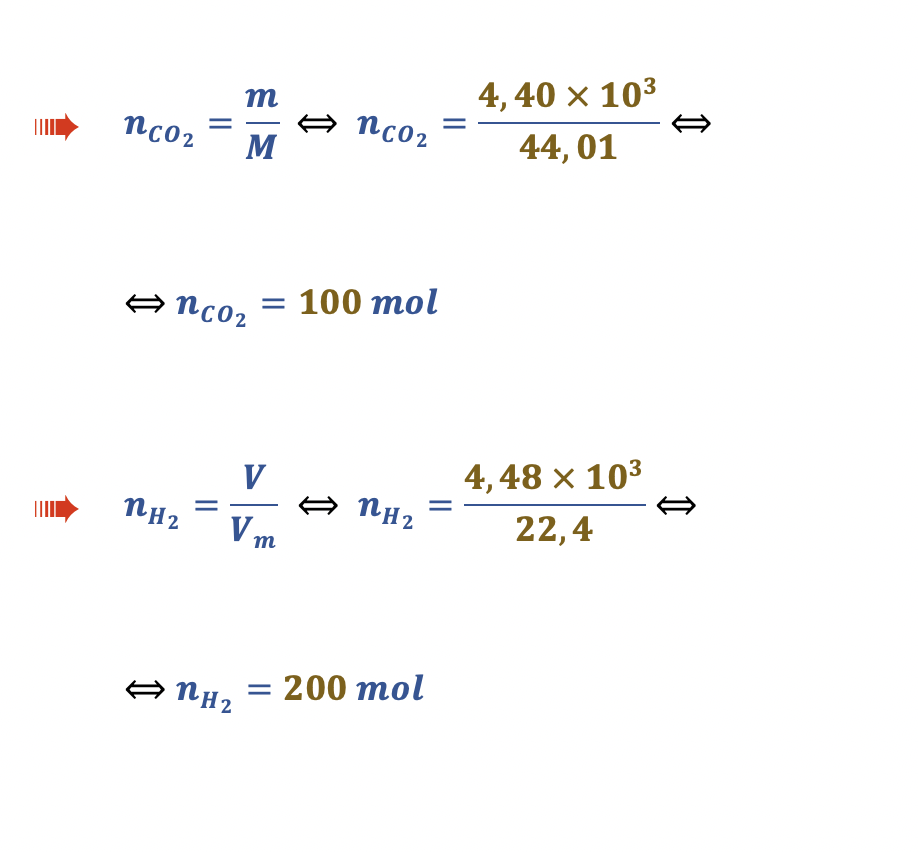
Neste teste, faz-se reagir 4,40 kg de CO2 (M = 44,01 g mol-1) com 4,48 x 103 dm3 de H2, medido em condições PTN.
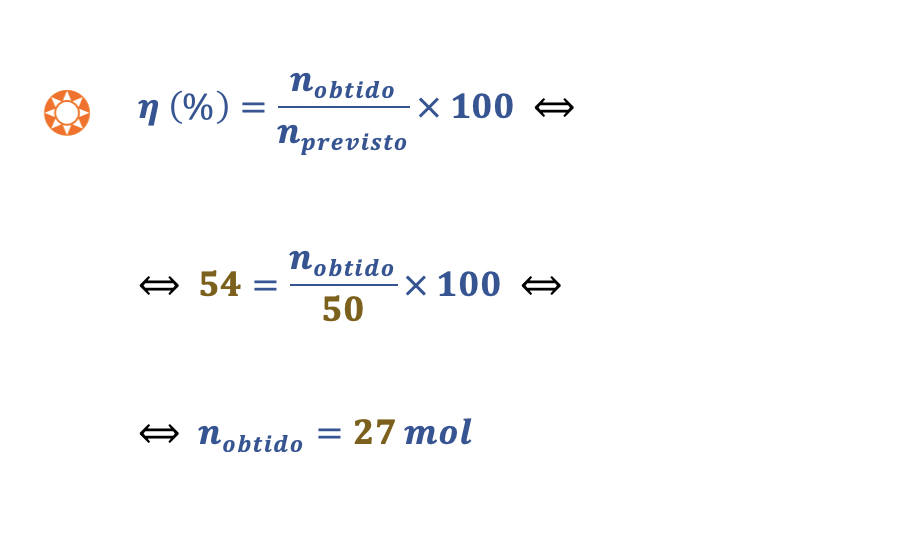
Considere que o rendimento da reação de formação de CH4 é 54%.
Qual é a quantidade de CH4 produzida?
(A) 27 mol
(B) 50 mol
(C) 54 mol
(D) 108 mol
- Opção (A) ……………. 10 pontos
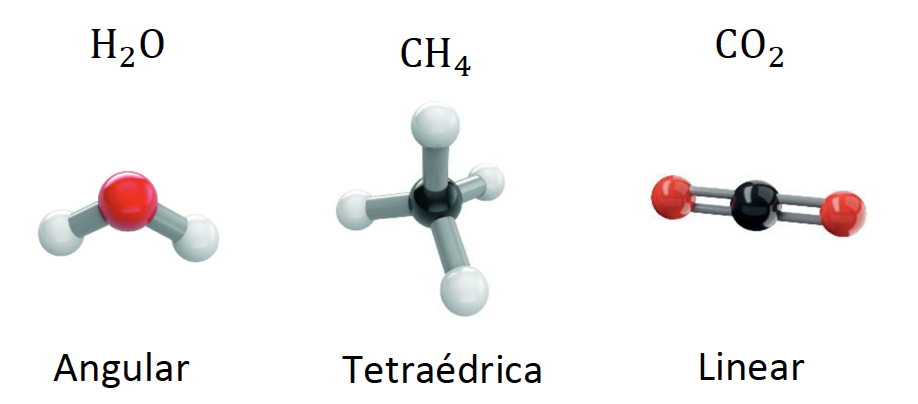
7.3. Associe as moléculas apresentadas na Coluna l às respetivas geometrias moleculares, que constam na Coluna II.
Escreva, na folha de respostas, cada letra da Coluna l, seguida do número correspondente da Coluna II.
A cada letra corresponde apenas um número.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ (a) – (2)
⇒ (b) – (3)
⇒ (c) – (5)
🛑 Entende-se por geometria molecular o modo como os átomos ou grupos de átomos ligados ao átomo central se localizam no espaço em torno desse átomo central.
É possível prever a geometria da maior parte das moléculas com base na teoria da repulsão dos pares eletrónicos de valência. Esta teoria considera que a disposição espacial dos átomos em torno de um átomo central é a que conduz à máxima estabilidade da molécula, ou seja, às menores repulsões entre as nuvens eletrónicas (correspondentes às ligações covalentes e aos eletrões não compartilhados).
- Dióxido de carbono: os pares eletrónicos que constituem as duas ligações duplas afastam-se o mais possível. Por isso, a molécula é linear.
- Metano: os quatro pares eletrónicos correspondentes às quatro ligações afastam-se o mais possível entre si. A molécula é tetraédrica.
- Água: os quatro pares eletrónicos localizam-se em torno do oxigénio o mais afastados possível uns dos outros, ou seja, segundo uma disposição, aproximadamente, tetraédrica. Dois destes pares eletrónicos são não ligantes e os dois restantes formam as duas ligações, o que confere à molécula uma geometria angular.
🟡 (A) – (2) ;
🟡 (B) – (3) ;
🟡 (C) – (5) ;
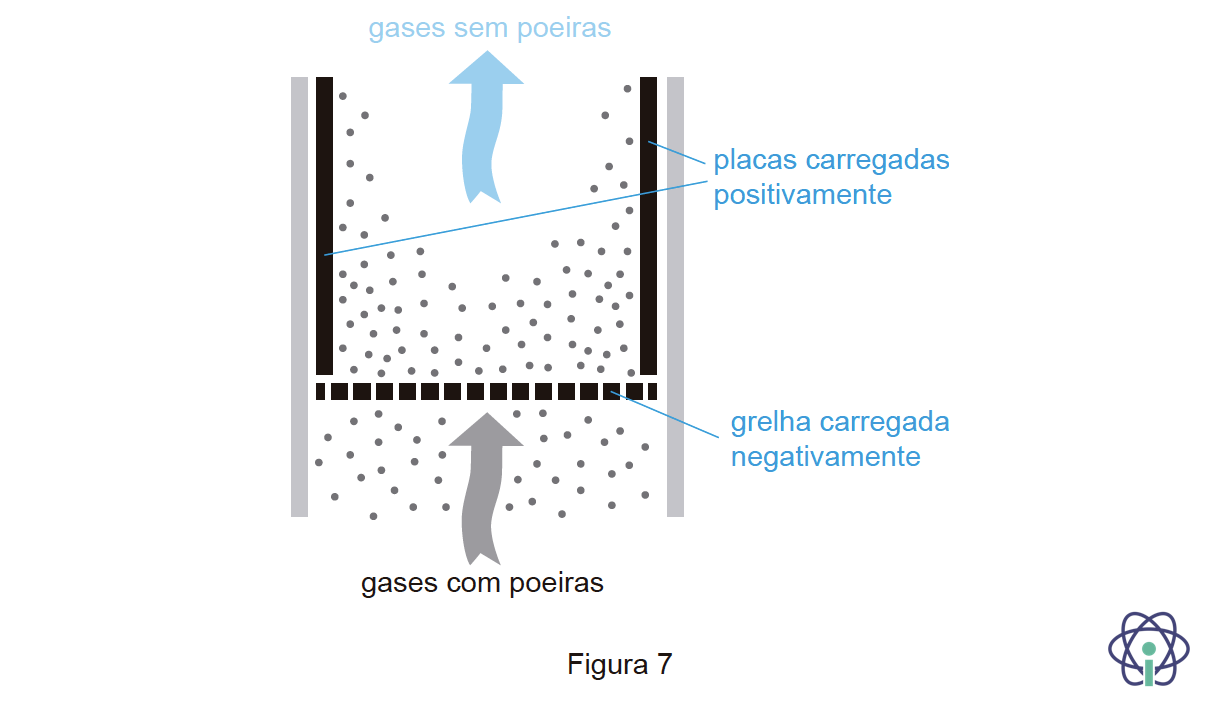
8. No âmbito das suas metas ambientais, uma indústria cimenteira instalou um precipitador eletrostático (dispositivo que remove poeiras) numa chaminé, como esquematizado na Figura 7.
8.1. As partículas constituintes dos gases de exaustão, ao atravessarem a grelha carregada negativamente, adquirem carga elétrica negativa.
Posteriormente, são atraídas pelas placas carregadas positivamente, ficando aí aprisionadas.
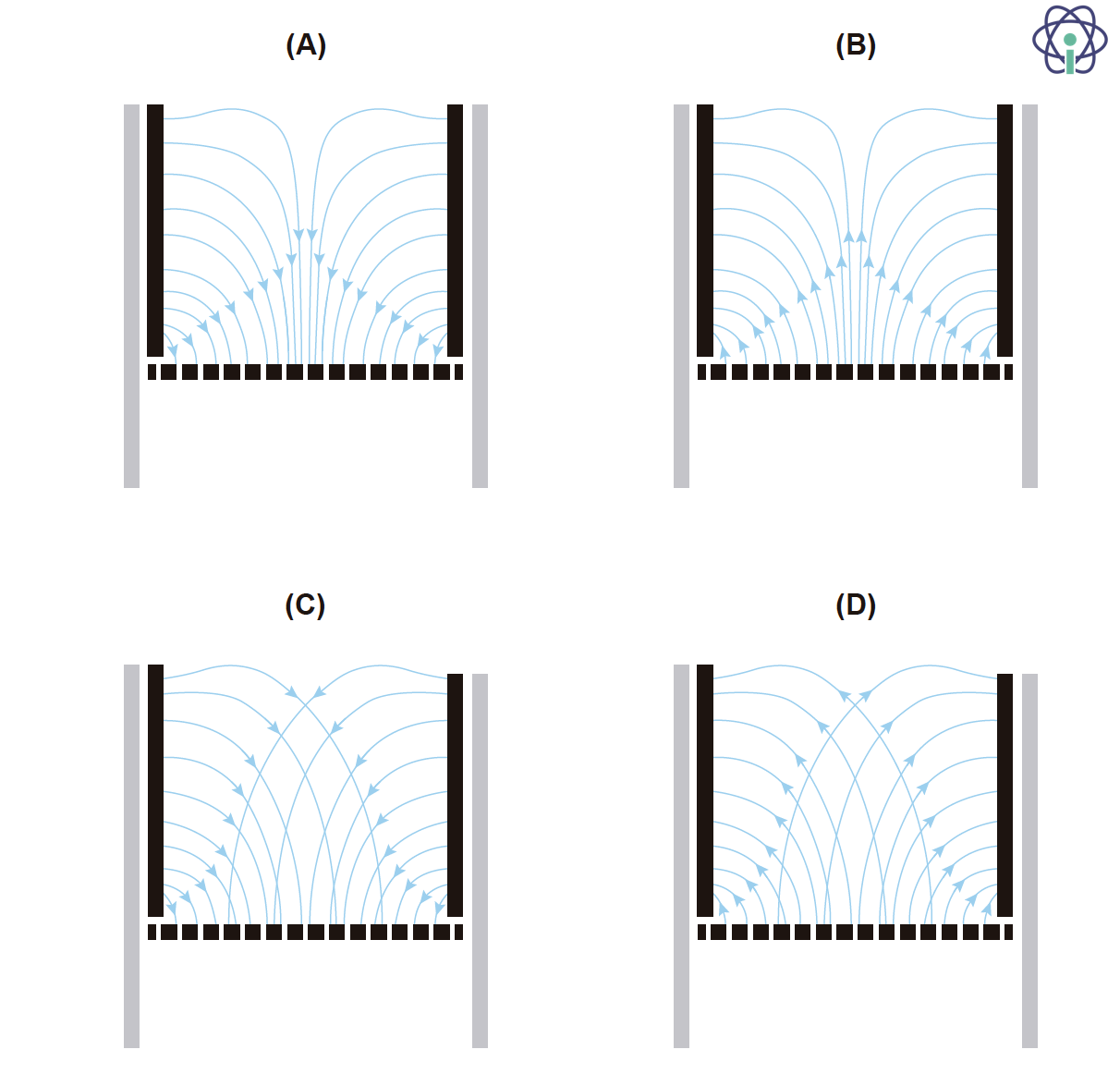
Qual das opções seguintes pode representar as linhas de campo elétrico que se geram no dispositivo que remove poeiras?
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (A) ……………. 10 pontos
8.2. Na monitorização do ar à saída do precipitador, é avaliada a concentração de material particulado.
PM, constituído fundamentalmente por partículas em suspensão.
Considere que, a partir de uma amostra de 1 m3 de gases de exaustão, se obtém, por filtração, uma massa de 5,00 x 10-5 g de material particulado.
Admita um valor médio de 2,62 x 10-20 g de massa para uma partícula de PM.
Qual é a quantidade de PM, em unidades SI, na amostra considerada?
(A) 5,24 x 10-6
(B) 3,15 × 108
(C) 1,91 x 1015
(D) 3,17 × 10-9
- Opção (D) ……………. 10 pontos
8.3. A utilização de carvão nas cimenteiras é responsável pela presença de dióxido de enxofre, SO2, nos gases à saída do precipitador eletrostático.
Admita que:
- o teor de enxofre, S (s), no carvão é 3,5% (em massa);
- na queima de 1,0 tonelada de carvão, todo o enxofre se espalha na atmosfera, sob a forma de SO2 (g), numa área circular de 1,0 km de raio (A = πr2);
- a precipitação nesta área arrasta os produtos gasosos resultantes da combustão e origina uma «toalha» líquida no solo de 10 mm de altura;
- todo o enxofre presente no combustível fóssil é oxidado a ião sulfato, SO42- (ag).
As duas reações que ocorrem podem ser traduzidas por
S (s) + O2 (g) → SO2 (g)
2 SO2 (g) + O2 (g) + 6 H2O (l) → 2 SO42- (aq) + 4 H3O+ (ag)
Determine o pH da água da chuva nesta área, após a queima de 1,0 tonelada de carvão.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
A massa de enxofre em uma tonelada de carvão é:
- 𝑚S = 0,035 × 103 kg = 3,5 × 104 g
A correspondente quantidade de matéria é:
O volume da «toalha» de água é:
- 𝑉 = 10 × 10−3 × π × (1,0 × 103 )2 = 3,14 × 104 m3 = 3,14 × 107 dm3
Admite-se que 𝑛(S) = 𝑛(SO2) e, de acordo com a estequiometria das reações, 𝑛(H3O+) = 2 𝑛(SO2)
Sendo o:
- pH = − log |H3O+| = − log (6,94 × 10−5) = 4,2
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula a quantidade de enxofre numa tonelada de carvão (1,09 x 103 mol) (ver nota) ……….. 3 pontos
🛑 Calcula o volume de água da chuva na área considerada (3,14 x 107 dm3) (ver nota) ……….. 2 pontos
🛑 Calcula, de acordo com a estequiometria das equações, a concentração de H3O+ na água da chuva (6,94 x 10-5 mol dm-3) ………… 3 pontos
🛑 Calcula o pH da água da chuva (4,2) ………….. 2 pontos
Nota ‒ A ordem das duas primeiras etapas é arbitrária
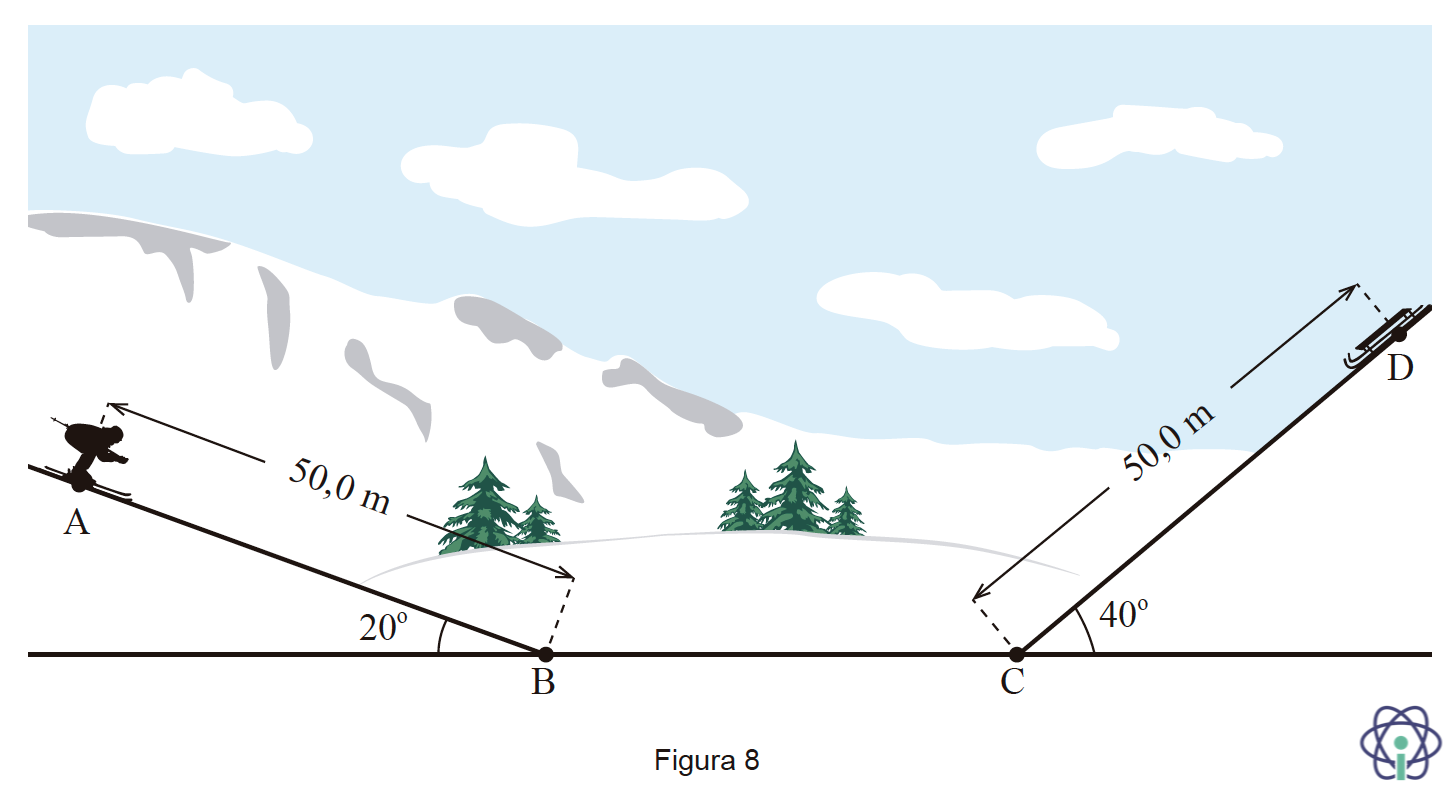
9. Uma esquiadora (e) desliza ao longo de uma encosta gelada.
No instante em que a esquiadora passa na posição A, um trenó (t), inicialmente em repouso, desprende-se de uma encosta do lado oposto, tal como se representa na Figura 8, que não está à escala.
Os dois corpos, após a descida das encostas, passam a mover-se no plano horizontal.
Admita que:
- ambos os corpos percorrem 50,0 m nas vertentes inclinadas das encostas;
- Mesaviadora = 3 mtrenó ;
- os dois corpos descrevem sempre trajetórias retilíneas;
- o atrito e a resistência do ar são desprezáveis;
- a esquiadora e o trenó podem ser representados pelos seus centros de massa, segundo o modelo da partícula material;
- o troço horizontal BC é o nível de referência da energia potencial gravítica.
9.1. Qual das opções seguintes pode representar a relação entre o módulo da aceleração da esquiadora, ae, e o do trenó, at, e a relação entre o módulo da variação da energia potencial gravítica do sistema esquiadora + Terra, AEpe, e o do sistema trenó + Terra, AEpt, nos deslocamentos AB e DC, respetivamente?
(A) | ae | > | at | e | ΔEpe | > | ΔEpt |
(B) | ae | > | at | e | ΔEpe | < | ΔEpt |
(C) | ae | < | at | e | ΔEpe | > | ΔEpt |
(D) | ae | < | at | e | ΔEpe | < | ΔEpt |
- Opção (C)
- ΔEp = m g Δh
- Δh = d sen α
- me = 3 mt
A aceleração adquirida ao longo de um plano inclinado (rampa) é :
- Fr = ma ⇔ Px = ma ⇔ m g sen α = m a ⇔ a = g sen α
🛑 Para a esquiadora:
- |ae| = 9,8 x sen 20º = 3,35 m s-2
- ΔEpe = m g Δh = 3 mt g d sen α = 3 mt g 50 sen 20º = 51,3 mt g J
🛑 Para o trenó:
- |at| = 9,8 x sen 40º = 6,30 m s-2
- ΔEpt = mt g Δh = mt g d sen α = mt g 50 sen 40º = 32,1 mt g J
- Opção (C) ……………. 10 pontos
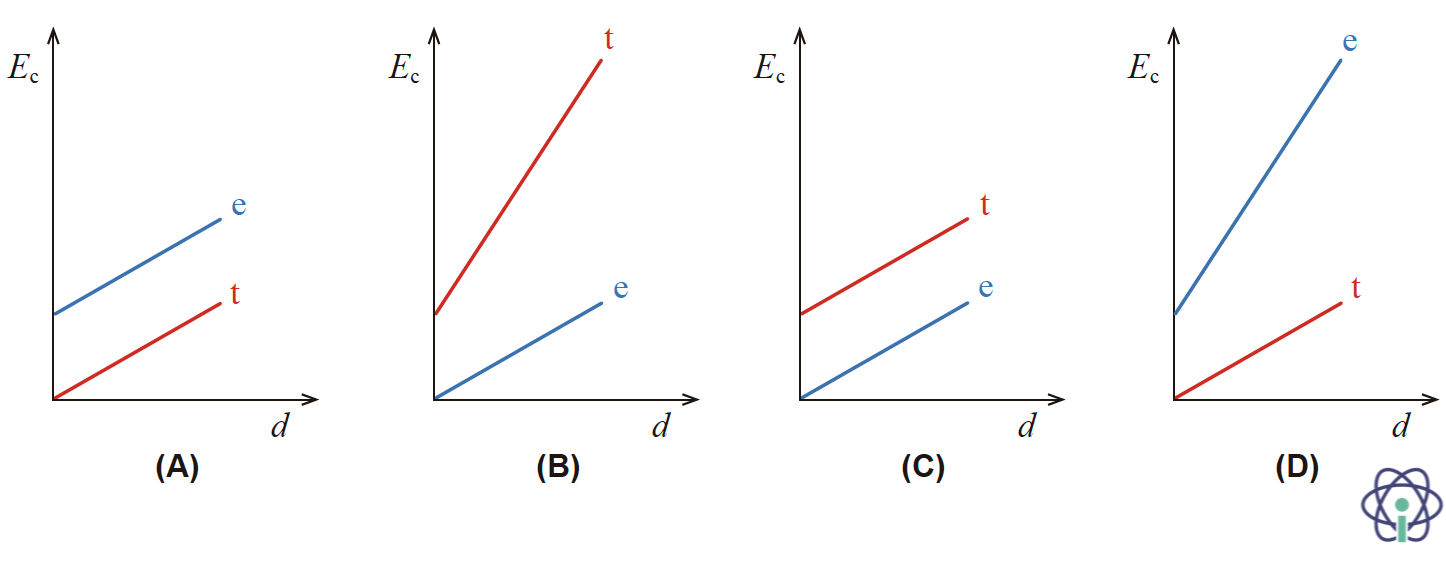
9.2. Qual das opções seguintes corresponde ao esboço do gráfico da energia cinética, Ec, da esquiadora e do trenó, em função da distância, d, percorrida ao longo das encostas, AB e DC, respetivamente?
- Opção (D) ……………. 10 pontos
9.3. Após o percurso AB, a esquiadora, no plano horizontal, cruza-se com o trenó, deslocando-se ambos com velocidades de igual módulo.
Determine o módulo da velocidade da esquiadora no instante em que o trenó se desprende.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
A esquiadora e o trenó encontram-se no plano horizontal com o mesmo módulo de velocidade, v.
🛑 Dado que o trenó parte do repouso em D e como há conservação de energia mecânica, pode escrever-se, para o trenó:
- Ecf = Epi ⇔ ½ mt vt2 = mt g 50,0 sen 40º ⇔ vt2 = 2 x 9,8 x 50,0 sen 40º ⇔ vt2 = 6,30 x 102 ⇔ vt = 25,1 m s-1
Para a esquiadora, a velocidade final é 25,1 m s-1
- Ecf = Epi ⇔ ½ me ve2 = me g 50,0 sen 20º + ½ me vei2 ⇔ vei2 = ve2 – 2 x 9,8 x 50,0 sen 20º ⇔ vei2 = 25,12 – 100 x 9,8 x 50,0 sen 20º ⇔ vei2 = 2,95 x 102 ⇔ vei = 17,1 m s-1
A velocidade com que a esquiadora parte da posição A é, em módulo, igual a 17,1 m s−1
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula o módulo da velocidade atingida pelo trenó em C (25,1 m s-1) …….. 5 pontos
🛑 Calcula o módulo da velocidade da esquiadora em A (17 m s-1) …….. 5 pontos
10. No laboratório, é comum aquecerem-se amostras de água.
10.1. Considere que uma amostra de água no estado líquido é aquecida numa placa elétrica, utilizando-se um copo de precipitação.
Minimizam-se as perdas de massa e de energia para o exterior se o copo de precipitação estiver
(A) destapado e o seu diâmetro for igual ao da placa elétrica.
(B) tapado e o seu diâmetro for igual ao da placa elétrica.
(C) destapado e o seu diâmetro for inferior ao da placa elétrica.
(D) tapado e o seu diâmetro for inferior ao da placa elétrica.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (B)
🛑 Se o copo de precipitação estiver tapado, impede-se a troca de massa com o exterior (o sistema copo + água é fechado).
🛑 Se o copo de precipitação tiver o diâmetro da placa de aquecimento, minimiza-se a perda de energia, pois, no caso de a placa ter um diâmetro superior ao do copo de precipitação, o ar por cima do excesso de área da placa seria aquecido e subiria por convecção, sendo renovado por ar mais frio.
🛑 A energia útil para aquecimento da água seria menor.
- Opção (B) ……………. 10 pontos
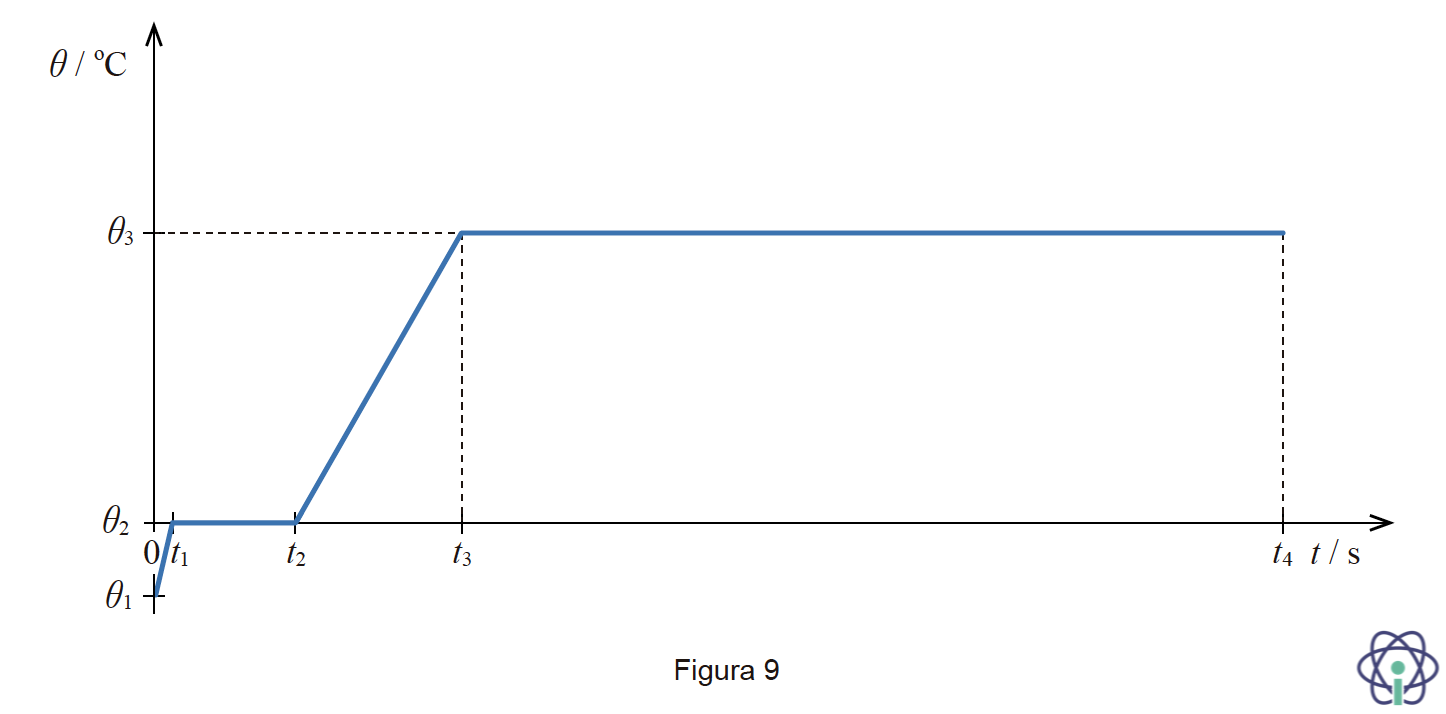
10.2. A Figura 9 apresenta o gráfico teórico da temperatura, θ, de uma amostra de água de massa m, em função do tempo, t, desde o estado sólido (gelo) até à sua vaporização completa, a pressão constante.
Admita que a amostra é aquecida numa placa elétrica de potência, P, constante e que o rendimento no processo de aquecimento é 100%
10.2.1. Qual das expressões seguintes permite calcular a capacidade térmica mássica do gelo?
Despreze as perdas de massa durante o aquecimento do gelo.
- Opção (B) ……………. 10 pontos
10.2.2. Complete o texto seguinte, selecionando a opção adequada a cada espaço.
Escreva, na folha de respostas, cada uma das letras seguida do número que corresponde à opção selecionada.
A cada letra corresponde um só número.
De acordo com a informação apresentada no gráfico da Figura 9, pode concluir-se que, durante as mudanças de fase da amostra de água, a temperatura da água ___ (a) ___ e a sua energia interna ___ (b) ___. A energia necessária para a vaporização completa da amostra de água foi ___ (c) ___ à energia necessária para a sua fusão completa.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ (a) – (2)
⇒ (b) – (1)
⇒ (c) – (1)
🛑 Durante as mudanças de fase, a energia absorvida quebra as ligações entre as moléculas (ligações intermoleculares), não aumentando, em média, a energia cinética das moléculas, consequentemente, a temperatura mantêm-se.
🛑 A energia interna do sistema aumenta uma vez que o sistema está a absorver energia da placa.
🛑 Como potência absorvida é constante, a energia absorvida é diretamente proporcional ao tempo decorrido.
🛑 A mudança de fase ocorre quando a temperatura é constante, e verifica-se no gráfico que o tempo decorrido foi maior para a temperatura 𝜃3 (evaporação) do que para a temperatura 𝜃2 (fusão).