2019 – Época Especial – Prova Escrita de FQ A
Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: Época especial – 2019
GRUPO I
1. A Figura 1 representa um gerador de sinais ligado a um altifalante e um microfone ligado a um osciloscópio. O gerador de sinais produz um sinal elétrico que é convertido num sinal sonoro pelo altifalante.
Este sinal sonoro é detetado pelo microfone, que o converte num sinal elétrico que é visualizado no ecrã do osciloscópio.
A Figura 2 representa o sinal elétrico visualizado no ecrã do osciloscópio, quando a base de tempo do osciloscópio está regulada para 250 μs por divisão e o amplificador vertical está regulado para 5 mV por divisão.
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
1.1. O sinal visualizado no ecrã do osciloscópio tem um período de _____ e uma amplitude de _____.
(A) 1,1 ms … 14 mV
(B) 4,5 ms … 14 mV
(C) 1,1 ms … 28 mV
(D) 4,5 ms … 28 mV
- Opção (A)
⇒ O Período do sinal é igual ao intervalo de tempo que decorre entre dois instantes na mesma fase, o intervalo de tempo entre dois máximos consecutivos da onda observada no osciloscópio.
⇒ A amplitude da onda é igual ao módulo do valor máximo (ou mínimo) da onda.
 Assim:
Assim:
⇒ A = 2,8 x 5 mV = 14 mV
⇒ T = 4,4 x 250 μs = 1,1 x 103 μs = 1,1 x 103 x 10-3 ms = 1,1 ms
- Opção (A) ……………. 7 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
- 11ºano – Física – A.l. – 2.1 – Características do som
1.2. O sinal sonoro produzido pelo altifalante e o sinal sonoro detetado pelo microfone terão frequências _____ e intensidades _____ .
(A) diferentes … iguais
(B) diferentes … diferentes
(C) iguais … iguais
(D) iguais … diferentes
- Opção (D)
⇒ O sinal sonoro tem a mesma frequência da fonte, o altifalante que por que o produziu.
⇒ Esta frequência não se altera devido ao meio em que se propaga e, portanto o sinal recebido pelo microfone tem a mesma frequência.
⇒ A intensidade depende energia do sinal transporta em cada ponto.
⇒ A onda sonora propaga-se em três dimensões, transferindo energia progressivamente para as camadas de ar à medida que se afasta do altifalante.
- Assim, o som vai diminuindo de intensidade com a distância altifalante.
- Opção (D) ……………. 7 pontos
- 11ºano – Física – Domínio 2 – subdomínio 2 (Eletromagnetismo)
2*. A Figura 3 representa um microfone de indução.
Este microfone é constituído, essencialmente, por uma membrana e por uma bobina ligadas entre si e, ainda, por um íman fixo colocado na proximidade da bobina. Explique como é que um sinal sonoro é convertido num sinal elétrico, neste tipo de microfones. Apresente, num texto estruturado e com linguagem científica adequada, a explicação solicitada.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
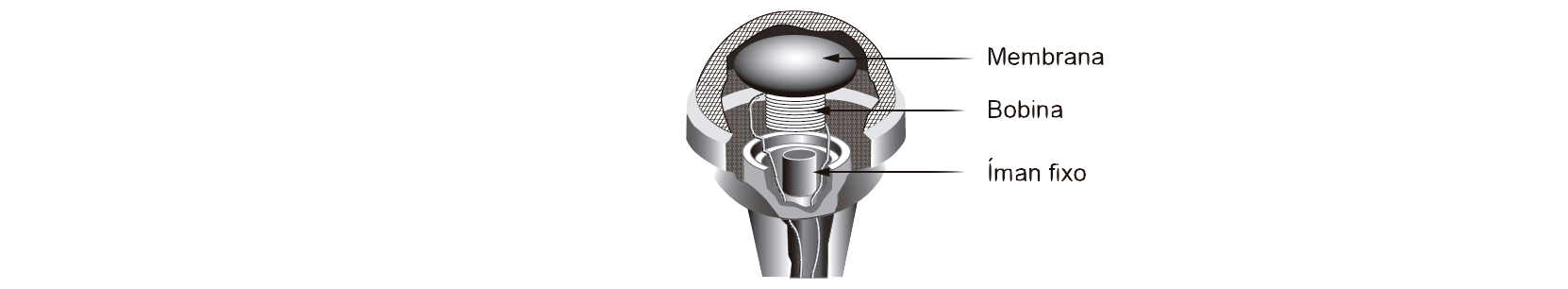
Figura 3
⇒ Oscilação da membrana do microfone, provocada por um sinal sonoro, origina o movimento oscilatório da bobina.
⇒ Este movimento da bobina ocorre num campo magnético gerado pelo íman fixo, pelo que haverá uma variação do fluxo magnético que atravessa as superfícies delimitadas pelas espiras da bobina.
⇒ De acordo com a lei de Faraday, a variação temporal do fluxo magnético nas espiras da bobina origina uma força eletromotriz induzida nos seus terminais e, consequentemente, uma corrente induzida na bobina, e assim é produzido um sinal elétrico.
- A resposta deve apresentar os seguintes elementos:
A) A oscilação da membrana, provocada por um sinal sonoro, origina um movimento oscilatório da bobina.
B) O movimento da bobina ocorre num campo magnético (ou ocorre na proximidade de um íman fixo), pelo que haverá uma variação do fluxo magnético que atravessa as superfícies delimitadas pelas espiras da bobina.
C) A variação do fluxo magnético origina uma força eletromotriz induzida nos terminais da bobina e, consequentemente, uma corrente elétrica induzida na bobina.

GRUPO II
A Figura 4 apresenta as curvas características, a 25 ºC, de um painel fotovoltaico, para três irradiâncias diferentes.
Estas curvas representam a corrente elétrica, I, fornecida pelo painel, em função da diferença de potencial elétrico, U, nos seus terminais.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1. Qual é o esboço do gráfico que pode representar, para uma mesma irradiância, a potência elétrica, P, fornecida pelo painel, em função da diferença de potencial elétrico, U, nos seus terminais?
- Opção (C)
- A potência elétrica é P = UI
⇒ Para valores de corrente elétrica, I, ou de diferença de potencial, U, iguais a zero, a potência elétrica é nula.
⇒ Da análise do gráfico da figura 4, para uma dada irradiância (por exemplo, 600 W m–2), verifica-se que, para o intervalo de valores de diferença de potencial de 0 V a cerca de 30 V, a corrente elétrica diminui muito pouco, é praticamente constante, pelo que a potência elétrica aumenta de forma quase linear com o aumento da diferença de potencial; em seguida, verifica-se uma diminuição brusca da corrente elétrica para uma diferença de valores de diferença de potencial pequena, de 30 V até 35 V, aproximadamente, pelo que a potência elétrica diminui bruscamente desde o valor máximo até zero.
⇒ Em resultado desta análise, conclui-se que o esboço do gráfico que, para a mesma irradiância, pode representar a potência elétrica fornecida pelo painel, em função da diferença de potencial nos seus terminais.
- Opção (C) ……………. 7 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2. A corrente elétrica fornecida por um painel fotovoltaico para uma resistência exterior nula designa-se por corrente de curto-circuito.
Conclua, com base no gráfico da Figura 4, se a corrente de curto-circuito é (ou não) diretamente proporcional à irradiância.
Mostre como chegou à conclusão solicitada.
⇒ Para concluir se a corrente de curto-circuito é ou não diretamente proporcional à irradiância tem de se determinar os quocientes entre as irradiâncias e as correspondentes correntes de curto-circuito, Er/I.

⇒ Dentro das incertezas de medição podem considerar-se iguais os pacientes determinados.
⇒ Desta forma concluiu-se que as correntes de curto-circuito são diretamente proporcionais às irradiâncias (a potência da radiação incidente numa unidade de área do painel).
- A resposta deve incluir os seguintes passos:
(A) Determinação dos quocientes entre as correntes de curto circuito e as correspondentes irradiâncias
- ou dos inversos desses quocientes
ou
Determinação dos quocientes entre as correntes de curto-circuito e dos quocientes entre as correspondentes irradiâncias
- ou dos inversos desse quocientes.
(B) Referência ao facto de aqueles quocientes serem aproximadamente constantes.
(C) Conclusão (a corrente de curto-circuito é diretamente proporcional à irradiância)

GRUPO III
1. Na Figura 5 (que não se encontra à escala), está representado um carrinho de brincar, de massa m, que é largado da posição A, sobre um plano inclinado.
O carrinho desce esse plano, passa nas posições B e C e inverte o sentido do movimento na posição D.

Figura 5
Admita que a intensidade da resultante das forças dissipativas que atuam no carrinho se mantém constante nos percursos entre as posições A e B e entre as posições C e D.
Entre as posições B e C, as forças dissipativas que atuam no carrinho são desprezáveis. Considere que o carrinho pode ser representado pelo seu centro de massa (modelo da partícula material).
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1.1. Desde a posição A até à posição D, a diminuição da energia potencial gravítica do sistema carrinho + Terra é igual a _____, sendo o trabalho realizado pela força gravítica que atua no carrinho igual a _____.

- Opção (D) ……………. 7 pontos
- 11ºano – Física – Domínio 1 – subdomínio 1 (Tempo, posição e velocidade)
1.2. Qual é o esboço do gráfico que pode representar o módulo da velocidade, v, do carrinho em função do tempo, t, entre as posições A e D?
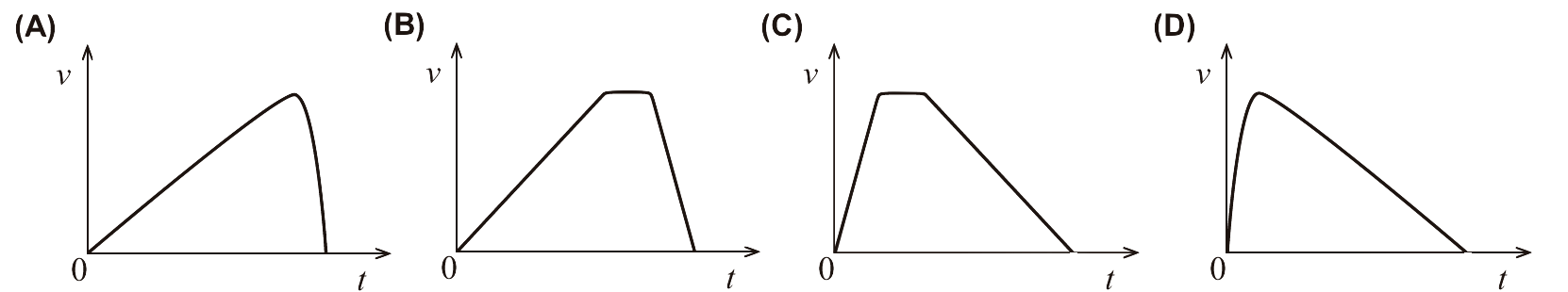
- Opção (B)
⇒ Nos percursos de A a B e de C a D a intensidade das forças que atuam sobre o carrinho – forças dissipativas e a componente tangencial às rampas da força gravítica – são iguais.
Contudo, de A a B, as forças dissipativas têm sentido de B para A, enquanto de C a D têm sentido descendente (de D para C).
⇒ Como a componente tangencial da força gravítica em ambos os trajetos tem sentido descendente, no trajeto de A a B, a intensidade da resultante das forças que atuam sobre o carrinho é inferior à intensidade da que atua de C para D, pelo que o valor da aceleração entre A e B é inferior ao valor da aceleração entre C e D.
- Consequentemente, o declive da reta que traduz v = f(t) é menor de A a B.
⇒ Uma vez que as forças dissipativas de B a C são desprezáveis e que a resultante das forças que atuam sobre o carrinho é nula, a velocidade neste percurso é constante.
- Opção (B) ……………. 7 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1.3. Compare a soma dos trabalhos realizados pelas forças que atuam no carrinho entre as posições A e B com a soma dos trabalhos realizados pelas forças que atuam no carrinho entre as posições C e D.

⇒ A soma dos trabalhos realizados pelas forças que atuam sobre o carrinho é igual ao trabalho realizado pela resultante das forças que sobre ele atuam.
⇒ Para determinar os trabalhos realizados pela resultante das forças que atuam sobre o carrinho entre A e B e o realizado entre C e D, recorre-se ao Teorema da Energia Cinética:

Nas posições A e D, a velocidade é nula, bem como os respetivos valores de energia cinética.
⇒ Dado que, no percurso de B a C, a resultante das forças que atuam sobre o carrinho é nula, então o módulo da velocidade em B é igual à velocidade em C, pelo que os valores da energia cinética nestas posições são iguais.

- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.4. Considere o movimento do carrinho na descida do plano inclinado, a partir da posição A.
Se a altura h for 40 cm, o carrinho atingirá a posição B com velocidade de módulo 2,0 m s-1.
Considere um referencial Ox coincidente com a trajetória do carrinho, com origem na posição A e com o sentido do movimento.
Determine a componente escalar da aceleração, ax, do carrinho, segundo o eixo Ox, no seu movimento entre as posições A e B.
Utilize as equações do movimento x (t) e v (t) .
Apresente todas as etapas de resolução, explicitando todos os cálculos efetuados.
- Etapas de resolução:
⇒ Determinação da distância percorrida pelo carrinho entre as posições A e B (d = 1,17 m) …….. 3 pontos
⇒ Escrita das equações x(t) e v(t) substituídas (1,17 = ½ ax t e 2,0 = ax t ) …….. 3 pontos
⇒ Determinação da componente escalar da aceleração do carrinho (ax = 1,7 m s-2) …….. 4 pontos
2. Galileu idealizou uma experiência na qual uma esfera, largada sempre de uma mesma altura h sobre um plano inclinado, subiria, na ausência de forças de atrito, um segundo plano inclinado até à altura da qual tinha sido largada, qualquer que fosse a inclinação θ do segundo plano.
Esta situação está representada na Figura 6.
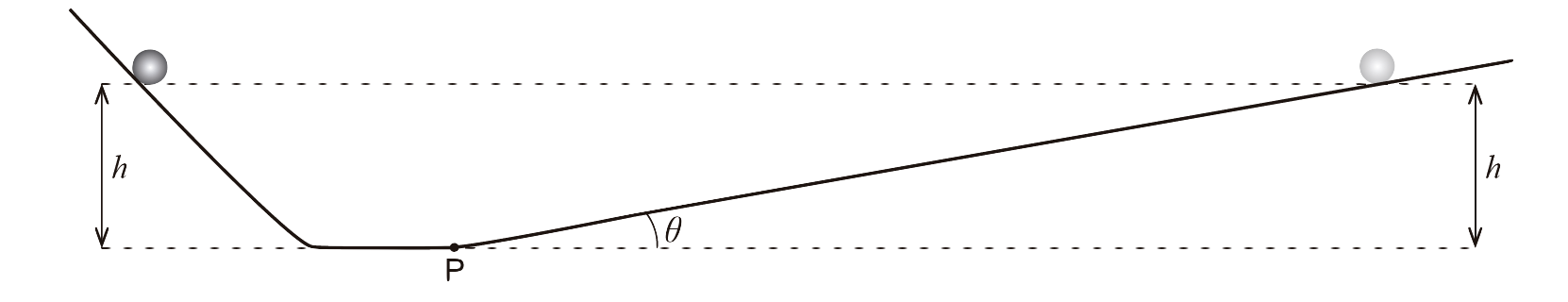
Considere que a esfera pode ser representada pelo seu centro de massa (modelo da partícula material).
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2.1. Na subida do segundo plano, desde a posição P até à posição de altura h,
(A) a resultante das forças que atuam na esfera não depende de θ.
(B) a soma dos trabalhos realizados pelas forças que atuam na esfera depende de θ.
(C) o trabalho realizado pela força gravítica que atua na esfera não depende de θ.
(D) a intensidade da força gravítica que atua na esfera depende de θ.
- Opção (C)
⇒ A subida, sobre a esfera atuam a força normal, que realiza um trabalho nulo por ser perpendicular ao deslocamento, e a força gravítica.
⇒ A resultante das forças sobre a esfera é a componente da força gravítica na direção do plano, de módulo mg sin θ, que realizou trabalho, – mgh, o qual depende da altura, e não depende inclinação do plano.
- Opção (C) ……………. 7 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.2. Que tipo de movimento teria a esfera a partir da posição P, se a amplitude do ângulo θ fosse 0º ?
- Movimento retilíneo uniforme
⇒ Se o ângulo θ for nulo, então a partir do ponto P a esfera desloca-se na horizontal.
⇒ Usando o modelo da partícula material, no seu deslocamento a esfera está somente sujeita ao peso e à força normal.
⇒ Quando a esfera se desloca horizontalmente, a força normal é vertical, tendo a mesma intensidade e sentido oposto ao peso.
⇒ A resultante das forças é nula e a esfera apresenta aceleração nula e a velocidade constante, deslocando-se com movimento retilíneo uniforme.
- Movimento retilíneo uniforme. …….. 7 pontos
GRUPO IV
- 10ºano – Química – Domínio 1 – subdomínio 1 (Massa e tamanho dos átomos)
1. Os dois isótopos mais abundantes do enxofre, S, são o enxofre-32 e o enxofre-34.
Os átomos destes isótopos têm
(A) número atómico diferente.
(B) número de eletrões diferente.
(C) o mesmo número de neutrões.
(D) o mesmo número de protões.
- Opção (D)
⇒ Isótopos de um elemento são átomos com o mesmo número atómico, Z, mas diferente número de massa, A.
⇒ Têm o mesmo número de protões e de eletrões, diferindo, somente, no número de neutrões.
- Opção (D) ……………. 7 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
2. A partir da configuração eletrónica do átomo de enxofre, S, indique quantas energias de remoção eletrónica apresentará o átomo de enxofre no estado fundamental.
Mostre como chegou ao valor solicitado.
- Cinco energias de remoção eletrónica
⇒ A configuração eletrónica para o átomo de enxofre no estado fundamental é 16S – 1s2 2s2 2p6 3s2 3p4.
⇒ No estado fundamental, os eletrões do átomo de enxofre distribuem-se por três níveis, (n = 1, n = 2 e n = 3) e cinco subníveis de energia, ( 1s, 2s, 2p, 3s e 3p ).
⇒ Como a cada subnível de energia corresponde uma energia de remoção eletrónica, o átomo de enxofre no estado fundamental apresentará cinco energias de remoção eletrónica.
- A resposta deve incluir os seguintes passos:
A) Apresentação da configuração eletrónica do átomo de enxofre no estado fundamental (1s2 2s2 2p6 3s2 3p4).
B) Referência ao facto de os eletrões do átomo de enxofre no estado fundamental se distribuírem por cinco subníveis de energia.
C) Indicação de que o átomo de enxofre no estado fundamental apresentará cinco energias de remoção eletrónica.

- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3. No estado gasoso, a maior energia de remoção eletrónica do enxofre é 239 MJ mol-1, e a menor energia de remoção eletrónica do enxofre é 1,0 MJ mol-1.
A energia de ionização do enxofre é
(A) 1,0 × 10-6 J mol-1
(B) 2,39 × 108 J mol-1
(C) 1,0 × 106 J mol-1
(D) 2,39 × 10-4 J mol-1
- Opção (C)
⇒ A energia de ionização de um átomo é a energia mínima necessária para remover um eletrão de um átomo isolado, no estado fundamental.
⇒ Se o elemento se encontrar no estado gasoso, a energia de primeira ionização, é igual à menor energia de remoção eletrónica.
- 1,0 MJ mol-1 = 1,0 x 106 J mol-1
- Opção (C) ……………. 7 pontos
4. O enxofre, S, pode existir em pequenas quantidades no aço.
Numa análise de controlo de qualidade, converteu-se todo o enxofre existente numa amostra de aço, de massa 8,30 g , em dióxido de enxofre, SO2 (g).
Admita que todo o dióxido de enxofre formado reagiu com uma solução de peróxido de hidrogénio, H2O2 (aq), à qual se tinha adicionado uma solução de hidróxido de sódio, NaOH (aq).
A reação que ocorre pode ser traduzida por
SO2 (g) + H2O2 (aq) + 2 OH– (aq) → SO42- (aq) + 2 H2O (l)
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
4.1. Nesta reação, o número de oxidação do enxofre ______ , sendo o SO2 a espécie que se _____ .
(A) aumenta … oxida
(B) aumenta … reduz
(C) diminui … oxida
(D) diminui … reduz
- Opção (A)
⇒ Cálculo do n.o. do enxofre em:
- (SO2) : x + 2 x (-2) = 0 ⇔ x = + 4
⇒ Cálculo do n.o. do enxofre em :
- (SO42-) : x + 4 x (-2) = -2 ⇔ x = + 6
⇒ O n.o. do enxofre aumenta de +4, em SO2, para +6, em SO42-, o que significa que, nesta reação, a espécie SO42-liberta eletrões, sofrendo, portanto, oxidação.
- O SO2 é a espécie que se oxida.
- Opção (A) ……………. 7 pontos
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
4.2. Considere que à solução de peróxido de hidrogénio se tinha adicionado 2,000 × 10-2 dm3 de NaOH (aq), de concentração 5,00 x 10-2 dm-3.
Após todo o SO2 (g) ter reagido, verificou-se que a quantidade de OH– (aq) na solução era 7,065 x 10-4 mol.
Determine a percentagem, em massa, de enxofre, S (M = 32,06 g mol-1), na amostra de aço.
Apresente todas as etapas de resolução, explicitando todos os cálculos efetuados.
 Quantidade de hidróxido de sódio adicionada:
Quantidade de hidróxido de sódio adicionada:
 Quantidade de anião hidróxido que reagiu:
Quantidade de anião hidróxido que reagiu:

De acordo com a estequiometria da reação, 1 (SO2) : 2 (OH–), a quantidade de dióxido de enxofre na amostra é 1/2 da quantidade de anião hidróxido gasta.
Percentagem de enxofre na amostra: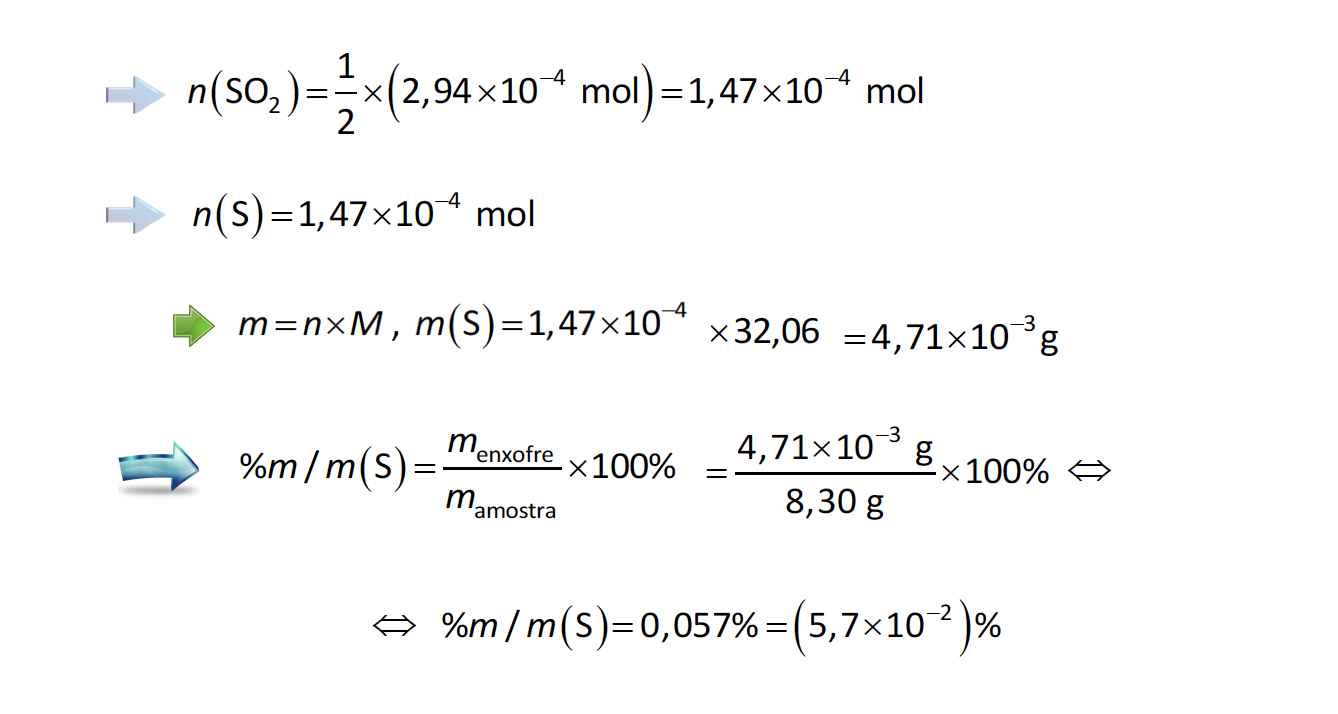
- Etapas de resolução:
⇒ Cálculo da quantidade de OH– (aq) adicionada (n = 1,000 x 10-3 mol) …….. 2 pontos
⇒ Cálculo da quantidade de OH– (aq) que reagiu (n = 2,94 x 10-4 mol) …….. 2 pontos
⇒ Cálculo da massa de enxofre na amostra (m = 4,71 x 10-3 g) …….. 4 pontos
⇒ Cálculo da percentagem, em massa, de enxofre na amostra (5,7 x 102 %) …….. 2 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
5. No âmbito de um estudo sobre poluição, recolheu-se, numa zona da troposfera, uma amostra de ar.
Verificou-se que, por cada 1,0 x 1012 moléculas existentes na amostra, 4,0 x 102 # moléculas eram de SO2 (M = 64,06 g mol-1).
Determine a concentração em massa (em g dm-3) de SO2 na amostra, nas condições normais de pressão e de temperatura (PTN).
Apresente todas as etapas de resolução, explicitando todos os cálculos efetuados.
- Etapas de resolução:
⇒ Cálculo do volume ocupado por 1,0 x 1012 moléculas, nas condições PTN (V = 3,72 x 10-11 dm3) …….. 4 pontos
⇒ Cálculo da massa de 4,0 x 102 moléculas de SO2 (m = 4,25 x 10-20 g) …….. 4 pontos
⇒ Determinação da concentração em massa de SO2 na amostra, nas condições PTN
(Cm = 1,1 x 10-9 g dm-3) …….. 2 pontos
ou
⇒ Cálculo da quantidade de SO2 por mole de moléculas da amostra (n = 4,00 x 10-10 mol) …….. 4 pontos
⇒ Cálculo da massa de SO2 por mole de moléculas da amostra (m = 2,56 x 10-8 g) …….. 3 pontos
⇒ Determinação da concentração em massa de SO2 na amostra, nas condições PTN
(Cm = 1,1 x 10-9 g dm-3) …….. 3 pontos
GRUPO V
1. A água, H2O, é um líquido à pressão de 1 atm e a 25 ºC.
Nas mesmas condições de pressão e de temperatura, o sulfureto de hidrogénio, H2S , é um gás.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
1.1. As moléculas de H2O e de H2S _____ o mesmo número de eletrões de valência ligantes, _____ a mesma geometria.
(A) não têm … apresentando
(B) têm … não apresentando
(C) não têm … não apresentando
(D) têm … apresentando
- Opção (D)
O oxigénio e o enxofre são elementos do grupo 16 da TP.
- Ambos têm, portanto, 6 eletrões de valência.
As moléculas de H2O e de H2S apresentam 2 x 1 + 6 = 8 eletrões de valência.
⇒ Em ambas, esses 8 eletrões (4 pares) distribuem-se em torno do átomo O ou S, respetivamente, sendo 2 pares de eletrões ligantes, correspondentes às duas ligações covalentes O–H ou S–H, e 2 pares não ligantes, localizados no átomo central, O ou S.
⇒ O maior afastamento possível destes quatro pares obtém-se quando eles se dispõem no espaço de modo aproximadamente tetraédrico, conferindo ao conjunto H2O e H2S uma geometria angular.
- Opção (D) ……………. 7 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
1.2. As ligações que se estabelecem entre moléculas de H2S resultam predominantemente de _____ , sendo mais ______ do que as ligações que se estabelecem entre moléculas de H2O.
(A) forças de van der Waals … fortes
(B) forças de van der Waals … fracas
(C) ligações de hidrogénio … fortes
(D) ligações de hidrogénio … fracas
- Opção (B)
⇒ As ligações de hidrogénio surgem em casos em que átomos de hidrogénio se encontram ligados, por covalência, a átomos com grande tendência para captarem eletrões com, pelo menos, um par de eletrões não ligantes (como F, N ou O).
⇒ Entre moléculas de água, estabelecem-se pontes de hidrogénio, que são muito mais intensas do que as forças de van der Waals, que se estabelecem entre moléculas de H2S.
- Opção (B) ……………. 7 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2. Em qual das seguintes reações a água se comporta como um ácido de Brönsted-Lowry?
(A) HS– (aq) + OH– (aq) S2- (aq) + H2O (l)
(B) HS– (aq) + H2O (l) S2- (aq) + H3O+ (aq)
(C) H2S (aq) + H2O (l) HS– (aq ) + H3O+ (aq)
(D) S2- (aq ) + 2 H3O+ (aq) H2S (aq) + 2 H2O (l)
- Opção (A)
⇒ Segundo a teoria de Brönsted-Lowry, um ácido é toda a espécie química dadora de iões .
⇒ O comportamento da água como ácido de Brönsted-Lowry envolve o par ácido-base H2O/OH– correspondente à cedência de um hidrogenião traduzida pela equação:
H2O (l) → OH– (aq) + H+ (aq)
- Opção (A) ……………. 7 pontos
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
3. A dureza é um parâmetro que condiciona a utilização de uma água e que está relacionado com a concentração de determinados iões, entre os quais o ião Ca2+ (aq).
A adição de uma solução aquosa de sulfato de sódio, Na2SO4 (aq), a uma água contendo iões Ca2+ (aq) não altera significativamente a dureza dessa água.
No entanto, nas mesmas condições de temperatura, a adição de uma solução aquosa de carbonato de sódio, Na2CO3 (aq), à mesma água provoca uma diminuição da sua dureza.
Conclua qual dos sais, CaSO4 ou CaCO3, será menos solúvel em água, a uma mesma temperatura.
Mostre como chegou à conclusão solicitada.
⇒ A adição da solução aquosa de sulfato de sódio (NaSO4) não altera significativamente a dureza dessa água, isto é, não diminui significativamente a concentração de ião cálcio (para além do leve efeito de diluição), pois não ocorre precipitação de sulfato de cálcio (CaSO4).
⇒ A adição da solução aquosa de carbonato de sódio (NaCO3) diminui a dureza dessa água, isto é, diminui a concentração de ião cálcio, por ocorrer precipitação de carbonato de cálcio (CaCO3).
⇒ O carbonato de cálcio (CaCO3) é menos solúvel em água do que o sulfato de cálcio (CaSO4), à mesma temperatura.
- A resposta deve incluir os seguintes passos:
A) Referência ao facto de a ausência de alteração significativa da concentração de ião Ca2+ (aq), por adição de Na2SO4 (aq), indiciar que não ocorre precipitação de CaSO4.
B) Referência ao facto de a diminuição da concentração de ião Ca2+ (aq), por adição de Na2CO3 (aq), indiciar que ocorre precipitação de CaCO3.
C) Conclusão (CaCO3 será menos solúvel em água do que CaSO4).
4. Uma amostra de água de massa m, inicialmente a 26 ºC e contida num recipiente, foi introduzida num congelador.
Ao fim de um determinado intervalo de tempo, a temperatura da água estabilizou a – 20 ºC.
Na tabela seguinte, estão registados os valores de algumas propriedades físicas da água.

- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
4.1. Compare, quantitativamente, a energia envolvida na mudança de estado físico da amostra de água com a energia total envolvida nas variações de temperatura da amostra.
Apresente todas as etapas de resolução, explicitando todos os cálculos efetuados.
- Etapas de resolução:
⇒ Determinação da expressão que traduz a energia total envolvida nas variações de temperatura da amostra, em função da massa (E = 1,51 x 105 m) …….. 5 pontos
⇒ Apresentação da expressão que traduz a energia envolvida na mudança de estado físico da amostra, em função da massa (E = 3,34 x 105 m) …….. 2 pontos
⇒ Comparação solicitada (a energia envolvida na mudança de estado físico da amostra de água é 2,2 vezes superior à energia total envolvida nas variações de temperatura da amostra) …….. 3 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
4.2. Até atingir a temperatura de – 20 ºC, a água ______ vizinhança, através das paredes do recipiente, essencialmente por ______ .
(A) cede energia à … condução
(B) recebe energia da … condução
(C) cede energia à … convecção
(D) recebe energia da … convecção
- Opção (A)
⇒ A diminuição de temperatura da água ocorre quando ela cede energia à vizinhança.
⇒ No recipiente, um sólido, predomina a transferência de energia por condução.
- Opção (A) ……………. 7 pontos
GRUPO VI
Considere que, num reator de volume variável, existem apenas as substâncias A, B e C, todas em fase gasosa, que reagem entre si de acordo com
A (g) + 3 B (g) x C (g)
sendo x o coeficiente estequiométrico de C.
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
1. Numa reação química, em sistema fechado, poderá ocorrer variação
(A) da massa do sistema.
(B) da carga elétrica total.
(C) do número total de eletrões.
(D) do número total de moléculas.
- Opção (D)
⇒ Em qualquer reação química, a massa total dos reagentes tem de ser igual à massa total dos produtos (Lei de Lavoisier).
⇒ Não há indicação da libertação de eletrões na reação, a carga elétrica total não varia.
⇒ O número total de moléculas pode variar desde que haja variação do número de moles de moléculas na passagem de reagentes a produtos.
- Opção (D) ……………. 7 pontos
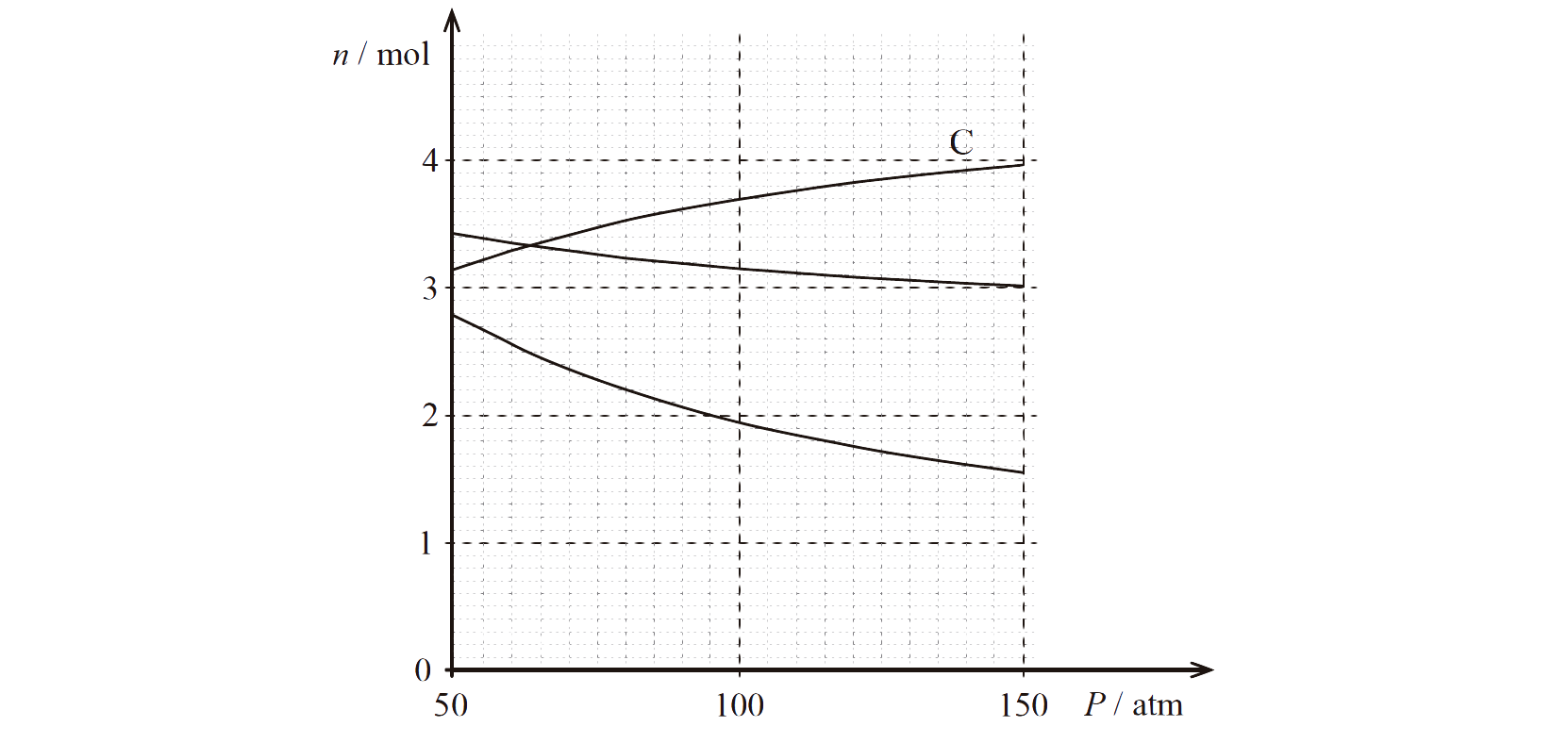
2. O gráfico da Figura 7 representa, à temperatura de 327 ºC, as quantidades de equilíbrio de A (g) , B (g) e C (g) existentes no reator, em função da pressão, P.
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
2.1. Aumentando o volume do reator, a quantidade de equilíbrio de C (g) , o que significa que a reação é favorecida.
(A) diminui … direta
(B) aumenta … direta
(C) diminui … inversa
(D) aumenta … inversa
- Opção (C)
⇒ Aumentando o volume do gás contido no reator, diminui a pressão a temperatura constante.
⇒ Por observação da figura 7, constata-se que, diminuindo a pressão do sistema no reator fechado a temperatura constante, diminui a quantidade de C.
⇒ O aumento do volume do reator, a quantidade de equilíbrio do produto C diminui, o que significa que a reação no sentido inverso é favorecida.
- Opção (C) ……………. 7 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
2.2. Admita que, a 327 ºC e à pressão de 100 atm, o volume molar dos gases A, B e C é 0,49 dm3 mol-1.
Determine a constante de equilíbrio, Kc , da reação considerada, a 327 ºC.
Apresente todas as etapas de resolução, explicitando todos os cálculos efetuados.
As quantidades de reagentes gastas e de produtos formadas, estão de acordo com os respetivos coeficientes estequiométricos.
Considerando, por exemplo, uma alteração de estado de equilíbrio a 327ºC por variação de pressão de 50 atm para 150 atm, o coeficiente estequiométrico de C seria:
Volume molar dos gases a 327 ºC e 100 atm:
- Vm = 0,49 dm3 mol-1
De acordo com o gráfico representado na figura 7, as quantidades em equilíbrio a 327 ºC e 100 atm são:
- nA = 3,15 mol ;
- nB = 1,95 mol ;
- nC = 3,70 mol ;
Soma das quantidades de equilíbrio a 327 ºC e 100 atm:
- ntotal = 3,15 mol + 1,95 mol + 3,70 mol = 8,80 mol
Volume do sistema em equilíbrio a 327 ºC e 100 atm:
- Vsistema = Vm x ntotal = 0,49 dm3 mol-1 x 8,80 mol = 4,31 dm3
As concentrações no equilíbrio a 327 ºC e 100 atm, serão:

- Etapas de resolução:
⇒ Determinação do coeficente estequiométrico x (x = 2) …….. 3 pontos
⇒ Determinação do volume do sistema, nas condições de pressão e de temperatura consideradas
(V = 4,31 dm3) …….. 4 pontos
⇒ Determinação da constante de equilíbrio da reação considerada, a 327 ºC (Kc = 11) …….. 3 pontos
FIM
Cotações











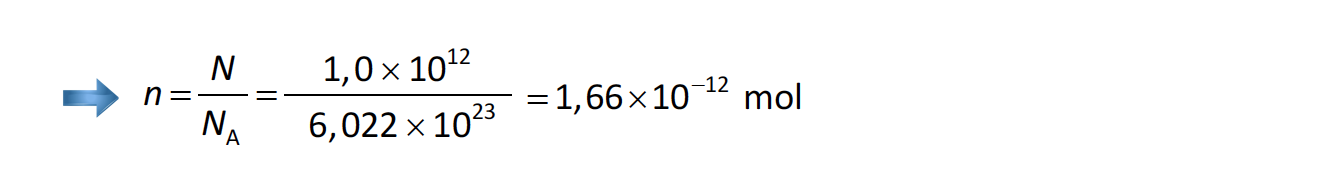

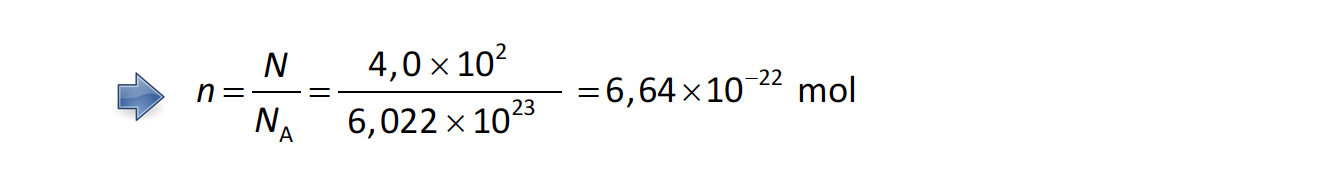

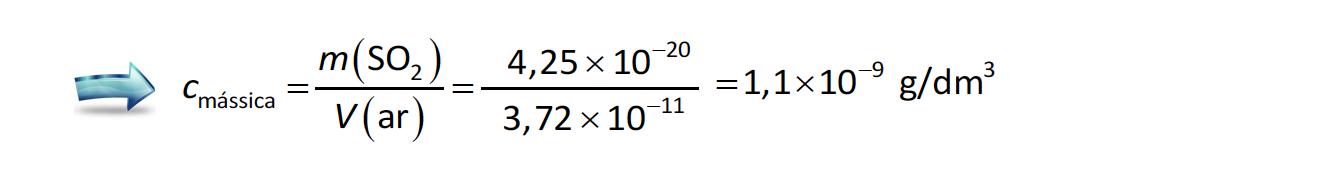
 S2- (aq) + H2O (l)
S2- (aq) + H2O (l)