2009 – Teste Intermédio – 11ºAno – março – Química
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 11ºAno – 2009
- Duração do Teste: 90 minutos | 17.03.2009
- Química
1. As abundâncias dos principais elementos químicos têm uma distribuição surpreendentemente semelhante no Universo.
- 10ºano – Química – Domínio 1 – subdomínio 1 (Massa e tamanho dos átomos)
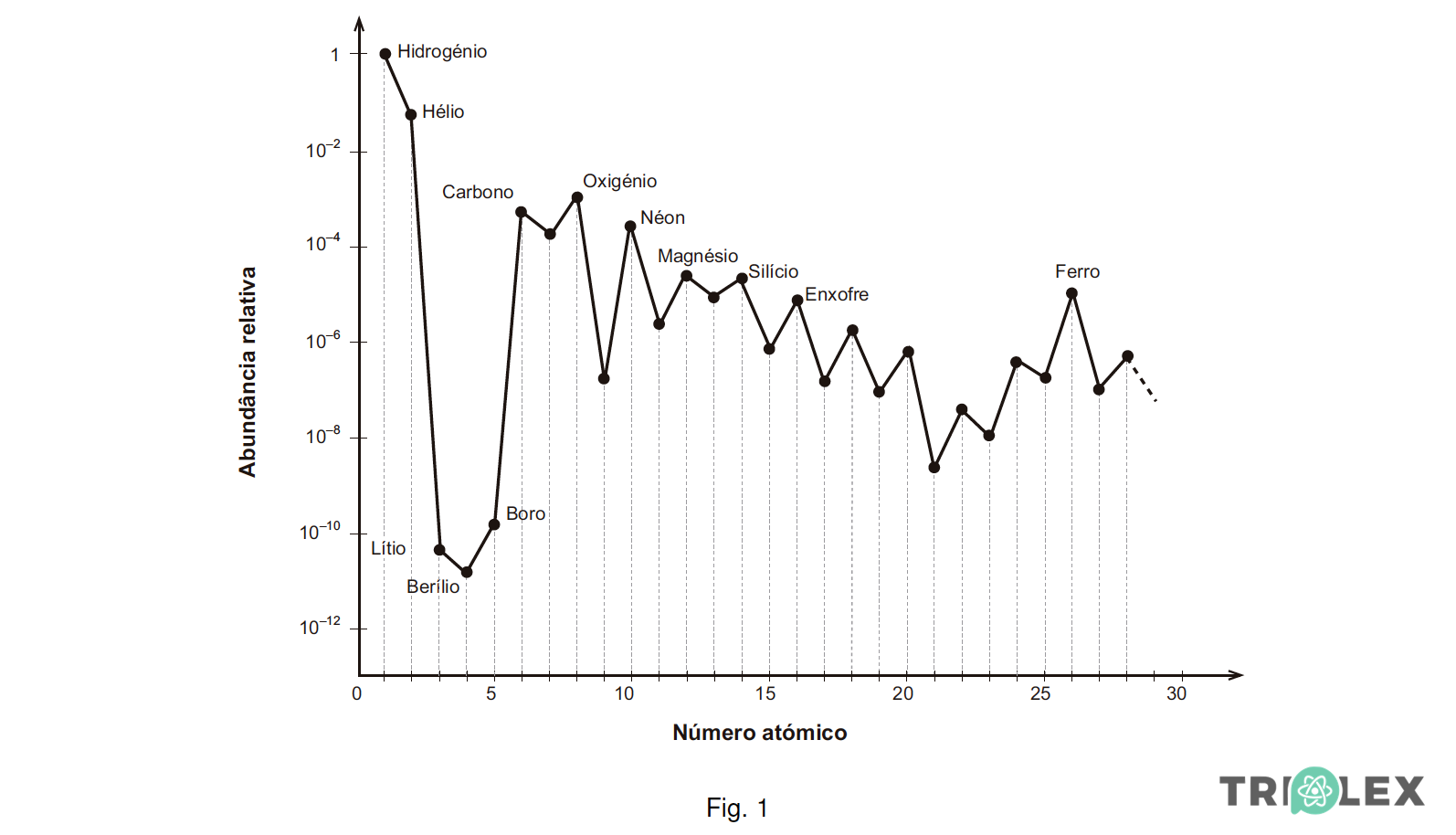
1.1. O gráfico da figura 1 representa as abundâncias relativas de alguns elementos no Universo, tomando como referência o hidrogénio.
Seleccione a alternativa correcta, com base neste gráfico.
(A) O carbono é o terceiro elemento mais abundante no Universo.
(B) O lítio é o metal alcalino mais abundante no Universo.
(C) O oxigénio é cerca de dez vezes menos abundante do que o azoto.
(D) O flúor e o cloro têm aproximadamente a mesma abundância.
—————————————————————————————————————————————————————————————————————————-
- Opção (D)
⇒ (A) Falsa.
- porque o terceiro elemento mais abundante é o oxigénio;
⇒ (B) Falsa.
- porque o gráfico mostra que o sódio e o potássio são mais abundantes do que o lítio;
⇒ (C) Falsa.
- porque o oxigénio é mais abundante que o azoto (elemento com Z = 7).
- Opção (D)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
1.2. No Sol, o hidrogénio também é o elemento predominante, sendo o combustível que permite a sua (e nossa) existência.
Seleccione a alternativa correcta, relativamente ao átomo de hidrogénio.
(A) Nas transições electrónicas entre estados excitados, não há emissão de radiações na zona do ultravioleta.
(B) Nas transições electrónicas entre estados excitados, ocorre sempre emissão de radiação.
(C) O conjunto de todas as radiações emitidas na desexcitação do átomo de hidrogénio constitui um espectro contínuo.
(D) O átomo de hidrogénio, no estado de menor energia, pode ser excitado por radiações na zona do visível.
- Opção (A)
⇒ (B) Falsa.
- porque pode também ocorrer absorção de radiação e, mesmo em transições eletrónicas descendentes, nem sempre ocorre emissão de radiação (caso da desexcitação por choque entre átomos);
⇒ (C) Falsa.
- porque o espetro é de riscas;
⇒ (D) Falsa.
- porque as transições eletrónicas entre o estado fundamental e o primeiro estado excitado correspondem a radiação ultravioleta.
- Opção (A)…………. 8 pontos
1.3. O Sol emite radiações que atingem a Terra, sendo a radiação verde a mais intensa.
Considere que um feixe monocromático de luz verde, ao incidir numa placa metálica, origina a ejecção de electrões, com uma determinada energia cinética.
Seleccione a alternativa correcta, relativamente a este fenómeno.
(A) Utilizando um feixe de luz vermelha, a energia cinética de cada um dos electrões ejectados é maior.
(B) Utilizando um feixe de luz violeta, a energia de remoção de cada um dos electrões ejectados é menor.
(C) Utilizando um feixe de luz violeta, a energia cinética de cada um dos electrões ejectados é maior.
(D) Utilizando um feixe de luz vermelha, a energia de remoção de cada um dos electrões ejectados é menor.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B)
⇒ (A) Falsa.
- porque, como a energia por fotão da radiação vermelha (Everm.) é inferior à correspondente energia da radiação verde (Everde), a diferença Ecin = Everm. – Erem. é menor (e não maior) do que Ecin = Everde – Erem. ;
⇒ (B) e (D) Falsas.
- porque a energia de remoção (Erem.) só depende da natureza do metal e não da radiação incidente.
- Opção (C)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
1.4. A Tabela Periódica dos Elementos é um instrumento organizador de conhecimentos sobre os elementos químicos.
Após várias tentativas de organização desses conhecimentos, é com Dmitri Mendeleev (1834-1898) que surge, embora com imprecisões, uma tabela muito semelhante à actual.
Escreva um texto sobre a localização dos elementos representativos na Tabela Periódica e o modo como variam algumas das suas propriedades, abordando os seguintes tópicos:
• Relação entre a configuração electrónica dos átomos dos elementos e o período e o grupo aos quais esses elementos pertencem;
• O raio atómico, em função do aumento do número atómico, para elementos de um mesmo período, assim como para elementos de um mesmo grupo;
• A energia de ionização, em função do aumento do número atómico, para elementos de um mesmo período, assim como para elementos de um mesmo grupo.
- Opção (D)
⇒ Os elementos representativos situam-se nos grupos 1, 2, 13, 14, 15, 16, 17 e 18 da TP.
⇒ O número de eletrões da última camada (eletrões de valência) é igual ao último dígito do número que indica o grupo. O número quântico principal da última camada (n) corresponde ao período.
⇒ Exemplificando:
5 eletrões: grupo 15
1s2 – 2s2 2p6 – 3s2 3p3
n = 3: 3.° período
⇒ O raio atómico, para elementos representativos do mesmo grupo, aumenta com o aumento do número atómico (Z), devido ao aumento do número de camadas eletrónicas e ao facto de a carga dos eletrões das camadas interiores repelir os eletrões periféricos.
⇒ O raio atómico, para elementos representativos do mesmo período, diminui com Z, pelo facto de o aumento progressivo da carga nuclear provocar um aumento da força atrativa núcleo-eletrões superior ao aumento da repulsão intereletrónica.
⇒ A primeira energia de ionização, para elementos representativos do mesmo grupo, diminui com o aumento do número atómico (Z). Esta variação deve-se ao facto de a atração efetiva entre o núcleo e os eletrões periféricos diminuir, pois é contrariada pelas repulsões entre os eletrões que blindam ou protegem o núcleo.
⇒ A primeira energia de ionização, para elementos representativos do mesmo período, aumenta com Z, pelo facto de a carga nuclear aumentar a força atrativa núcleo-eletrão, para eletrões situados na mesma camada periférica.
- A resposta deve abordar os seguintes tópicos:
⇒ O número quântico principal que caracteriza o nível de energia em que se encontram os electrões de valência corresponde ao período, e o número de electrões de valência corresponde ao grupo.
⇒ No mesmo período, à medida que o número atómico aumenta, diminui o raio atómico. No mesmo grupo, à medida que o número atómico aumenta, aumenta o raio atómico.
⇒ No mesmo período, de um modo geral, à medida que o número atómico aumenta, aumenta a energia de ionização. No mesmo grupo, à medida que o número atómico aumenta, diminui a energia de ionização.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2. A atmosfera terrestre funciona como um filtro da radiação solar, como resultado das interacções desta com a matéria existente nas diversas camadas da atmosfera.
Seleccione a alternativa correcta, relativamente às radiações ultravioleta (UV) provenientes do Sol.
(A) Na troposfera é absorvida a maior parte das radiações UV de maior energia.
(B) Na estratosfera são absorvidas praticamente todas as radiações UV de energia intermédia.
(C) Na termosfera é absorvida a maior parte das radiações UV de menor energia.
(D) Na mesosfera são absorvidas praticamente todas as radiações UV.
- Opção (B)
⇒ (A) Falsa.
- porque as radiações ultravioleta de maior energia são absorvidas em camadas mais externas da atmosfera;
⇒ (C) Falsa.
- porque as radiações ultravioleta de menor energia chegam à troposfera;
⇒ (D) Falsa.
- porque as radiações ultravioleta de média energia atravessam a mesosfera e são absorvidas na estratosfera, enquanto as de menor energia atravessam a troposfera.
- Opção (B)…………. 8 pontos
3. A atmosfera terrestre tem vindo a ser contaminada por diversos gases poluentes, como CO2, CH4, NOx, SO2, etc., sendo alguns deles responsáveis pelas chuvas ácidas.
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
3.1. Uma das reacções que está na origem das chuvas ácidas é a reacção do dióxido de enxofre, SO2 (g), com o oxigénio da atmosfera, O2 (g), originando trióxido de enxofre, SO3 (g), traduzida por
2 SO2 (g) + O2 (g) ⇋ 2 SO3 (g)
O gráfico da figura 2 representa uma das possíveis evoluções das concentrações dos componentes da mistura reaccional em função do tempo, em recipiente fechado contendo inicialmente uma mistura de SO2 (g) e O2 (g).
Seleccione a alternativa que contém a sequência que refere a evolução das concentrações de SO2 (g), O2 (g) e SO3 (g), respectivamente.
(A) III, II e I.
(B) II, III e I.
(C) III, I e II.
(D) II, I e III.
- Opção (A)
⇒ porque é a única em que os reagentes SO2 e O2 se consomem na razão 2:1 e se forma SO3 na proporção 2:2.
- Opção (A)…………. 8 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
3.2. A chuva normal tem, usualmente, pH cerca de 5,6.
Indique o gás que, ao dissolver-se, é responsável por este valor.
- CO2
- Dióxido de carbono (ou CO2)…………. 8 pontos
4. O dióxido de carbono, CO2 (g), é um dos principais gases que contribuem para o efeito de estufa, sendo conhecidas diversas acções conducentes à redução das suas emissões para a atmosfera.
No entanto, além do dióxido de carbono, o vapor de água, H2O (g), e o metano, CH4 (g), também contribuem para esse efeito.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
4.1. Tanto a molécula H2O como a molécula CO2 têm um átomo central, respectivamente de oxigénio e de carbono.
Seleccione a alternativa que corresponde à geometria correcta dessas moléculas.
(A) A molécula H2O é linear, assim como a molécula CO2.
(B) A molécula H2O é linear, enquanto a molécula CO2 é angular.
(C) A molécula H2O é angular, assim como a molécula CO2.
(D) A molécula H2O é angular, enquanto a molécula CO2 é linear.
- Opção (D)
⇒ (A) Falsa.
- porque a molécula de água é angular;
⇒ (B) Falsa.
- pela razão anterior e por a molécula de CO2 ser linear;
⇒ (C) Falsa.
- porque a molécula de CO2 é linear.
- Opção (D)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
4.2. O metano, CH4, é o alcano mais simples, com apenas um átomo de carbono por molécula.
A cadeia carbonada dos alcanos pode ser ramificada ou não ramificada, ocorrendo a ramificação apenas a partir do butano, C4H10.
Considere o alcano de cadeia ramificada, cuja fórmula de estrutura está representada na figura 3.
Seleccione a alternativa que corresponde ao nome deste alcano, de acordo com as regras da IUPAC.
(A) 3 – metil-heptano.
(B) 2,4 – dimetil-hexano.
(C) 2 – etil – 4 – metilpentano.
(D) 3 – etil – 1,1 – dimetilbutano.
- Opção (B)
- Opção (B)…………. 8 pontos
5. O mercúrio contribui para a poluição atmosférica como material particulado.
Já um dos seus compostos, o metilmercúrio, quando em soluções aquosas, entra na cadeia alimentar, originando intoxicações.
A toxicidade do mercúrio e dos seus compostos deve-se à sua interferência em processos enzimáticos, impedindo a respiração e o metabolismo celular.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
5.1. Nos seres humanos, a concentração mínima de metilmercúrio (M = 215,63 g mol–1) no sangue, normalmente associada ao aparecimento de sintomas de intoxicação, é 0,20 mg/L.
Indique o valor desta concentração, expresso em mol dm–3.
- c = 9,3 x 10-7 mol dm-3 …………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
5.2. Cada ser humano não deve ingerir, em média, por dia, um valor superior a 2,3 x 10–4 mg de metilmercúrio por quilograma da sua massa corporal.
Analisou-se uma amostra de 25,0 g de peixe, originária de uma remessa que ia ser comercializada, verificando-se que continha 1,0 x 10–2 mg de metilmercúrio.
Mostre que a ingestão de 125 g daquele peixe pode provocar intoxicação numa pessoa de 60 kg.
Apresente todas as etapas de resolução.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Calcula a massa de metilmercúrio existente em 125 g de peixe (m = 5,0 x 10–2 mg).
⇒ Calcula a massa máxima de metilmercúrio que uma pessoa de 60 kg pode ingerir diariamente, relacionando com o valor anterior (mmáxima = 1,4 x 10–2 mg e, como m > mmáxima, pode provocar intoxicação).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
6. O amoníaco, obtido industrialmente pelo processo de Haber-Bosch, é uma substância relevante na nossa sociedade, pelas suas múltiplas utilizações.
É matéria-prima no fabrico de fertilizantes, de ácido nítrico, de explosivos, de detergentes, entre outros.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
6.1. O hidrogénio, H2 (g), usado no fabrico do amoníaco, é normalmente obtido a partir do gás natural, essencialmente constituído por metano, CH4 (g), reacção que pode ser traduzida pela equação química
CH4 (g) + H2O (g) → CO (g) + 3 H2 (g)
Calcule o volume de hidrogénio que se obtém, medido em condições PTN, considerando a reacção completa de 960 kg de metano com excesso de vapor de água.
Apresente todas as etapas de resolução.
M (CH4) = 16,04 g mol–1
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Calcula a quantidade de metano que reage (n(CH4) = 5,985 x 104 mol).
⇒ Calcula a quantidade de hidrogénio que se forma (n(H2) = 1,796 x 1023 mol).
⇒ Calcula o volume de hidrogénio correspondente a essa quantidade, medido em condições PTN (V(H2) = 4,02 x 106 dm3).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
6.2. Num recipiente fechado de capacidade 5,0 dm3, uma mistura constituída por 1,0 mol de H2 (g), 2,5 mol de N2 (g) e 2,0 mol de NH3 (g) encontra-se a 500 °C.
A essa temperatura, a constante de equilíbrio da reacção traduzida por
N2 (g) + 3 H2 (g) ⇋ 2 NH3 (g)
- é Kc = 0,30.
Mostre, com base no valor do quociente de reacção, Qc, que a concentração de amoníaco, na mistura reaccional, diminui até se estabelecer o equilíbrio.
Apresente todas as etapas de resolução.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Calcula as concentrações de cada uma das substâncias presentes ([N2] = 0,500 mol dm–3, [H2] = 0,200 mol dm–3 e [NH3] = 0,400 mol dm–3).
⇒ Calcula o quociente de reacção, relacionando com Kc (Qc = 40 e, como Qc > Kc , a reacção evolui no sentido inverso, com a consequente diminuição da concentração de amoníaco).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
6.3. Seleccione a alternativa correcta, relativamente à reacção de formação do amoníaco, indicada em 6.2.
(A) A espécie oxidante é o N2 (g) e o elemento que se reduz é o hidrogénio.
(B) A espécie redutora é o H2 (g) e o elemento que se oxida é o hidrogénio.
(C) A espécie redutora é o N2 (g) e o elemento que se oxida é o azoto.
(D) A espécie oxidante é o H2 (g) e o elemento que se reduz é o azoto.
- Opção (B)
⇒ (A) Falsa.
- porque o H não se reduz (o seu número de oxidação passa de 0 a + 1);
⇒ (C) Falsa.
- porque N2 atua como oxidante (o seu número de oxidação passa de 0 a – 3);
⇒ (D) Falsa.
- porque o H não é oxidante, mas sim redutor (é oxidado).
- Opção (B)…………. 8 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
6.4. O amoníaco, resultante da decomposição da ureia presente na urina, é um dos responsáveis pelo odor desagradável nas casas de banho.
A sua ionização em água pode ser traduzida por
NH3 (aq) + H2O (l) ⇋ NH4+ (aq) + OH– (aq)
Indique um dos pares conjugados ácido-base envolvidos nesta reacção.
- NH4+ / NH3 ou H2O / OH–
- (NH4+ ; NH3) ou (H2O ; OH–) …………. 8 pontos
7. Num laboratório, um grupo de alunos pretende preparar, com rigor, uma solução aquosa neutra, por meio de uma reacção de neutralização, e aproveitar essa solução para verificar como o produto iónico da água, Kw, varia com a temperatura.
A solução aquosa neutra foi preparada misturando 50 mL de ácido clorídrico, HCl (aq), de concentração 0,100 mol dm–3, com um determinado volume de uma solução aquosa de hidróxido de sódio, NaOH (aq), de concentração 0,500 mol dm–3.
Em seguida, mediram o pH dessa solução a diferentes temperaturas, o que lhes permitiu verificar como Kw varia com a temperatura.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- 11ºano – Química – A.l. – 2.1 – Titulação ácido-base
7.1. Seleccione a alternativa que permite obter uma afirmação correcta.
Na preparação, com rigor, da solução aquosa neutra, o volume de NaOH (aq) que tiveram de utilizar foi…
(A) … 5,0 mL.
(B) … 10 mL.
(C) … 15 mL.
(D) … 20 mL.
- Opção (B)
⇒ n (HCl) = 0,050 L x 0,100 mol L-1 = 0,0050 mol
⇒ n (NaHO) = n (HCl) = 0,0050 mol = V (NaHO) x 0,500 mol L-1 ⇔ V = 0,010 L = 10 mL.
- Opção (B)…………. 8 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- 11ºano – Química – A.l. – 2.1 – Titulação ácido-base
- A.l. – Medições
7.2. Seleccione a alternativa que corresponde ao material de vidro que deve ser utilizado na medição do volume de NaOH (aq).
(A) Pipeta graduada.
(B) Proveta graduada.
(C) Copo de precipitação.
(D) Pipeta de Pasteur.
- Opção (A)
⇒ por não existir uma pipeta volumétrica … e porque as soluções de NaHO danificam o material calibrado de vidro e sofrem carbonatação atmosférica…
- Opção (A)…………. 8 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- 11ºano – Química – A.l. – 2.1 – Titulação ácido-base
7.3. Na tabela seguinte apresentam-se os valores de pH dessa solução neutra, a diversas temperaturas.
Indique, justificando a sua resposta, como varia o produto iónico da água, Kw , em função da temperatura, com base nesta tabela.
⇒ A elevação da temperatura conduz a menor pH, ou seja, a maior [H+ (aq)]
⇒ Como a solução é neutra, [H+ (aq)] = [HO– (aq)], ambas as concentrações aumentaram e o produto delas (Kw) aumentou com o aumento da temperatura.
⇒ Assim, o produto iónico da água, Kw, aumenta com a elevação da temperatura.
- A resposta deve conter os seguintes elementos:
⇒ pH diminui com o aumento da temperatura, logo [H3O+] aumenta;
⇒ [H3O+] = [OH– ] e Kw = [H3O+] x [OH– ], logo o aumento de [H3O+] implica o aumento de Kw.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
FIM