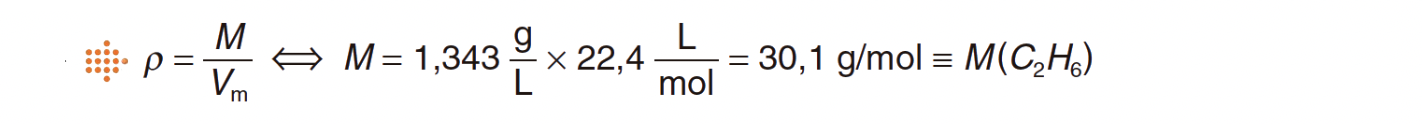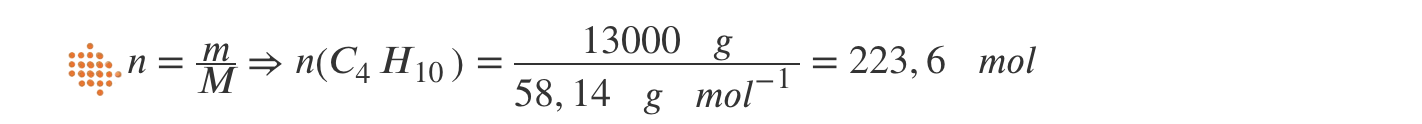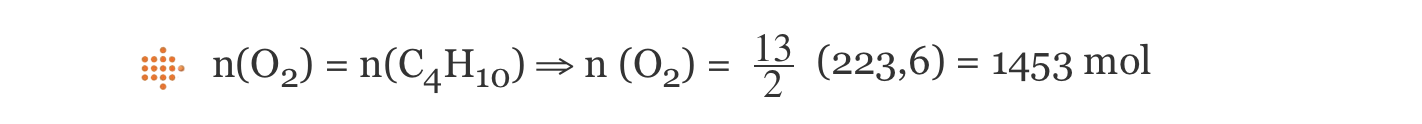2008 – Teste Intermédio – 11ºAno – abril
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 11ºAno – 2008
- Duração do Teste: 90 minutos | 22.04.2008
Grupo I
1. Leia atentamente o seguinte texto.
Conta a lenda que no século XVII o italiano Galileu Galilei tendo deixado cair uma pedra grande e uma pedra pequena do cimo da torre de Pisa, verificou que ambas chegavam ao chão, aproximadamente, ao mesmo tempo.
Qual é a pedra que deve, de facto, cair primeiro, se se ignorar a resistência do ar? A pedra grande, ou a pedra pequena? Ignorar a resistência do ar significa que se imagina que não há atmosfera.
Se fizermos a experiência na Terra, deixando cair dois objectos do mesmo material, um muito grande e outro muito pequeno, constatamos que cai primeiro o objecto maior. Somos, então, levados pela intuição a concluir que devia cair primeiro a pedra grande, mesmo que se “desligasse” a resistência do ar.
A Natureza nem sempre está, porém, de acordo com as nossas intuições mais imediatas. Se se “desligasse” a resistência do ar, a pedra grande e a pedra pequena cairiam ao mesmo tempo.
No chamado “tubo de Newton” (um tubo de vidro onde se faz o vácuo) pode-se deixar cair, da mesma altura, objectos diferentes, por exemplo, uma chave e uma pena, e observar que chegam ao fundo do tubo exactamente ao mesmo tempo. Esse instrumento permite efectuar, em condições ideais, a hipotética experiência de Galileu na torre de Pisa.
Adaptado de Física Divertida, Carlos Fiolhais, Gradiva, 1991
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.1. Com base na informação apresentada no texto, seleccione a alternativa que completa correctamente a frase seguinte.
Na ausência de resistência do ar, o tempo de queda de um objecto depende…
(A) … da sua forma.
(B) … da sua massa.
(C) … da sua densidade.
(D) … da altura de queda.
- Opção (D)
⇒ Se um corpo for deixado cair de uma certa altura, com resistência do ar desprezável, ele cairá sempre da mesma maneira, seja qual for a sua forma ou outras propriedades suas.
⇒ A aceleração da queda é a aceleração gravítica, que apenas depende da Terra e não do corpo.
- Opção (D) …………. 8 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.2. Considere um objecto que, após ter sido abandonado do cimo da torre de Pisa, cai verticalmente até ao solo.
Sendo apreciável o efeito da resistência do ar sobre esse objecto, ele acaba por atingir a velocidade terminal.
Escreva um texto, no qual caracterize o movimento de queda desse objecto, abordando os seguintes tópicos:
• Identificação das forças que sobre ele actuam, descrevendo o modo como variam as intensidades dessas forças, durante a queda;
• Descrição, fundamentada, da variação do módulo da sua aceleração durante a queda;
• Identificação dos dois tipos de movimento que ele adquire durante a queda.
⇒ Um corpo ao ser largado fica sujeito à força gravítica (o peso), a qual é vertical, de sentido descendente e constante.
Desta forma, o corpo inicia um movimento acelerado.
⇒ A força de resistência do ar é contrária ao sentido do movimento e o seu valor aumenta quando aumenta a velocidade do corpo.
⇒ Depois de o corpo iniciar o seu movimento fica sujeito a uma força descendente constante, o peso, e a uma ascendente, a força de resistência do ar, cujo valor vai aumentado.
⇒ O movimento é acelerado (a velocidade aumenta), mas a aceleração do corpo, com sentido descendente, vai diminuindo de valor, até que se anula.
⇒ A partir desse instante, a força gravítica é anulada pela força de resistência do ar. Então, o corpo inicia um movimento uniforme (aceleração nula).
- A resposta deve contemplar os seguintes tópicos:
⇒ As forças que actuam sobre o objecto são o peso, cuja intensidade se mantém constante durante a queda, e a resistência do ar, cuja intensidade aumenta durante a queda.
⇒ Como as forças que actuam no corpo têm sentidos opostos, o módulo da aceleração diminui à medida que a intensidade da resistência do ar aumenta, tornando-se nulo quando a intensidade da resistência do ar iguala a intensidade do peso.
⇒ O objecto adquire inicialmente um movimento acelerado, passando depois a mover-se com movimento uniforme.
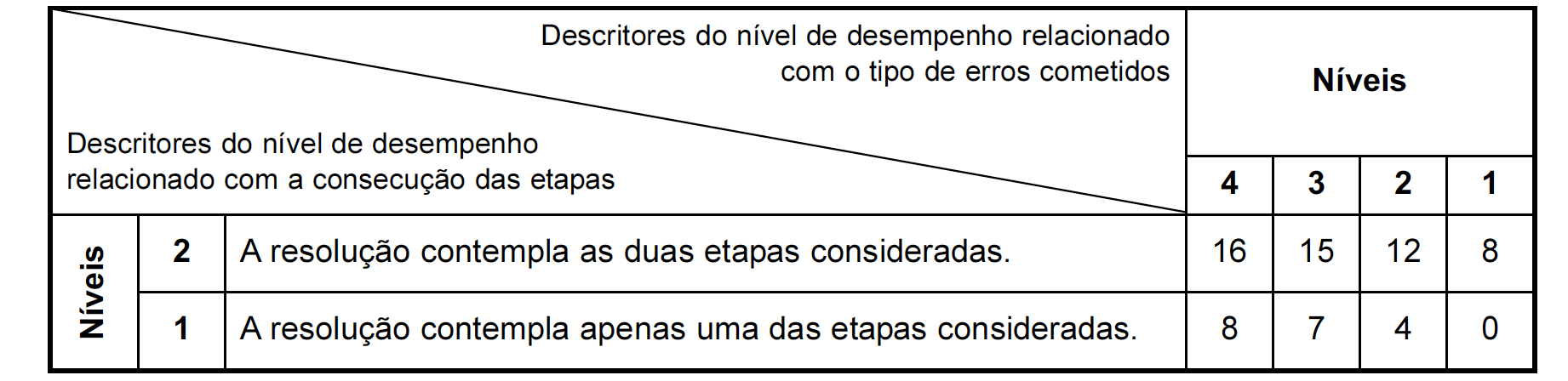
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
- 11ºano – Física – A.l. – 1.3 – Movimento uniformemente retardado
1.3. Nos seus estudos sobre o movimento dos corpos, para além da experiência descrita no texto, Galileu terá idealizado outras, utilizando planos inclinados.
Analogamente, é habitual usar, nos laboratórios das escolas, calhas para o estudo dos movimentos.
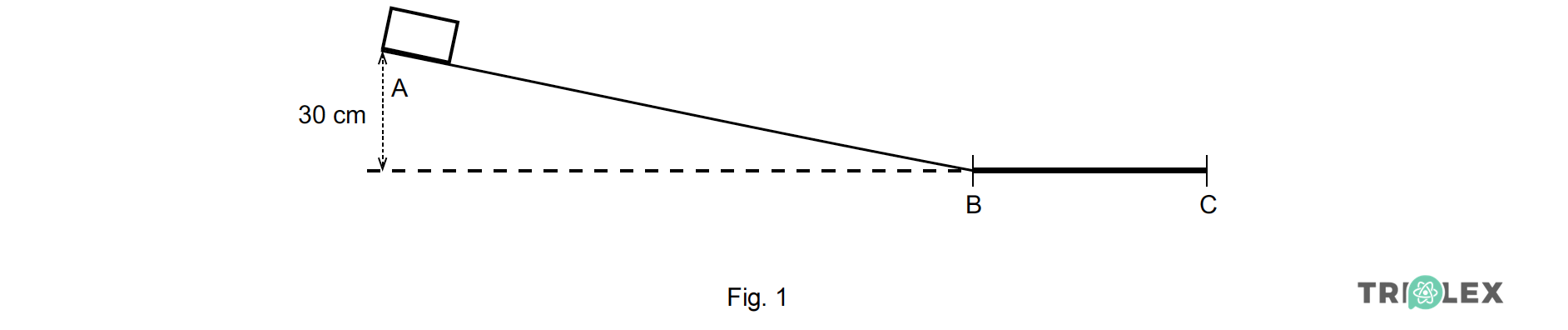
A figura 1 representa uma calha, inclinada entre os pontos A e B, que termina num tro.o horizontal BC.
O desnível entre o ponto A e o troço horizontal é de 30 cm.
Um bloco, de massa 100 g, colocado no ponto A, desliza ao longo da calha, atingindo o ponto C com velocidade nula. Entre os pontos A e B considera-se desprezável o atrito.
Entre os pontos B e C a superfície da calha é rugosa e, por isso, passa a actuar sobre o bloco uma força de atrito de intensidade 0,50 N.
Calcule o tempo que o bloco demora a percorrer o troço BC.
Apresente todas as etapas de resolução.

⇒ Para determinar o tempo que o bloco demora a percorrer o troço BC, tem de se calcular a velocidade com que atinge a posição B e a aceleração que adquire entre B e C.
⇒ Como as forças dissipativas entre A e B são desprezáveis há conservação de energia durante este percurso.
- EpA = EpB ⇔ mghA = ½ m vB2 ⇔ vB = 2,45 m s-1
⇒ Recorrendo à 2.ª Lei de Newton determina-se a aceleração entre B e C.
- Fr = Fa ⇔ ma = Fa ⇔ a = Fa/m ⇔ a = 5,0 m s-2
vC = vB – a t ⇒ 0 = 2,45 – 5,0 t ⇔ t = 0,49 s
- O bloco demorou a percorrer o troço BC 0,49 s.
- A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correta:
⇒ Calcula o módulo da velocidade com que o bloco atinge o ponto B (vB = 2,45 m s–1).
⇒ Calcula o módulo da aceleração do bloco no troço BC (a = 5,00 m s–2).
⇒ Calcula o tempo que o bloco demora a percorrer o troço BC (t = 0,49 s).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

2. No século XIX, J. P. Joule mostrou que a queda de objectos podia ser aproveitada para aquecer a água contida num recipiente.
Contudo, foram os seus estudos quantitativos sobre a energia libertada por um condutor quando atravessado por corrente eléctrica, que permitiram o desenvolvimento de alguns sistemas de aquecimento de água, usados actualmente em nossas casas, como as cafeteiras eléctricas.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2.1. Nessas cafeteiras a resistência eléctrica encontra-se geralmente colocada no fundo.
Indique qual é o mecanismo de transferência de energia como calor que se pretende aproveitar com esta posição da resistência e descreva o modo como esta transferência ocorre.
⇒ A água nas cafeteiras aquece devido, essencialmente, ao mecanismo de convecção.
⇒ A água que está junto ao fundo aquece e fica menos densa, o que origina a sua subida e a troca de energia com a água que encontra na subida.
⇒ Por outro lado, a água mais fria desce, originando-se, com estes movimentos de massas, o que se denomina por correntes de convecção.
⇒ As camadas mais frias descem, aquecendo depois por contacto com o fundo, e as camadas mais quentes, no fundo, sobem através do resto do líquido.
⇒ Pretende-se aproveitar o mecanismo de convecção.
⇒ A água que se encontra perto da resistência aquece, ficando menos densa do que a restante e, por esse motivo, sobe na cafeteira. À medida que sobe, vai transferindo energia para as regiões vizinhas, pelo que vai arrefecendo. A sua densidade vai assim aumentar de novo, voltando essa água a descer até ao fundo da cafeteira, onde volta a receber energia…
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2.2. A figura 2 representa um gráfico da variação da temperatura, ΔT, de uma amostra de água contida numa cafeteira eléctrica, em função da energia, E, que lhe é fornecida.

Sabendo que essa amostra tem uma massa m e uma capacidade térmica mássica c, seleccione a alternativa que contém a expressão que traduz o declive da recta representada na figura 2.

- Opção (D)
⇒ A expressão que relaciona a energia fornecida com a variação da temperatura durante um aquecimento é:
- E = m c ΔT (1)
⇒ Como o gráfico traduz ΔT = f(E), o declive do segmento de reta correspondente ao aquecimento da água é:
- declive = ΔT/E
Da expressão (1), conclui-se que
 ⇒ A alternativa que contém a expressão que traduz o declive da reta representada na figura 2 é a (D).
⇒ A alternativa que contém a expressão que traduz o declive da reta representada na figura 2 é a (D).
- Opção (D)…………. 8 pontos
3. Muitos dos sistemas de aquecimento utilizados, tanto a nível industrial, como doméstico, recorrem às reacções de combustão dos alcanos, uma vez que estas reacções são fortemente exotérmicas.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
3.1. O metano, CH4, o etano, C2H6, o propano, C3H8, e o butano, C4H10, são gases nas condições normais de pressão e temperatura (PTN).
Nessas condições, a densidade de um desses gases é aproximadamente 1,343 g dm–3.
Seleccione a alternativa que refere o g.s que apresenta esse valor de densidade.
(A) Metano, CH4
(B) Etano, C2H6
(C) Propano, C3H8
(D) Butano, C4H10
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
3.2. A reacção de combustão do butano (M = 58,14 g mol–1) no ar pode ser traduzida pela seguinte equação química:
2 C4H10 (g) + 13 O2 (g) → 8 CO2 (g) + 10 H2O (g)
Considerando que uma botija de butano contém 13,0 kg desse gás, calcule o volume de oxigénio, nas condições PTN, necessário para a combustão completa dessa massa de butano.
Apresente todas as etapas de resolução.
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula a quantidade de O2 (g) necessária para a combustão completa do butano (n = 1,453 × 103 mol).
⇒ Calcula o volume de O2 (g) necessário (V = 3,26 × 104 dm3).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
4. As moléculas de amoníaco, NH3 (g), e de metano, CH4 (g), são constituídas por átomos de hidrogénio ligados a um átomo de um elemento do 2.º Período da Tabela Periódica, respectivamente azoto e carbono.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
4.1. As transições electrónicas que ocorrem entre níveis de energia, n, no átomo de hidrogénio, estão associadas às riscas que se observam nos espectros de emissão e de absorção desse átomo.
Relativamente a essas transições classifique como verdadeira (V) ou falsa (F), cada uma das afirmações seguintes.
(A) A transição electrónica de n = 3 para n = 1 ocorre com emissão de radiação ultravioleta.
(B) A transição electrónica de n = 3 para n = 4 está associada a uma risca vermelha no espectro de absorção do átomo.
(C) A transição electrónica de n = 5 para n = 3 ocorre com emissão de radiação infravermelha.
(D) A transição electrónica de n = 4 para n = 2 está associada a uma risca colorida no espectro de emissão do átomo.
(E) Qualquer transição electrónica para n = 2 está associada a uma risca da série de Balmer.
(F) Os valores absolutos das energias envolvidas nas transições electrónicas de n = 4 para n = 1, e de n = 1 para n = 4, são iguais.
(G) A série de Lyman corresponde às transições electrónicas de qualquer nível para n = 1.
(H) A uma risca colorida no espectro de absorção do átomo corresponde uma risca negra no respectivo espectro de emissão.
- Verdadeiras : (A), (C), (D), (F), (G)
- Falsas : (B), (E), (H)
⇒ (B) A transição eletrónica de n = 3 para n = 4 está associada a uma risca na zona do infravermelho no espetro de absorção do átomo.
⇒ (E) Qualquer transição eletrónica de n > 2 para n = 2 está associada a uma risca da série de Balmer.
⇒ (H) A uma risca colorida no espetro de emissão corresponde uma risca negra no respetivo espetro de absorção.
4.2. No estado fundamental, a configuração electrónica do átomo de azoto é 1s2 2s2 2p3, sendo cada orbital atómica caracterizada por um conjunto de números quânticos (n, l, m).
Seleccione a alternativa que corresponde ao conjunto de números quânticos que caracteriza uma das orbitais do átomo de azoto que, no estado fundamental, contém apenas um electrão.
(A) (2, 1, 2)
(B) (2, 1, 1)
(C) (2, 0, 1)
(D) (2, 0, 0)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B)
⇒ Na configuração 1s2 2s2 2p3, de acordo com o princípio da energia mínima e com a regra de Hund existem duas orbitais s (1s e 2s) totalmente preenchidas e três orbitais p (2px ; 2py e 2pz) semipreenchidas.
⇒ Cada uma das orbitais 2p (n = 2 e = 1) contém apenas um electrão.
⇒ O número quântico de momento magnético só pode ter valores inteiros de –l a +l.
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
4.3. No estado fundamental, a configuração electrónica do átomo de carbono, C, é 1s2 2s2 2p2, enquanto a do átomo de silício, Si, é [Ne] 3s2 3p2.
Relativamente a estes dois elementos, seleccione a alternativa que contém os termos que devem substituir as letras (a) e (b), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
O átomo de carbono tem __(_a_)__ energia de ionização e __(_b_)__ raio atómico do que o átomo de silício.
(A) … maior … menor …
(B) … maior … maior …
(C) … menor … menor …
(D) … menor … maior …
- Opção (A)
⇒ O carbono e o silício estão no mesmo grupo (14), mas o carbono encontra-se no 2.º período e o silício no 3.º.
⇒ Os electrões de valência do silício estão no nível de energia n = 3 e os do carbono no nível n = 2, por isso os do silício são mais fáceis de retirar.
⇒ O carbono tem, então, maior energia de ionização.
⇒ Como o carbono tem menos níveis, os electrões de valência encontram-se menos afastados do núcleo e ele tem menor raio atómico.
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
4.4. Os átomos de carbono e de azoto podem ligar-se entre si de modos diferentes. Em alguns compostos a ligação carbono–azoto é tripla (C ≡ N), enquanto noutros compostos a ligação carbono–azoto é simples (C – N).
O valor da energia m.dia de uma dessas ligações é 276 kJ mol–1, enquanto o valor relativo à outra ligação é 891 kJ mol–1. Em relação ao comprimento médio dessas ligações, para uma o valor é 116 pm, enquanto para a outra é 143 pm.
Seleccione a alternativa que cont.m os valores que devem substituir as letras (a) e (b), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
O valor da energia média da ligação tripla carbono–azoto (C ≡ N) é __(_a_)__, e o valor do comprimento médio dessa ligação é __(_b_)__.
(A) … 276 kJ mol–1 … 116 pm.
(B) … 276 kJ mol–1 … 143 pm.
(C) … 891 kJ mol–1 … 116 pm.
(D) … 891 kJ mol–1 … 143 pm.
- Opção (C)
⇒ A ligação tripla carbono-azoto é mais forte e mais curta que a ligação simples carbono-azoto.
⇒ Assim, a energia média da ligação tripla é superior à da ligação simples e o comprimento médio da ligação tripla é menor que o da ligação simples.
⇒ A alternativa a que corresponde o maior valor da energia de ligação (891 kJ mol-1) e o menor valor de comprimento de ligação, (116 pm), correspondentes à ligação tripla carbono-azoto, é a (C).
- Opção (C)…………. 8 pontos
5. O amoníaco é uma base, segundo a teoria de Bronsted-Lowry, sendo a sua reacção de ionização em água traduzida pela seguinte equação:
NH3 (aq) + H2O (l) ⇋ NH4+ (aq) + OH– (aq)
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
5.1. Considerando que a espécie NH3 (aq) é uma base mais fraca do que a espécie OH– (aq), seleccione a alternativa que corresponde a uma afirmação correcta.
(A) A espécie NH3 (aq) aceita iões H+ com maior facilidade do que a espécie OH– (aq).
(B) A espécie NH4+ (aq) cede iões H+ com maior facilidade do que a espécie H2O (l).
(C) A espécie H2O (l) aceita iões H+ com maior facilidade do que a espécie NH3 (aq).
(D) A espécie OH– (aq) cede iões H+ com maior facilidade do que a espécie NH4+ (aq).
- Opção (B)
Como a espécie NH3 (aq) é uma base mais fraca do que a espécie HO– (aq), e, quanto mais fraca é uma base menor é a sua facilidade para aceitar iões H+ (aq), a espécie HO– (aq) aceita iões H+ (aq) com maior facilidade.
⇒ (B) Verdadeira.
Quanto mais fraca é uma base, mais forte é o respetivo ácido conjugado. Assim, a espécie NH4+ (aq), ácido conjugado de NH3 (aq), cede iões H+ (aq) com maior facilidade que a espécie H2O (l), ácido conjugado de HO– (aq).
⇒ (C) Falsa.
Como a espécie NH3 (aq) é uma partícula básica em solução aquosa, e de acordo com a equação de protólise apresentada, a espécie NH3 (aq) aceita iões H+ (aq) com maior facilidade que a espécie H2O (l).
⇒ (D) Falsa.
A espécie NH4 + (aq), como é uma partícula ácida, cede iões H+ (aq) com maior facilidade que a espécie HO– (aq), que é uma partícula básica.
- Opção (B)…………. 8 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
- pHO = 14 – 10,95 = 3,05
- pHO = – log [HO– (aq)], logo [HO– (aq)] = 10-3,05 = 8,9 x 10-4 mol/dm3
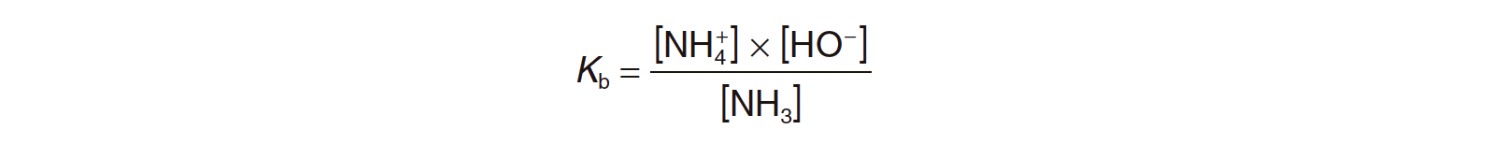 ⇒ Atendendo à estequiometria do equilíbrio, [HO– (aq)] = [NH4+ (aq)].
Substituindo os valores conhecidos na expressão de Kb, vem:
⇒ Atendendo à estequiometria do equilíbrio, [HO– (aq)] = [NH4+ (aq)].
Substituindo os valores conhecidos na expressão de Kb, vem:
 ⇒ A concentração de NH3 (aq) na solução é de 4,4 x 10-2 mol dm-3.
⇒ A concentração de NH3 (aq) na solução é de 4,4 x 10-2 mol dm-3.
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula a concentração de OH– (aq) na solução ([OH–] = 8,9 × 10–4 mol dm–3).
⇒ Substitui, adequadamente, os valores conhecidos, na expressão de Kb e calcula a concentração da espécie NH3 (aq) na solução ([NH3] = 4,4 × 10–2 mol dm–3).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
5.3. Considerando que a molécula de amoníaco, NH3, possui três pares de electrões de valência ligantes e um par de electrões de valência não ligante, seleccione a alternativa que completa correctamente a frase seguinte.
A geometria da molécula de amoníaco é piramidal trigonal, sendo os ângulos de ligação menores do que os ângulos de um tetraedro regular, porque…
(A) … apenas o par de electrões não ligante exerce repulsão sobre os pares de electrões ligantes.
(B) … as repulsões entre o par de electrões não ligante e os pares de electrões ligantes têm a mesma intensidade que as repulsões entre os pares ligantes.
(C) … as repulsões entre o par de electrões não ligante e os pares de electrões ligantes são mais fortes do que as repulsões entre os pares ligantes.
(D) … apenas os pares de electrões ligantes exercem repulsão sobre o par de electrões não ligante.
- Opção (C)
⇒ A geometria de uma molécula é aquela que conduz à máxima estabilidade do sistema molecular.
⇒ Segundo o método da repulsão dos pares eletrónicos de valência, estes dispõem-se no espaço o mais afastados possível, de modo a conduzir às menores repulsões eletrónicas possíveis.
⇒ No caso da molécula NH3, os pares eletrónicos de valência que rodeiam o átomo central são três pares de eletrões ligantes, correspondentes às três ligações covalentes N – H e o par eletrónico não ligante localizado no azoto.
⇒ O maior afastamento possível destes quatro pares obtém-se quando eles se dispõem no espaço de modo, aproximadamente, tetraédrico, conferindo ao conjunto NH3 uma geometria piramidal trigonal.
⇒ Os ângulos de ligação na molécula de amoníaco são menores que os ângulos de um tetraedro regular, devido ao facto de o efeito repulsivo entre os pares de eletrões não ligante-ligante ser superior ao efeito repulsivo entre os pares de eletrões ligante-ligante.
- Opção (C)…………. 8 pontos
6. A reacão de síntese do sal complexo, sulfato de tetraminocobre (II) mono-hidratado, [Cu(NH3)4]SO4 . H2O, pode ser feita por cristalização lenta deste sal, a partir de uma reação de precipitação entre soluções aquosas de amoníaco e de sulfato de cobre (II).
Dissolvendo em água 5,00 g de cristais de sulfato de cobre penta-hidratado, CuSO4 . 5 H2O, e adicionando amoníaco em excesso, obtém-se uma determinada massa de sal complexo.
6.1. Considere que no armazém de reagentes da sua escola s. existia sulfato de cobre (II) penta-hidratado impuro, contendo 15% (m/m) de impurezas, ao qual tinha de recorrer para realizar esta síntese.
Seleccione a alternativa que apresenta o valor da massa de reagente impuro que teria de medir para obter a mesma massa de sal complexo, admitindo o mesmo rendimento para o processo de síntese.
(A) 5,88 g
(B) 5,75 g
(C) 5,15 g
(D) 5,64 g
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (A)…………. 8 pontos
6.2. Os cristais de sulfato de cobre (II) penta-hidratado devem ser inicialmente reduzidos a pó num almofariz, antes de se efectuar a pesagem deste reagente.
Apresente uma razão justificativa deste procedimento experimental.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Os cristais de sulfato de cobre (II) penta-hidratado devem ser reduzidos a pó.
⇒ Deste modo aumenta-se a superfície de contacto com o amoníaco da solução, facilitando a dissolução.
- Tornar a dissolução do sal mais rápida ou aumentar a superfície de contacto soluto/solvente………….. 8 pontos
6.3. Após a cristalização do sal complexo há que separar, por decantação e filtração, o líquido sobrenadante dos cristais depositados no fundo do recipiente.
Sabendo que os cristais que se obtém nesta síntese são muito finos, indique o tipo de filtração mais adequado.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Como os cristais são finos deve fazer-se uma filtração a pressão reduzida (por vácuo, por sucção).
⇒ É mais rápida e vai permitir aumentar o rendimento.
Deve também ter-se cuidado na escolha do tamanho dos poros do papel de filtro.
- Filtração a pressão reduzida …………. 8 pontos
FIM