2009 – Teste Intermédio – 10ºAno – junho
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 10ºAno – 2009
- Duração do Teste: 90 minutos | 03.06.2009
1. A Terra é o único planeta do sistema solar que possui uma atmosfera rica em oxigénio.
1.1. A atmosfera terrestre constitui um filtro natural para as radiações provenientes do Sol, em especial para as radiações ultravioleta de maior energia, as UV-C, e as radiações ultravioleta de energia intermédia, as UV-B.
Elabore um texto relativo às radiações ultravioleta provenientes do Sol, abordando os tópicos seguintes:
• Camadas da atmosfera onde as radiações ultravioleta UV-C e UV-B são predominantemente absorvidas.
• Reacções que traduzem o efeito das radiações ultravioleta nas moléculas de oxigénio (O2) e de ozono (O3), na estratosfera.
• Significado de o índice de protecção solar (IPS) de um dado creme protector ser igual a 20.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ As radiações solares UV-C, as de maior energia que chegam à atmosfera terrestre, são predominantemente absorvidas na termosfera por moléculas pequenas, como O2, que sofrem fotólise produzindo oxigénio atómico:
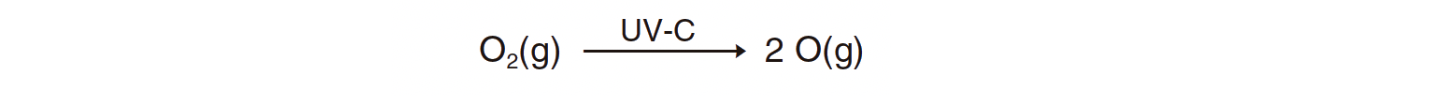
⇒ As radiações UV-B, de menor energia, são predominantemente absorvidas na estratosfera pelo ozono e sofrem, igualmente, decomposição fotolítica – originando dioxigénio e átomos de oxigénio:

⇒ Os protetores solares absorvem as radiações UV que atingem a superfície terrestre e poderiam causar danos aos seres vivos. Um protetor solar com IPS = 20 permite uma exposição ao Sol sem consequências nocivas durante um período 20 vezes maior que o permitido na ausência de protetor.
- A resposta deve abordar os tópicos seguintes:
⇒ As radiações UV-C são predominantemente absorvidas na termosfera e na mesosfera, enquanto as UV-B s o predominantemente absorvidas na estratosfera.
⇒ Na estratosfera a radiação UV provoca a dissociação das moléculas de oxigénio e das moléculas de ozono (ou O2 → 2 O e O3 → O2 + O).
⇒ Significa que a utilização adequada desse creme protector permite que uma pessoa fique, em princípio, vinte vezes mais protegida relativamente aos efeitos das radiações ultravioleta sobre a pele, do que se não utilizar qualquer protecção.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

1.2. A composição da atmosfera terrestre tem variado, desde a sua formação até aos tempos actuais.
Na figura 1 apresenta-se a composição da atmosfera terrestre em três momentos da sua existência – gráficos 1, 2 e 3.
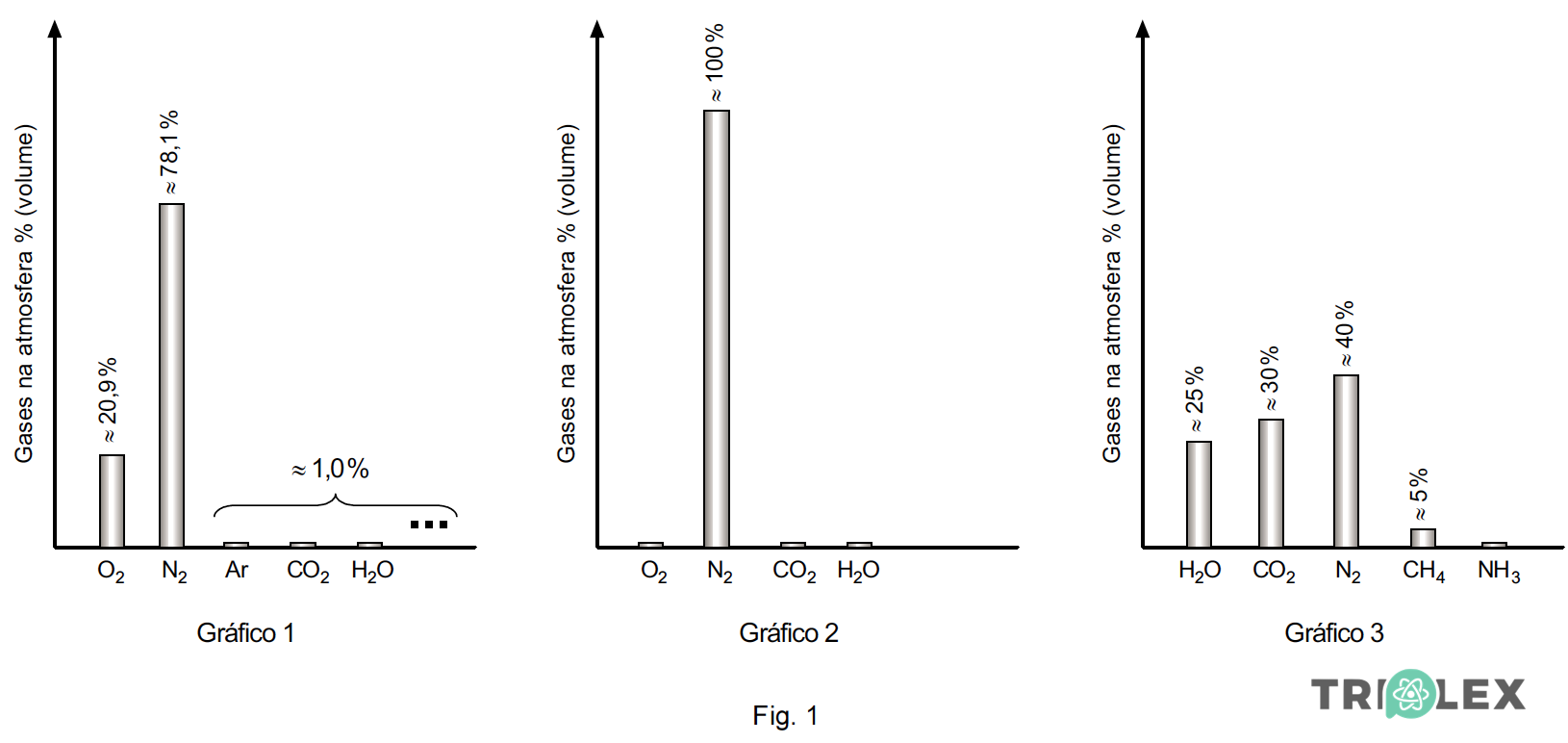
Seleccione a única alternativa que contém a sequência correcta dos gráficos da composição da atmosfera da Terra, ordenados da mais antiga para a actual.
(A) Gráfico 3, Gráfico 2 e Gráfico 1.
(B) Gráfico 2, Gráfico 3 e Gráfico 1.
(C) Gráfico 3, Gráfico 1 e Gráfico 2.
(D) Gráfico 1, Gráfico 2 e Gráfico 3.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (A)
- Opção (A)…………. 8 pontos
2. Os elementos químicos predominantes no Universo são o hidrogénio e o hélio, os dois elementos mais leves. Cerca de 98% do Universo é constituído por esses elementos.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
2.1. Os espectros de emissão e de absorção atómica são espectros de riscas, estando estas riscas relacionadas com as transições electrónicas que ocorrem nos átomos.
Na figura 2 estão esquematizados alguns níveis de energia do átomo de hidrogénio (sendo n o número quântico principal correspondente a cada um desses níveis de energia), bem como algumas transições electrónicas, T1 a T4.
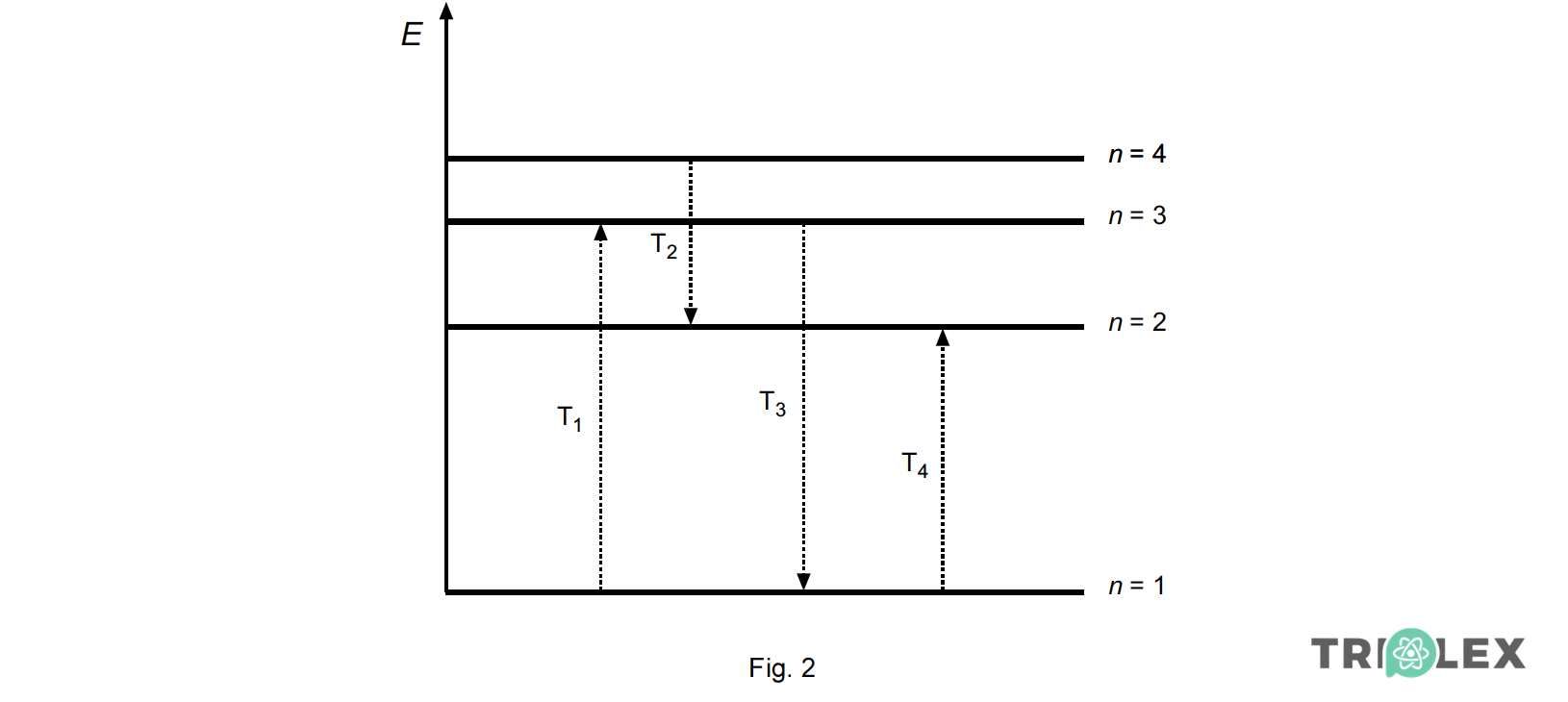
Seleccione a única alternativa que corresponde a uma afirmação correcta, tendo em consideração o esquema da figura 2.
(A) A transição electrónica T1 pode ocorrer por absorção de energia sob a forma de uma radiação electromagnética na zona do visível.
(B) A transição electrónica T2 corresponde a uma risca, na zona do infravermelho, do espectro de emissão do átomo de hidrogénio.
(C) A transição electrónica T3 pode ocorrer por emissão de energia sob a forma de uma radiação electromagnética na zona do infravermelho.
(D) A transição electrónica T4 corresponde a uma risca negra, na zona do ultravioleta, do espectro de absorção do átomo de hidrogénio.
- Opção (D)
⇒ (A) Falsa.
- porque a transição T1 corresponde a absorção no UV
⇒ (B) Falsa.
- porque a transição T2 corresponde a emissão no visível;
⇒ (C) Falsa.
- a transição T3 corresponde a emissão no UV.
- Opção (D)…………. 8 pontos
2.2. Seleccione a única alternativa que corresponde a uma afirmação correcta, relativamente ao átomo de hélio, He.
(A) No estado de menor energia, a configuração electrónica do átomo de hélio é 1s1 2s1.
(B) No estado de menor energia, os electrões do átomo de hélio têm número quântico de spin, ms, simétrico.
(C) Num estado excitado, um dos electrões do átomo de hélio pode estar numa orbital em que n = 3, l = 0 e m = 1.
(D) No átomo de hélio, um electrão na orbital 2s tem a mesma energia que um electrão numa das orbitais 2p.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B)
⇒ (A) Falsa.
- porque é um estado excitado;
⇒ (C) Falsa.
- porque se l = 0, ml teria de ser também igual a zero;
⇒ (D) Falsa.
- porque o hélio não é hidrogenoide e, portanto, a energia depende também da subcamada.
- Opção (B)…………. 8 pontos
2.3. Seleccione a única alternativa que contém os termos que preenchem o espaço seguinte, de modo a obter uma afirmação correcta.
Nas mesmas condições de pressão e temperatura, o volume ocupado por 4,00 g de hélio, He(g), é aproximadamente ______ volume ocupado por 4,00 g de hidrogénio, H2 (g).
(A) igual ao
(B) o dobro do
(C) metade do
(D) o quádruplo do
- Opção (C)
- m(He) = 4,00 g ⇒ n(He) = 1 mol
- m(H2) = 4,00 g ⇒ n(H2) = 2 mol
⇒ Nas mesmas condições de temperatura e pressão, o volume de 1 mole de moléculas gasosas é metade do volume de 2 mol.
- Opção (C)…………. 8 pontos
3. A espectroscopia fotoelectrónica, que se baseia no efeito fotoeléctrico, é um processo que pode ser usado para determinar a energia de cada electrão de um átomo.
3.1. A energia mínima para remover um electrão do átomo de sódio, Na, é 8,24 x 10–19 J.
Determine o módulo da velocidade do electrão ejectado de um átomo de sódio, quando nele incide uma radiação de energia 2,00 x 10–18 J / fotão.
Apresente todas as etapas de resolução.
m(electrão) = 9,11 x 10–31 kg
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- A resolução deve apresentar, no mínimo, as etapas seguintes:
⇒ Calcula a energia cinética do electrão ejectado (Ec = 1,176 x 10–18 J).
⇒ Calcula o módulo da velocidade do electrão ejectado (v = 1,61 x 106 m s–1).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3.2. As configurações electrónicas dos átomos dos metais alcalinos, no estado de menor energia, apresentam uma característica comum.
Indique essa característica.
- Configuração eletrónica de valência ns1, isto é, apenas 1 eletrão de valência.
- Apresentam apenas um eletrão de valência (ou equivalente) …………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
3.3. Seleccione a única alternativa que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
A energia de ionização do átomo de sódio, Na, é ______ do que a do átomo de magnésio, Mg, enquanto o raio do átomo de sódio é ______ do que o do átomo de magnésio.
(A) maior … maior
(B) maior … menor
(C) menor … menor
(D) menor … maior
- Opção (D)
⇒ A primeira energia de ionização, para elementos representativos do mesmo período, aumenta com Z pelo facto de o aumento da carga nuclear aumentar a força atrativa núcleo-eletrão para eletrões situados na mesma camada periférica.
⇒ O raio atómico, para elementos representativos do mesmo período, diminui com Z, pelo facto de o aumento progressivo da carga nuclear provocar um aumento da força atrativa núcleo-eletrões superior ao aumento da repulsão intereletrónica.
- Opção (D)…………. 8 pontos
4. O azoto e o oxigénio formam moléculas diatómicas homonucleares, N2 e O2, respectivamente.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
4.1. Em condições normais de pressão e temperatura (condições PTN), a substância azoto, N2, é um gás.
Seleccione a única alternativa que contém a expressão que permite obter o valor da densidade do azoto, N2 (g), nessas condições, expresso em g cm–3.

- Opção (B)
- Opção (B)…………. 8 pontos
4.2. Seleccione a única alternativa que corresponde ao número aproximado de átomos que existem em 48,0 g de oxigénio, O2 (g).
(A) 6,02 x 1023
(B) 9,03 x 1023
(C) 1,20 x 1024
(D) 1,81 x 1024
- Opção (D)
- m(O2) = 48,0 g ⇒ n(O2) = 1,5 mol
⇒ 3,0 mol de átomos de oxigénio 6,02 x 1023 átomos mol-1 x 3,0 mol = 1,81 x 1024 átomos
- Opção (D)…………. 8 pontos
5. Para arrefecer a água contida num copo, será mais eficaz adicionar-lhe água líquida a 0 ºC ou gelo à mesma temperatura?
Para responder a esta pergunta através de uma actividade experimental, um grupo de alunos procedeu do modo seguinte:
• Numa tina de vidro, introduziram alguns cubos de gelo e uma pequena quantidade de água, e aguardaram até que se atingisse o equilíbrio térmico, a 0 ºC.
• Aqueceram água, que repartiram por dois gobelés, A e B, tendo colocado 200 g de água em cada um e medido a temperatura inicial em cada um deles, que era 42,3 ºC.
• Adicionaram, ao gobelé A, 51 g de água a 0 ºC, e foram medindo a temperatura da mistura, até ter sido atingido o equilíbrio térmico, que ocorreu a 34,7 ºC.
• Adicionaram, ao gobelé B, 51 g de gelo a 0 ºC, e foram medindo a temperatura da mistura, até que todo o gelo fundisse e fosse atingido o equilíbrio térmico, que ocorreu a 22,4 ºC.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
5.1. Determine, com base nos resultados experimentais obtidos, o calor de fusão do gelo, Lfusão, admitindo que não ocorreram trocas de energia com o exterior.
Apresente todas as etapas de resolução.
c (capacidade térmica mássica da água) = 4,18 x 103 J kg–1 ºC–1
- Gobelé A:
⇒ mA = 200 g
⇒ θAi = 42,3 ºC
⇒ mágua = 51 g
⇒ θágua = 0 ºC
⇒ θAf = 34,7 ºC
- Gobelé B:
⇒ mB = 200 g
⇒ θBi = 42,3 ºC
⇒ m = 51 g
⇒ θ = 0 ºC
⇒ θBf = 22,4 ºC
- Lfusão = ?
A energia transferida como calor pela água contida no gobelé B ao gelo é igual à energia por este absorvida, até que o sistema atinja o equilíbrio térmico.
- EB = Efusão + E
⇔ mB cágua (θBi – θBf) = m Lfusão + m cágua (θBf – θ) ⇔
⇔ 200 x 4,18 x 103 x (42,3 – 22,4) = 51 x Lfusão + 51 x 4,18 x 103 x (22,4 – 0) ⇔
⇔ 1,66 x 107 = 51 x Lfusão + 4,78 x 106 ⇔
⇔ Lfusão = 2,32 x 105 J kg-1
- O calor de fusão do gelo é 2,32 x 105 J kg-1.
- A resolução deve apresentar, no mínimo, as etapas seguintes:
⇒ Calcula a energia cedida pela água inicialmente contida no gobelé B (|Q1| = 1,66 x 104 J).
⇒ Calcula a energia absorvida pela gua que se obteve a partir da fus o do gelo (|Q2| = 4,78 x 103 J).
⇒ Calcula o calor de fusão do gelo (Lfusão = 2,3 x 105 J kg–1).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
5.2. Cálculos teóricos permitem prever que o equilíbrio térmico, no gobelé B, seria atingido a 17,5 ºC, em vez de a 22,4 ºC, conforme obtido experimentalmente.
Indique uma razão que possa explicar esta diferença.
⇒ Como a temperatura de equilíbrio térmico é superior à teoricamente prevista, conclui-se que o sistema não está isolado, havendo transferência de energia do exterior, o meio ambiente.
- O sistema não está isolado (ou equivalente) ………… 8 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
5.3. De acordo com os resultados experimentais obtidos, conclui-se que, para arrefecer a água contida num copo, é mais eficaz usar cubos de gelo do que água à mesma temperatura do gelo, uma vez que a temperatura à qual se atingiu o equilíbrio térmico é inferior no primeiro caso.
Justifique aquela conclusão, tendo em consideração o fenómeno que ocorre quando se utiliza gelo para arrefecer a água.
⇒ O fenómeno responsável pelo arrefecimento da água ser mais eficaz quando se utiliza cubos de gelo é a fusão do gelo, pois esta mudança de estado é um processo endotérmico.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
5.4. Como se designa o mecanismo de transferência de energia sob a forma de calor que ocorre, predominantemente, no arrefecimento da água contida no gobelé A?
⇒ O mecanismo de transferência de energia sob a forma de calor que ocorre no arrefecimento da água contida no gobelé A é a convecção, pois, em fluidos, este mecanismo é o predominante na transferência de energia como calor.
- Convecção …………. 8 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
5.5. Quando colocamos a mão em água e em gelo, ambos à temperatura de 0 ºC, aparentemente o gelo está mais frio do que a água.
Seleccione a única alternativa que contém a interpretação correcta deste facto.
(A) A energia transferida como calor da pele para o gelo é menor do que a energia transferida da pele para a água, no mesmo intervalo de tempo.
(B) A energia transferida como calor da água para a pele é maior do que a energia transferida do gelo para a pele, no mesmo intervalo de tempo.
(C) A energia transferida como calor do gelo para a pele é maior do que a energia transferida da água para a pele, no mesmo intervalo de tempo.
(D) A energia transferida como calor da pele para a água é menor do que a energia transferida da pele para o gelo, no mesmo intervalo de tempo.
- Opção (D)
⇒ O gelo (água no estado sólido) apresenta uma condutividade térmica superior à da água líquida.
⇒ Assim, a energia transferida como calor da pele para o gelo, por unidade de tempo, é superior à transferida da pele para a água líquida, o que origina uma maior sensação de frio.
- Opção (D)…………. 8 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
6. Numa central hidroeléctrica, a água cai de uma altura de 100 m, com um caudal mássico de 2,0 toneladas por segundo.
Seleccione a única alternativa que cont.m o valor que corresponde à energia transferida, por segundo, para as pás das turbinas, admitindo que toda a energia resultante da queda da água é transferida para as turbinas.
(A) E = 2,0 x 103 J
(B) E = 2,0 x 10–3 J
(C) E = 2,0 x 106 J
(D) E = 2,0 x 10–6 J
- Opção (C)
⇒ A energia transferida para as pás das turbinas, em cada segundo, é igual à variação de energia potencial gravítica da água.
- Caudal mássico = m/Δt = 2,0 ton s-1 = 2,0 x 103 kg s-1
- Δh = 100 m
- Δt = 1,0 s
⇒ ΔEp = m g Δh = (m/Δt) g Δh Δt = 2,0 x 103 x 10 x 100 x 1,0 = 2,0 x 106 J
- Opção (C)…………. 8 pontos
7. Imagine que, numa plataforma suspensa por dois cabos, se encontrava um caixote de madeira com massa 50 kg.
Por acidente, um dos cabos partiu-se e a plataforma ficou com uma inclinação de 20º com a horizontal, conforme esquematizado na figura 3.
 Devido a esse acidente, o caixote escorregou, tendo percorrido 6,0 m até ao extremo da plataforma.
Admita que o atrito é desprezável.
Devido a esse acidente, o caixote escorregou, tendo percorrido 6,0 m até ao extremo da plataforma.
Admita que o atrito é desprezável.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
7.1. Seleccione a única alternativa que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
À medida que o caixote escorrega pela plataforma inclinada, a sua energia cinética ______, e a sua energia potencial gravítica ______.
(A) aumenta … diminui
(B) aumenta … aumenta
(C) diminui … diminui
(D) diminui … aumenta
- Opção (A)
⇒ Como o atrito é desprezável, há conservação de energia mecânica do sistema.
- ΔEm = 0 ⇔ ΔEp + ΔEc = 0
⇒ À medida que o caixote escorrega pela plataforma, a sua altura em relação à horizontal diminui, logo, a sua energia potencial gravítica diminui e, consequentemente, aumenta a sua energia cinética.
- Opção (A)…………. 8 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
7.2. Determine o trabalho realizado pelo peso do caixote no seu deslocamento, desde a posição inicial até ao extremo da plataforma.
Apresente todas as etapas de resolução.
⇒ O trabalho realizado pelo peso do caixote, desde a posição inicial até ao extremo da plataforma, é independente da trajetória, pois o peso é uma força conservativa cujo trabalho é simétrico da variação da sua energia potencial gravítica.
- Wp = -ΔEp ⇔ Wp = – m g (hf – hi)
⇒ Como hf = 0 m e hi = d sin α, substituindo na expressão anterior, tem-se:
- Wp = – m g ( 0 – d sin α) = m g d sin α = 50 x 10 x 6,0 x sin 20º = 1,03 x 103 J
⇒ O trabalho realizado pelo peso do caixote no seu deslocamento, desde a posição inicial até ao extremo da plataforma, é cerca de 1,0 x 103 J.
- A resolução deve apresentar, no mínimo, as etapas seguintes:
⇒ Calcula o valor do peso do caixote (P = 500 N).
⇒ Calcula o trabalho realizado pelo peso do caixote (W = 1,0 x 103 J).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

FIM


