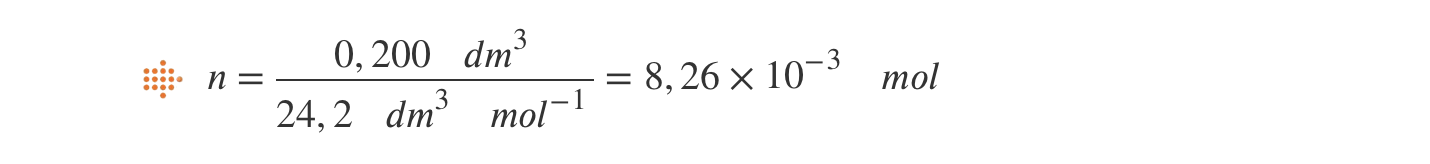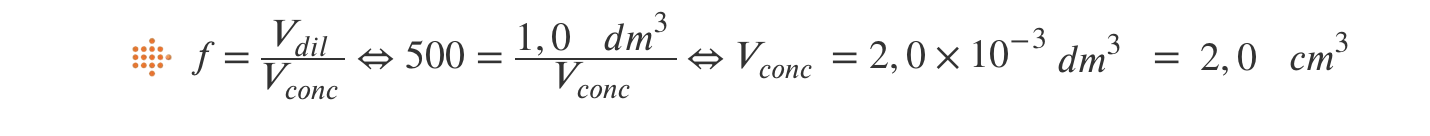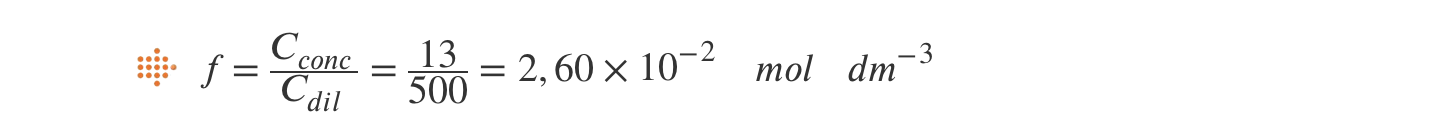2013 – Teste Intermédio – 11ºAno
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 11ºAno – 2013
- Duração do Teste: 90 minutos | 29.04.2013
GRUPO I
O diapasão, inventado pelo músico inglês John Shore em 1711, consiste numa barra de aço de secção quadrangular dobrada em forma de U, tal como se representa na Figura 1. Batendo num dos ramos do diapasão, ele fica a vibrar, emitindo um som. Um mesmo diapasão vibra sempre com a mesma frequência, emitindo um som de maior ou de menor intensidade conforme a intensidade da força com que se lhe bate. No caso de o diapasão ser igual ao que se utiliza na afinação dos instrumentos musicais, o tempo de uma vibração é igual a 1/440 do segundo.
Rómulo de Carvalho, História do telefone, 2.ª ed., Atlântida, 1962 (adaptado)

- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
1. Quanto maior for a intensidade da força com que se bate num dos ramos de um diapasão, mais
(A) alto será o som emitido pelo diapasão.
(B) forte será o som emitido pelo diapasão.
(C) grave será o som emitido pelo diapasão.
(D) fraco será o som emitido pelo diapasão.
- Opção (B)
⇒ De acordo com o texto: um mesmo diapasão vibra sempre com a mesma frequência, pelo que a altura do som emitido é a mesma (grave ou agudo); a intensidade do som emitido (forte ou fraco) depende da intensidade da força com que se bate num dos seus ramos.
⇒ Quanto mais intensa é a força aplicada maior é a amplitude da vibração e mais forte é o som emitido pelo diapasão.
- Opção (B)…………. 8 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
2. Qual é a frequência, expressa na unidade do Sistema Internacional (SI), do som emitido pelo diapasão que, de acordo com o texto, é utilizado na afinação dos instrumentos musicais?
- 440 Hz …………. 8 pontos
3. O som emitido por um diapasão pode ser analisado se o sinal sonoro for convertido num sinal elétrico, que é registado num osciloscópio.
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
3.1 Identifique o dispositivo que deve ser ligado ao osciloscópio para que seja possível analisar o som emitido por um diapasão.
⇒ O dispositivo que deve ser ligado ao osciloscópio é o microfone, pois este converte um sinal sonoro num sinal elétrico.
- Microfone …………. 8 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
3.2 A Figura 2 representa o ecrã de um osciloscópio no qual está registado um sinal elétrico resultante da conversão de um sinal sonoro emitido por um diapasão.
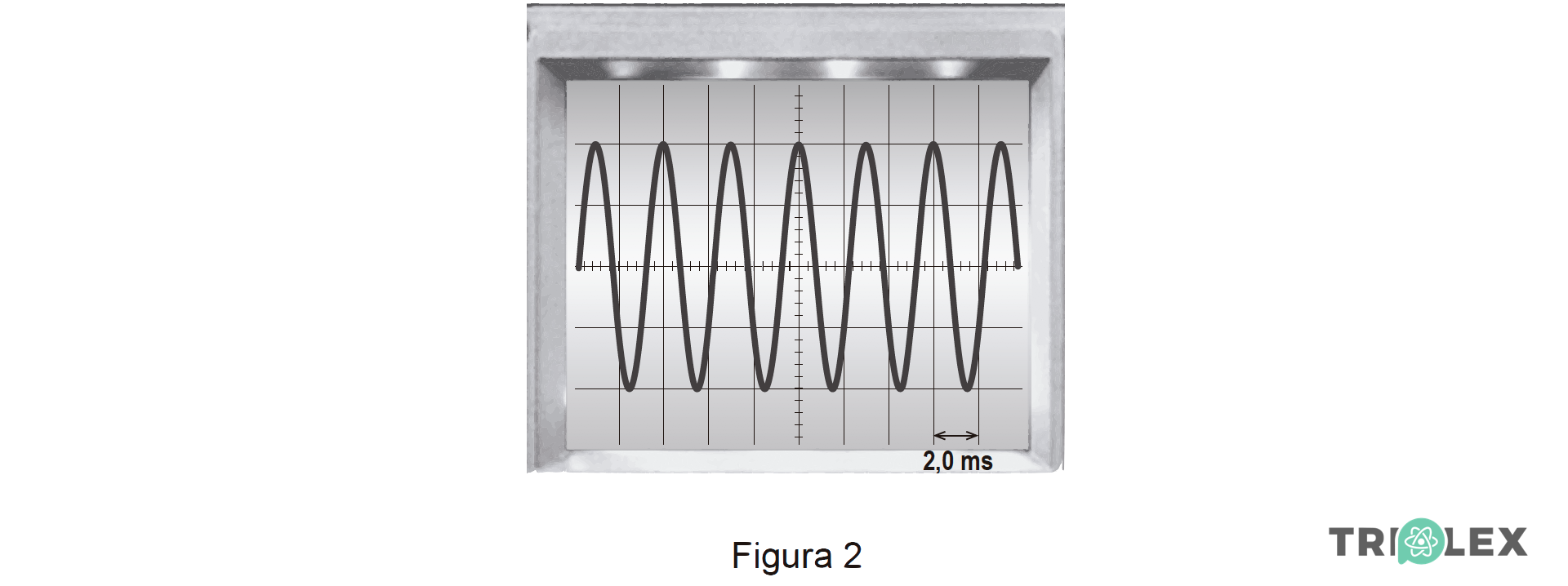
Na experiência realizada, a base de tempo do osciloscópio estava regulada para 2,0 ms/div.
O valor tabelado da velocidade de propagação do som no ar, nas condições em que foi realizada a experiência, é 343 m s-1.
Determine o comprimento de onda do som, no ar, nas condições em que foi realizada a experiência.
Apresente todas as etapas de resolução.
- λ = ?
⇒ Para calcular o comprimento de onda do som recorre-se à figura 2 do enunciado para determinar o período, pois
- λ = v T
⇒ De facto, visualizam-se 2,0 períodos correspondentes a 3 divisões (ver figura):
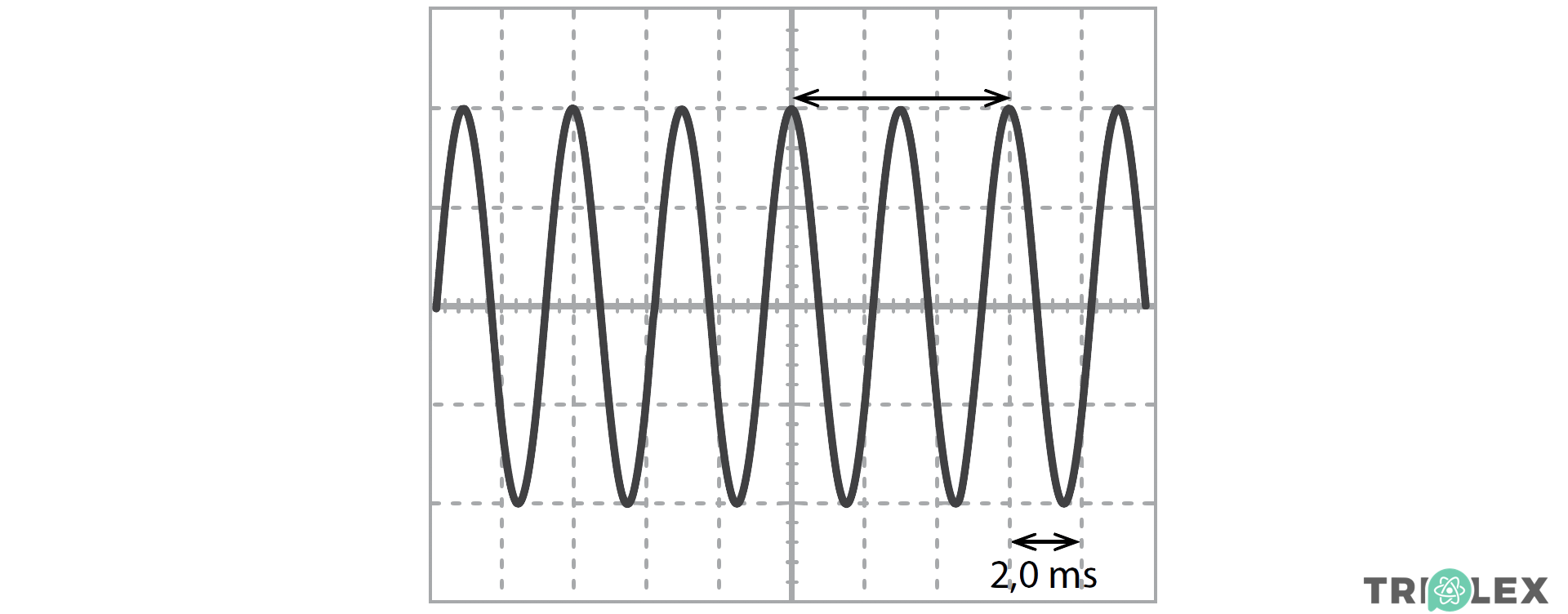
- 3 x base de tempo = 2,0 T ⇒ 3 x 2,0 = 2,0 T ⇔ T = 3,0 ms; T = 3,0 x 10-3 s
- λ = 343 x 3,0 x 10-3 = 1,0 m
⇒ O comprimento de onda do som emitido, nas condições em que a experiência foi realizada é de 1,0 m.
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Determinação do período do sinal (T = 3,0 ms).
B) Cálculo do comprimento de onda do som, no ar (λ = 1,0 m).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos*.
GRUPO II
A Figura 3 (que não está à escala) representa uma pequena bola, colocada sob um sensor de movimento, e um referencial unidimensional de eixo vertical, Oy.

A bola foi abandonada, caindo no ar até atingir o solo.
1. A bola foi abandonada, no instante t = 0 s, da posição representada na figura, caindo 1,40 m até ao solo.
A partir dos dados adquiridos com o sensor de movimento, concluiu-se que a componente escalar, segundo o eixo Oy, da posição, y, da bola variava com o tempo, t, de acordo com a equação
y = 0,20 + 5,0 t 2 (SI)
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
- 11ºano – Física – A.l. – 1.1 – Queda livre força gravítica
1.1 Apresente o gráfico da componente escalar da posição, y, da bola em função do tempo, t , desde o instante em que a bola foi abandonada até ao instante em que atingiu o solo.
Utilize a calculadora gráfica.
Na sua resposta, deve reproduzir o gráfico obtido com a calculadora, no intervalo de tempo considerado, indicando no gráfico:
• as grandezas representadas e as respetivas unidades;
• as coordenadas dos pontos que correspondem ao instante em que a bola foi abandonada e ao instante em que a bola atingiu o solo.
⇒ Antes de recorrer à calculadora gráfica, determina-se analiticamente a posição inicial da bola em relação à origem do referencial (sensor), y0, a sua posição ao atingir o solo, ys, e o tempo de queda, ts, de modo a conseguir visualizar na janela da calculadora o gráfico y = f(t).
- y = 0,20 + 5,0 t2 (SI)
⇒ Para t = 0 s, y0 = 0,20 m;
⇒ Como ys – y0 = 1,40 m, então, ys – 0,20 = 1,40 ⇔ ys = 1,60 m;
⇒ Para ys = 1,60 m, tem-se 1,60 = 0,20 + 5,0 t2 ⇔ t = 0,53 s
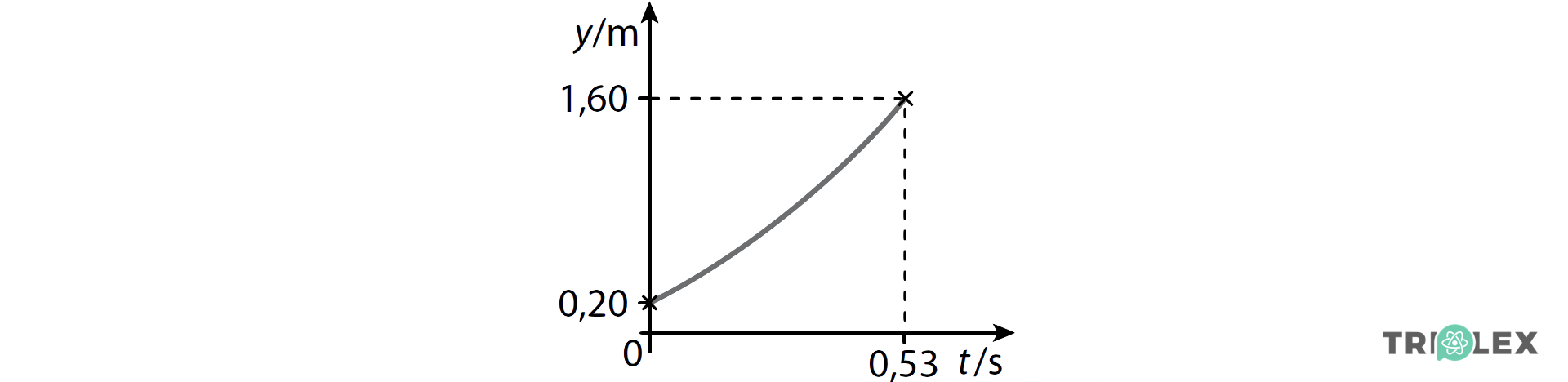

- Na resposta, é reproduzido o gráfico obtido com a calculadora, com indicação, no gráfico, das:
⇒ grandezas representadas (ver notas 1 e 2) ……………………………………………… 4 pontos
⇒ unidades em que estão expressas as grandezas representadas .. (1 + 1) …….. 2 pontos
⇒ coordenadas do ponto que corresponde ao instante em que a bola foi abandonada ………….. 3 pontos
⇒ coordenadas do ponto que corresponde ao instante em que a bola atingiu o solo …………….. 3 pontos
Notas:1. Se o aluno não indicar corretamente as grandezas representadas, esta etapa não é considerada para efeito de classificação.
2. Se o aluno apresentar um gráfico que não corresponda ao intervalo de tempo considerado, ou se apresentar um gráfico no qual esse intervalo de tempo não se encontre definido, a pontuação a atribuir nesta etapa deverá ser desvalorizada em dois pontos.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
- 11ºano – Física – A.l. – 1.1 – Queda livre força gravítica
1.2 Que distância percorreu a bola desde o instante em que foi abandonada até ao instante t = 0,30 s?
(A) 0,85 m
(B) 0,75 m
(C) 0,65 m
(D) 0,45 m
- Opção (D)
⇒ A distância percorrida até t = 0,30 s é d = |y – 0,20|
- d = 5,0 x 0,302 = 0,45 m
- Opção (D)…………. 8 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
- 11ºano – Física – A.l. – 1.1 – Queda livre força gravítica
1.3 Explique porque é que se pode admitir que a força de resistência do ar não influenciou o movimento de queda da bola.
⇒ Comparando a equação do movimento da bola, y = 0,20 + 5,0 t2, com a equação y = y0 + ½ a t2, constata-se que a aceleração de queda é de 10 m s-2, pois ½ a = 5,0 m s– 2, igual ao módulo da aceleração gravítica, g, de um corpo junto à superfície terrestre (ver Tabela de Constantes).
⇒ De acordo com a 2.ª Lei de Newton, Fr = m a , o valor da aceleração adquirida por um corpo é diretamente proporcional à intensidade da resultante das forças que sobre ele atuam.
⇒ Como a = g e considerando-se que sobre a bola apenas atuam a força gravítica, Fg = m g, e a resistência do ar, conclui-se que esta força não influenciou o movimento de queda da bola, pois a força resultante é igual à gravítica.
- Na resposta, são apresentados os seguintes tópicos:
A) [De acordo com a equação do movimento,] a bola caiu com uma aceleração de módulo 10 ms-2, que corresponde ao módulo da aceleração gravítica [de um corpo junto à superfície da Terra].
B) Considerando [ainda] que as únicas forças que atuam na bola [durante o seu movimento de queda no ar] são a força gravítica e a força de resistência do ar, a resultante das forças que atuam na bola pode [assim] ser identificada com a força gravítica, pelo que se poderá admitir que a força de resistência do ar não influenciou o movimento de queda da bola.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Física – subdomínio 1 (Energia e movimentos)
- 10ºano – Física – A.l. – 1.2 – Movimento vertical de queda e ressalto de uma bola
2. Considere que a bola, chegando ao solo com velocidade de módulo v, ressalta, dissipando 20% da sua energia mecânica.
Após o ressalto, a bola inicia a subida com velocidade de módulo

- Opção (D)
⇒ Energia antes do ressalto = Eantes = ½ m v2
⇒ Energia após o ressalto = Eapós = ½ m v2após
⇒ Como a energia dissipada durante a colisão com o solo é de 20%, então a energia após o ressalto é igual a 80% da energia com que a bola atinge o solo.
- Eapós = 0,80 Eantes ⇔ ½ m v2após ⇔ v2após = 0,80 v2 ⇔ vapós = √0,80 v
- Opção (D)…………. 8 pontos
GRUPO III
Uma bola, de massa 57,0 g, foi atada a uma corda e posta a rodar, num mesmo plano horizontal, descrevendo circunferências de raio 0,30 m, com velocidade de módulo constante.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1. Considere o trabalho realizado pela força gravítica que atua na bola, WFg .
Quando a bola descreve metade de uma circunferência, a energia potencial gravítica do sistema bola + Terra
(A) não se mantém constante e WFg = 0
(B) não se mantém constante e WFg ≠ 0
(C) mantém-se constante e WFg = 0
(D) mantém-se constante e WFg ≠ 0
- Opção (C)
⇒ A energia potencial gravítica do sistema bola + Terra (Ep = m g h) mantém-se constante, pois a bola roda num mesmo plano horizontal, logo a altura a que se encontra do solo é constante.
⇒ O trabalho realizado pela força gravítica, WFg, é nulo, pois a força gravítica é em cada instante perpendicular à trajetória.
- Opção (C)…………. 8 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2. Admita que a bola descreve cada uma das circunferências em 1,0 s.
Determine a intensidade da resultante das forças que atuam na bola.
Apresente todas as etapas de resolução.
m = 57,0 g = 57,0 x 10-3 kg;
R = 0,30 m; T = 1,0 s
- FR = ?
⇒ Como a bola descreve uma circunferência com velocidade de módulo constante, conclui-se que está animada de movimento circular uniforme, sendo a resultante das forças igual à força centrípeta.
- FR = m ac
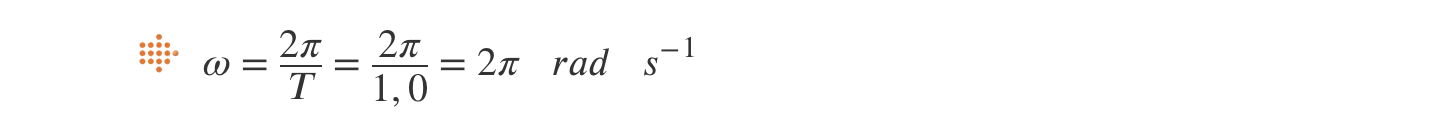
⇒ ac = w2 R = (2 π)2 x 0,30 = 11,8 m s-2
- FR = 57,0 x 10-3 x 11,8 = 0,67 N
⇒ A intensidade da resultante das forças que atuam sobre a bola é igual a 0,67 N.
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo do módulo da velocidade da bola (v = 1,88 m s-1)
ou
- Cálculo do módulo da velocidade angular da bola (ω = 6,28 rad s-1).
B) Cálculo do módulo da aceleração da bola (a = 11,8 m s-2).
C) Cálculo da intensidade da resultante das forças que atuam na bola (F = 0,67 N).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
GRUPO IV
O amoníaco obtém-se industrialmente através do processo de Haber-Bosch, fazendo reagir, em condições apropriadas, hidrogénio e nitrogénio gasosos.
A reação de síntese do amoníaco pode ser traduzida por
3 H2 (g) + N2 (g) ⇋ 2 NH3 (g)
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
1. Fazendo reagir 6 moles de H2 (g) com 3 moles de N2 (g), seria possível obter
(A) 4 moles de NH3(g), sendo o N2(g) o reagente limitante.
(B) 4 moles de NH3(g), sendo o H2(g) o reagente limitante.
(C) 6 moles de NH3(g), sendo o N2(g) o reagente limitante.
(D) 6 moles de NH3(g), sendo o H2(g) o reagente limitante.
- Opção (B)
⇒ A equação química apresentada mostra que 3 moles de H2 (g) reagem com 1 mole de N2 (g), ou seja, a proporção estequiométrica entre os reagentes é de 3:1.
⇒ Assim, para reagirem 3 moles de N2 (g) necessitariam de 9 moles de H2 (g); como só se fizeram reagir 6 moles de H2 (g), este reagente está em defeito, e por isso é o reagente limitante.
Notar que, como:
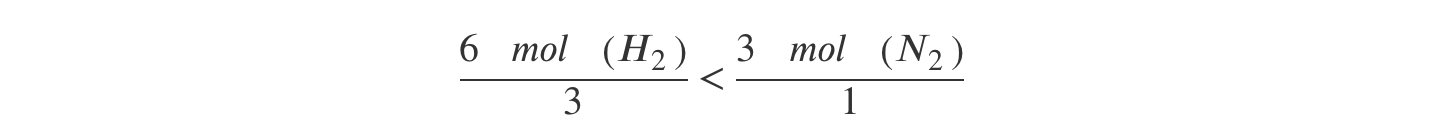
- H2 é o reagente limitante
⇒ Se o rendimento da reação fosse de 100%, e de acordo com a estequiometria da reação, (a proporção estequiométrica entre o H2 (g) e o NH3 (g) é de 3:2 a partir de 6 moles de H2 (g) seria possível obter 4 moles de NH3 (g), o que está de acordo com a opção (B).
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
2. Considere que a variação de energia associada à formação de 2 moles de amoníaco, a partir da reação acima indicada, é – 92 kJ.
A formação de 12 moles de amoníaco, a partir da mesma reação, envolverá
(A) a libertação de (6 × 92) kJ.
(B) a absorção de (6 × 92) kJ.
(C) a libertação de (12 × 92) kJ.
(D) a absorção de (12 × 92) kJ.
- Opção (A)
⇒ A variação de energia associada à formação de amoníaco segundo a reação apresentada é negativa, o que significa que esta reação é exoenergética (dizendo-se exotérmica se liberta energia como calor).
⇒ Se, para formar 2 moles de amoníaco se libertam 92 kJ, a formação de 12 moles de amoníaco envolverá a libertação de
- (12/2) x 92 kJ = 6 x 92 kJ
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
3. O amoníaco é um gás à pressão e à temperatura ambientes.
Considere que a densidade do NH3(g) nas condições normais de pressão e de temperatura é 1,08 vezes maior do que a densidade desse gás à pressão e à temperatura ambientes.
Determine o número de moléculas de amoníaco que existem numa amostra pura de 200cm3 de NH3(g), à pressão e à temperatura ambientes.
Apresente todas as etapas de resolução.
⇒ ρ(NH3)PTN = 1,08 x ρ(NH3)P e T ambiente
⇒ V(NH3)P e T ambiente = 200 cm3
⇒ N(NH3)P e T ambiente = ?
⇒ (Vm)PTN = 22,4 dm3 mol-1
⇒ NA = 6,02 x 1023 mol-1
⇒ Cálculo do volume molar (Vm) do gás à pressão e temperatura ambiente:
Como
- ρ(NH3)PTN = 1,08 x ρ(NH3)P e T ambiente vem:
Assim, (Vm)P e T ambiente = 1,08 x 22,4 = 24,2 dm3 mol-1
⇒ Cálculo do número de moléculas (N) de amoníaco existentes na amostra, a pressão e temperatura ambiente:
- Como n = V/Vm, a quantidade de gás (n) existente na amostra nestas condições de pressão e temperatura é:
⇒ O número de moléculas de amoníaco correspondente a 8,26 x 10-3 mol deste gás é:
- N(NH3) = n x NA = 8,26 x 10-3 x 6,02 x 1023 = 4,98 x 1021 moléculas.
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo do volume molar do gás, à pressão e à temperatura ambientes (Vm = 24,19 dm3 mol-1).
B) Cálculo do número de moléculas de amoníaco que existem na amostra, à pressão e à temperatura ambientes (N = 4,98 x 1021).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
GRUPO V
O amoníaco é uma base fraca, cuja reação de ionização em água pode ser traduzida por
NH3 (aq) + H2O (l) ⇋ NH+4 (aq) + OH–(aq)
1. As soluções aquosas de amoníaco habitualmente utilizadas em laboratório são preparadas por diluição de soluções aquosas comerciais, muito concentradas.
Considere uma solução aquosa comercial de amoníaco, de concentração 13 mol dm-3 e de densidade 0,91 g cm-3, que é posteriormente diluída 500 vezes.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.1 Qual das expressões seguintes permite calcular a percentagem, em massa, de amoníaco (M = 17,04 g mol-1) na solução comercial?
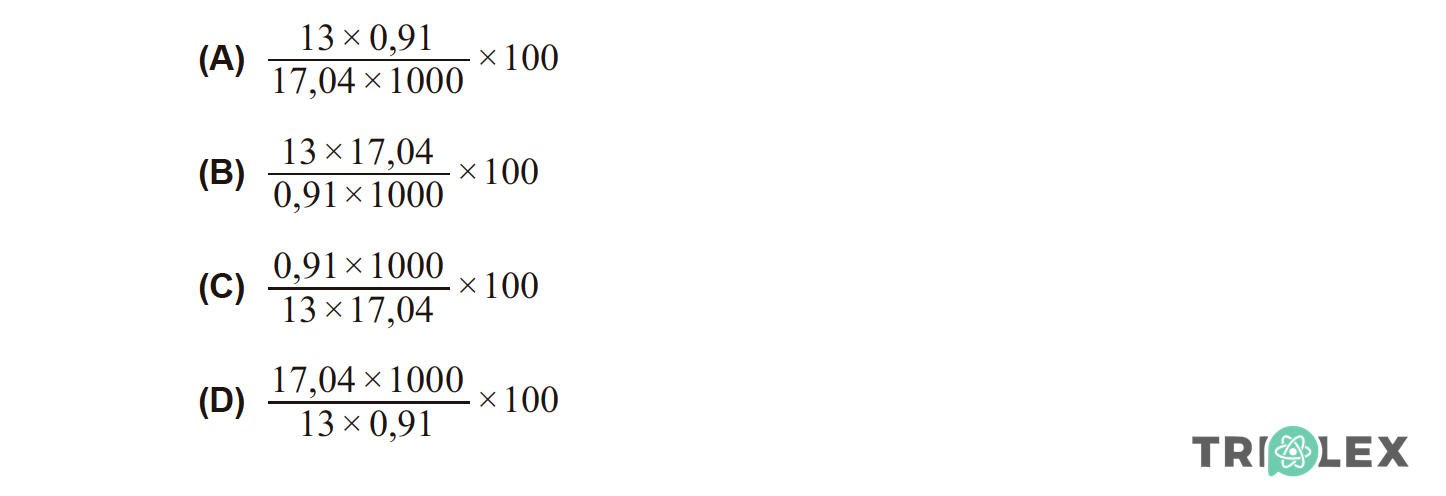
- Opção (B)
c(NH3 (aq))comercial = 13 mol dm-3
ρ(NH3 (aq))comercial = 0,91 g cm-3
M(NH3) = 17,04 g mol-1
⇒ c(NH3 (aq))comercial = 13 mol dm-3 significa que em 1,000 dm3 de solução existem 13 moles de NH3.
⇒ Como m = n x M, a massa de soluto existente em 1,000 dm3 de solução é: m = 13 x 17,04 g.
Como

⇒ a massa de solução existente em 1,000 dm3 de solução é:
- msolução = ρsolução x Vsolução ⇔ msolução = 0,91 x 1000 g
⇒ Considerando 1,000 dm3 de solução, e de acordo com a expressão que define a %(m/m) de uma solução:
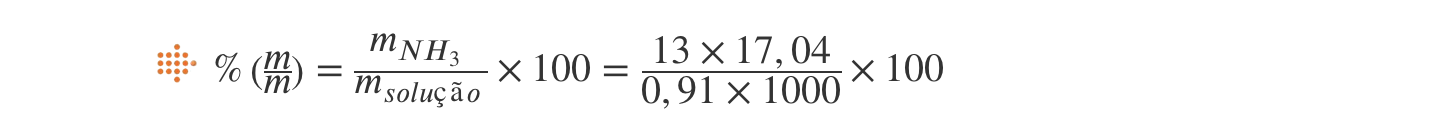
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.2 Para preparar 1,0 dm3 da solução de amoníaco mais diluída, o volume a utilizar da solução comercial será
(A) 500,0 cm3
(B) 200,0 cm3
(C) 5,0 cm3
(D) 2,0 cm3
- Opção (D)…………. 8 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1.3 A solução de amoníaco, obtida por diluição da solução comercial, tem um pH de 10,83, a 25 ºC.
Determine a concentração de amoníaco não ionizado na solução mais diluída.
Apresente todas as etapas de resolução.
- pH (solução diluída de NH3) = 10,83, a 25 °C
⇒ Cálculo da concentração da solução de amoníaco mais diluída:
Como o fator de diluição é igual a 500
⇒ Cálculo da concentração de amoníaco ionizado na solução mais diluída:
Equação química que traduz a reação de ionização parcial do NH3 (aq):
NH3 (aq) + H2O (l) ⇋ NH+4 (aq) + HO– (aq)
Como, a 25 °C, pH + pOH = 14, temos: pOH = 14 – 10,83 = 3,17
⇒ De acordo com a definição de pOH, pOH = – log [HO–], obtém-se a seguinte concentração do ião hidróxido:
⇒ [HO–(aq)] = 10 – 3,17 = 6,8 x 10-4 mol dm-3
⇒ Cálculo da concentração de amoníaco não ionizado na solução mais diluída:
De acordo com a estequiometria da reação de ionização do NH3(aq), a concentração de amoníaco não ionizado é:
⇒ [NH3]não ionizado = (2,60 – 0,068) x 10-2 = 2,53 x 10-2 mol dm-3
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo da concentração da solução de amoníaco, obtida por diluição da solução comercial (c = 2,60 x 10-2 mol dm-3).
B) Cálculo da concentração de amoníaco ionizado na solução mais diluída (c = 6,761 x 10-4 mol dm-3).
C) Cálculo da concentração de amoníaco não ionizado na solução mais diluída (c = 2,5 x 10-2 mol dm-3).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2. Escreva a equação química que traduz a reação do ião NH4+(aq) com a água.
Identifique, nessa reação, os pares conjugados ácido-base.
NH+4 (aq) + HO– (aq) ⇋ NH3 (aq) + H2O (l)
⇒ Pares conjugados ácido-base: NH+4 / NH3 e H3O+ / H2OGRUPO VI
Os testes laboratoriais de identificação do amoníaco, realizados em amostras padrão, permitem, posteriormente, concluir sobre a presença (ou a ausência) daquele composto em materiais de uso comum, como, por exemplo, produtos comerciais de limpeza.
1. O que são, no contexto em causa, amostras padrão?
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Amostras padrão são amostras em relação às quais existe a certeza da presença ou ausência de uma determinada espécie química, neste caso, o amoníaco.
⇒ A partir das observações verificadas numa amostra padrão, pode concluir-se a existência ou ausência de amoníaco em soluções-problema.
- Amostras relativamente às quais existe certeza sobre a presença [ou a ausência] de amoníaco. ……………. 8 pontos
2. Um dos testes de identificação do amoníaco consiste em aproximar uma vareta de vidro, previamente mergulhada em ácido clorídrico concentrado, da boca de um tubo de ensaio contendo a solução aquosa a analisar.
A presença de amoníaco é indicada pela formação de fumos brancos de cloreto de amónio, NH4Cl.
Escreva a equação química que traduz a reação que ocorre se a solução a analisar contiver amoníaco.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- NH3 (g) + HCl (g) → NH4Cl (s)
- NH3 (g) + HCl (g) → NH4Cl (s) …………….. 8 pontos
Nota – A omissão ou incorreção na indicação do estado físico de qualquer uma das substâncias intervenientes na reação não implica qualquer penalização.
3. Outro teste de identificação do amoníaco consiste em juntar, gota a gota, a solução aquosa a analisar a uma solução de sulfato de cobre (II), CuSO4 (aq), adicionando-se, posteriormente, excesso da solução a analisar.
Se a solução a analisar contiver amoníaco, as reações químicas que ocorrem, envolvidas no teste de identificação descrito, podem ser traduzidas por
Cu2+(aq) + 2 OH–(aq) ⇋ Cu(OH)2(s)
Cu(OH)2(s) + 4 NH3(aq) → [Cu (NH3)4]2+(aq) + 2 OH–(aq)
Interprete as reações químicas envolvidas no teste de identificação.
Comece por referir a principal fonte de iões OH–(aq) na solução a analisar, se esta contiver amoníaco.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Se a solução aquosa a analisar contiver amoníaco, esta partícula comporta-se como base, sofrendo ionização parcial na presença da água.
Esta reação, traduzida pela equação:
- NH3 (aq) + H2O (l) ⇋ NH+4 (aq) + HO– (aq)
é a principal fonte de iões HO– (aq) na solução a analisar.
⇒ Juntando, gota a gota, a solução a analisar que contém amoníaco a uma solução aquosa de sulfato de cobre, que contém iões Cu2+(aq) resultantes da dissociação completa do CuSO4 (aq), de acordo com a equação:
- CuSO4 (aq) → Cu2+ (aq) + SO42- (aq)
forma-se um precipitado azul-claro de Cu(OH)2.
⇒ A equação de precipitação ocorrida é traduzida pela equação:
- Cu2+ (aq) + 2 HO– (aq) → Cu(HO)2 (s)
⇒ A adição de solução aquosa de amoníaco em excesso, provoca a dissolução do precipitado Cu(HO)2 (s), obtendo-se uma solução límpida, azul-forte, devida à formação do ião complexo tetraaminocobre (II), [Cu(NH3)4]2+ (aq), de acordo com a equação:
Cu(HO)2 (s) + 4 NH3 (aq) → [Cu(NH3)4]2+ (aq) + 2 HO– (aq)
- Na resposta, são apresentados os seguintes tópicos:
A) [Se a solução a analisar contiver amoníaco,] a principal fonte de iões OH-(aq) é a ionização parcial do amoníaco em água.
ou
[Se a solução a analisar contiver amoníaco,] a principal fonte de iões OH– (aq) é a reação do amoníaco com a água.
B) Juntando [gota a gota] a solução a analisar a uma solução contendo iões Cu2+ (aq), formar-se-á [inicialmente] um precipitado de [hidróxido de cobre (II),] Cu(OH)2.
C) [Se a solução a analisar contiver amoníaco,] a adição de excesso da solução provoca a dissolução do precipitado de Cu(OH)2, formando-se o ião [Cu(NH3)4]2+ (aq).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

FIM