2011 – Teste Intermédio – 10ºAno – março
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 10ºAno – 2011
- Duração do Teste: 90 minutos | 03.03.2011
Grupo I
O carbono tem vários isótopos naturais, que existem em abundâncias relativas muito diferentes, sendo identificados de acordo com o seu número de massa.
Existem dois isótopos estáveis, o carbono-12 (12C) e o carbono-13 (13C), e um isótopo instável, radioativo, o carbono-14 (14C).
- 10ºano – Química – Domínio 1 – subdomínio 1 (Massa e tamanho dos átomos)
1. Quantos neutrões existem no núcleo de um átomo de carbono-13?
- 7 neutrões.
⇒ Como o número de massa é 13 e o número atómico é 6, o número de neutrões é igual a 13 – 6 = 7.
- Sete (7) neutrões …………. 8 pontos
2. Qual deve ser o valor de X para que a equação seguinte traduza uma reação nuclear em que ocorre a formação de carbono-12?
84Be + X2He → 126C
(A) 4
(B) 6
(C) 8
(D) 12
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (A)
⇒ X = 4
⇒ Como a soma dos números de massa das partículas reagentes é igual à soma dos números de massa das partículas dos produtos, vem:
- 8 + X= 12 ⇔ X= 4.
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3. No átomo de carbono no estado fundamental, os eletrões encontram-se distribuídos por
(A) duas orbitais.
(B) três orbitais.
(C) quatro orbitais.
(D) seis orbitais.
- Opção (C)
⇒ Os eletrões estão distribuídos pelas orbitais:
- 1s, 2s, 2px e 2py
ou
- 1s, 2s, 2pz e 2py
ou
- 1s, 2s, 2pz e 2px
- Opção (C)…………. 8 pontos
4. Um dos eletrões de valência do átomo de carbono no estado fundamental pode ser caracterizado pelo conjunto de números quânticos
(A) ( 1 , 1 , 0 , +½)
(B) ( 2 , 0 , 0 , +½)
(C) ( 2 , 1 , 2 , -½)
(D) ( 1 , 0 , 0 , -½)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B)
⇒ É um eletrão 2s (n = 2, l = 0, m = 0 e s = +½ ).
⇒ Os conjuntos de números quânticos representados por (A) e (C) são impossíveis e o conjunto representado por (D) refere-se a um eletrão 1s, que pertence ao cerne do átomo de C.
- Opção (B)…………. 8 pontos
Grupo II
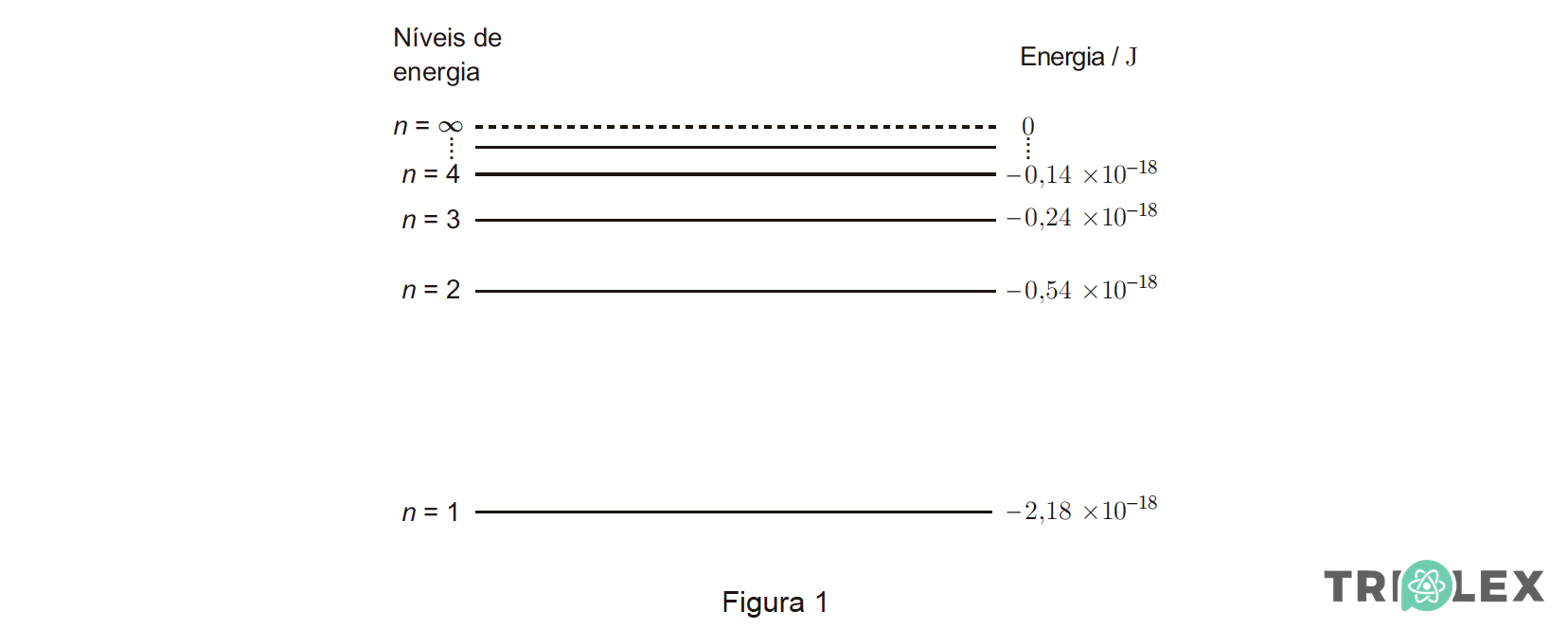
A Figura 1 representa um diagrama de níveis de energia do átomo de hidrogénio.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
1. No átomo de hidrogénio, a variação de energia associada à transição do eletrão do nível 2 para o nível 1 pode ser traduzida pela expressão
(A) (-2,18 × 10-18 + 0,54 × 10-18 ) J
(B) (-2,18 × 10-18 – 0,54 × 10-18 ) J
(C) (0,54 × 10-18 + 2,18 × 10-18 ) J
(D) (-0,54 × 10-18 + 2,18 × 10-18 ) J
- Opção (A)
⇒ ΔE = E1 – E2 = [- 2,18 x 10-18 – (- 0,54 x 10-18 )] J = (- 2,18 x 10-18 + 0,54 x 10-18) J
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
2. No átomo de hidrogénio, qualquer transição do eletrão para o nível 1 envolve
(A) emissão de radiação visível.
(B) absorção de radiação visível.
(C) emissão de radiação ultravioleta.
(D) absorção de radiação ultravioleta.
- Opção (C)
⇒ No átomo de hidrogénio, as transições para o nível 1 estão associadas a emissões de radiações UV.
⇒ As riscas espetrais correspondentes formam a chamada série de Lyman.
- Opção (C)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3. De que tipo é o espectro de emissão do átomo de hidrogénio na região do visível?
⇒ É um espetro de emissão de riscas.
⇒ Os átomos de hidrogénio só emitem certas radiações de energias bem definidas, porque a energia dos eletrões nos átomos está quantificada.
- Espectro de riscas.
OU
- Espectro descontínuo. —————————– 8 pontos
Grupo III
O dióxido de carbono, CO2 , desempenha um papel importante na regulação da temperatura superficial da Terra.
O teor médio de CO2 na troposfera tem aumentado de forma continuada nos últimos 150 anos, apresentando atualmente um valor de cerca de 3,9 x 10-2 %, em volume.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1. O teor de CO2 na troposfera, expresso em partes por milhão, em volume (ppmV), pode ser determinada a partir da expressão

- Opção (B)
⇒ Por definição:
- % V/V = VCO2/Var x 100
- ppmV = VCO2/Var x 106
⇒ Comparando as duas definições, vem:
- ppmV= % V/V x 104
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2. Refira dois fatores, de natureza antropogénica, que possam justificar o aumento do teor médio de CO2 na troposfera.
⇒ Uso de combustíveis fósseis e incêndios florestais provocados pelo Homem.
A resposta deve apresentar dois dos seguintes tópicos:
A) Aumento da queima dos combustíveis fósseis.
OU
Outro fator relacionado (aumento da circulação automóvel, etc.).
B) Aumento da desflorestação.
OU
Outro fator relacionado (aumento da limpeza e da queima de terrenos florestais, etc.).
C) Atividade das indústrias transformadoras.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
3. Calcule o número de moléculas de CO2 que existem numa amostra de 10,0 dm3 de ar troposférico, em condições PTN.
Apresente todas as etapas de resolução.⇒ Como o teor médio de CO2 na troposfera apresenta atualmente um valor de:
- 3,9 x 10-2 % em 10 dm3 de ar teremos:
⇒ Sendo o volume molar igual a 22,4 dm3 mol-1 (NA), a quantidade (n) de CO2 e o número de moléculas por mol igual a 6,022 x 1023, que existe nesta amostra de ar será:

⇒ Número de moléculas (N) é:
- N = n x NA ⇔ N = (1,74 x 10-4 mol) x (6,022 x 1023 mol-1) = 1,0 x 1020 moléculas
A resolução deve apresentar as seguintes etapas:
A) Determinação do volume de CO2 na amostra de ar troposférico (V = 3,90 x 10-3 dm3).
B) Determinação da quantidade de CO2 que existe na amostra de ar troposférico, em condições PTN (n = 1,74 x 10-4 mol).
C) Determinação do número de moléculas de CO2 que existem na referida amostra (N = 1,0 x 1020 moléculas).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
4. Qual é a percentagem, em massa, de carbono em 1 mole de moléculas de CO2?
- 27,29 % —————————– 8 pontos
Nota – O resultado pode ser apresentado com um n mero diferente de algarismos significativos.
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
5. Selecione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correta.
O carbono e o oxigénio são elementos que pertencem ao mesmo _______ da Tabela Periódica, sendo a energia de ionização do carbono ________ à energia de ionização do oxigénio.
(A) período … superior
(B) grupo … superior
(C) período … inferior
(D) grupo … inferior
- Opção (C)
⇒ De acordo com as configurações eletrónicas do carbono e oxigénio,
- C – 1s2 2s2 2p2
- O – 1s2 2s2 2p4
⇒ Verifica-se que o número quântico principal máximo é 2 para os dois elementos, logo pertencem ao mesmo período.
⇒ O número de eletrões de valência do carbono é 4 e o número de eletrões de valência do oxigénio é 6, pelo que pertencem aos grupos 14 e 16, respetivamente.
⇒ Como a energia de ionização aumenta ao longo do período, a energia de ionização de carbono é inferior à do oxigénio.
- Opção (C)…………. 8 pontos
Grupo IV
A atmosfera da Terra é constituída por sucessivas camadas gasosas, que apresentam diferentes propriedades físicas e químicas.
1. Na Figura 2 apresenta-se o gráfico que relaciona a temperatura da atmosfera com a altitude, até cerca de 80 km.
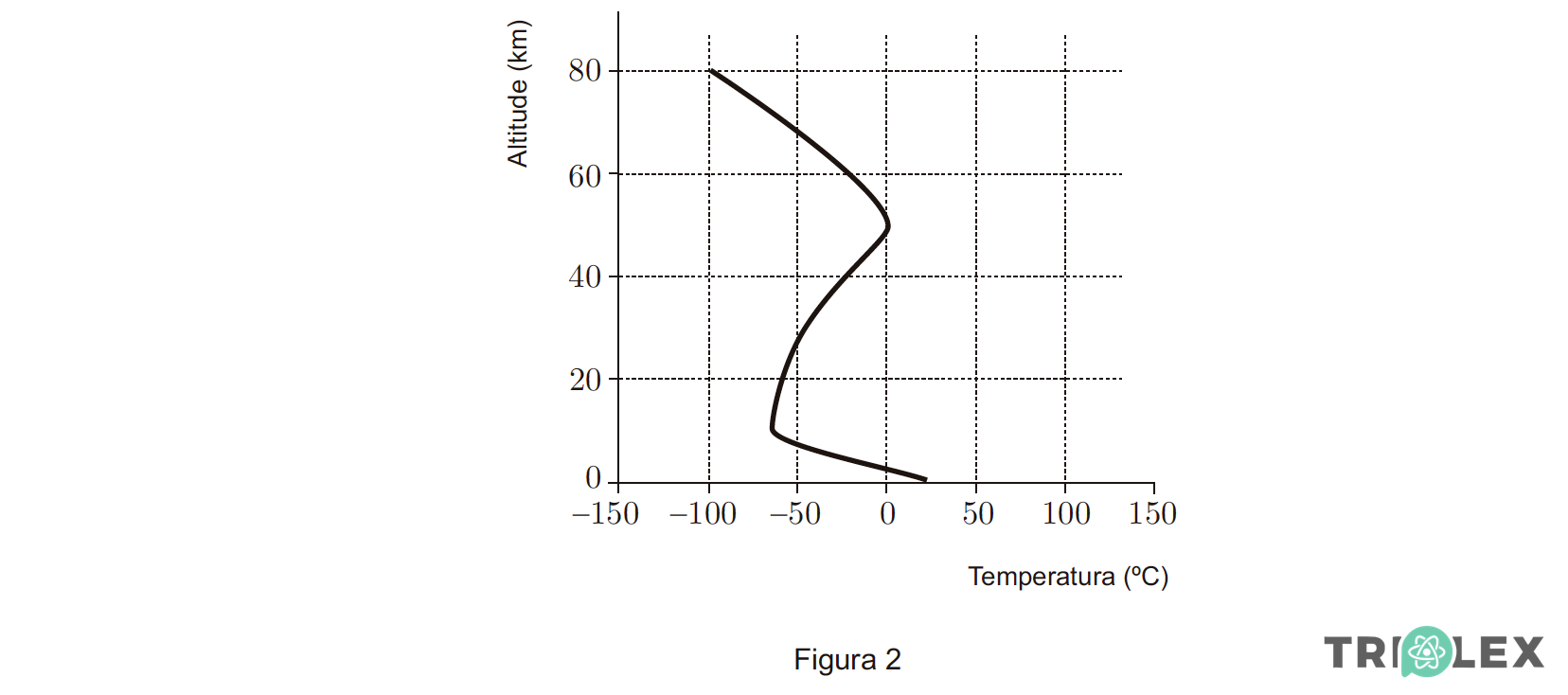
1.1. Qual é o valor aproximado da temperatura atmosférica a uma altitude de 10 km?
(A) 0 ºC
(B) – 20 ºC
(C) – 60 ºC
(D) – 90 ºC
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
⇒ De acordo com o gráfico, a temperatura atmosférica para a altitude de 10 km terá de estar compreendida entre – 100 ºC e – 50 ºC.
- Opção (C)…………. 8 pontos
1.2. Indique, justificando com base no gráfico, quantas camadas existem na atmosfera, desde a superfície da Terra até a uma altitude de cerca de 80 km.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Três camadas, porque a curva apresenta duas inflexões de temperatura (duas zonas de transição entre as três camadas distintas, baseadas no modo como varia a temperatura da atmosfera com a altitude).
A resposta deve apresentar dois dos seguintes tópicos:
A) Existem três camadas na atmosfera, desde a superfície da Terra até a uma altitude de cerca de 80km.
B) A curva representada no gráfico apresenta três zonas distintas de dependência da temperatura em relação à altitude OU equivalente.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2. A diminuição da concentração de ozono (O3) na estratosfera está relacionada, entre outros fatores, com reações que envolvem os CFC.
Qual das seguintes fórmulas de estrutura representa um CFC?

- Opção (D)
⇒ Se se considerar CFC qualquer composto com carbono, cloro e flúor.
⇒ Neste caso, poderia ser denominado HCFC.
- Opção (D)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
3. Comparando as ligações C – C e C ≡ C, a ligação C ≡ C apresenta
(A) maior energia de ligação e menor comprimento de ligação.
(B) menor energia de ligação e menor comprimento de ligação.
(C) maior energia de ligação e maior comprimento de ligação.
(D) menor energia de ligação e maior comprimento de ligação.
- Opção (A)
⇒ A ligação tripla é mais forte e mais curta que a ligação simples.
- Opção (A)…………. 8 pontos
Grupo V
1. No laboratório, um aluno preparou, com rigor, uma solução aquosa de cloreto de sódio, a partir do reagente sólido.
- 11ºano – Física – A.l. – Medições
- 10ºano – Química – A.l. – 2.2 – Soluções a partir de solutos sólidos
1.1. Para preparar a solução, o aluno mediu a massa necessária de cloreto de sódio, utilizando uma balança digital que apresentava uma incerteza de leitura de 0,01 g.
Dos seguintes valores de massa, qual deve o aluno ter registado?
(A) 8,341 g
(B) 8,34 g
(C) 8,3 g
(D) 8 g
- Opção (B)
⇒ Como a incerteza da balança digital é de 0,01 g, este valor é o menor valor lido no aparelho, logo, a leitura deve ser feita até à centésima do g.
⇒ Assim, o algarismo 4 (duvidoso) deve ser o último registado. Os seguintes não têm qualquer significado.
- Opção (B)…………. 8 pontos
- 11ºano – Física – A.l. – Medições
- 10ºano – Química – A.l. – 2.2 – Soluções a partir de solutos sólidos
1.2. O volume de solução preparada foi 250,0 cm3.
Apresente o valor acima referido expresso em dm3 , mantendo o número de algarismos significativos.
⇒ 250,0 cm3 = 0,2500 dm3 = 2,500 x 10-1 dm3
- 0,2500 dm3 Ou 2,500 x 10-1 dm3 —————————– 8 pontos
2. Em seguida, foi pedido ao aluno que preparasse, com rigor, 50,0 cm3 de uma solução aquosa de cloreto de sódio de concentração 0,23 mol dm-3, a partir da solução inicialmente preparada de concentração 5,71 × 10-1 mol dm-3.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
- 10ºano – Química – A.l. – 2.3 – Diluição de soluções
2.1. Calcule o volume de solução inicial necessário para preparar o volume referido de solução diluída de cloreto de sódio.
Apresente todas as etapas de resolução.
⇒ Solução diluída:
- cd = 0,23 mol dm-3
- Vd = 50,0 cm3
Numa diluição, a quantidade, n, de soluto, NaCl, mantém-se.
⇒ Assim, a quantidade de NaCl necessária para a preparação da solução diluída é:
- nd = cd x Vd = 50,0 x 0,23 x 10-3 mol = 1,15 x 10-2 mol
⇒ Solução concentrada:
- cc = 5,71 x 10-1 mol = 1,15 x 10-2 mol dm-3
⇒ Devemos diluir a 50,0 cm3 um volume V desta solução que contenha 1,15 x 10-2 mol de NaCl:
- Vc x (5,71 x 10-1 mol dm-3) = 1,15 x 10-2 mol

A resolução deve apresentar as seguintes etapas:
A) Determinação da quantidade de cloreto de sódio necessária à preparação da solução diluída (n = 1,15 x 10-2 mol).
B) Determinação do volume de solução inicial de cloreto de sódio que contém aquela quantidade (V = 20 cm3).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
- 10ºano – Química – A.l. – 2.3 – Diluição de soluções
2.2. Descreva o procedimento experimental seguido na preparação da solução diluída de cloreto de sódio, referindo, sequencialmente, as três principais etapas envolvidas nesse procedimento.
⇒ Com pipeta volumétrica transferia 20 cm3 de solução de NaCl de concentração 5,71 x 10-1 mol dm-3 para um balão volumétrico de 50,0 cm3 e adicionava seguidamente água destilada completando o volume até ao traço de referência (leitura pelo menisco inferior, evitando erros de paralaxe).
A resposta deve apresentar dois dos seguintes tópicos:
A) A primeira etapa é a medição do volume (OU de 20 cm3) de solução inicial de cloreto de sódio, utilizando uma pipeta (graduada ou volumétrica).
B) A segunda etapa é a transferência desse volume de solução para um balão volumétrico de 50,0 mL.
C) A terceira etapa é perfazer o volume de 50,0 cm3 com água destilada (adicionando água destilada até ao traço de referência do balão volumétrico).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

Grupo VI
Numa aula laboratorial, determinou-se a densidade relativa de uma solução aquosa de cloreto de sódio, pelo método do picnómetro.
A primeira operação efetuada foi a medição da massa do picnómetro vazio. Em seguida, mediu-se a massa do picnómetro cheio com água e a massa do picnómetro cheio com a solução aquosa de cloreto de sódio.
Estas pesagens foram realizadas à temperatura de 20 ºC. Os valores obtidos estão registados na tabela seguinte.
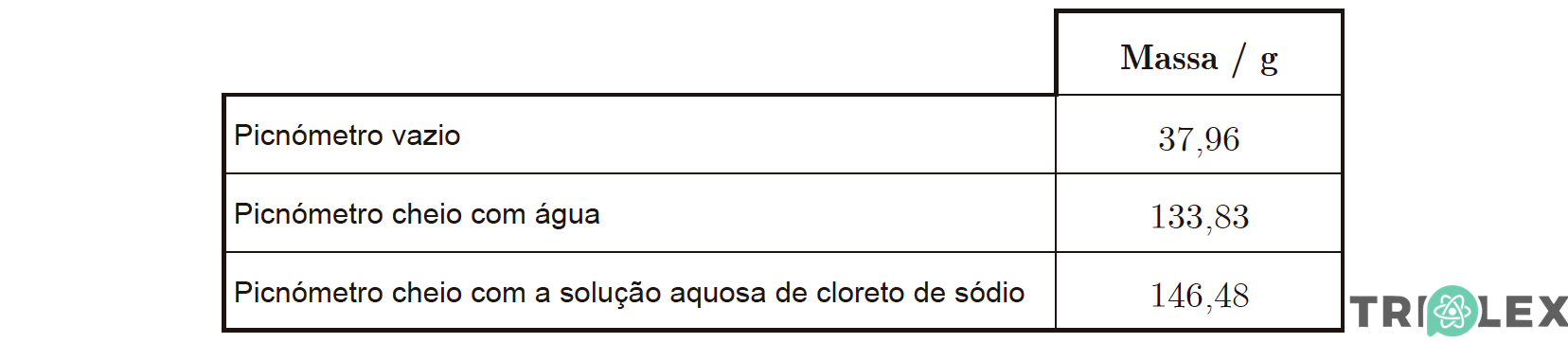
Calcule a densidade relativa da solução aquosa de cloreto de sódio.
Apresente todas as etapas de resolução.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
A resolução deve apresentar as seguintes etapas:
A) Determinação da massa de água (95,87 g) e da massa da solução aquosa de cloreto de sódio (108,52 g).
B) Determinação da densidade relativa da solução aquosa de cloreto de sódio (d = 1,132).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
FIM


