2007 – 1ª Fase – Prova Escrita de Física e Química A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: 1.ª Fase – 2007
Os cientistas não têm dúvidas: o Sol morrerá. Mas podemos estar descansados só daqui a cerca de cinco mil milhões de anos é que a nossa estrela se transformará numa imensa nebulosa planetária. Antes disso, irá expandir-se, com diminuição da temperatura da sua parte mais superficial, dando origem a uma gigante vermelha. Neste processo, a temperatura no interior da estrela aumentará de tal modo que permitirá que, a partir da fusão nuclear de átomos de hélio, se produza carbono e oxigénio. No final das suas vidas, as estrelas gigantes vermelhas tornam-se instáveis e ejectam as suas camadas exteriores de gás, formando então as chamadas nebulosas planetárias.
Visão, n.º 729, 2006, p.81 (adaptado)
1.1. Explique em que consiste uma reacção de fusão nuclear como a que é referida no texto.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Uma reacção de fusão nuclear tem lugar entre núcleos atómicos de massa pequena, dando origem a um núcleo atómico de massa maior.
⇒ No processo de fusão há libertação de energia. São as reacções de fusão nuclear que ocorrem no Sol que estão na origem da energia emitida por esta estrela.
Nota: o processo de fusão nuclear é dificultado pelo facto de os núcleos terem carga eléctrica positiva.
Contudo, se houver energia suficiente para vencer a repulsão eléctrica e os núcleos se aproximarem suficientemente um do outro, entra em jogo a força nuclear forte que é muito atractiva e que é, afinal, a responsável pela fusão dos núcleos.
⇒ Nível 2 – Reacção em que pequenos núcleos atómicos se fundem, para produzir núcleos atómicos de maior massa, com elevada libertação de energia. …….. 10 pontos
⇒ Nível 1 – Refere apenas dois dos elementos de resposta, apresentados no nível anterior. ……… 5 pontos
1.2. A cor de uma estrela indica-nos a sua temperatura superficial, existindo uma relação de proporcionalidade inversa entre a temperatura de um corpo e o comprimento de onda para o qual esse corpo emite radiação de máxima intensidade.
Seleccione a opção que contém os termos que devem substituir as letras (a), (b) e (c), respectivamente, de modo a tornar verdadeira a afirmação seguinte. Se, no espectro contínuo de uma estrela predominar a cor __ (a) __ e, no espectro de uma outra estrela predominar a cor __(b)__, então a primeira terá uma __(c)__ temperatura superficial.
(A) … vermelha… azul… maior…
(B) … amarela… vermelha… menor…
(C) … azul… vermelha… maior…
(D) … violeta… vermelha… menor…
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
⇒ A cor da luz emitida por uma estrela depende da sua temperatura superficial.
⇒ Quanto mais elevada for a temperatura da estrela, menor é o comprimento de onda da radiação emitida.
⇒ Como a radiação azul tem menor comprimento de onda do que a radiação vermelha, a temperatura superficial da estrela que emite radiação azul é maior que a da que emite radiação vermelha.
- Opção (C)…………. 8 pontos
2. A Terra possui uma atmosfera que é maioritariamente constituída por uma solução gasosa com vários componentes, como o dióxido de carbono e o vapor de água, que, embora não sendo predominantes, são cruciais para a existência de vida na Terra.
No entanto, o aumento exagerado do teor de CO2 atmosférico, a destruição da camada de ozono e a qualidade da água que circula na atmosfera e cai sobre a superfície terrestre são problemas graves, interligados e resultantes, principalmente, da actividade humana.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2.1. O dióxido de carbono, CO2 ( M = 44,0 g mol-1), é o componente minoritário de maior concentração no ar atmosférico.
Considere V o volume de uma amostra de ar, m a massa de CO2 nela contida e Vm o volume molar de um gás.
Seleccione a alternativa que permite calcular a percentagem em volume de dióxido de carbono no ar atmosférico.
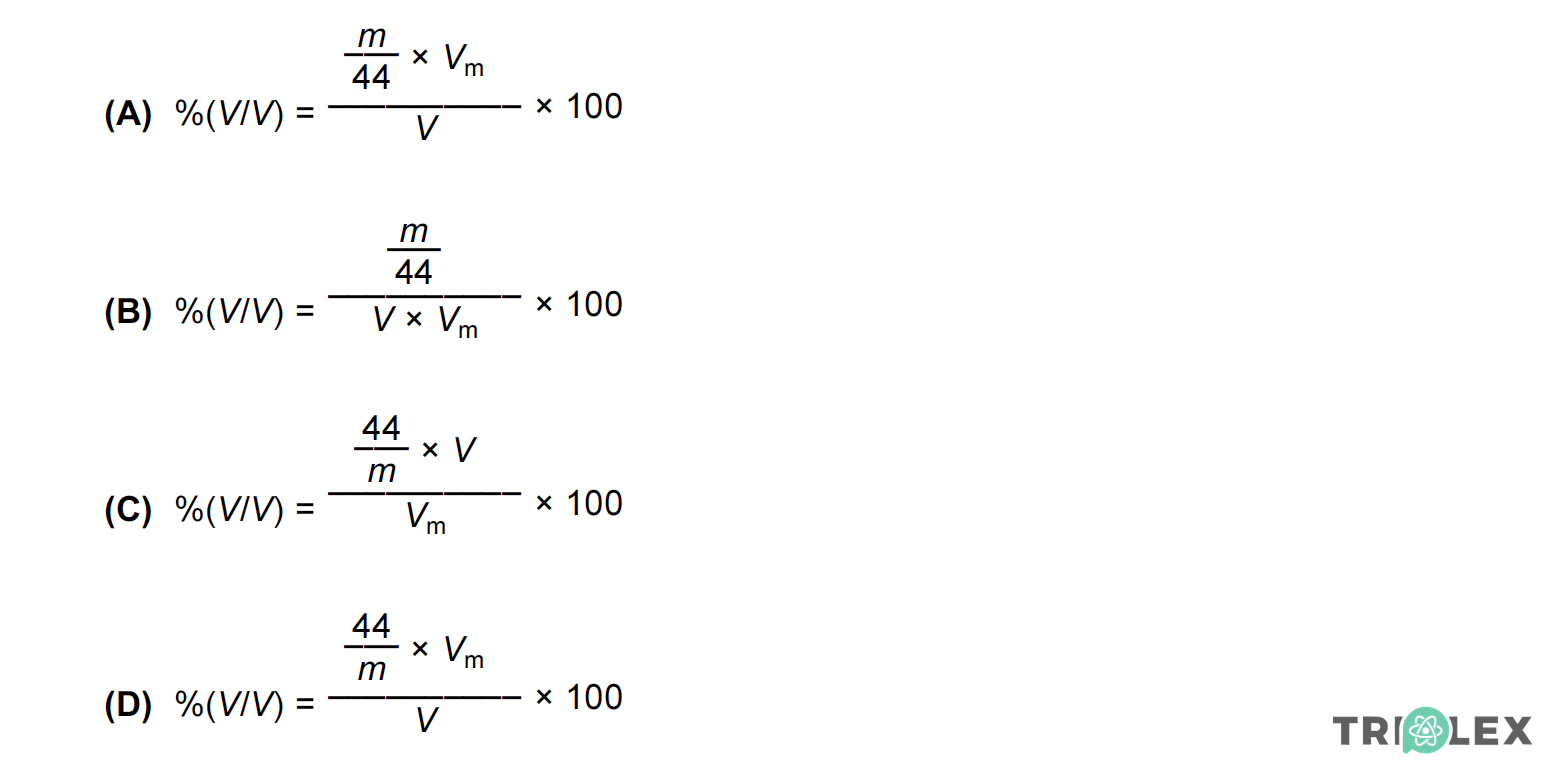
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
2.2 O problema da destruição da camada de ozono tem vindo a assumir cada vez maior relevância, tendo-se tornado um motivo de preocupação universal.
Descreva, num texto, como os CFC provocam a diminuição da camada de ozono, referindo as transformações químicas que ocorrem nesse processo.
Os CFC são clorofluorocarbonetos. São «hidrocarbonetos» onde os hidrogénios foram substituídos por átomos de cloro e de flúor.
A luz ultravioleta pode quebrar ligações C-X (em que X é o flúor ou o cloro), formando-se radicais X.
⇒ Estes radicais reagem com o ozono:- X. + O3 → O2 + OX
- OX + O3 → 2 O2 + X.
recomeçando o ciclo, até que dois radicais X . se encontrem e originem a molécula X2.
⇒ Este processo ocorre na estratosfera e, deste modo, causa uma diminuição da concentração de ozono (a camada de ozono).
A composição deve contemplar os seguintes tópicos:
⇒ Na estratosfera / camada de ozono, os CFC sofrem a acção das radiações ultravioleta.
⇒ Por acção das radiações ultravioleta, os CFC geram quantidades significativas de radicais livres de Cl•.
⇒ Os radicais livres de Cl•, por sua vez, reagem com o ozono, dando origem a outros compostos.
A classificação deste item utiliza os níveis de desempenho registados nos critérios gerais, apresentados de acordo com os tópicos descritos.

Se o examinando referir apenas 1 dos tópicos:
⇒ atribuir a classificação de 4 pontos se este estiver correcto;
⇒ atribuir a classificação de 3 pontos se for utilizada, ocasionalmente, uma terminologia científica não adequada e/ou com incorrecções.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2.3. As moléculas de água, H2O, e de dióxido de carbono, CO2, têm estruturas bem definidas, a que correspondem propriedades físicas e químicas distintas.
Classifique como verdadeira (V) ou falsa (F) cada uma das afirmações seguintes.
(A) Na molécula de CO2, existem quatro pares de electrões não ligantes.
(B) Na molécula de H2O, existem dois pares de electrões partilhados.
(C) As duas moléculas (H2O e CO2) apresentam geometria linear.
(D) Na molécula de H2O, existe um par de electrões não ligantes.
(E) Na molécula de CO2, as ligações carbono-oxigénio têm diferentes comprimentos.
(F) O ângulo de ligação, na molécula de H2O, é superior ao ângulo de ligação, na molécula de CO2.
(G) Na molécula de H2O, existem quatro electrões ligantes e quatro não ligantes.
(H) Na molécula de CO2, nem todos os electrões de valência são ligantes.
- Verdadeiras – (A), (B), (G) e (H)
- Falsas – (C), (D), (E) e (F)
Por cada átomo de oxigénio existem dois pares de eletrões de valência não ligantes.
⇒ (B) Verdadeira.
Para cada ligação O–H contribui um par de eletrões partilhados. Como na molécula de água existem duas ligações O–H, existem dois pares de eletrões partilhados.
⇒ (C) Falsa.
A molécula de CO2 apresenta geometria linear, mas a molécula de H2O apresenta uma geometria angular.
⇒ (D) Falsa.
Na molécula de H2O existem dois pares de eletrões de valência não ligantes.
⇒ (E) Falsa.
Na molécula de CO2 as ligações carbono-oxigénio são equivalentes, pelo que têm o mesmo comprimento.
⇒ (F) Falsa.
O ângulo de ligação na molécula de CO2 é de 180° (molécula linear), enquanto que a molécula de H2O apresenta uma geometria angular, pelo que tem um ângulo inferior a 180°.
⇒ (G) Verdadeira.
Na molécula de H2O existem quatro eletrões de valência ligantes que formam as duas ligações O–H e existem dois pares de eletrões de valência não ligantes no O.
⇒ (H) Verdadeira.
Na molécula de CO2 há quatro pares de eletrões de valência não ligantes.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
2.4. As moléculas de água e de dióxido de carbono são constituídas, no seu conjunto, por átomos de hidrogénio, carbono e oxigénio.
Seleccione a afirmação CORRECTA.
(A) A configuração electrónica do átomo de oxigénio no estado de energia mínima é 1s22s22p6.
(B) O raio do átomo de oxigénio é superior ao raio do átomo de carbono.
(C) A primeira energia de ionização do oxigénio é superior à do carbono.
(D) O raio do átomo de oxigénio é superior ao raio do anião O2-.
- Opção (C)
⇒ (A) Falsa.
O átomo de oxigénio só tem oito eletrões. A configuração eletrónica do átomo de oxigénio (8O) no estado de energia mínima é: 1s2 2s2 2p4.
⇒ (B) Falsa.
O raio do átomo de oxigénio é inferior ao raio do átomo de carbono. O átomo de oxigénio, 8O, e o átomo de carbono, 6C, têm o mesmo número de camadas eletrónicas ocupadas, pelo que estes elementos pertencem ao mesmo período da TP. O átomo de oxigénio tem mais dois protões no núcleo, que provocam um aumento de carga nuclear e consequente aumento da força atrativa núcleo-eletrões. Embora as repulsões entre os eletrões no átomo de oxigénio sejam superiores às existentes no átomo de carbono (o crescente número atómico aumenta o número de eletrões do átomo), o efeito do aumento da carga nuclear é dominante porque a blindagem pelos eletrões interiores é a mesma.
⇒ (C) Verdadeira.
O oxigénio tem mais dois protões no núcleo e mais dois eletrões que o carbono. O número de camadas eletrónicas ocupadas nos dois átomos é o mesmo, pelo que não há alteração significativa do efeito de blindagem. Como a carga nuclear que atua nos eletrões é maior no oxigénio que no carbono, é necessária mais energia para os remover.
⇒ (D) Falsa.
Quando o átomo de oxigénio se transforma em ião negativo (anião) ganha dois eletrões. A atração nuclear é praticamente a mesma que se verifica no átomo neutro, mas a repulsão entre os eletrões aumenta, pelo que o raio do anião O2- é superior ao do átomo de O.
- Opção (C)…………. 8 pontos
2.5. No âmbito de um projecto sobre chuva ácida, foram medidos, a uma mesma temperatura, os valores de pH de duas amostras de água da chuva: uma amostra da água que pingava das agulhas de um pinheiro e outra, da água que escorria pelo tronco.
Os valores obtidos estão indicados na figura.
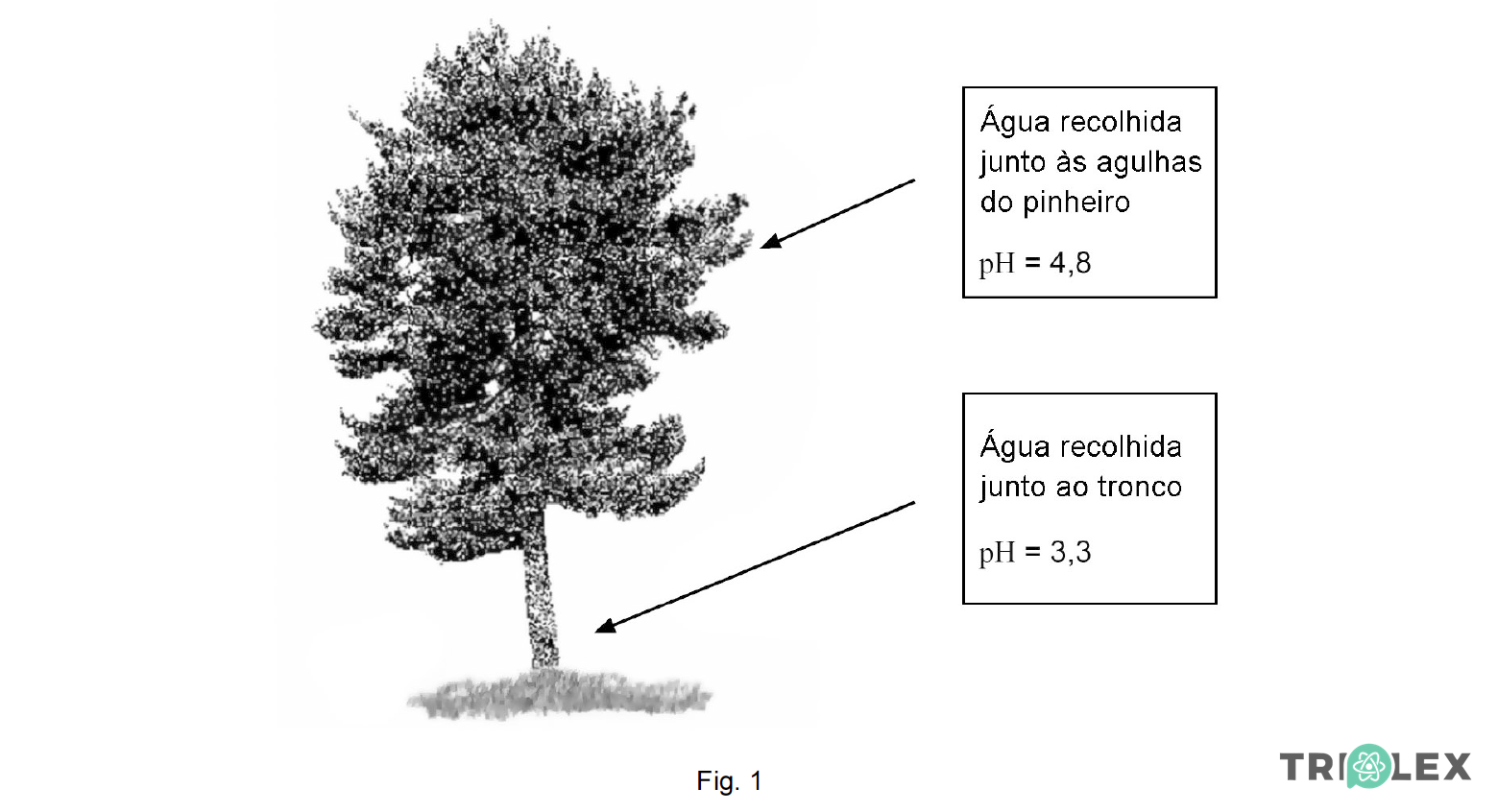
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2.5.1. Com base na informação dada, seleccione a afirmação CORRECTA.
(A) A água da chuva recolhida junto às agulhas do pinheiro é mais ácida do que a água recolhida junto ao tronco.
(B) A água da chuva recolhida junto ao tronco do pinheiro tem menor valor de pOH do que a água recolhida junto às agulhas.
(C) A água da chuva recolhida junto ao tronco do pinheiro tem menor concentração de iões H3O+ do que a água recolhida junto às agulhas.
(D) A água da chuva recolhida junto às agulhas do pinheiro e a água da chuva recolhida junto ao tronco apresentam igual valor de Kw.
- Opção (D)
⇒ (A) Falsa.
Como pH = – log [H3O+], quanto maior for o valor de pH, menor é a [H3O+]. De acordo com o indicado na figura, a água recolhida junto às agulhas do pinheiro apresenta um valor de pH de 4,8, superior ao da água recolhida junto ao tronco (3,3). Assim, a [H3O+] da água da chuva recolhida junto às agulhas do pinheiro é inferior à da recolhida junto ao tronco e, consequentemente, menos ácida.
⇒ (B) Falsa.
Como pH + pOH = pKw, quanto maior for o pH menor é o respetivo pOH. Como, de acordo com o indicado na figura, a água recolhida junto ao tronco do pinheiro apresenta um valor de pH inferior ao da água recolhida junto às agulhas, terá maior valor de pOH.
⇒ (C) Falsa.
Ver (A).
⇒ (D) Verdadeira.
Admitindo que a temperatura junto às agulhas do pinheiro e junto ao tronco é a mesma, e como Kw depende exclusivamente da temperatura, a afirmação é verdadeira.
- Opção (D)…………. 8 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2.5.2. Para confirmar o valor do pH da amostra de água da chuva recolhida junto ao tronco do pinheiro, titulou-se um volume de 100,0 mL daquela amostra com uma solução aquosa de concentração 0,005 mol dm–3 em hidróxido de sódio, NaOH(aq).
Calcule o volume de titulante que se gastaria até ao ponto de equivalência, admitindo que se confirmava o valor de pH da solução titulada.
Apresente todas as etapas de resolução.
- V = 100,0 mL
- pH = 3,3
- c (NaHO) = 0,005 mol dm-3
⇒ Cálculo da concentração de H3O+ na amostra de água recolhida junto ao tronco do pinheiro:
Para dar resposta à pergunta, tem de se admitir que a acidez da água da chuva é resultado da ionização de ácidos fortes.
Como pH = 3,3 (pH = – log [H3O+(aq)]) vem: [H3O+(aq)] = 10-3,3 mol dm-3 = 5,01 x 10-4 mol dm-3
⇒ Cálculo da quantidade de iões H3O+ existente em 100,0 mL da amostra, antes de ser titulada:
A quantidade de iões H3O+ existente em 100,0 mL da amostra antes de ser titulada é:
- n = c x V = 5,01 x 10-4 mol dm-3 x 0,1000 dm3 = 5,01 x 10-5 mol
⇒ Cálculo do volume de titulante gasto até ao ponto de equivalência da titulação:
Equação da titulação:
H3O+ (aq) + HO– (aq) → 2 H2O (l)
De acordo com a estequiometria da reação de titulação, a quantidade de HO– (aq) (e de NaHO), gasta até atingir o ponto de equivalência, é igual à quantidade de H3O+ inicialmente existente na amostra:
- n (NaHO) = 5,01 x 10-5 mol
Como n = c x V vem V = 5.01 x 105 / 0,005 = 0,010 dm3 = 10 mL
Uma metodologia de resolução correcta deverá apresentar, no mínimo, as seguintes etapas:
⇒ Calcula a concentração de H3O+ na amostra de água da chuva recolhida junto ao tronco do pinheiro (c = 5,01 × 10–4 mol dm–3).
⇒ Calcula a quantidade de H3O+ que existia em 100,0 mL da amostra, antes de ser titulada (n = 5,01 × 10–5 mol).
⇒ Calcula o volume de titulante gasto até ao ponto de equivalência da titulação (V = 10,0 mL).

Erros de tipo 1 – erros de cálculo numérico, transcrição incorrecta de dados, conversão incorrecta de unidades ou ausência de unidades / unidades incorrectas no resultado final.
Erros de tipo 2 – erros de cálculo analítico, erros na utilização de fórmulas, ausência de conversão de unidades(*) e outros erros que não possam ser incluídos no tipo 1.
(*) Qualquer que seja o número de conversões de unidades não efectuadas, contabilizar apenas como um erro de tipo 2.
⇒ Se a resposta apresentar ausência de metodologia de resolução ou metodologia de resolução incorrecta, ainda que com um resultado final correcto, a classificação a atribuir será de zero pontos.
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
2.5.3. Uma das substâncias que contribuem para aumentar a acidez da água das chuvas é o dióxido de enxofre, SO2, que, reagindo com o oxigénio atmosférico, se transforma em trióxido de enxofre, SO3.
Além de se dissolver, este composto reage com a água que circula na atmosfera, formando soluções diluídas de ácido sulfúrico, o que constitui um dos processos de formação da «chuva ácida».
Seleccione a alternativa que traduz correctamente a variação do número de oxidação do enxofre (S) na referida reacção de formação do trióxido de enxofre.
(A) +2 para +6
(B) +3 para 0
(C) +4 para +6
(D) +6 para +3
- Opção (C)
⇒ No SO2 o número de oxidação é +4 e no SO3 é +6.
- Opção (C)…………. 8 pontos
3. Numa instalação solar de aquecimento de água, a energia da radiação solar absorvida na superfície das placas do colector é transferida sob a forma de calor, por meio de um fluido circulante, para a água contida num depósito, como se representa na figura.

A variação da temperatura da água no depósito resultará do balanço entre a energia absorvida e as perdas térmicas que ocorrerem.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.1. Numa instalação solar de aquecimento de água para consumo doméstico, os colectores solares ocupam uma área total de 4,0 m2.
Em condições atmosféricas adequadas, a radiação solar absorvida por estes colectores é, em média, 800 W / m2.
Considere um depósito, devidamente isolado, que contém 150 kg de água. Verifica-se que, ao fim de 12 horas, durante as quais não se retirou água para consumo, a temperatura da água do depósito aumentou 30 ºC. Calcule o rendimento associado a este sistema solar térmico.
Apresente todas as etapas de resolução. c (capacidade térmica mássica da água) = 4,185 kJ kg–1 ºC–1
- A = 4,0 m2
- I = 800 W m-2
- Δt = 12 h = 12 x 3600 s ⇔ Δt = 4,32 x 104 s
- m(H2O) = 150 kg;
- ΔT = 30 ºC
- c(H2O) = 4,185 kJ kg-1 ºC-1 = 4,185 x 103 J kg-1 ºC-1
- Edispon = I x A x Δt = 800 x 4,0 x 4,32 x 104 = 1,38 x 108 J
⇒ A energia utilizada, Eútil, no aquecimento dos 150 kg de água, isto é, a energia transferida como calor para a água, :
- Eútil = Q = m(H2O) c(H2O) ΔT = 150 x 4,185 x 103 x 30 J = 1,88 x 107 J
 ⇒ O rendimento do processo de aquecimento é de 13,6%.
⇒ O rendimento do processo de aquecimento é de 13,6%.
Uma metodologia de resolução correcta deverá apresentar, no mínimo, as seguintes etapas:
⇒ Calcula a energia absorvida pelos colectores solares durante 12 horas (Efornecida = 1,38 × 108 J).
⇒ Calcula a energia utilizada para obter uma variação de temperatura da água igual a 30 ºC (Eútil = 1,88 × 107 J).
⇒ Calcula o rendimento do sistema solar térmico (η = 13,6 %).

Erros de tipo 1 – erros de cálculo numérico, transcrição incorrecta de dados, conversão incorrecta de unidades ou ausência de unidades / unidades incorrectas no resultado final.
Erros de tipo 2 – erros de cálculo analítico, erros na utilização de fórmulas, ausência de conversão de unidades(*) e outros erros que não possam ser incluídos no tipo 1.
(*) Qualquer que seja o número de conversões de unidades não efectuadas, contabilizar apenas como um erro de tipo 2.
⇒ Se a resposta apresentar ausência de metodologia de resolução ou metodologia de resolução incorrecta, ainda que com um resultado final correcto, a classificação a atribuir será de zero pontos.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.2. Numa instalação solar térmica, as perdas de energia poderão ocorrer de três modos: condução, convecção e radiação.
Explique em que consiste o mecanismo de perda de energia térmica por condução.
⇒ Embora o desvio para o vermelho da radiação das galáxias também seja uma evidência para o Big Bang, note-se que o texto não lhe faz referência.
4. A queda de um corpo abandonado, próximo da superfície terrestre, foi um dos primeiros movimentos que os sábios da Antiguidade tentaram explicar.
Mas só Galileu, já no séc. XVII, estudou experimentalmente o movimento de queda dos graves e o lançamento de projécteis.
Observe com atenção a figura 3, que mostra uma esfera a cair em duas situações:
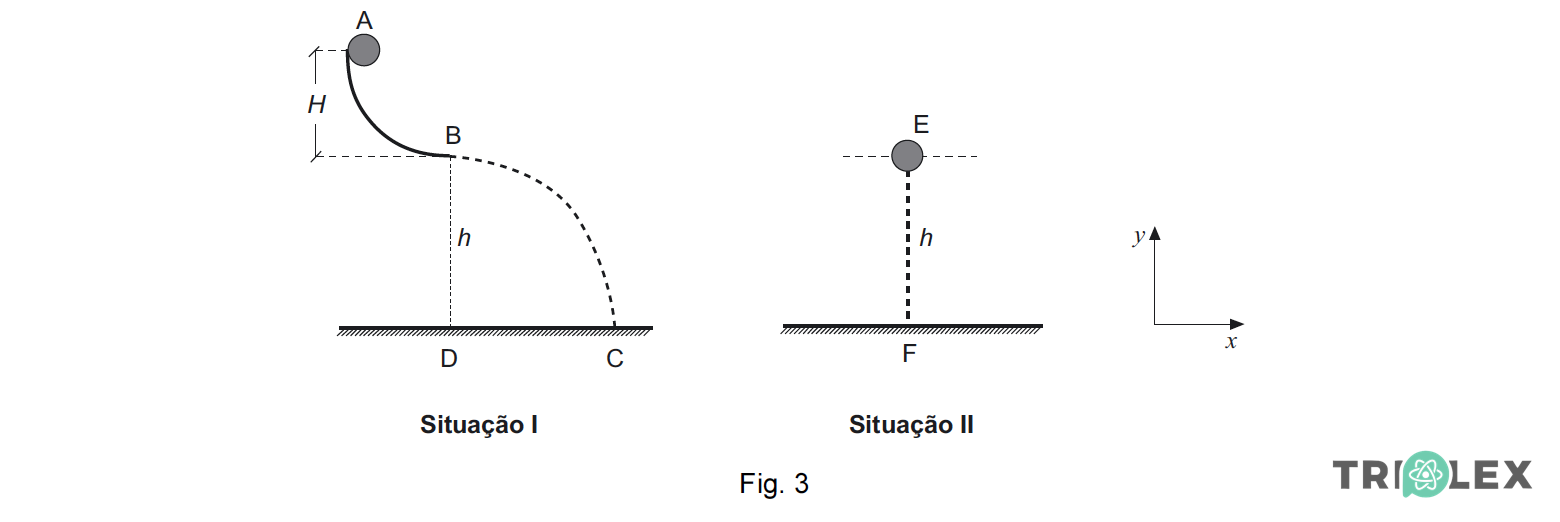
Na situação I, a esfera, inicialmente em repouso, é colocada no ponto A, deslizando sem atrito sobre a calha, até ao ponto B. No ponto B, abandona a calha, descrevendo um arco de parábola até ao ponto C.
Na situação II, a esfera é abandonada no ponto E, caindo na vertical da mesma altura,h.
Em qualquer das situações, considere o sistema de eixos de referência representado na figura, com origem no solo, desprezando o efeito da resistência do ar.
4.1. Considere a situação I representada na figura 3.
Determine a altura H, considerando que as distâncias BD e DC são iguais a 20,0 m.
Apresente todas as etapas de resolução.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
De B a C a esfera está apenas submetida à ação da gravidade, tendo abandonado a calha com velocidade horizontal, pelo que se trata de um lançamento horizontal de um projétil.
Assim:- v0x = vx = vB;
- y0 = h = 20,0 m
- para y = 0 ⇒ x = 20,0 m
- x = vx t (1)
- y = y0 – ½ g t2 (2)
- 0 = 20,0 – ½ x 10 t2 ⇔ t = 2,0 s
- 20,0 = 2,0 vx ⇔ vx = 10,0 m s-1
- EmA = EmB ⇔ EpA + EcA = EpB + EcB ⇔ 0 + mg(hA – hB) = mvB2
- 2 g H = vB2 ⇔ H = 5,0 m
Uma metodologia de resolução correcta deverá apresentar, no mínimo, as seguintes etapas:
⇒ Calcula o tempo de queda da esfera, a partir do ponto B (t = 2,0 s).
⇒ Determina o valor da velocidade da esfera no ponto B (vB = 10,0 m s–1), identificando o valor da velocidade inicial do lançamento horizontal com vB.
⇒ Calcula a altura, H (H = 5,0 m), aplicando a lei da conservação da energia mecânica.

Erros de tipo 1 – erros de cálculo numérico, transcrição incorrecta de dados, conversão incorrecta de unidades ou ausência de unidades / unidades incorrectas no resultado final.
Erros de tipo 2 – erros de cálculo analítico, erros na utilização de fórmulas, ausência de conversão de unidades(*) e outros erros que não possam ser incluídos no tipo 1.
(*) Qualquer que seja o número de conversões de unidades não efectuadas, contabilizar apenas como um erro de tipo 2.
⇒ Se a resposta apresentar ausência de metodologia de resolução ou metodologia de resolução incorrecta, ainda que com um resultado final correcto, a classificação a atribuir será de zero pontos.
4.2. Considere a situação II representada na figura.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
4.2.1. Seleccione o gráfico que traduz correctamente a variação da energia potencial gravítica, Ep, da esfera, em função do tempo de queda, t, até atingir o solo.
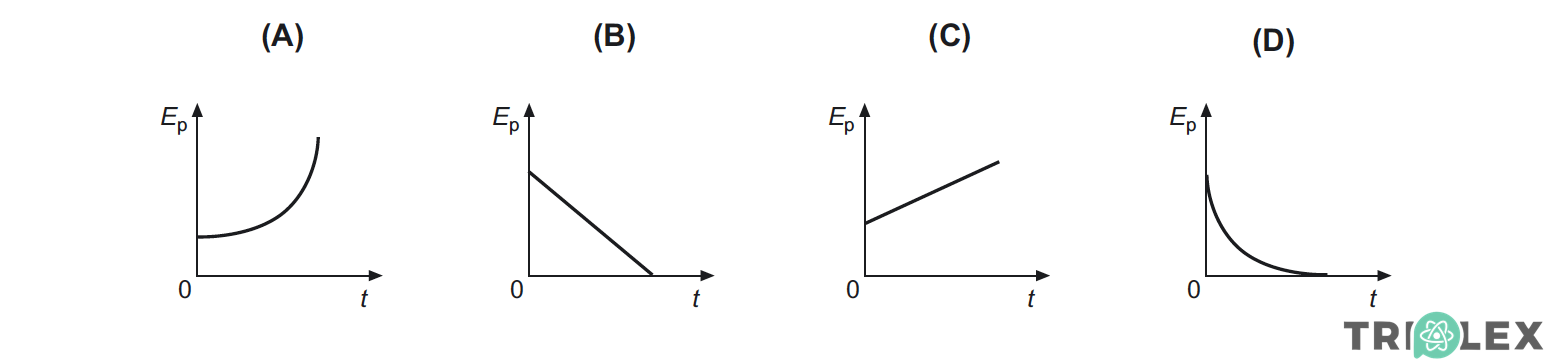
- Opção (X)…………. (item anulado) …… 7 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
4.2.2. Seleccione a alternativa que permite calcular o módulo da velocidade com que a esfera atinge o solo.

- Opção (B)
⇒ Entre as posições E e F há conservação de energia mecânica:
- EmE = EmF ⇔ EcE + EpE = EcF + EpF,
- m g h = ½ mvF2 ⇔ vF2 = 2 g h
- Opção (B)…………. 8 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
4.2.3. Seleccione a alternativa que apresenta os gráficos que traduzem correctamente a variação dos valores da velocidade, v, e da aceleração, a, em função do tempo, t, durante o movimento de queda da esfera.
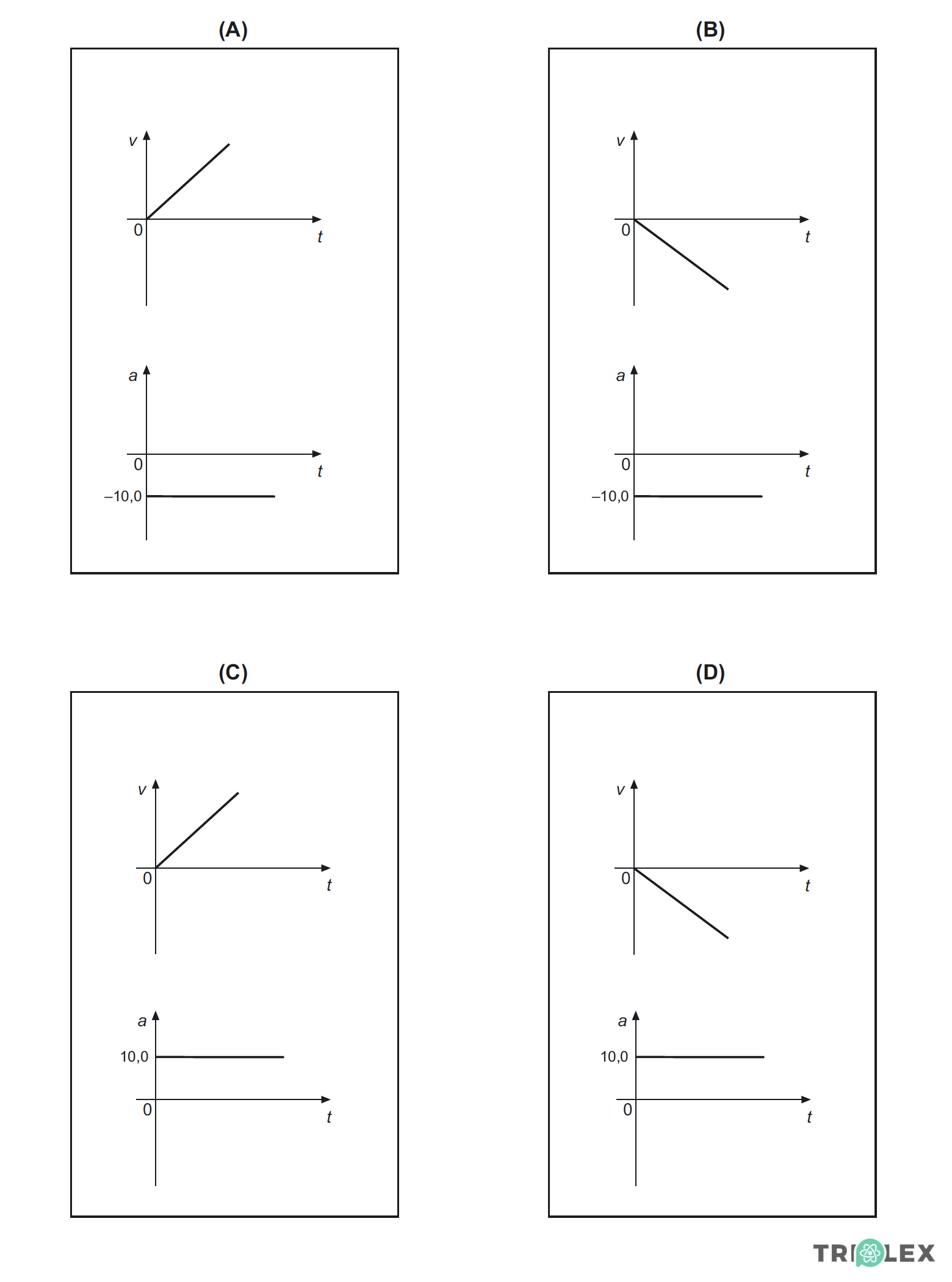
- Opção (B)
⇒ A aceleração é constante e de valor –10 m/s2. Portanto, as hipóteses (C) e (D) estão incorrectas.
⇒ Tem-se a = –g e v = –g t, ou seja, a velocidade varia linearmente com o tempo. O gráfico v (t) é uma recta que passa pela origem e com declive negativo.
⇒ Só a hipótese (B) satisfaz esta condição (notar que o declive de v (t) em (A) é positivo).
- Opção (B)…………. 8 pontos
4.3. Considere os tempos de permanência da esfera no ar, t1 e t2, respectivamente nas situações I e II.
(A) t1 = 2 t2
(B) t1 = ½ t2
(C) t1 = t2
(D) t1 = 10 t2
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)…………. 8 pontos
5. Nas comunicações a longas distâncias, a informação é transmitida através de radiações electromagnéticas que se propagam, no vazio, à velocidade da luz.
5.1. Um dos suportes mais eficientes na transmissão de informação a longas distâncias é constituído pelas fibras ópticas.
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
5.1.1. Seleccione a alternativa que completa correctamente a frase seguinte.
O princípio de funcionamento das fibras ópticas baseia-se no fenómeno da…
(A) … refracção da luz.
(B) … reflexão parcial da luz.
(C) … difracção da luz.
(D) … reflexão total da luz.
- Opção (D)
⇒ A utilização de fibras ópticas justifica-se pela fácil e eficiente propagação da luz, com muito pouca absorção.
Contudo, esta propriedade não faz parte da lista de opções apresentadas.
⇒ Na fibra óptica, a luz está confinada ao seu interior, já que não existe refracção, pelo que as hipóteses (A) e (B) ficam eliminadas (fala-se aí em reflexão parcial que, não sendo um termo de utilização consagrada, pressupõe que ocorra alguma refracção).
⇒ O fenómeno da difracção não ocorre na fibra, pelo que resta a opção (D).
⇒ O revestimento da fibra tem de ser tal que não permita que a fibra possa ter curvas de pequeno raio. Só assim se garante que sempre que haja reflexão esta seja total.
- Opção (D)…………. 8 pontos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
5.1.2. Num determinado tipo de fibra óptica, o núcleo tem um índice de refracção de 1,53, e o revestimento possui um índice de refracção de 1,48.
Seleccione a alternativa que permite calcular o ângulo crítico, θc, para este tipo de fibra óptica.

- Opção (B)…………. 8 pontos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
5.2. As microondas constituem um tipo de radiação electromagnética muito utilizado nas telecomunicações.
Indique duas propriedades das microondas que justificam a utilização deste tipo de radiação nas comunicações via satélite.
⇒ A radiação electromagnética propaga-se em linha recta, sendo pouco absorvida na atmosfera. A reflexão de microondas também não se dá nas interfaces de separação de meios opticamente diferentes da atmosfera. Também não difractam, pelo que emissor e receptor devem estar em linha de vista.
Nota: as microondas têm frequência relativamente elevada, suportando uma modulação de frequência com larguras de banda relativamente grandes, o que permite o carregamento de muita informação. Este facto deveria também ser considerado como correcto (embora não figure nos critérios de correcção).
6. O amoníaco, NH3, obtém-se industrialmente através do processo de Haber-Bosch, fazendo reagir, em condições apropriadas, hidrogénio e azoto gasosos.
Este processo de formação do amoníaco ocorre em sistema fechado, em condições de pressão e temperatura constantes, na presença de um catalisador, de acordo com o equilíbrio representado pela seguinte equação química:
N2 (g) + 3 H2 (g) ⇋ 2 NH3 (g)
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
6.1. O gráfico representado na figura 4 traduz a variação do valor da constante de equilíbrio, para aquela reacção, em função da temperatura, T, no intervalo de 700 K a 1000 K.

Com base na informação dada pelo gráfico, seleccione a afirmação CORRECTA.
(A) O aumento de temperatura favorece o consumo de H2(g) e N2(g).
(B) A diminuição de temperatura aumenta o rendimento da reacção.
(C) A constante de equilíbrio da reacção é inversamente proporcional à temperatura.
(D) A reacção evolui no sentido inverso se se diminuir a temperatura.
- Opção (B)
⇒ (A) Falsa.
De acordo com o gráfico da figura 4, o aumento de temperatura conduz a uma diminuição de Kc . A diminuição de Kc corresponde à diminuição da concentração de NH3 e/ou aumento das concentrações de N2 e H2. Assim, o aumento da temperatura conduz a um consumo de NH3 e à formação de N2 e H2.
⇒ (B) Verdadeira.
De acordo com o descrito em (A), a diminuição de temperatura conduz a um aumento da concentração de NH3 e diminuição das concentrações de N2 e H2, aumentando assim o rendimento da reação.
⇒ (C) Falsa.
Kc e T seriam inversamente proporcionais se Kc fosse proporcional a 1/T.
Se assim fosse viria: Kc T = constante.
Considerando dois pontos:
(Kc = 0,30; T ≈ 700 K) ⇒ Kc T = 210 K (Kc = 0,05; T ≈ 775 K) ⇒ Kc T = 39 K
logo, não são inversamente proporcionais, pois o produto Kc T não é constante.
De acordo com o descrito em (A) e (B), se se diminuir a temperatura, a reação evolui no sentido direto.
- Opção (B) …………. 8 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
6.2. O sulfato de tetraminocobre(II) mono-hidratado, [Cu(NH3)4] SO4.H2O, (M= 245,6g mol–1), é um sal complexo, obtido a partir da reacção entre o sulfato de cobre(II) penta-hidratado, CuSO4.5H2O, e o amoníaco.
Esta reacção é descrita pela seguinte equação química:
CuSO4. H2O (s) + 4 NH3 (aq) → [Cu(NH3)4] . H2O (s) + 4 H2O (l)
A 8,0 mL de uma solução aquosa de amoníaco de concentração 15,0 mol dm–3, adicionaram-se 0,02 mol de sulfato de cobre penta-hidratado.
Calcule a massa de sal complexo que se formaria, admitindo que a reacção é completa.
Apresente todas as etapas de resolução
- V(NH3) = 8,0 mL
- c (NH3) = 15,0 mol dm-3
- n (CuSO4.5 H2O) = 0,02 mol
⇒ Cálculo da quantidade de amoníaco:
- n (NH3) = c x V = 15,0 mol dm-3 x 8,0 x 10-3 dm3 = 0,12 mol
⇒ Cálculo do reagente limitante:
De acordo com a estequiometria da reação entre CuSO4.5 H2O e NH3, 1:4, 0,02 mol de CuSO4.5 H2O necessitam de 4 x 0,02 = 0,08 mol de NH3.
Como existem 0,12 mol de NH3, concluímos que o NH3 está em excesso e, portanto, o reagente limitante é o CuSO4.5 H2O.
⇒ Cálculo da massa de sal complexo formado:
De acordo com a equação química, a quantidade de sal complexo formado é igual à quantidade de sulfato de cobre (II) penta-hidratado gasta.
Como há 0,02 mol de sulfato de cobre (II) penta-hidratado e se admite que a reação é completa, devem obter-se 0,02 mol de sal complexo.
Como n = m/M ⇔ m = n x M = 0,02 mol x 245,6 g mol-1 = 4,9 g
Uma metodologia de resolução correcta deverá apresentar, no mínimo, as seguintes etapas:
⇒ Calcula a quantidade de amoníaco (n = 0,12 mol).
⇒ Refere a estequiometria da reacção entre CuSO4.5H2O e NH3 (1:4) e utiliza a relação estequiométrica para identificar o reagente limitante (CuSO4.5H2O).
⇒ Calcula a massa de [Cu(NH3)4]SO4.H2O que se formaria (m = 4,9 g).

Erros de tipo 1 – erros de cálculo numérico, transcrição incorrecta de dados, conversão incorrecta de unidades ou ausência de unidades / unidades incorrectas no resultado final.
Erros de tipo 2 – erros de cálculo analítico, erros na utilização de fórmulas, ausência de conversão de unidades(*) e outros erros que não possam ser incluídos no tipo 1.
(*) Qualquer que seja o número de conversões de unidades não efectuadas, contabilizar apenas como um erro de tipo 2.
⇒ Se a resposta apresentar ausência de metodologia de resolução ou metodologia de resolução incorrecta, ainda que com um resultado final correcto, a classificação a atribuir será de zero pontos.
FIM
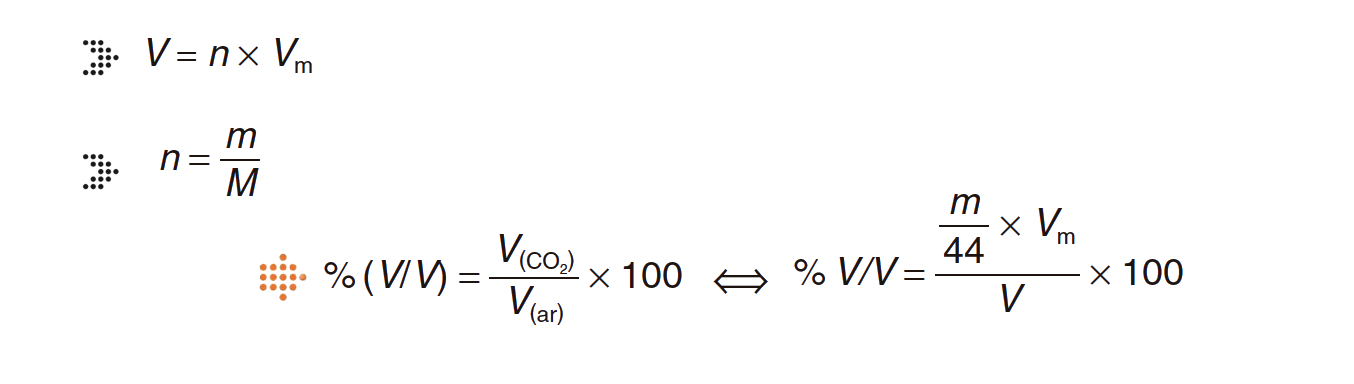

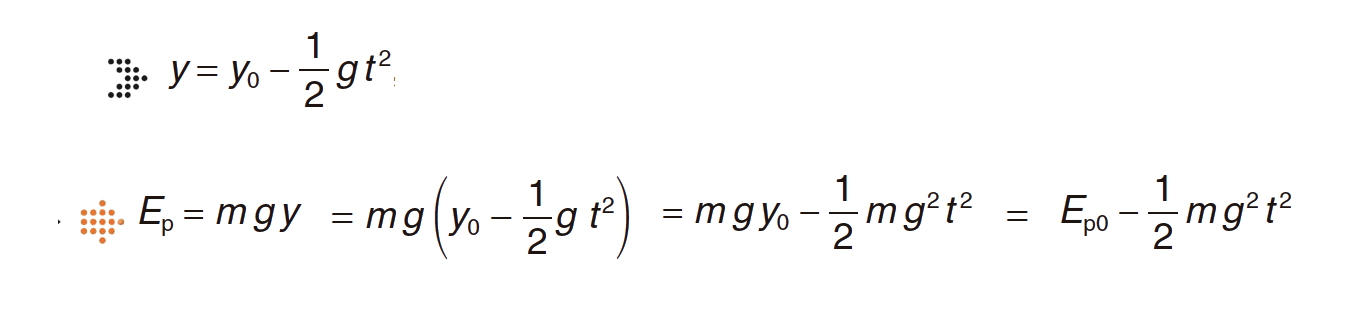






Tudo é muito aberto com um claro esclarecimento da desafios. Foi verdadeiramente informativo. É seu site útil. Obrigado por partilha!
Olá Estou no trabalho navegação do meu novo blog iphone 4 ! Só queria dizer que eu amo lendo seu blog e estamos ansiosos para todos os seus posts! Continuar o fantástico trabalhar!
Devo Obrigado pelos esforços tem Coloque escrevendo isso site . Espero ver o mesmo alto grau conteúdo de você mais tarde também. Na verdade, suas habilidades de escrita criativa tem incentivou eu conseguir minha própria site agora 😉
Você na verdade torná-lo parece tão fácil junto com seu apresentação no entanto eu em encontrar isto tópico ser realmente uma coisa que acho Talvez nunca entender. Meio que se sente também complicado e extremamente grande para mim. Eu sou olhando frente na sua subsequentes acondicionados, eu vou tentar se o balançar disso!