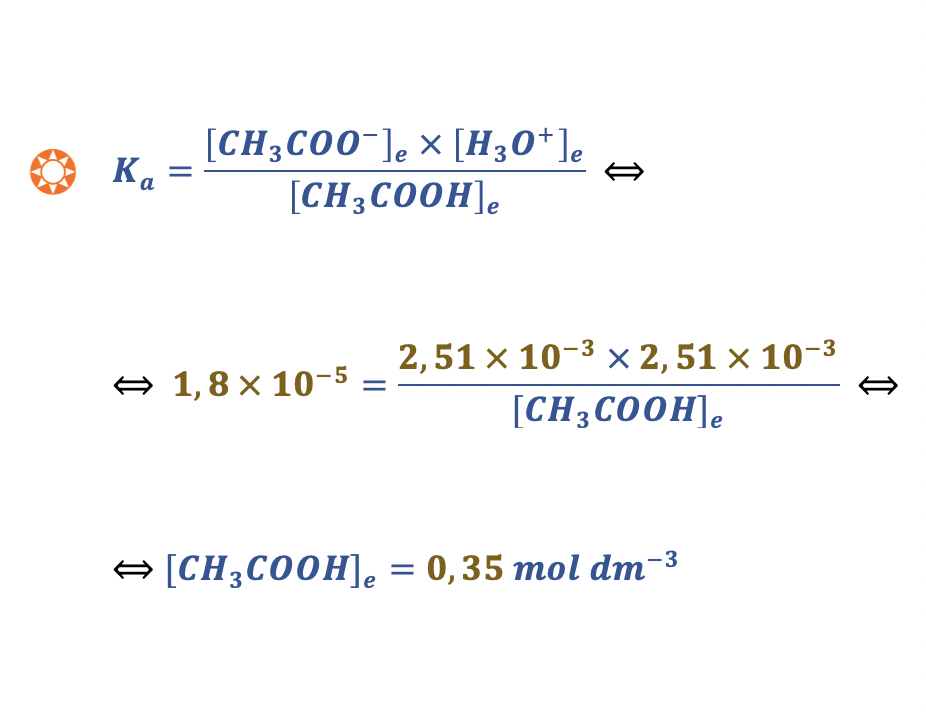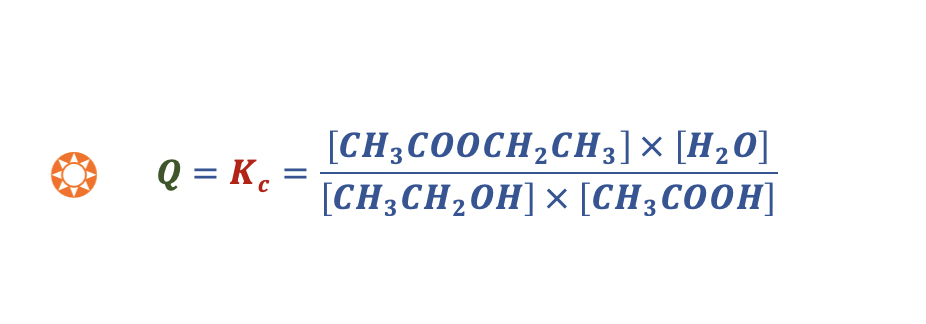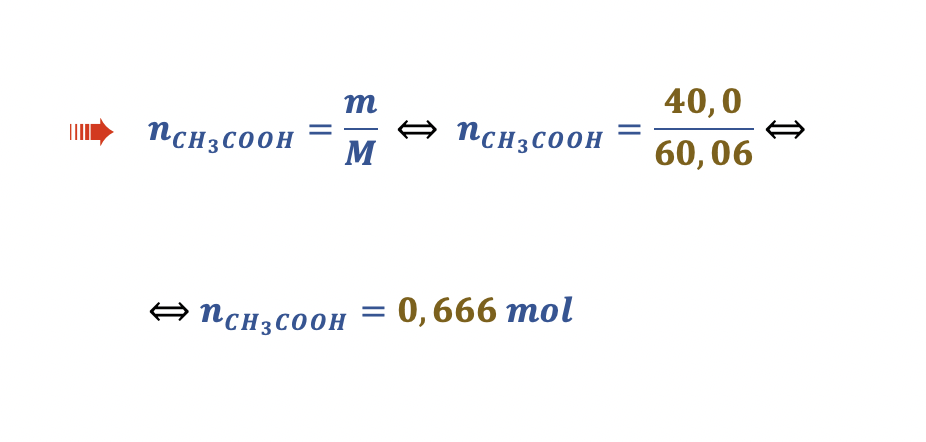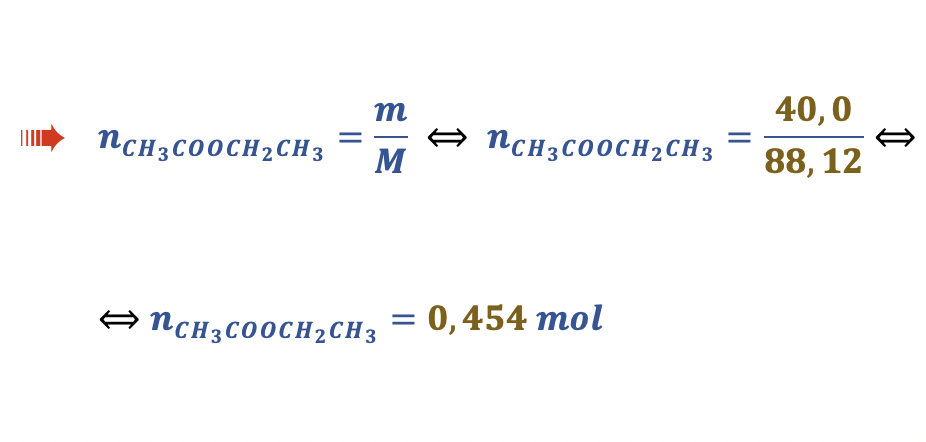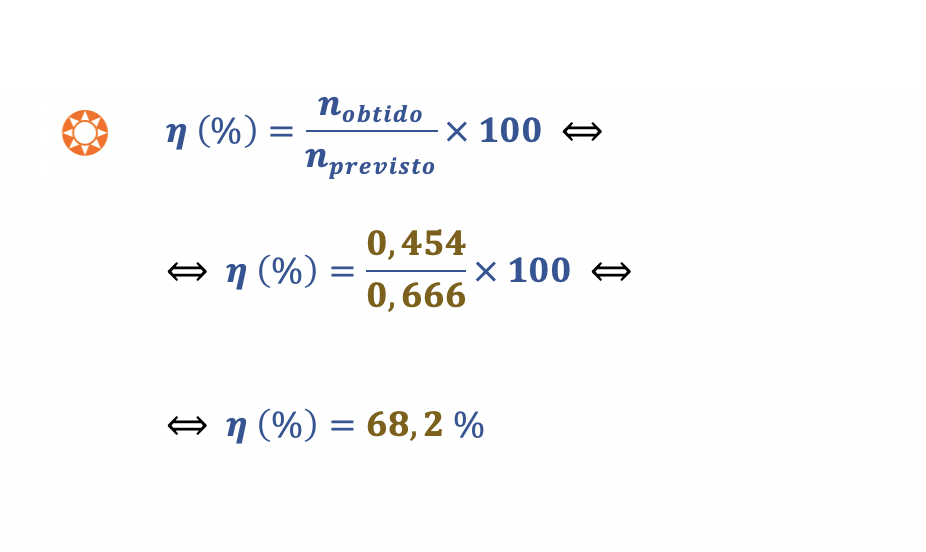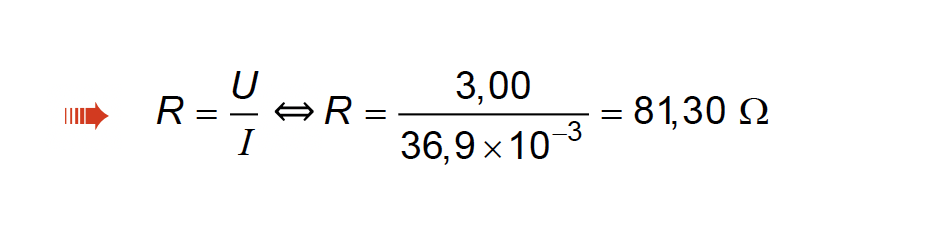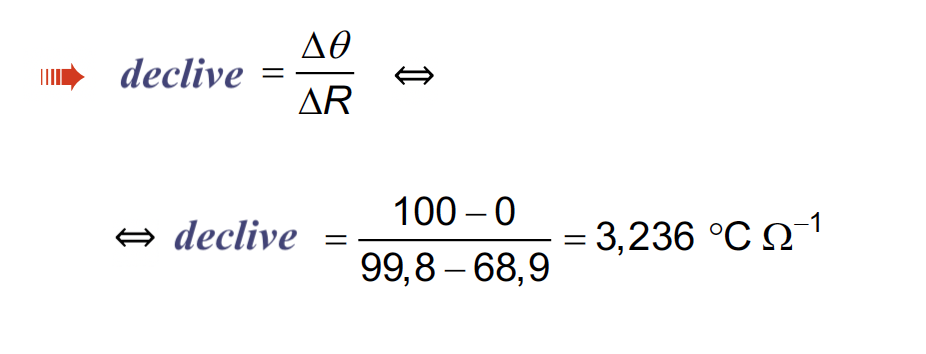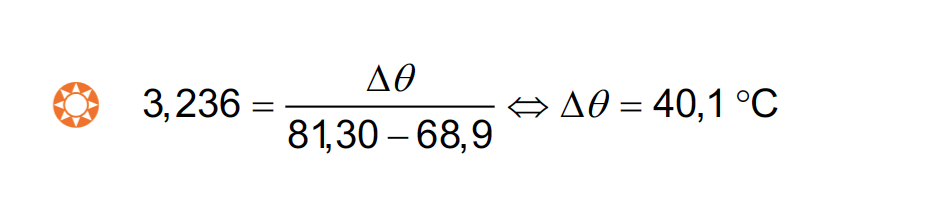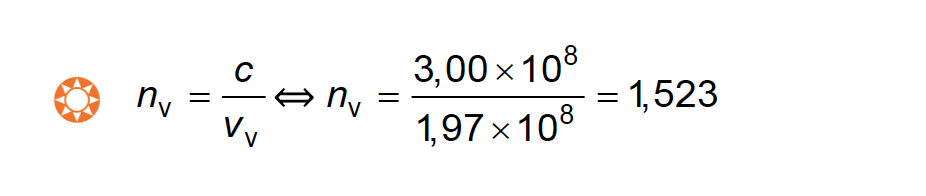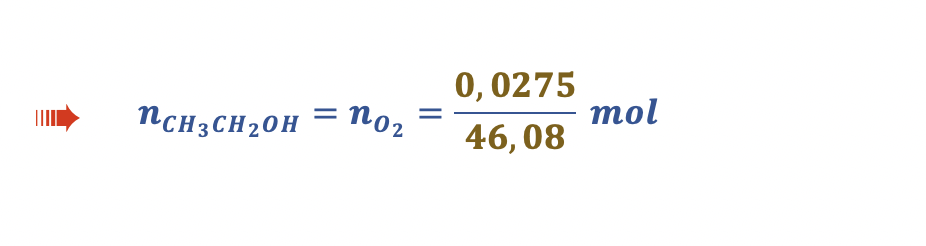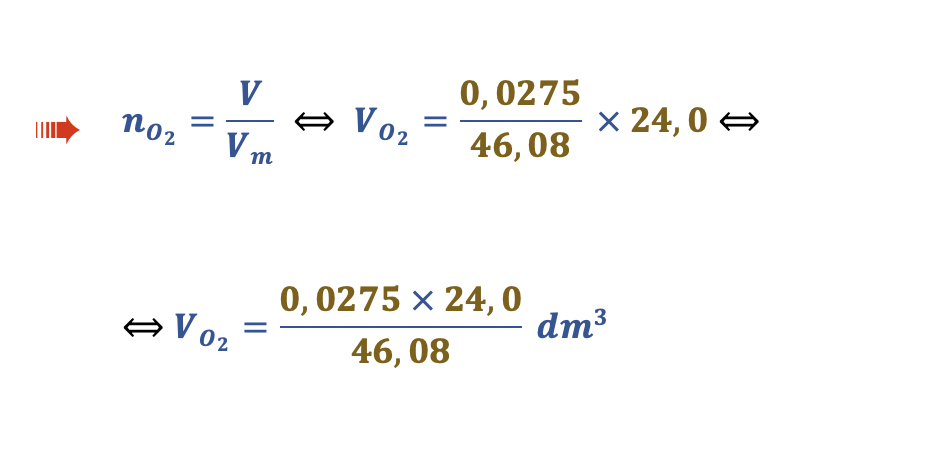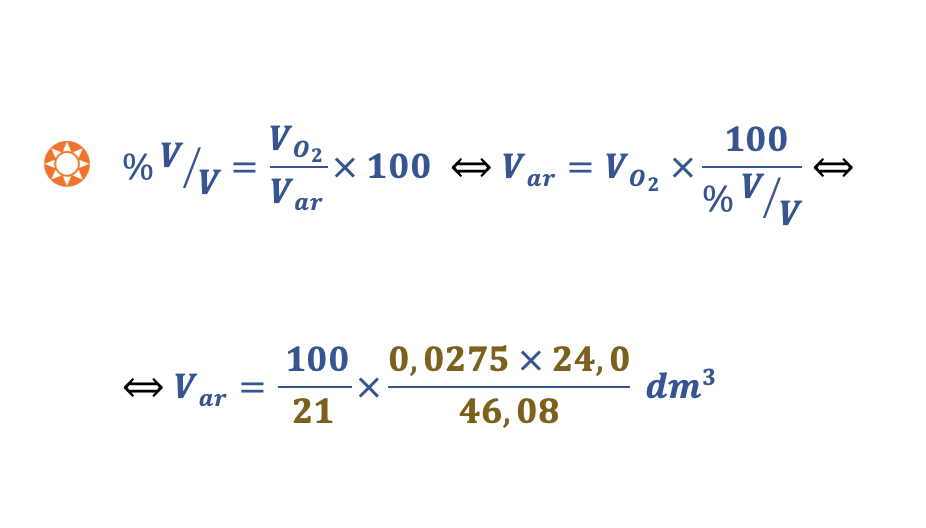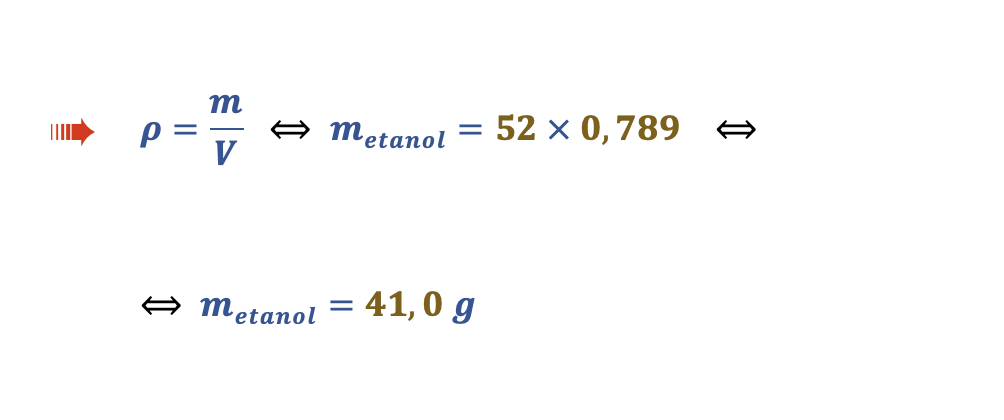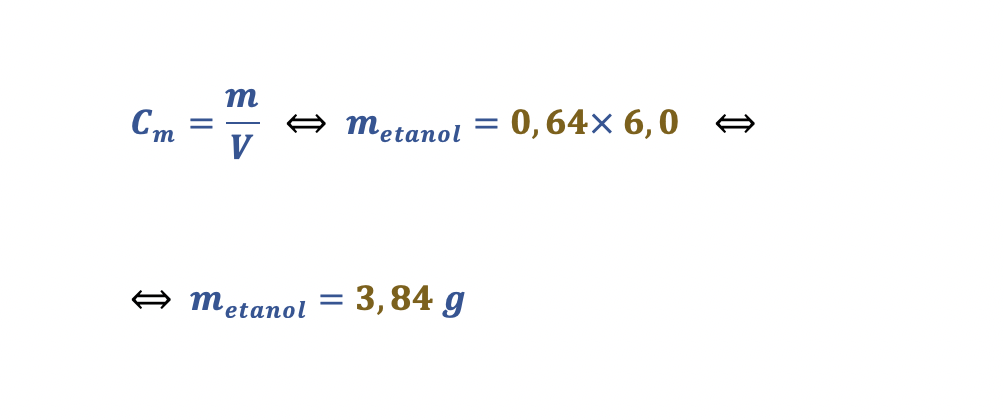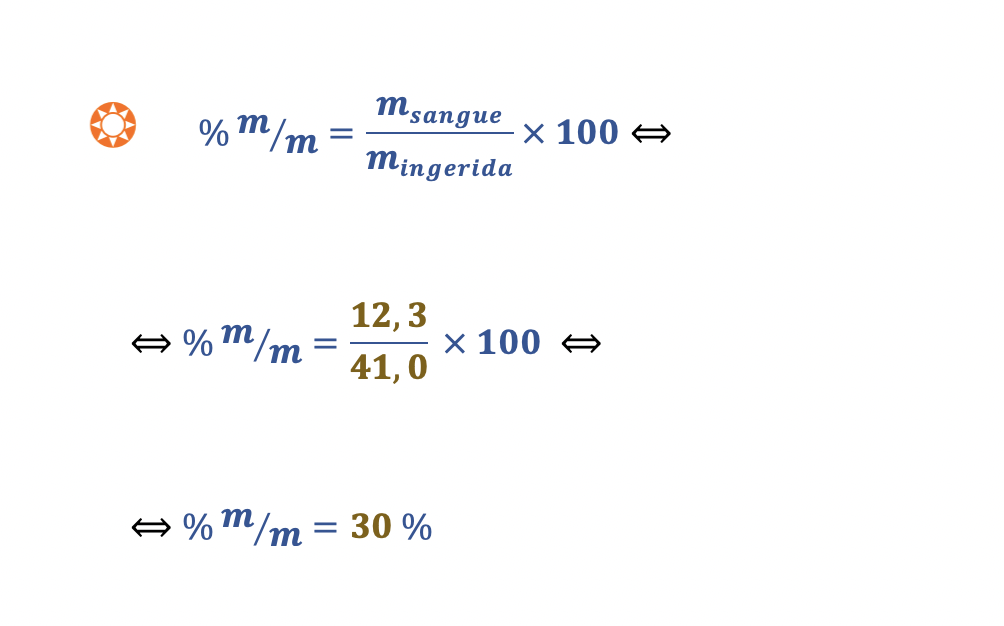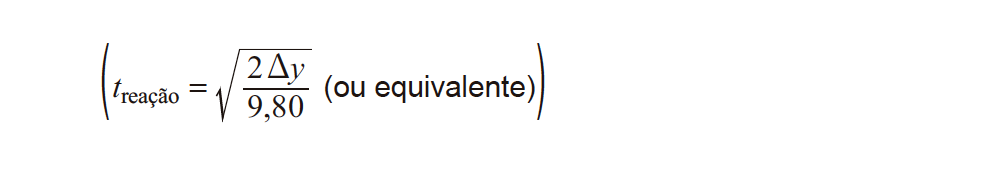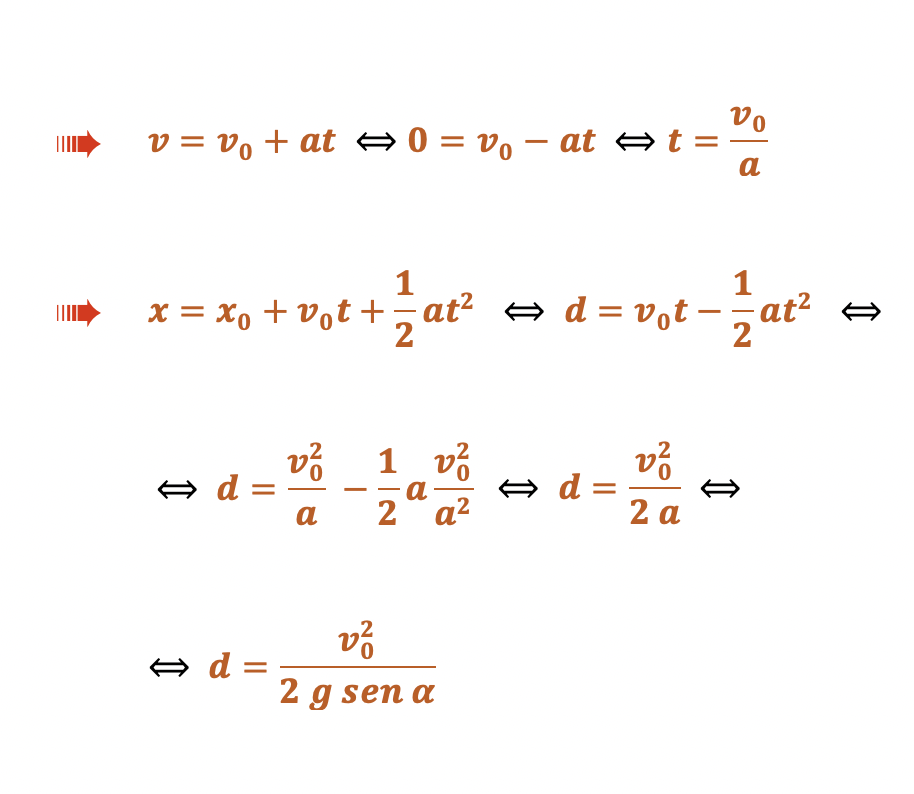Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: Época Especial – 2023
A prova inclui 16 itens, devidamente identificados no enunciado, cujas respostas contribuem obrigatoriamente para a classificação final.
Dos restantes 8 itens da prova, apenas contribuem para a classificação final os 4 itens cujas respostas obtenham melhor pontuação.
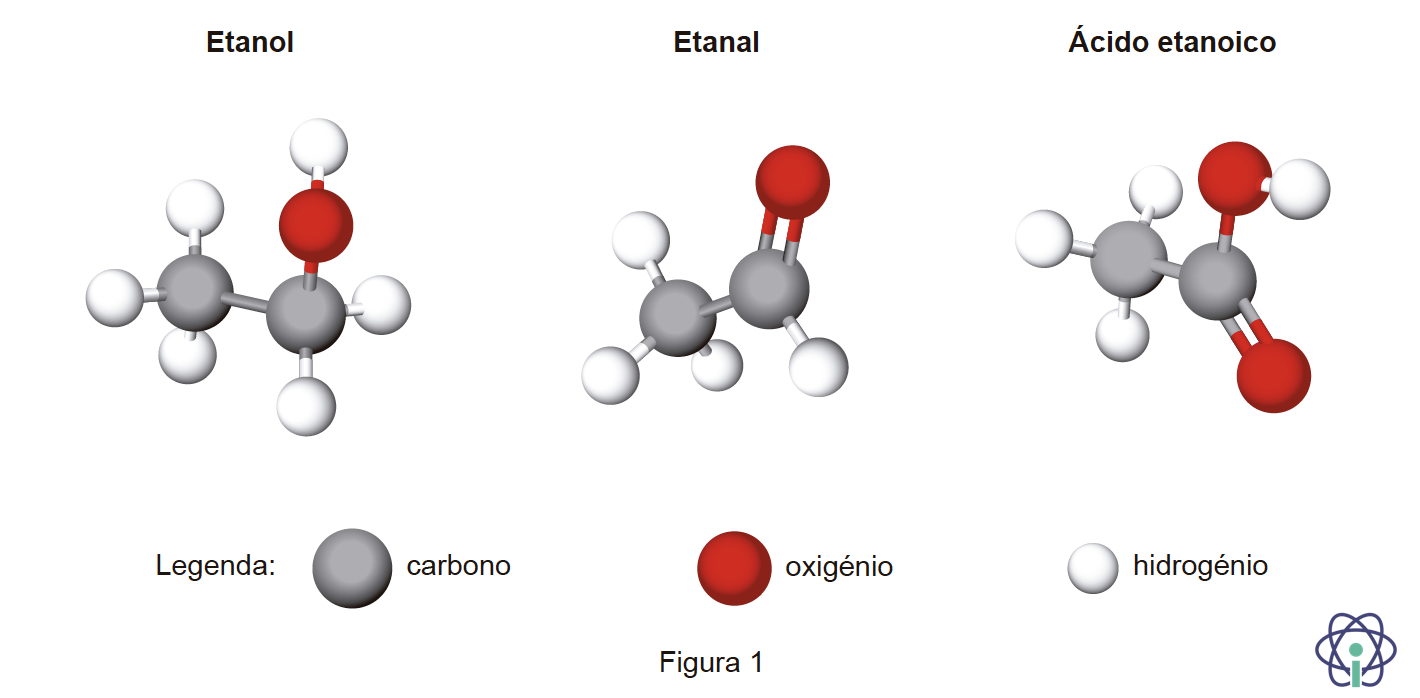
1. O etanol, CH3CH2OH, faz parte da composição de bebidas alcoólicas e pode ser utilizado como combustível.
O etanal, CH3CHO, pode ser obtido a partir do etanol, e a sua principal utilização é a produção de ácido etanoico.
O ácido etanoico, CH3COOH, tem utilizações variadas, destacando-se o fabrico de essências artificiais.
A Figura 1 representa modelos tridimensionais das moléculas de etanol, etanal e ácido etanoico.
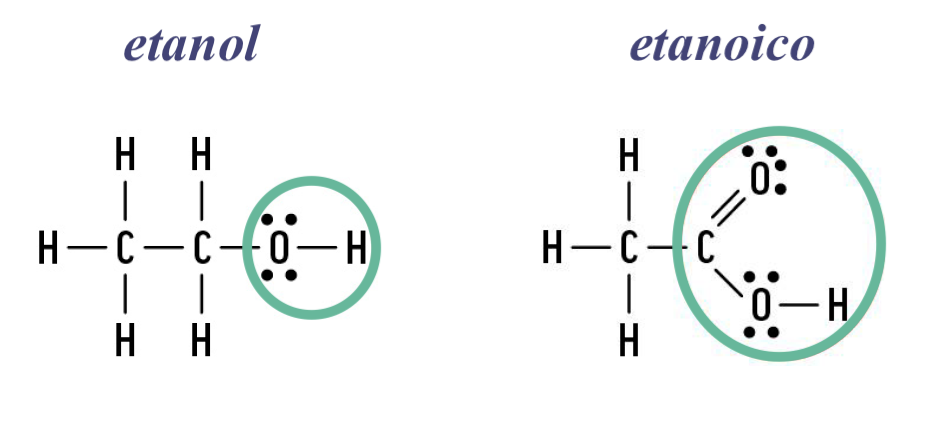
1.1. Os grupos funcionais nas moléculas de etanol e de ácido etanoico são, respetivamente, …
(A) … carbonilo e hidroxilo.
(B) … hidroxilo e carboxilo.
(C) … carbonilo e carboxilo.
(D) … hidroxilo e carbonilo.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (B) ……………. 10 pontos
1.2. Na molécula de etanal, os números de pares de eletrões ligantes e de pares de eletrões não ligantes são, respetivamente, …
(A) … seis e um.
(B) … sete e um.
(C) … seis e dois.
(D) … sete e dois.
- Opção (D)
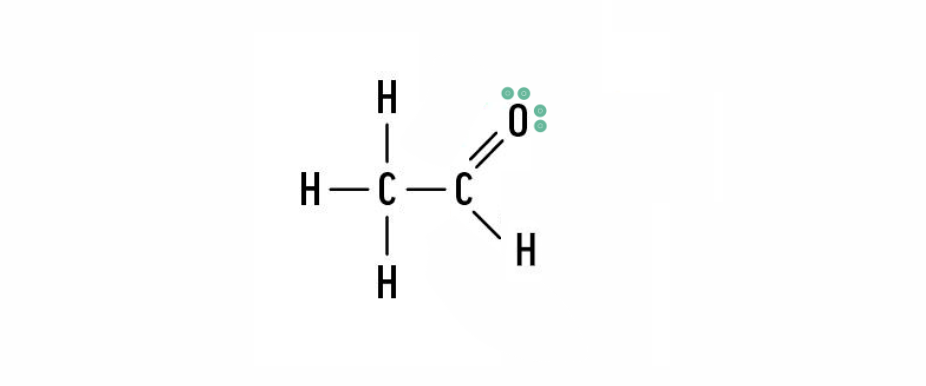
🛑 As moléculas de etanal ou aldeído acético (CH2CHO) podem ser representadas através da notação de Lewis por:
🛑 Neste esquema, os pares de eletrões de valência ligantes (eletrões envolvidos nas ligações covalentes) estão assinalados por um traço, e os eletrões não ligantes associados a cada átomo estão assinalados por um ponto cada um.
🛑 O número de pares de eletrões de valência ligantes é sete e o número de pares de eletrões não ligantes é dois.
- Opção (D) ……………. 10 pontos
1.3. Em solução aquosa, o ácido etanoico, CH3COOH (aq), ioniza-se parcialmente, originando CH3COO– (aq) e H3O+ (aq).
Esta reação pode ser traduzida por
CH3COOH (aq) + H2O (l) ⇋ CH3COO– (aq) + H3O+ (aq) Ka = 1,8 × 10-5, à temperatura T
Após ionização, à temperatura T, uma solução aquosa de CH3COOH apresenta um pH de 2,6.
1.3.1. Determine a concentração de CH3COOH em equilíbrio, à temperatura T.
Apresente todos os cálculos etetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Cálculo da concentração de H3O+ em equilíbrio:
- pH = – log [H3O+] ⇔ [H3O+] = 10-2,6 ⇔ [H3O+] = 2,51 x 10-3 mol dm-3
Cálculo da concentração de CH3COOH em equilíbrio:
Desprezando a quantidade de proveniente da autoionização da água, e de acordo com a estequiometria da reação de ionização do ácido etanóico.
- [ CH3COO– ] = [ H3O+ ] ⇒ 1 : 1
- [ CH3COO– ]e = [ H3O+ ]e = 2,51 x 10-3 mol dm-3
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula a concentração de H3O+ em equilíbrio (2,51 x 10-3 mol dm-3) ……….. 4 pontos
🛑 Calcula a concentração de CH3COOH em equilíbrio (0,35 mol dm-3) ………… 6 pontos
1.3.2. Qual das opções seguintes apresenta um par conjugado ácido-base resultante da ionização do ácido etanoico em água?
(A) CH3COOH (aq) / CH3COO– (aq)
(B) CH3COOH (ag) / H2O (l)
(C) CH3COO– (aq) / H3O+ (aq)
(D) CH3COO– (aq) / H2O (l)
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (A) ……………. 10 pontos
1.4. Fazendo reagir etanol com ácido etanoico, obtém-se etanoato de etilo, CH3COOCH2CH3, e água, num equilíbrio traduzido por
CH3CH2OH (l) + CH3COOH (l) ⇋ CH3COOCH2CH3 (l) + H2O (l)
1.4.1. Para otimizar o processo, pode recorrer-se ao uso de catalisadores e de um equipamento de laboratório que permite remover a água produzida.
Considere que a temperatura se mantém constante.
Quando se ______ , o quociente da reação, Q, passa a ser ______ à constante de equilíbrio, Kc.
(A) adicionam os catalisadores … superior
(B) remove a água produzida … superior
(C) remove a água produzida … inferior
(D) adicionam os catalisadores … inferior
- Opção (C)
🛑 A adição de catalisadores não tem efeito sobre a posição de equilíbrio da reação. O papel dos catalisadores é, exclusivamente, aumentar a velocidade da reação, mantendo-se Q = Kc.
Como a temperatura se mantém constante, a constante de equilíbrio, Kc, também se mantém constante.
🛑 Se for removida a água produzida, (produto da reação), o quociente da reação, Q, torna-se inferior a Kc.
🛑 Para se atingir um novo estado de equilíbrio, isto é, para que iguale , as concentrações dos produtos devem aumentar, ou seja, ocorre uma evolução do sistema no sentido direto.
- Opção (C) ……………. 10 pontos
1.4.2. Num laboratório, juntaram-se 40,0 g de CH3COOH (M = 60,06 g mol-1) a etanol em excesso e obtiveram-se 40,0 g de CH3COOCH2CH, (M = 88,12 g mol-1).
Determine o rendimento da reação.
Apresente todos os cálculos etetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Determinação da quantidade de CH3COOCH2CH3 máxima produzida, isto é, se a reação fosse completa:
- Se o etanol está em excesso, o reagente limitante é o ácido etanoico ou acético.
A proporção estequiométrica 1 : 1 entre o reagente limitante e o produto acetato de etilo, prevê-se que se poderiam teoricamente originar 0,666 mol de CH3COOCH2CH3
Determinação do rendimento da reação:
A quantidade de efetivamente produzida
O rendimento da reação é
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula a massa de CH3COOCH2CH3 que se formaria a partir do reagente limitante se a reação fosse completa (58,69 g) ……….. 5 pontos
🛑 Calcula o rendimento da reação (68,2 %) ………… 5 pontos
2. Os primeiros termómetros baseavam-se na dilatação regular de uma substância líquida termométrica perante o aumento de temperatura.
Galileu Galilei foi um dos primeiros construtores de termómetros, tendo usado a água como substância termométrica.
Posteriormente, foram desenvolvidos termómetros de etanol, por Ole Römer, Gabriel Fahrenheit e outros.
2.1. Na tabela, estão registadas temperaturas aproximadas de fusão e de ebulição de duas substâncias termométricas, à pressão normal.
Uma vantagem do uso do etanol como substância termométrica, relativamente à água, é permitir a medição de temperaturas (à pressão normal)
(A) entre -114 °C e 0 °C.
(B) abaixo de -114 °C.
(C) entre 78 °C e 100 °C.
(D) acima de 100 °C.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (A)
Como os termómetros se baseavam na dilatação de uma substância termométrica no estado líquido, e de acordo com os valores da tabela (água de 0 ºC a 100 ºC ; álcool de -114 ºC a 78 ºC ):
🛑 O álcool está no estado gasoso acima de 78ºC.
🛑 O álcool está no estado sólido abaixo de -114 ºC.
- O uso de etanol como substância termométrica, em relação à água (ponto de fusão 0 ºC), permite a medição de temperaturas entre -114 ºC e 0 ºC.
- Opção (A) ……………. 10 pontos
2.2. A verificação experimental de que a resistência elétrica de certos metais variava com a temperatura permitiu o desenvolvimento dos termómetros de resistência (termorresistências).
Uma termorresistência pode ser construída enrolando um fio de cobre que, posteriormente, é percorrido por uma corrente elétrica.
O enrolamento do fio de cobre, ao ser mergulhado num líquido a uma determinada temperatura, θ, acaba por atingir essa temperatura.
As medições da diferença de potencial nos terminais do enrolamento e da corrente elétrica que o percorre permitem obter a resistência elétrica, R, do fio de cobre.
A determinação de R, por sua vez, permite obter a temperatura, θ, do líquido.
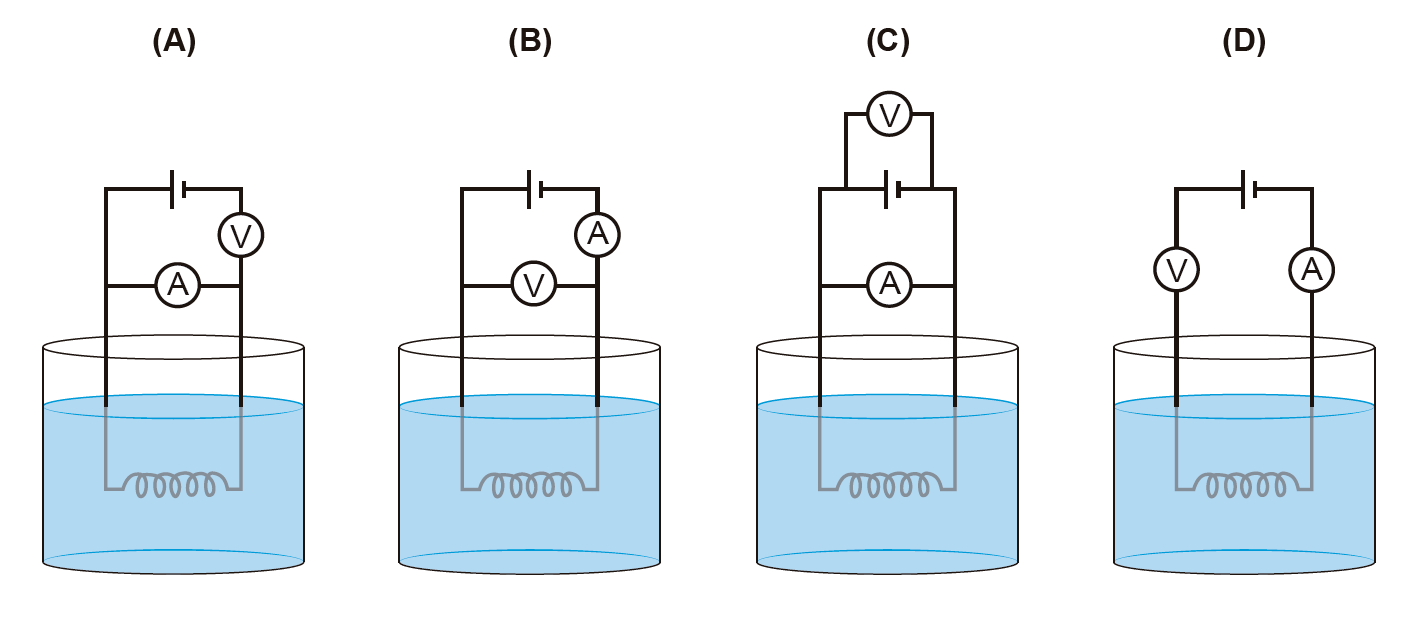
2.2.1. Qual dos esquemas seguintes pode representar o circuito elétrico do termómetro de resistência, acima descrito?
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (B) ……………. 10 pontos
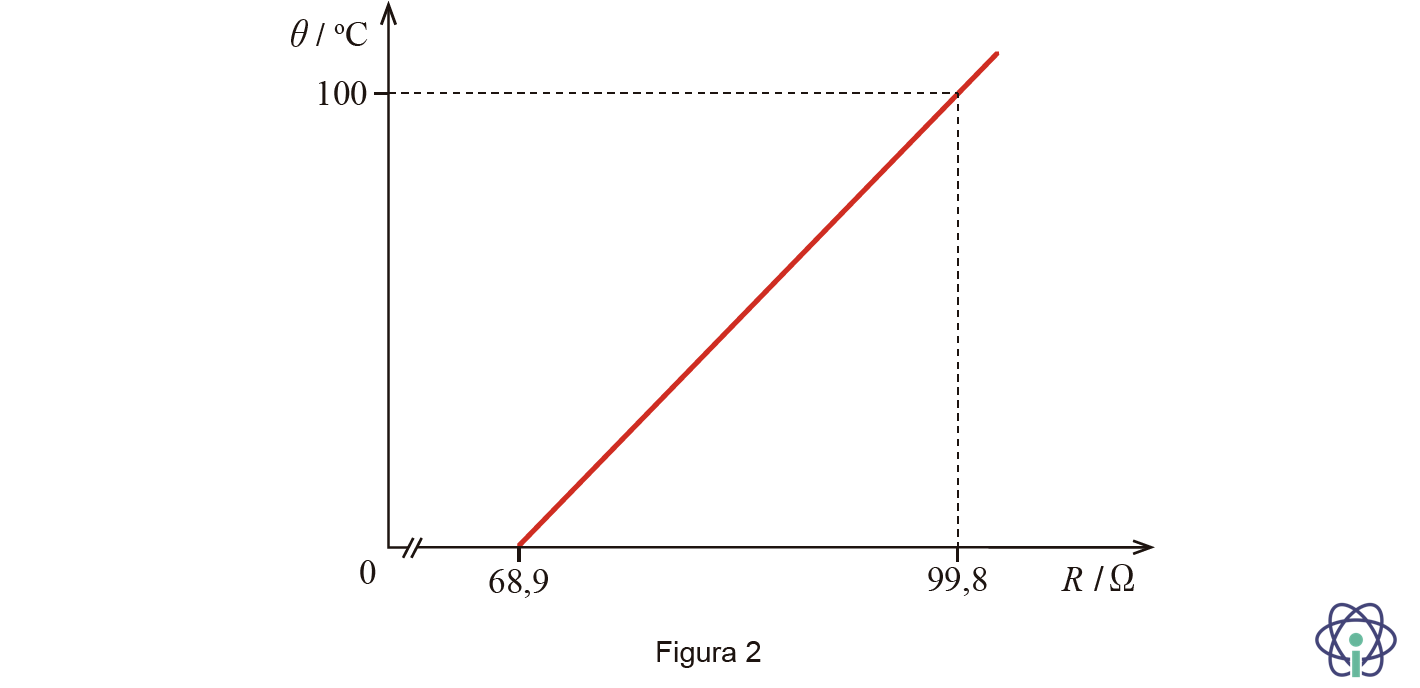
2.2.2. O gráfico da Figura 2 mostra a reta de calibração de uma termorresistência.
Admita que o fio de cobre apresenta um comportamento óhmico e que, depois de entrar em equilíbrio térmico com um líquido a uma certa temperatura, A, o fio foi atravessado por uma corrente elétrica de 36,9 mA, estando sujeito a uma diferença de potencial de 3,00V nos seus terminais
Determine a temperatura, e, do líquido.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula a resistência R (81,30 Ω) (ver nota) ………… 3 pontos
🛑 Calcula o declive da reta de calibração (3,236 ºC / Ω) (ver nota) ………… 3 pontos
🛑 Calcula a temperatura, θ, do líquido (40,1 ºC) ………… 4 pontos
Nota ‒ A ordem das duas primeiras etapas é arbitrária.
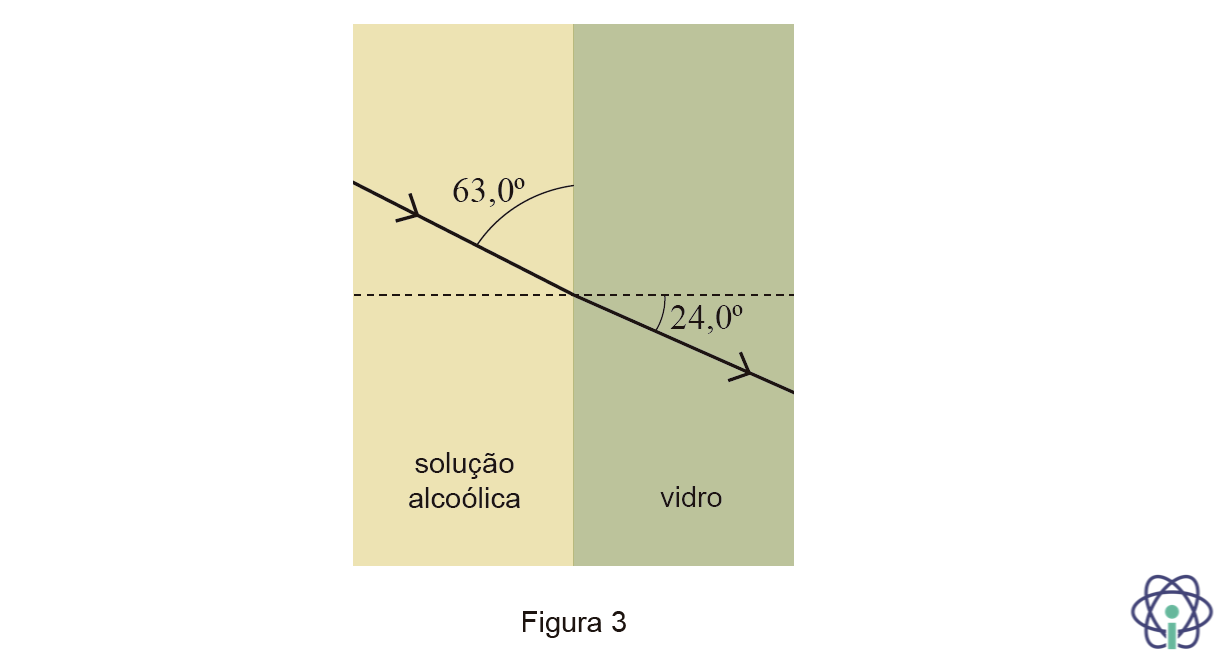
3. Uma solução alcoólica é armazenada numa garrafa de vidro.
Um feixe de luz, que se propaga na solução alcoólica, sofre um desvio na sua direção de propagação ao atravessar a superfície de separação entre a solução alcoólica e o vidro, como se representa na Figura 3
Considere que a velocidade do feixe de luz no vidro é 1,97 x 108 ms-1
Determine o índice de refração da solução alcoólica.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula o índice de refração do vidro (1,523) ……….. 4 pontos
🛑 Calcula o índice de refração da solução alcoólica (1,36) ………… 6 pontos
4. A presença de etanol, CH3CH2OH (M = 46,08 g mol-1), num indivíduo pode ser detetada por diferentes métodos.
4.1. Um dos métodos utilizados envolve um alcoolímetro.
No alcoolímetro, o etanol presente no ar expirado reage com o dioxigénio, O2, presente no ar, sendo convertido em ácido etanoico, CH3COOH.
Esta reação pode ser traduzida por
CH3CH2OH (g) + O2 (g) → CH3COOH (g) + H2O (g)
Considere que o ar contém 21%, em volume, de O2 e admita que o volume molar de um gás à temperatura e à pressão a que ocorre a reação é 24,0 dm3 mol-1.
Qual das expressões seguintes permite calcular, em dm3, o volume de ar necessário à reação completa de 0,0275 g de CH3CH2OH?
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (B) ……………. 10 pontos
4.2. Um condutor ingeriu duas canecas de cerveja contendo, cada uma, 0,50 L com 5,2%, em volume, de СН3СН2ОН.
Uma hora depois, o condutor foi submetido a uma análise laboratorial, tendo sido detetados 0,64 g de CH3CH2OH por litro de sangue.
Considere que:
- nem todo o etanol ingerido chega à corrente sanguínea;
- o condutor tem 6,0 L de sangue, e o seu organismo removeu, na primeira hora, 8,5 g de CH3CH2OH da corrente sanguínea;
- a massa volúmica do etanol é 0,789 g cm-3, à temperatura e à pressão do organismo do condutor.
Mostre que 30%, em massa, do CH3CH2OH ingerido chegou à corrente sanguínea durante a primeira hora, após a ingestão das duas canecas de cerveja.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
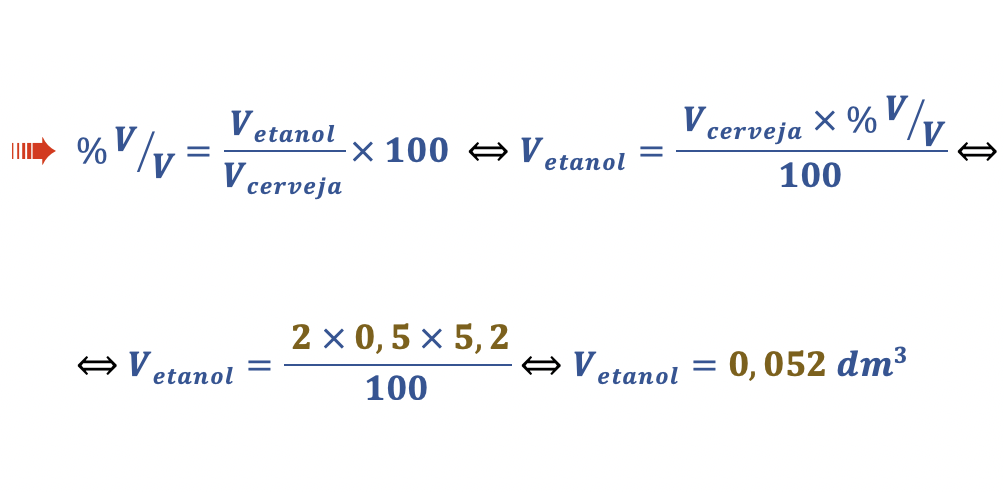
Cálculo da massa de etanol ingerido inicialmente:
Cálculo da massa de etanol no sangue do condutor após 1 hora:
Cálculo da massa de etanol que chegou ao sangue durante a primeira hora:
- mtotal = 3,84 + 8,5 = 12,3 g
Cálculo da percentagem, em massa, de etanol ingerido que chegou ao sangue durante a primeira hora:
Elementos de resposta:
🛑 Calcula a massa de CH3CH2OH inicialmente ingerido (41,0 g);
🛑 Calcula a massa de CH3CH2OH em 6 L de sangue do condutor, 1 h após a ingestão das cervejas (3,84 g);
🛑 Calcula a percentagem, em massa, de CH3CH2OH ingerido que chegou à corrente sanguínea durante a primeira hora, após a ingestão das duas canecas de cerveja (30%).
4.3. O primeiro dispositivo prático para a deteção de álcool no organismo humano ficou conhecido como «teste do balão».
A presença de CH3CH2OH no ar expirado era detetada por uma alteração de cor, devida à reação traduzida por
2 Cr2O72– + 16 H+ + 3 CH3CH2OH → 4 Cr3+ + 3 CH3COOH + 11 H2O
(laranja) (verde)
Na presença de CH3CH2OH, observa-se a cor ______ , sendo o Cr2O72- a espécie ______ .
(A) laranja … oxidante
(B) laranja … redutora
(C) verde … redutora
(D) verde … oxidante
- Opção (D)
🛑 O Cr3+ é um produto da reação de cor verde (o ácido etanoico e a água são incolores).
🛑 O número de oxidação do cromo em Cr2O72- é +6 e em Cr3+ é +3.
🛑 A variação do número de oxidação do cromo, Cr2O72-, é 3 – 6 = -3 .
🛑 O número de oxidação diminuiu, ocorreu um ganho de eletrões.
- A espécie foi reduzida, atuou como agente oxidante.
- Opção (D) ……………. 10 pontos
5. O tempo de reação é o intervalo de tempo entre a geração de um estímulo (visual, auditivo ou outro) e a resposta motora.
5.1. Na condução, sob o efeito de álcool, há um aumento do tempo de reação e, consequentemente, do risco de acidentes rodoviários.
Um condutor, ao observar um obstáculo na estrada, reage e coloca o pé no travão até imobilizar o veículo.
Considere t = 0 s o instante em que o condutor observa o obstáculo.
Na Figura 4, apresentam-se os gráficos do módulo da velocidade, v, de um condutor (sistema veículo + condutor), em função do tempo, t, quando estava sóbrio e quando se encontrava sob o efeito de álcool.
Sob o efeito de álcool, o condutor percorreu mais ______ do que quando estava sóbrio.
(A) 70,0 m
(B) 37,5 m
(C) 17,5 m
(D) 87,5 m
- Opção (C)
🛑 De acordo com a figura, verifica-se que o condutor sob o efeito do álcool levou 1,5 s a reagir, e, se estivesse sóbrio, levaria 0,8 s.
🛑 O intervalo de tempo entre as duas situações é:
- Δt = 1,5 – 0,8 = 0,7 s
🛑 Como a velocidade é constante, o condutor percorreu mais :
- d = v Δt ⇔ d = 25 x 0,7 ⇔ d = 17,5 m
- Opção (C) ……………. 10 pontos
5.2. Considere a experiência seguinte, que permite estimar o tempo de reação de uma pessoa recorrendo unicamente a uma régua.
Uma pessoa, A, segura a extremidade superior de uma régua posicionada verticalmente, enquanto outra pessoa, B, coloca a sua mão na parte inferior da régua, na marcação O cm, sem a segurar.
A pessoa A larga a régua, e a pessoa B, sem alterar a posição da mão, segura-a, tal como é ilustrado na Figura 5.
Considere desprezável a resistência do ar.
Deduza a expressão matemática que permite estimar o tempo de reação da pessoa B, com base na medição a efetuar nesta experiência.
Na sua resposta, explicite o significado da grandeza que consta na expressão e que é medida nesta experiência.
Utilize uma linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
6. Algumas condições estruturais das vias rápidas e autoestradas contribuem para a segurança rodoviária na circulação de veiculos.
Nas saídas das autoestradas, constroem-se vias aproximadamente circulares para efetuar alterações de sentido e rampas de emergência para diminuir drasticamente o módulo da velocidade.
6.1. Numa determinada via, um automóvel realiza uma trajetória circular, de raio 85 m, como se representa na Figura 6.
Considere que o automóvel tem energia cinética constante de 2,40 x 105 J.
Qual é a intensidade da resultante das forças que atuam no automóvel, enquanto este percorre esta via?
(A) 5,6 x 103 N
(B) 2,8 x 103 N
(C) 4,1 x 107 N
(D) 2,0 x 107 N
- Opção (A) ……………. 10 pontos
6.2. Um camião em movimento num percurso retilíneo, de desnível acentuado, sofre uma falha no sistema de travagem.
O motorista dirige o camião para uma rampa de emergência com inclinação α, de acordo com a Figura 7.
Admita que o camião pode ser representado pelo seu centro de massa (modelo da partícula material) e que são desprezáveis todas as forças dissipativas que nele atuam ao longo da rampa de emergência.
Numa determinada ocasião, um camião de 1,3 x104 kg entra numa rampa de emergência com uma inclinação de 12°. A velocidade inicial do camião é, em módulo, 130 km h-1 e, nesta circunstância, o camião percorre uma distância, d, até parar.
Considere a existência de outras situações, em que se altera apenas uma das condições: módulo da velocidade inicial do camião, massa do camião ou inclinação da rampa de emergência.
Associe cada uma das situações, expressas na Coluna l, a uma das descrições da variação da distância percorrida pelo camião na rampa de emergência, até parar, que constam na Coluna II.
Escreva, na folha de respostas, cada letra da Coluna l seguida do número correspondente da Coluna lI.
A cada letra corresponde apenas um número.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ (a) – (1)
⇒ (b) – (3)
⇒ (c) – (4)
Como as forças dissipativas são desprezáveis, a resultante das forças que atua sobre o camião é igual à componente tangencial da força gravítica (paralela à rampa).
- Fr = Fg sen α ⇔ ma = m g sen α ⇔ a = g sen α
O camião desloca-se na rampa de emergência com movimento retilíneo uniformemente retardado até se imobilizar (vf = 0 m s-1) e percorre a distância, d.
🛑 Dados da situação inicial
- m = 1,3 x 104 kg
- v0 = 36,1 m s-1
- α = 12º
🟡 Se o módulo da velocidade inicial do camião for 120 km/h
- m = 1,3 x 104 kg
- v0 = 33,3 m s-1
- α = 12º
🟡 Se a massa do camião for 1,0 x 104 kg
- m = 1,0 x 104 kg
- v0 = 36,1 m s-1
- α = 12º
A distância, é independente da massa do camião, logo a distância percorrida mantém-se igual à da situação inicial.
🟡 Se a inclinação da rampa de emergência for 10º
- m = 1,3 x 104 kg
- v0 = 36,1 m s-1
- α = 10º
- ……………. 10 pontos
🟡 (A) – (1) ;
🟡 (B) – (3) ;
🟡 (C) – (4) ;
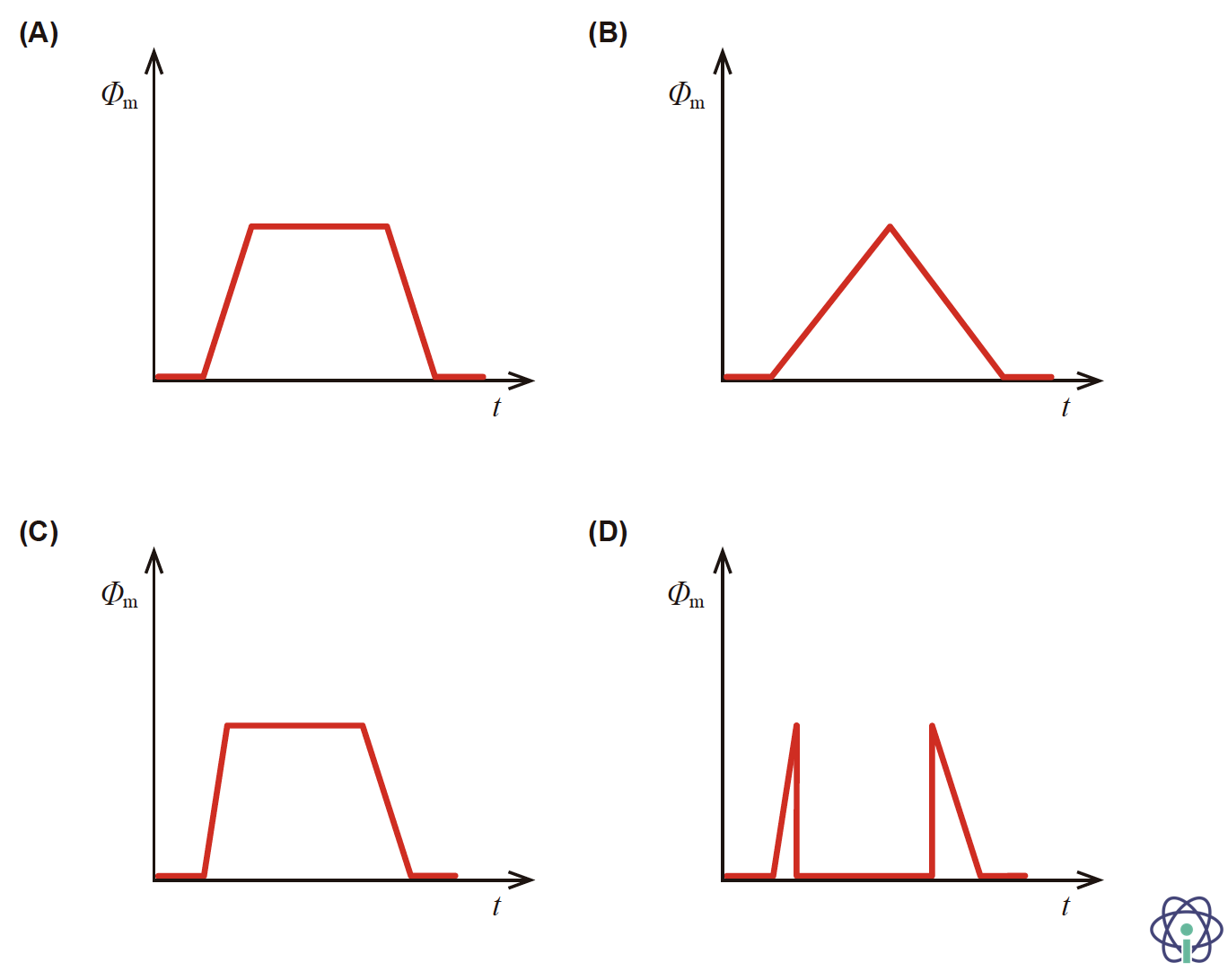
7. Uma espira metálica retangular, α, é colocada sobre um carrinho de fibra de vidro, e este sobe um plano inclinado com velocidade constante, atravessando uma região na qual foi criado um campo magnético uniforme, B, de direção perpendicular ao plano da espira, representado a sombreado na Figura 8.
Qual é o esboço do gráfico que pode representar o fluxo magnético, Φm, que atravessa a superfície delimitada pela espira, α, em função do tempo, t, à medida que o carrinho sobe o plano inclinado?
- Opção (A)
Dado que Φm = B A cos θ, e como o campo magnético tem a mesma direção da normal à superfície da espira:
- θ = 0º
- cos θ = 1
🛑 Antes de a espira atingir o campo magnético, o fluxo magnético, Φm
🛑 Durante a entrada da espira no campo magnético, a área A vai aumentando uniformemente, pelo que Φm aumenta linearmente até que toda a espira se encontre no interior do campo.
🛑 Enquanto a espira se desloca totalmente no interior do campo magnético, o fluxo magnético é máximo e mantém-se constante.
🛑 Como a velocidade é constante durante todo o trajeto, durante a saída da espira do campo magnético, o fluxo magnético diminui com módulo igual ao aumento verificado durante a entrada.
- Opção (A) ……………. 10 pontos
8. Em 1814, um físico detetou, no espectro do Sol, uma série de riscas negras que viriam a ser conhecidas como riscas de Fraunhofer.
Alguns anos depois, seria um químico, R. Bunsen, a identificar a causa destas riscas negras no espectro solar. No laboratório, Bunsen observou que certas substâncias, ao serem aquecidas no bico de Bunsen (testes de chama), originavam espectros de linhas brilhantes característicos e relacionou, para determinados elementos químicos, espectros de absorção com espectros de emissão.
Atualmente, a pesquisa de elementos químicos também é feita na atmosfera de exoplanetas. Na atmosfera do planeta WASP-121 b, foram inicialmente detetados dois elementos: o cálcio e um outro, aqui designado por X, letra que não corresponde ao símbolo do elemento químico. Recentemente, também foi detetada a presença de bário na atmosfera do exoplaneta.
8.1. Para determinar as energias de remoção dos eletrões dos átomos, utiliza-se a espectroscopia fotoeletrónica (PES).
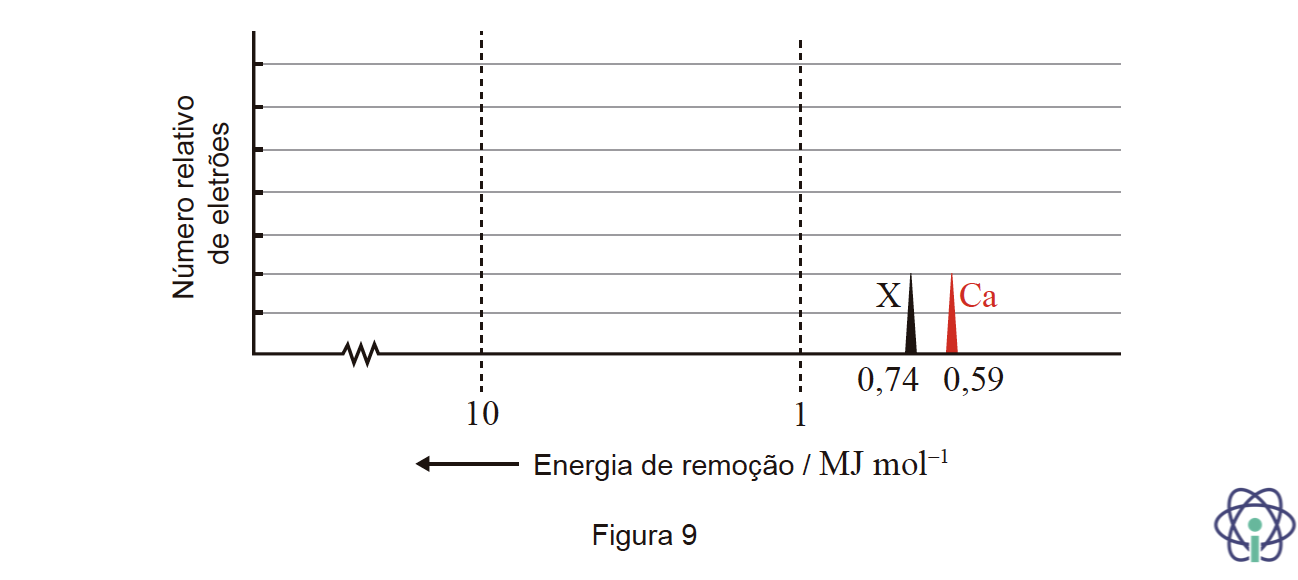
A Figura 9 mostra um excerto do espectro de dois elementos, do bloco s da Tabela Periódica, presentes na atmosfera do WASP-121 b, o Ca e o elemento X. No excerto, figuram as energias de remoção dos eletrões de valência destes dois elementos.
Os dois elementos pertencem ao mesmo ______ da Tabela Periódica, tendo o elemento X um número atómico ______ ao do cálcio.
(A) período … inferior
(B) grupo … inferior
(C) período … superior
(D) grupo … superior
- Opção (B)
🛑 A energia de remoção é a energia mínima necessária para extrair um eletrão (de um determinado subnível de energia En) de um átomo no estado gasoso e no estado fundamental, originando um catião monopositivo:
- Erem = E∞ – En = – En
🛑 Os eletrões com menor energia de remoção são aqueles que ocupam níveis de maior energia.
🛑 No caso da Figura reportam-se energias de remoção de eletrões de valência de dois elementos X e do bloco s; como 0,74 > 0,59, não podem ser de dois elementos do mesmo período.
🛑 O elemento vizinho do Ca na Tabela Periódica, com menor número atómico, o potássio, tem menos um protão, logo menor atração núcleo-eletrão e, consequentemente, menor energia de remoção.
🛑 Os outros elementos do mesmo período não são do bloco s.
🛑 O elemento X pertence, assim, ao mesmo grupo do cálcio e, como apresenta maior energia de remoção, tem de ter menor número atómico.
🛑 Para elementos do mesmo grupo, quanto menor for o número atómico, menor é o número de níveis de energia, menor é o número de eletrões internos e, consequentemente, a atração efetiva entre o núcleo e um dos seus eletrões mais externos aumenta.
- O elemento X deve ser o magnésio, dado que é do mesmo grupo do cálcio e tem maior carga nuclear efetiva (menor blindagem)
- Opção (B) ……………. 10 pontos
8.2. Uma amostra de um sal desconhecido foi aquecida com uma chama. Com um espectroscópio, obteve-se o seu espectro na região do visível.
Na Figura 10, representam-se o espectro da amostra e os espectros atómicos de X e do bário.
Complete o texto seguinte, selecionando a opção adequada a cada espaço.
Escreva, na folha de respostas, cada uma das letras seguida do número que corresponde à opção selecionada. A cada letra corresponde um só número.
De acordo com a informação da Figura 10, a amostra contém catiões de __ (a) __, uma vez que o seu espectro __ (b) __ tem riscas que resultam da __ (c) __ dos iões desse (s).
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ (a) – (2)
⇒ (b) – (1)
⇒ (c) – (2)
🛑 O espetro da amostra apresenta riscas coincidentes com o espetro do bário.
🛑 Cada risca do espetro corresponde à emissão de radiações eletromagnéticas com energia bem definida.
🛑 A energia é emitida na desexcitação dos átomos que inicialmente tinham sido excitados pela chama.
8.3. No Quadro I, indicam-se as cores das chamas associadas à presença de alguns catiões.
Numa aula de laboratório, realizou-se uma atividade que visava a identificação de catiões metálicos em três amostras distintas de alguns sais. Os catiões são representados por M, N, O, Te W (que não correspondem a simbolos químicos) e estão contemplados no Quadro l.
Para a atividade, os alunos dispunham de:
- cloreto de M, cloreto de N, cloreto de O, cloreto de T e cloreto de W;
- sulfato de M, sulfato de N, sulfato de O, sulfato de Te sulfato de W.
Os alunos embeberam pedaços de algodão em etanol, que colocaram em três cadinhos de porcelana, e adicionaram a mesma quantidade de cada um dos sais aos cadinhos.
Depois de provocar a ignição do etanol, observaram as cores presentes na chama.
Os resultados obtidos pelos grupos 1 e 2 foram registados no Quadro II.
Mostre, fundamentando, qual dos grupos não atingiu totalmente o objetivo da atividade.
Na sua resposta, explicite duas razões, uma relativa ao procedimento (controle de variáveis) e outra relativa à interpretação dos resultados obtidos.
Escreva um texto estruturado, utilizando linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- O grupo 2 não atingiu totalmente o objetivo proposto para a atividade.
🛑 Como os três sais escolhidos por este grupo não tinham o mesmo anião, não se podia comparar o efeito do anião de cada sal na cor da chama.
🛑 A cor obtida com o sulfato de M registada no Quadro II pelo grupo 2 não coincide com nenhuma das incluídas no Quadro I fornecido, não permitindo conclusões.
Elementos de resposta:
🛑 Identifica o grupo que não atingiu totalmente o objetivo da atividade (grupo 2);
🛑 Explicita uma razão relativa ao procedimento (refere que não foi controlado o efeito do anião do sal na cor da chama, porque os três sais estudados não eram constituídos pelo mesmo anião);
🛑 Explicita uma razão relativa à interpretação dos resultados obtidos (refere que uma das amostras do grupo 2, o sulfato de M, apresenta um resultado inconclusivo, porque a cor observada não coincide com nenhuma das cores indicadas no Quadro I).
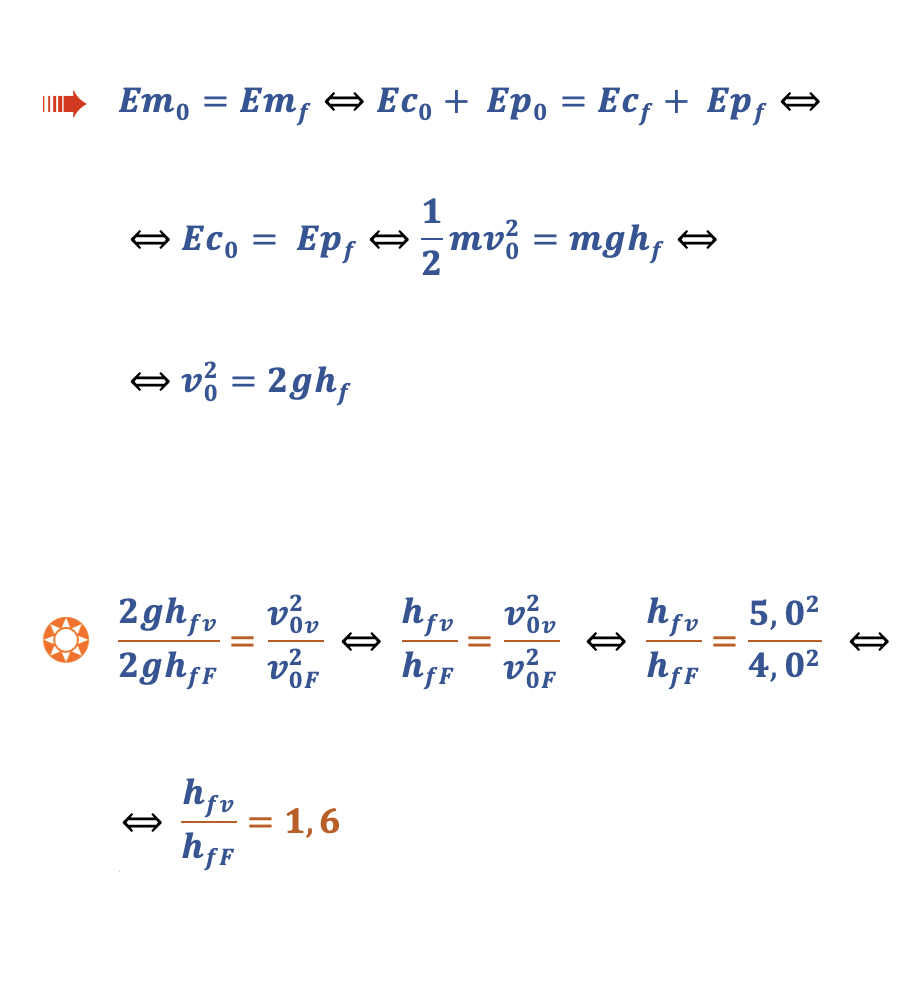
9. Uma bola de voleibol, V, e uma bola de futebol, F, foram lançadas verticalmente, de baixo para cima, a partir da mesma posição, Y, com velocidades iniciais de módulos 5,0 m s-1 e 4,0 m s-1, respetivamente, de acordo com a Figura 11.
Admita que:
- Y é o nível de referência da energia potencial gravítica;
- a resistência do ar é desprezável;
- as bolas podem ser representadas pelo seu centro de massa modelo da partícula material).
9.1. Determine, mediante considerações energéticas, a razão entre a altura máxima atingida pela bola de voleibol, Ymáx, v, e a altura máxima atingida pela bola de futebol, Ymáx, F.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
🛑 Como a resistência do ar é desprezável, a energia mecânica de cada uma das bolas, durante a subida, é constante.
🛑 Partem da posição zero e atingem a altura máxima, altura final, com velocidade nula, pode escrever-se:
- A relação entre a altura máxima atingida pela bola de voleibol e a atingida pela bola de futebol é 1,6 .
9.2.
Determina o valor solicitado, percorrendo as etapas seguintes:
🛑 Calcula, considerando ΔEp = – ΔEc , ymáx, v (1,28 m) …….. 4 pontos
🛑 Calcul, considerando ΔEp = – ΔEc , ymáx, F (0,816 m) …….. 4 pontos
🛑 Calcula ymáx, v/ymáx, F (1,6) …….. 2 pontos
9.2. Considere que a bola de voleibol foi lançada no instante t = 0 s e que a bola de futebol foi lançada 3 s depois.
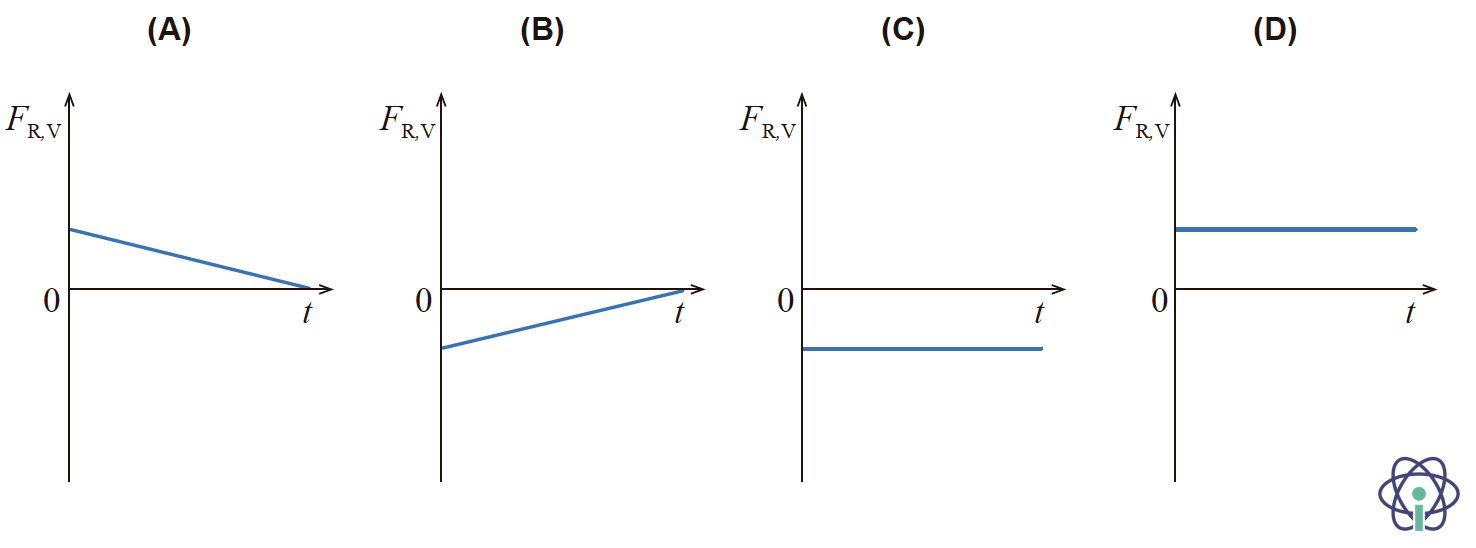
9.2.1. Qual dos esboços seguintes pode representar a componente escalar da força resultante que atua na bola de voleibol, Frv, em função do tempo, t, desde o instante em que a bola é lançada até ao instante em que atinge a altura máxima?
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (C) ……………. 10 pontos
9.2.2. Qual das opções seguintes pode representar a equação que permite obter a componente escalar da velocidade da bola de futebol, v, em função do tempo, t, expressa nas unidades base do SI?
(A) vF = 4,0 + 9,80 (t – 3) se t ≥ 3
(B) vF = 4,0 – 9,80 (t – 3) se t ≥ 3
(C) vF = 4,0 + 9,80 (t + 3) se t ≥ 3
(D) vF = 4,0 – 9,80 (t + 3) se t ≥ 3
- Opção (B)
Como a origem do tempo (t = 0 s) é o instante em que a bola de voleibol foi lançada, e a bola de futebol foi lançada depois, então tF = t – 3 s.
Como o movimento da bola de futebol é uniformemente variado, a equação da componente escalar da velocidade da bola é:
🛑 vF = v0F – g (t – 3) (SI)
🛑 vF = 4,0 – 9,80 x (t – 3) para t ≥ 3 s
- Opção (B) ……………. 10 pontos