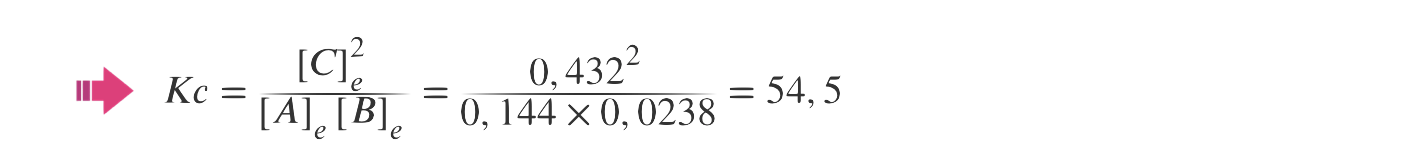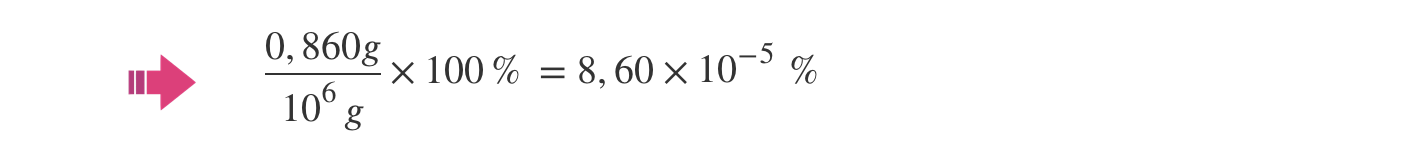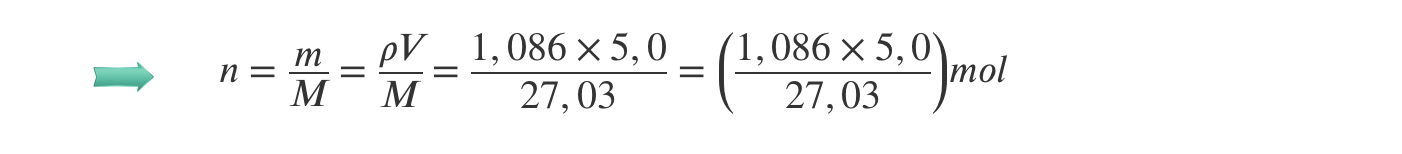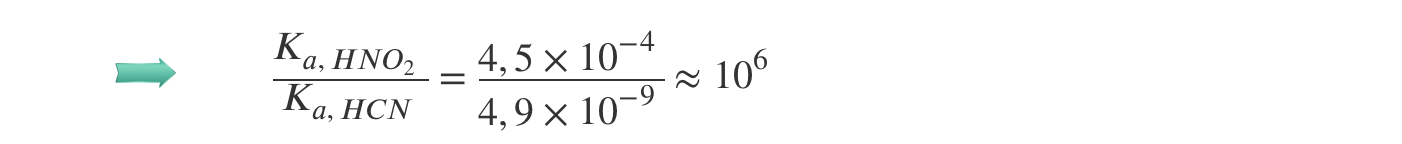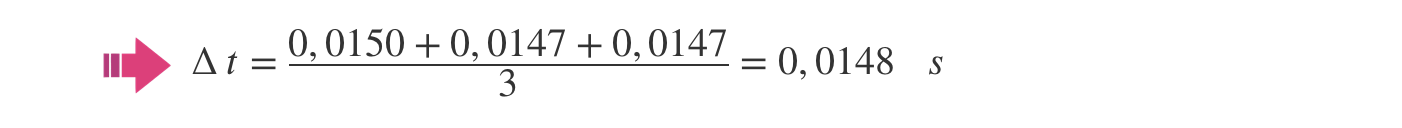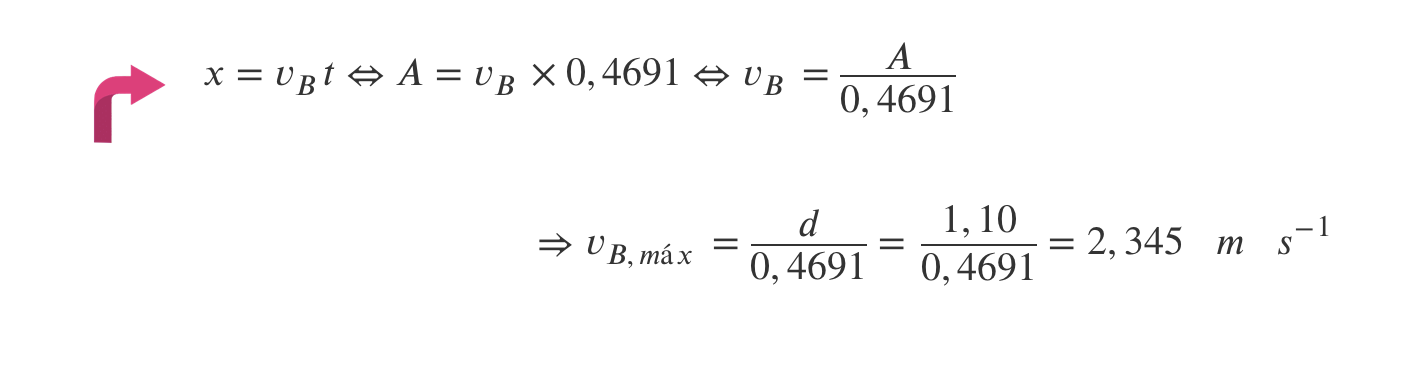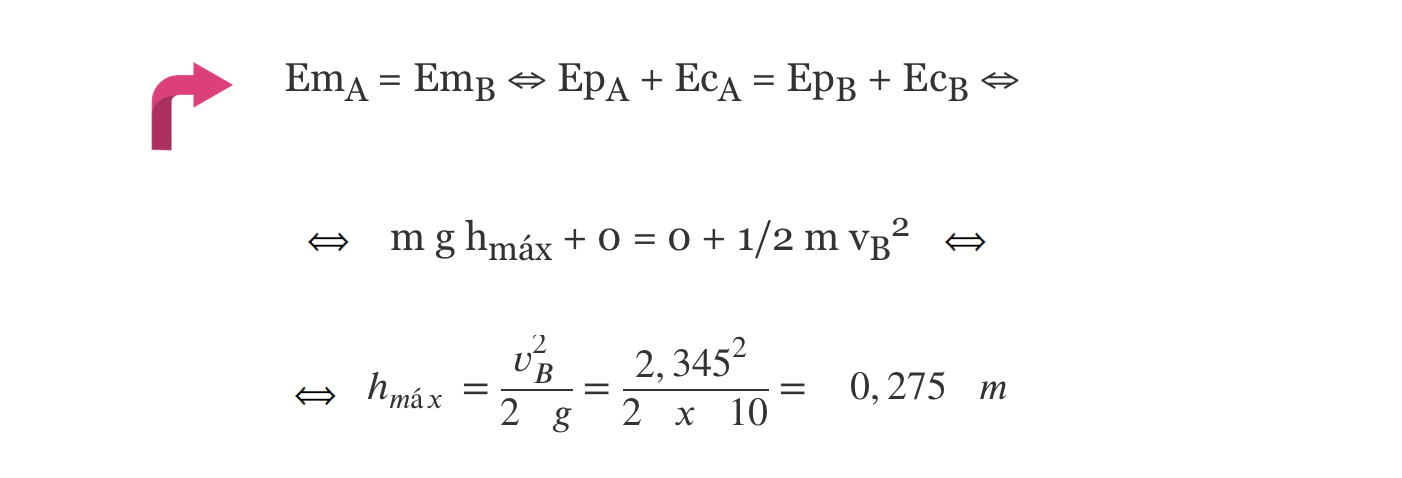2013 – 1ªFase – Prova Escrita de FQ A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: 1.ª Fase – 2013
GRUPO I
Quando um sistema químico, no qual ocorra uma reação química reversível, se encontra num estado de equilíbrio – o que, em rigor, só é possível se não houver trocas, nem de matéria nem de energia, entre o sistema e o exterior –, as concentrações dos reagentes e dos produtos envolvidos na reação mantêm-se constantes ao longo do tempo, não existindo alterações visíveis no sistema.
O facto de as propriedades macroscópicas de um sistema químico em equilíbrio não sofrerem alteração pode sugerir que terá deixado de ocorrer qualquer reação. No entanto, a nível molecular, tanto a reação direta, na qual os reagentes se convertem em produtos, como a reação inversa, na qual os produtos se convertem em reagentes, continuam efetivamente a dar-se, em simultâneo, ocorrendo ambas à mesma velocidade. O equilíbrio químico não significa, portanto, ausência de reação.
Assim, num sistema químico em equilíbrio, os reagentes e os produtos encontram-se todos presentes, em simultâneo, em concentrações que não variam ao longo do tempo.
Baseado em A. Pereira e F. Camões, Química 12.o ano, 2001
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
1. Identifique uma das «propriedades macroscópicas» a que o texto se refere.
—————————————————————————————————————————————————————————————————-
⇒ Concentrações de reagentes ou concentrações de produtos ou temperatura ou pressão.
⇒ Composição química ou concentração [de reagentes e de produtos]
ou
⇒ Temperatura
ou
⇒ Pressão
ou
⇒ Volume
ou
⇒ Densidade. ………….. 5 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
2. O equilíbrio que se estabelece num sistema químico é dinâmico porque
(A) as concentrações dos reagentes e dos produtos se mantêm constantes ao longo do tempo.
(B) não existem alterações visíveis no sistema.
(C) tanto a reação direta como a reação inversa se continuam a dar.
(D) os reagentes e os produtos se encontram todos presentes, em simultâneo.
- Opção (C)
⇒ O equilíbrio é dinâmico porque as reações químicas não cessam.
⇒ No equilíbrio, os reagentes continuam a transformar-se em produtos e vice-versa, ocorrendo essas transformações à mesma velocidade.
- Opção (C) …………. 5 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
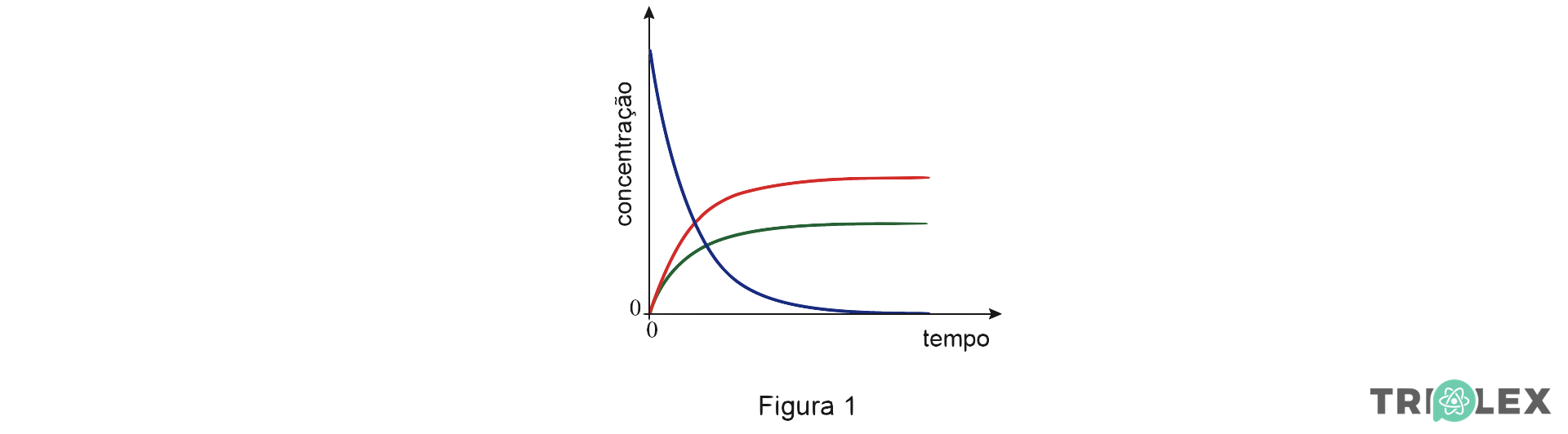
3. A Figura 1 apresenta o esboço do gráfico da concentração, em função do tempo, de três espécies que participam numa reação química.
Transcreva do texto a afirmação que permite justificar que o esboço do gráfico apresentado não pode traduzir o estabelecimento de um estado de equilíbrio químico.
⇒ “Assim, num sistema químico em equilíbrio, os reagentes e os produtos encontram-se todos presentes, em simultâneo, em concentrações que não variam ao longo do tempo.”
- «[…] num sistema químico em equilíbrio, os reagentes e os produtos encontram-se todos presentes, em simultâneo […]» …………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
4. «[…] se não houver trocas, nem de matéria nem de energia, entre o sistema e o exterior […]», o sistema químico será um sistema
(A) fechado e a sua energia interna manter-se-á constante.
(B) isolado e a sua energia interna manter-se-á constante.
(C) fechado e a sua energia interna variará.
(D) isolado e a sua energia interna variará.
- Opção (B)
⇒ Como não há trocas de matéria nem de energia, o sistema é isolado.
⇒ A energia interna de um sistema isolado não varia dado que o sistema não cede nem recebe energia.
- Opção (B) …………. 5 pontos
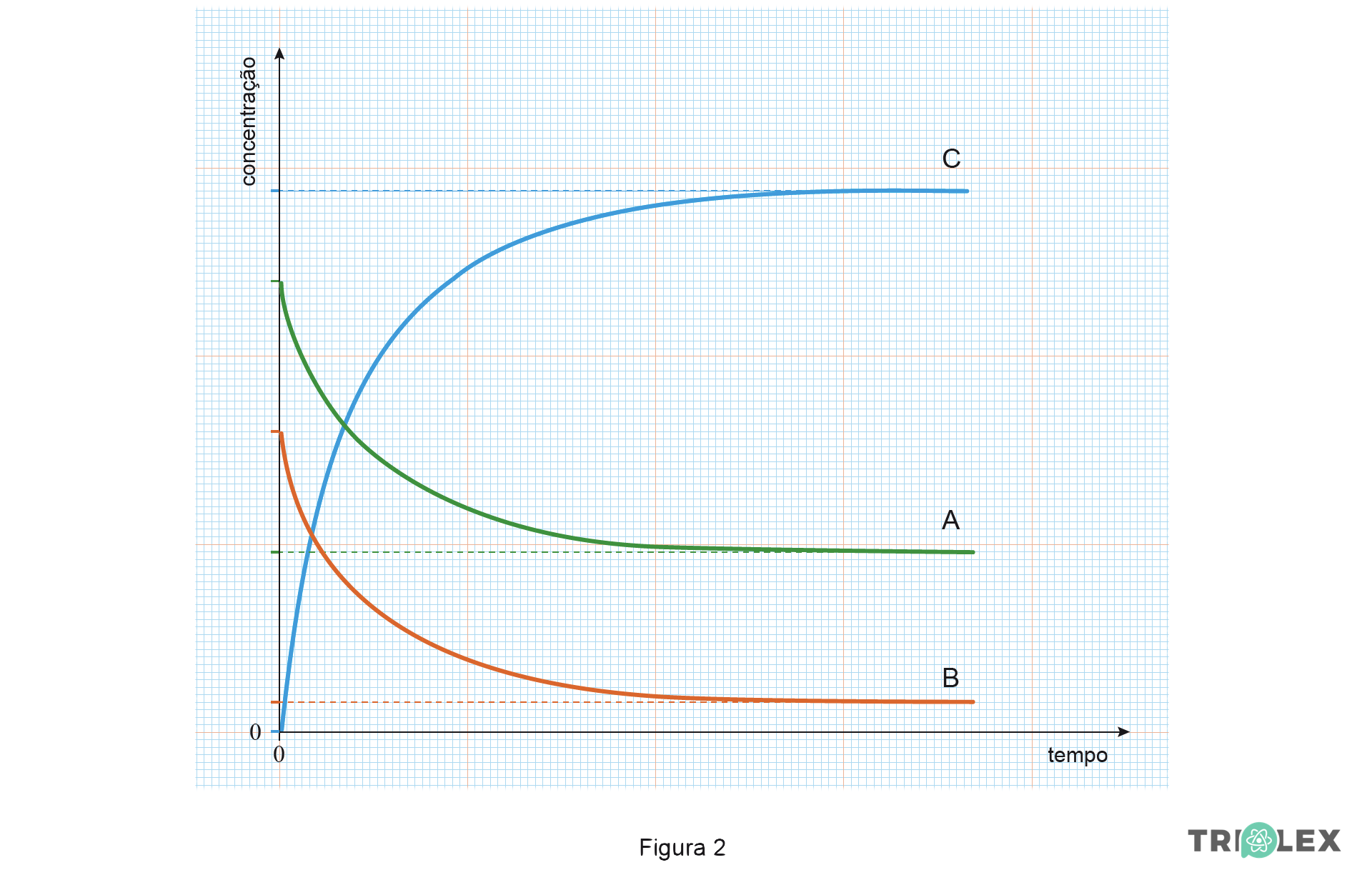
5. A Figura 2 apresenta o gráfico que traduz a evolução da concentração, ao longo do tempo, das espécies A, B e C que intervêm numa reação química em fase gasosa, à temperatura T.
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
5.1 Na tabela seguinte, estão registadas concentrações de equilíbrio das espécies A, B e C, relativas a um mesmo estado de equilíbrio do sistema químico, à temperatura T.
Determine a constante de equilíbrio, Kc, da reação considerada, à temperatura T.
Apresente todas as etapas de resolução.
- Estabelecimento da proporção estequiométrica de reagentes e produtos da reação:
Em unidades arbitrárias, a concentração de C aumenta de 14,4 unidades e as concentrações de A e de B diminuem ambas de um valor correspondente a metade do aumento de C, 7,2 unidades; conclui-se que 1 mole de A reage com 1 mole de B, formando-se 2 moles de C (a estequiometria é 1 mole A : 1 mole B : 2 moles C) e a equação pode ser escrita como: A (g) + B (g) ⇋ 2 C (g)
- Cálculo da constante de equilíbrio:
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Indicação da estequiometria da reação considerada (1 mol A : 1 mol B : 2 mol C).
B) Cálculo da constante de equilíbrio da reação considerada, à temperatura T (Kc = 54,4).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
5.2 Considere que a reação de formação da espécie C é uma reação exotérmica.
Conclua, justificando, como variará a constante de equilíbrio, Kc, da reação considerada se a temperatura aumentar.
⇒ De acordo com o Princípio de Le Châtelier, o aumento de temperatura favorece a transformação que ocorre com absorção de energia (reação endotérmica) isto é, o sentido em que se retira energia do meio.
⇒ Como a reação direta, a de formação de C, é exotérmica, segue-se que a reação inversa, a de formação de A e B, é endotérmica. Assim, quando a temperatura aumenta a concentração de C diminui, aumentando as concentrações de A e B, pelo que se conclui que a constante de equilíbrio da reação:
- irá diminuir.
- Na resposta, são apresentados os seguintes tópicos:
A) De acordo com o Princípio de Le Châtelier, o aumento da temperatura favorece a reação endotérmica.
B) [Como a reação de formação da espécie C é exotérmica,] o aumento da temperatura conduz a uma diminuição da concentração da espécie C e a um aumento das concentrações das espécies A e B.
C) Conclui-se, assim, que a constante de equilíbrio da reação considerada diminuirá [se a temperatura aumentar].
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
GRUPO II
1. Uma lata contendo um refrigerante foi exposta à luz solar até ficar em equilíbrio térmico com a sua vizinhança.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1.1 Sob que forma foi transferida a energia do Sol para a lata?
⇒ Radiação
- Radiação …………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1.2 Quando o sistema lata + refrigerante ficou em equilíbrio térmico com a sua vizinhança, a temperatura média do sistema passou a ser constante.
Estabelecido o equilíbrio térmico, o sistema
(A) deixou de absorver energia do exterior.
(B) deixou de trocar energia com o exterior.
(C) passou a emitir e a absorver energia à mesma taxa temporal.
(D) passou a emitir e a absorver energia a taxas temporais diferentes.
- Opção (C)
⇒ No equilíbrio térmico a temperatura do sistema lata + refrigerante permanece constante, logo também a energia interna.
⇒ Para que a energia interna não varie, as energias emitida e absorvida, como radiação, por unidade de tempo, devem ser iguais.
- Opção (C)…………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1.3 A lata continha 0,34 kg de um refrigerante de capacidade térmica mássica 4,2 × 103 J kg-1 oC-1.
Considere que a área da superfície da lata exposta à luz solar era 1,4 × 102 cm2 e que a intensidade média da radiação solar incidente era 6,0 × 102 W m-2.
Verificou-se que, ao fim de 90 min de exposição, a temperatura do refrigerante tinha aumentado 16,5 oC.
Determine a percentagem da energia incidente na área da superfície da lata exposta à luz solar que terá contribuído para o aumento da energia interna do refrigerante, no intervalo de tempo considerado.
Apresente todas as etapas de resolução.
- Cálculo da energia incidente na lata no intervalo de tempo considerado:
⇒ A = 1,4 x 102 cm2 = 1,4 x 10-2 m2
⇒ Δt = 90 min = 90 x 60 s = 5,4 x 103 s
⇒ E incidente = P Δt = I A Δt = 6,0 x 102 x 1,4 x 10-2 x 5,4 x 103 = 4,54 x 104 J
- Cálculo da variação de energia interna do refrigerante no mesmo intervalo de tempo:
⇒ ΔU = E absorvida = m c Δt = 0,34 x 4,2 x 103 x 16,5 = 2,36 x 104 J
- Cálculo da percentagem da energia incidente na lata que contribui para o aumento da energia interna do refrigerante:
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo do aumento da energia interna do refrigerante, no intervalo de tempo considerado (ΔU = 2,36 × 104 J).
B) Cálculo da energia incidente na área da superfície da lata exposta à luz solar, no intervalo de tempo considerado (E = 4,54 × 104 J).
C) Cálculo da percentagem da energia incidente na área da superfície da lata exposta à luz solar que terá contribuído para o aumento da energia interna do refrigerante, no intervalo de tempo considerado (52%).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2. Uma cafeteira com água previamente aquecida foi abandonada sobre uma bancada até a água ficar à temperatura ambiente.
Conclua, justificando, se a taxa temporal de transferência de energia como calor, através das paredes da cafeteira, aumentou, diminuiu ou se manteve constante, desde o instante em que se abandonou a cafeteira com água sobre a bancada até ao instante em que a água ficou à temperatura ambiente.
⇒ Para o mesmo material, a mesma área de superfície e a mesma espessura das paredes, a taxa de transferência de energia como calor é diretamente proporcional à diferença de temperatura entre a água e o ambiente.
⇒ À medida que o tempo passa, a água vai arrefecendo, diminui a diferença de temperatura entre a água e o ambiente e, em consequência, diminui também a taxa temporal de transferência de energia, como calor, através das paredes da cafeteira.
- Na resposta, são apresentados os seguintes tópicos:
A) A taxa temporal de transferência de energia como calor, através das paredes da cafeteira, é tanto maior quanto maior for a diferença entre a temperatura a que se encontra a água e a temperatura ambiente.
ou
- A taxa temporal de transferência de energia como calor, através das paredes da cafeteira, é tanto menor quanto menor for a diferença entre a temperatura a que se encontra a água e a temperatura ambiente.
B) À medida que a temperatura a que se encontra a água diminui, essa diferença [de temperatura] diminui, pelo que a taxa temporal de transferência de energia como calor, através das paredes da cafeteira, diminui [desde o instante em que se abandonou a cafeteira sobre a bancada até ao instante em que a água ficou à temperatura ambiente].
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
GRUPO III
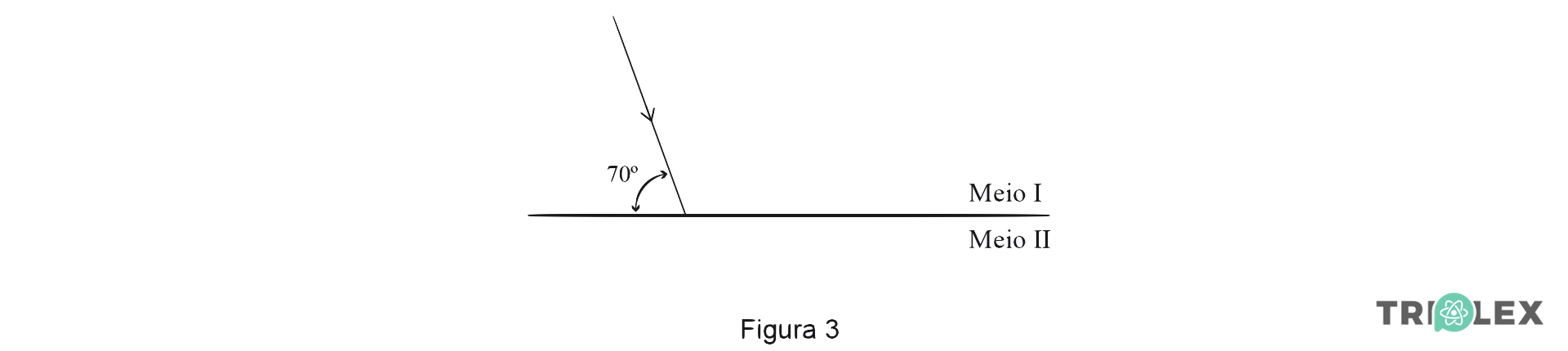
A Figura 3 representa um feixe de luz monocromática, muito fino, que incide na superfície de separação de dois meios transparentes, I e II.
Uma parte do feixe incidente sofre reflexão nessa superfície e outra parte é refratada, passando a propagar-se no meio II.
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
1. Qual é o ângulo entre o feixe incidente e o feixe refletido?
(A) 20o
(B) 40o
(C) 60o
(D) 70o
- Opção (B)…………. 5 pontos
2. Admita que, para a radiação considerada, o índice de refração do meio I é o dobro do índice de refração do meio II.
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
2.1 Comparando o módulo da velocidade de propagação dessa radiação nos meios I e II, respetivamente vI e vII, e o seu comprimento de onda nos meios I e II, respetivamente mI e mII, conclui-se que
(A) vI = 2 vII e λI = 2 λII
(B) vI = 2 vII e λI = ½ λII
(C) vI = ½ vII e λI = 2 λII
(D) vI = ½ vII e λI = ½ λII
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
2.2 Qual é o ângulo de incidência a partir do qual ocorre reflexão total da radiação considerada na superfície de separação dos meios I e II?
(A) 10o
(B) 28o
(C) 30o
(D) 40o
- Opção (C)…………. 5 pontos
GRUPO IV
1. O carbono é um elemento químico que entra na constituição de um grande número de compostos.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
1.1 Quantos valores diferenciados de energia apresentam os eletrões de um átomo de carbono no estado fundamental?
(A) Seis.
(B) Quatro.
(C) Três.
(D) Dois.
- Opção (C)
⇒ Configuração eletrónica do átomo de carbono no estado fundamental:
- 1s2 2s2 2p2
⇒ Existem eletrões com três valores diferenciados de energia: os da orbital 1s, os da orbital 2s e os das orbitais 2p que são degeneradas (as orbitais 2p têm a mesma energia).
- Opção (C)…………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
1.2 Qual das configurações eletrónicas seguintes pode corresponder a um átomo de carbono num estado excitado?
(A) 1s2 2s2 2px1 2py1 2pz0
(B) 1s2 2s1 2px1 2py1 2pz1
(C) 1s2 2s2 2px1 2py0 2pz1
(D) 1s2 2s1 2px0 2py0 2pz3
- Opção (B)
⇒ As configurações 1s2 2s2 2px1 2py1 2pz0 e 1s2 2s2 2px1 2py0 2pz1 correspondem ao estado fundamental do átomo de carbono.
⇒ A configuração 1s2 2s2 2px0 2py0 2pz3 é impossível dado que o número máximo de eletrões por orbital é de 2 e, nessa configuração, a orbital 2pz surge com 3 eletrões.
⇒ Na configuração 1s2 2s1 2px1 2py1 2pz1 um dos eletrões da orbital 2s foi promovido para uma das orbitais 2p.
⇒ O estado é excitado dado que a orbital 2p tem mais energia do que a 2s.
- Opção (B)…………. 5 pontos
2. O ião cianeto, CN–, constituído pelos elementos químicos carbono e nitrogénio, é muito tóxico.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2.1 O ião cianeto apresenta, no total, o mesmo número de eletrões que a molécula N2.
O ião CN– apresenta, assim, no total,
(A) catorze eletrões, seis dos quais são de valência.
(B) dez eletrões, sete dos quais são de valência.
(C) dez eletrões, seis dos quais são de valência.
(D) catorze eletrões, dez dos quais são de valência.
- Opção (D)
⇒ O ião CN– apresenta o mesmo número de eletrões que N2 .
⇒ O nitrogénio tem número atómico 7 e, portanto, o átomo de azoto tem 7 eletrões.
⇒ A molécula N2 constituída por 2 átomos de azoto tem 2 x 7 = 14 eletrões.
O nitrogénio é do grupo 15.
- Portanto, deve apresentar 5 eletrões de valência.
⇒ Conclui-se que a molécula N2 tem 2 x 5 = 10 eletrões de valência.
⇒ Assim, CN– também deverá ter 10 eletrões de valência.
- Opção (D)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2.2 No ião cianeto, a ligação entre o átomo de carbono e o átomo de nitrogénio é uma ligação covalente tripla, tal como a ligação entre os átomos de nitrogénio na molécula N2.
Preveja, justificando com base nas posições relativas dos elementos carbono e nitrogénio na tabela periódica, qual das ligações, C ≡ N ou N ≡ N, apresentará maior energia de ligação.
⇒ Como o carbono antecede o nitrogénio no mesmo período da tabela periódica e o raio atómico diminui, em geral, ao longo do período, prevê-se que o raio atómico do nitrogénio seja menor do que o raio atómico do carbono.
Em consequência, o comprimento da ligação N ≡ N deverá ser menor do que o comprimento da ligação C ≡ N.
Para situações semelhantes a um menor comprimento da ligação corresponde uma ligação mais forte.
Assim, prevê-se que a energia de ligação N ≡ N seja maior do que a energia de ligação C ≡ N.
ou
⇒ O nitrogénio segue-se ao carbono no mesmo período da tabela periódica.
Ao longo do período verifica-se o predomínio do efeito do aumento da carga nuclear, prevendo-se que os eletrões de valência do nitrogénio sejam mais atraídos do que os do carbono.
Assim em N2 há maior atração dos núcleos sobre os eletrões da ligação comparativamente a CN– .
Prevê-se, portanto, que a ligação em N2 sega mais forte o que significa maior energia de ligação.
- Na resposta, são apresentados os seguintes tópicos:
A) Como o carbono antecede o nitrogénio no mesmo período da tabela periódica [e como o raio atómico tende a diminuir ao longo do período], o átomo de nitrogénio terá menor raio do que o átomo de carbono.
B) Assim, o comprimento da ligação N ≡ N será menor do que o comprimento da ligação C ≡ N.
C) [Quanto menor for o comprimento da ligação, mais forte será a ligação.] Será, assim, de prever que a ligação N ≡ N apresente maior energia de ligação.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
3. O cianeto de hidrogénio, HCN, que tem um cheiro característico a amêndoa amarga, apresenta um ponto de ebulição de 26 oC, à pressão de 1 atm.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
3.1 Um teor de HCN, no ar, de 0,860 ppm corresponde a um teor, expresso em percentagem em massa, de
(A) 8,60 × 10-7 %
(B) 8,60 × 10-5 %
(C) 8,60 × 10-2 %
(D) 8,60 × 103 %
- Opção (B)
⇒ 0,860 ppm em massa significa 0,860 g de HCN por cada 106 g de ar, o que expresso em percentagem é:
- Opção (B)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
3.2 Considere que a densidade do HCN (g) (M = 27,03 g mol-1), à pressão de 1atm e à temperatura de 30 oC, é 1,086 g dm-3.
Qual das expressões seguintes permite calcular a quantidade de HCN (g) que existe numa amostra pura de 5,0 dm3 desse gás, nas condições de pressão e de temperatura referidas?
- Opção (A)…………. 5 pontos
GRUPO V
O cianeto de hidrogénio dissolve-se em água, dando origem ao ácido cianídrico, HCN(aq), um ácido monoprótico fraco, cuja constante de acidez é 4,9 × 10-10, a 25 oC.
A reação do ácido cianídrico com a água pode ser traduzida por
HCN (aq) + H2O (l) ⇋ CN– (aq) + H3O+ (aq)
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1. Escreva a equação química que traduz a reação do ião cianeto, CN– (aq), com a água.
Refira, justificando, se esse ião se comporta, nessa reação, como um ácido ou como uma base segundo Brönsted-Lowry.
- Equação química:
CN– (aq) + H2O (l) ⇋ HCN (aq) + HO– (aq)
⇒ CN– comporta-se como base dado que aceita um ião H+ , originando o ácido cianídrico HCN
- Na resposta, são apresentados os seguintes tópicos:
A) CN– (aq) + H2O (l ) ⇋ HCN (aq) + OH– (aq)
B) O ião CN– (aq) comporta-se [, nessa reação,] como uma base [segundo Brönsted-Lowry], uma vez que aceita um protão [, originando a espécie HCN (aq)].
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
2. O ácido nitroso, HNO2 (aq), é outro ácido monoprótico fraco, cuja constante de acidez é 4,5 × 10-4, a 25 oC.
A reação do ácido nitroso com a água pode ser traduzida por
HNO2 (aq) + H2O (l) ⇋ NO2– (aq) + H3O+ (aq)
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2.1 Comparando, em termos das respetivas ordens de grandeza, a força do ácido nitroso com a força do ácido cianídrico, conclui-se que o ácido nitroso é cerca de
(A) 106 vezes mais forte do que o ácido cianídrico.
(B) 104 vezes mais forte do que o ácido cianídrico.
(C) 106 vezes mais fraco do que o ácido cianídrico.
(D) 104 vezes mais fraco do que o ácido cianídrico.
- Opção (A)…………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2.2 Considere uma solução de ácido nitroso cujo pH, a 25 oC, é 2,72.
Determine a concentração inicial de HNO2 na solução, à mesma temperatura.
Apresente todas as etapas de resolução.
⇒ Cálculo da concentração do ião H3O+ no estado de equilíbrio:
- [H3O+] = 10-pH mol dm-3 = 10-2,72 mol dm-3 = 1,905 x 10-3 mol dm-3
⇒ Cálculo da concentração de HNO2 no estado de equilíbrio:
Pela estequiometria da reação, e desprezando a contribuição da autoionização da água, conclui-se que:
- [NO2–] = [ H3O+]
⇒ Cálculo da concentração inicial de HNO2:
- [HNO2]ionizado = [NO2–]
então:
- [HNO2]inicial = [HNO2]e + [NO2–]e = 8,068 x 10-3 + 1,905 x 10-5 = 1,0 x 10-2 mol dm-3
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Cálculo da concentração de ácido nitroso não ionizado (c = 8,06 × 10-3 mol dm-3).
B) Cálculo da concentração inicial de HNO2 na solução (c = 1,0 × 10-2 mol dm-3).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
GRUPO VI
Colocou-se um balão cheio de ar (com alguns feijões no seu interior) sob um sensor de movimento ligado a um sistema de aquisição de dados adequado. Seguidamente, largou-se o balão, de modo que caísse verticalmente segundo uma trajetória retilínea, coincidente com o eixo Oy de um referencial unidimensional.
A Figura 4 representa o gráfico da componente escalar, segundo o eixo Oy, da velocidade, vy, do balão em função do tempo, t, no intervalo de tempo em que os dados foram registados.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1. Considere o deslocamento do balão, de massa 4,8 g , no intervalo de tempo [1,3 ; 1,7] s.
Determine o trabalho realizado pelo peso do balão nesse deslocamento.
Apresente todas as etapas de resolução.
⇒ Cálculo do deslocamento do balão:
no intervalo de tempo considerado a velocidade permanece constante logo o valor do deslocamento do balão é
- Δy = vy Δt = 1,7 x (1,7 -1,3) = 0,68 m
⇒ Cálculo do trabalho realizado pelo peso do balão:
- Wp = P d cos 0º = m g Δy cos 0º = 4,8 x 10-3 x 10 x 0,68 x 1 = 3,3 x 10-2 J
ou
⇒ Cálculo da variação de altura do balão:
- no intervalo de tempo considerado a velocidade permanece constante logo o valor do deslocamento do balão é
Δy = vy Δt = 1,7 x (1,7 -1,3) = 0,68 m.
- Como o balão desce na vertical a sua altura diminui de um valor idêntico, isto é
Δh = – Δy = – 0,68 m
⇒ Cálculo do trabalho realizado pelo peso do balão:
- Wp = -ΔEp = -m g Δh = – 4,8 x 10-3 x 10 x (-0,68) = 3,3 x 10-2 J
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Determinação do módulo do deslocamento do balão no intervalo de tempo considerado (Δy = 0,680 m).
B) Cálculo do trabalho realizado pelo peso do balão no deslocamento considerado (W = 3,3 × 10-2 J).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2. No intervalo de tempo [0,4 ; 1,7] s, a energia mecânica do sistema balão + Terra
(A) diminuiu sempre.
(B) diminuiu e depois manteve-se constante.
(C) aumentou sempre.
(D) aumentou e depois manteve-se constante.
- Opção (A)
⇒ Do gráfico decorre que a aceleração, declive da tangente ao gráfico, não permanece constante durante a queda.
- Conclui-se que a resistência do ar não é desprezável.
⇒ A força de resistência do ar é uma força dissipativa cujo trabalho se traduz numa diminuição de energia mecânica do sistema balão + Terra.
- Opção (A)…………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
3. Considere o solo como nível de referência da energia potencial gravítica.
Qual é o esboço do gráfico que pode representar a energia potencial gravítica do sistema balão + Terra em função da altura, h, em relação ao solo?
- Opção (D)
⇒ A energia potencial gravítica do sistema balão + Terra é diretamente proporcional à altura medida em relação a um determinado nível de referência.
- Opção (D)…………. 5 pontos
GRUPO VII
Para estudar a relação entre o módulo da velocidade de lançamento horizontal de uma esfera e o seu alcance, um grupo de alunos montou, sobre uma mesa, uma calha polida, que terminava num troço horizontal, situado a uma determinada altura em relação ao solo, tal como esquematizado na Figura 5 (a figura não se encontra à escala). Junto à posição B, os alunos colocaram uma célula fotoelétrica ligada a um cronómetro digital e, no solo, colocaram uma caixa com areia onde a esfera, E, deveria cair.
Os alunos realizaram vários ensaios nos quais abandonaram a esfera de diversas posições sobre a calha, medindo, em cada ensaio, o tempo, Δt, que a esfera demorava a passar em frente à célula fotoelétrica e o alcance do lançamento horizontal.
1. Num primeiro conjunto de ensaios, os alunos abandonaram a esfera, de diâmetro 27,0 mm, sempre da posição A sobre a calha.
A tabela seguinte apresenta os tempos, Δt, que a esfera demorou a passar em frente à célula fotoelétrica.
Calcule o valor mais provável do módulo da velocidade com que a esfera passa na posição B, em frente à célula fotoelétrica, quando é abandonada da posição A.
Apresente todas as etapas de resolução.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Determinação do valor mais provável do tempo que a esfera demorou a passar em frente à célula fotoelétrica (Δt = 0,0148 s).
B)Determinação do valor mais provável do módulo da velocidade com que a esfera passa na posição B (v = 1,82 m s-1).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
2. Os alunos realizaram, ainda, outros conjuntos de ensaios, em cada um dos quais abandonaram a esfera de uma mesma posição sobre a calha.
Para cada um desses conjuntos de ensaios, determinaram o módulo da velocidade de lançamento da esfera (módulo da velocidade com que a esfera passava na posição B) e o respetivo alcance.
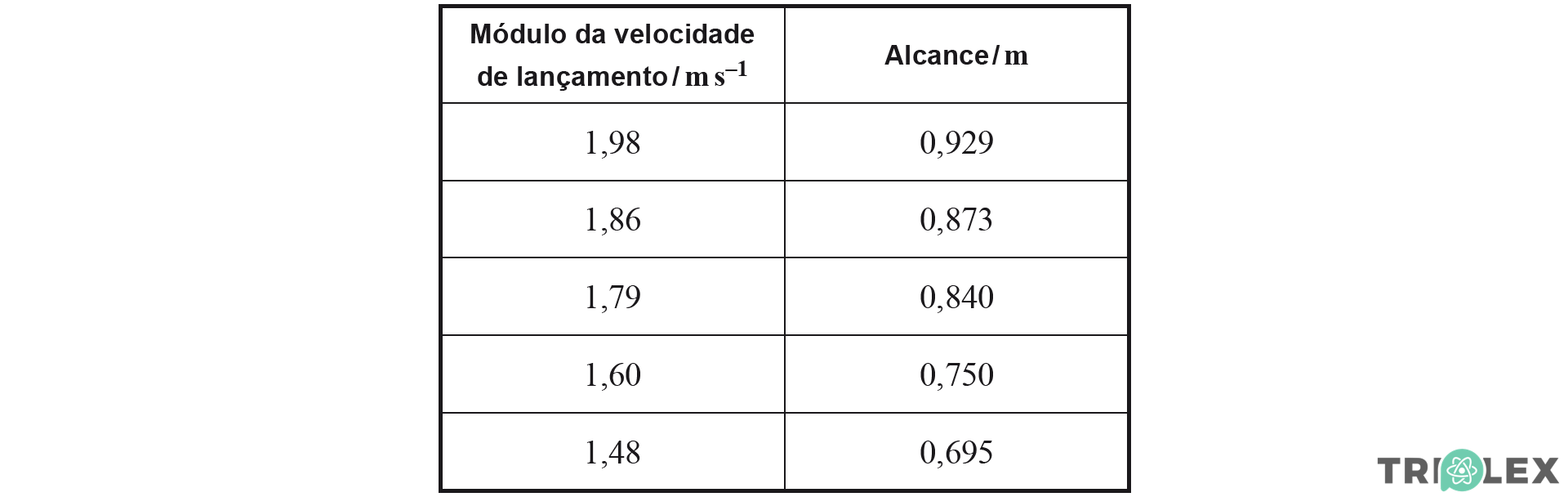
Os valores obtidos estão registados na tabela seguinte.
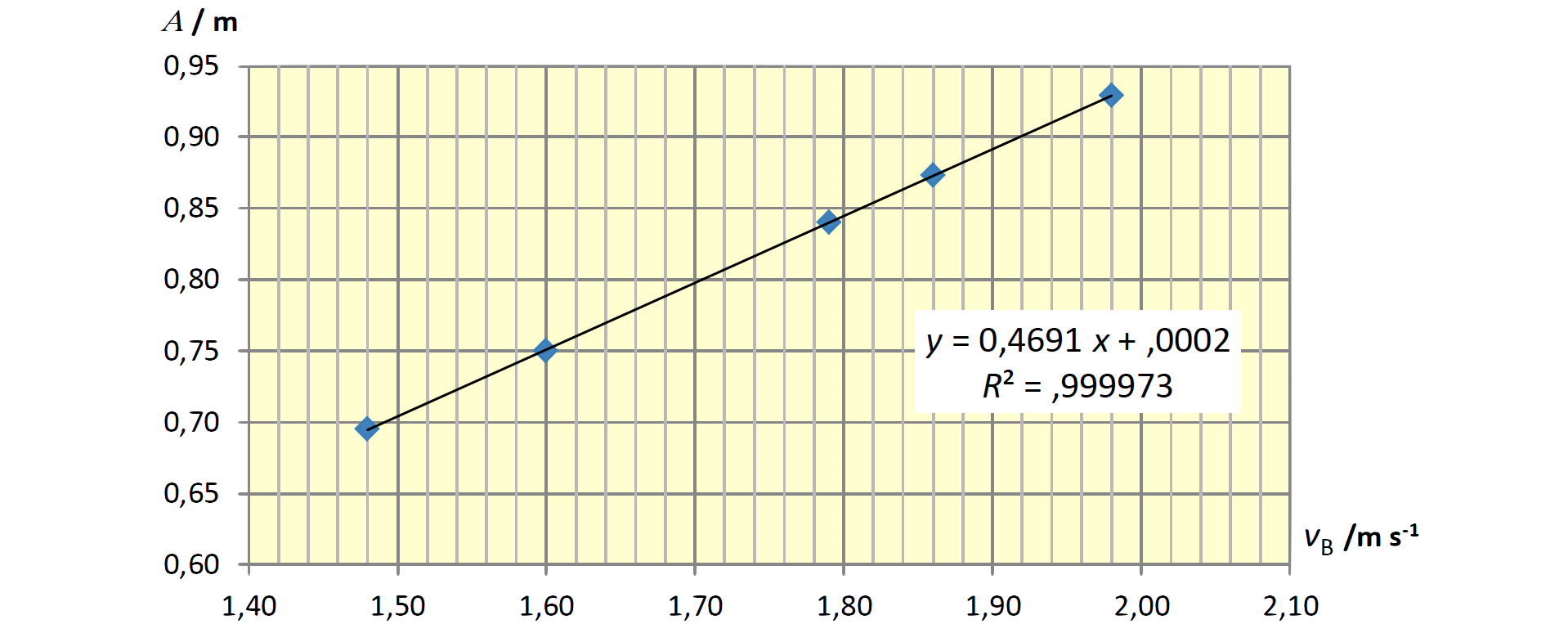
Os alunos traçaram, na calculadora gráfica, o gráfico do alcance em função do módulo da velocidade de lançamento, obtendo a equação da reta que melhor se ajusta ao conjunto de valores apresentados na tabela.
2.1 Qual é o significado físico do declive da reta obtida?
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Tempo de queda OU tempo de voo OU intervalo de tempo decorrido desde o instante em que passa no ponto B até ao instante em que atinge o ponto E OU equivalente.
- Tempo de voo [da esfera] ou tempo que a esfera demora a cair no ar ou equivalente. …………. 5 pontos
2.2 Considere que a distância d representada na Figura 5 é 1,10 m.
Considere que são desprezáveis todas as forças dissipativas e admita que a esfera pode ser representada pelo seu centro de massa (modelo da partícula material).
Calcule a altura máxima, hmáx , em relação ao tampo da mesa, da qual a esfera pode ser abandonada, de modo a cair na caixa com areia.
Comece por apresentar a equação da reta que melhor se ajusta ao conjunto de valores apresentados na tabela.
Apresente todas as etapas de resolução.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Equação da reta de ajuste aos dados experimentais:
- y = 0,4691 x + 2 x 10-4 ⇒ A = 0,4691 vB + 2 x 10-4 = 0,4691 vB (SI)
em que A designa o alcance e vB o módulo da velocidade de lançamento da esfera.
⇒ O módulo da velocidade de lançamento pode ser determinado a partir da projeção no eixo horizontal do movimento da esfera (movimento uniforme):
Como de A para B se desprezam as forças dissipativas há conservação da energia mecânica (a reação normal não realiza trabalho).
⇒ Admitindo válido o modelo da partícula material:
- Na resposta, são apresentadas as seguintes etapas de resolução:
A) Determinação, para o gráfico do alcance em função do módulo da velocidade de lançamento, da equação da reta que melhor se ajusta ao conjunto de valores apresentados na tabela (x = 0,4691 v + 2 × 10-4 (SI) ou y = 0,4691 x + 2 × 10-4 (SI)).
B) Determinação do módulo da velocidade de lançamento que conduz a um alcance de 1,10 m (v = 2,345 m s-1).
C)Determinação da altura máxima, em relação ao tampo da mesa, da qual a esfera pode ser abandonada (hmáx = 0,27 m).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.
A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos
FIM