2008 – Teste Intermédio – 10ºAno – maio
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 10ºAno – 2008
- Duração do Teste: 90 minutos | 30.05.2008
Grupo I
1. Leia atentamente o seguinte texto.A figura 1 representa as várias zonas em que a atmosfera se divide e a variação da temperatura com a altitude, na atmosfera.
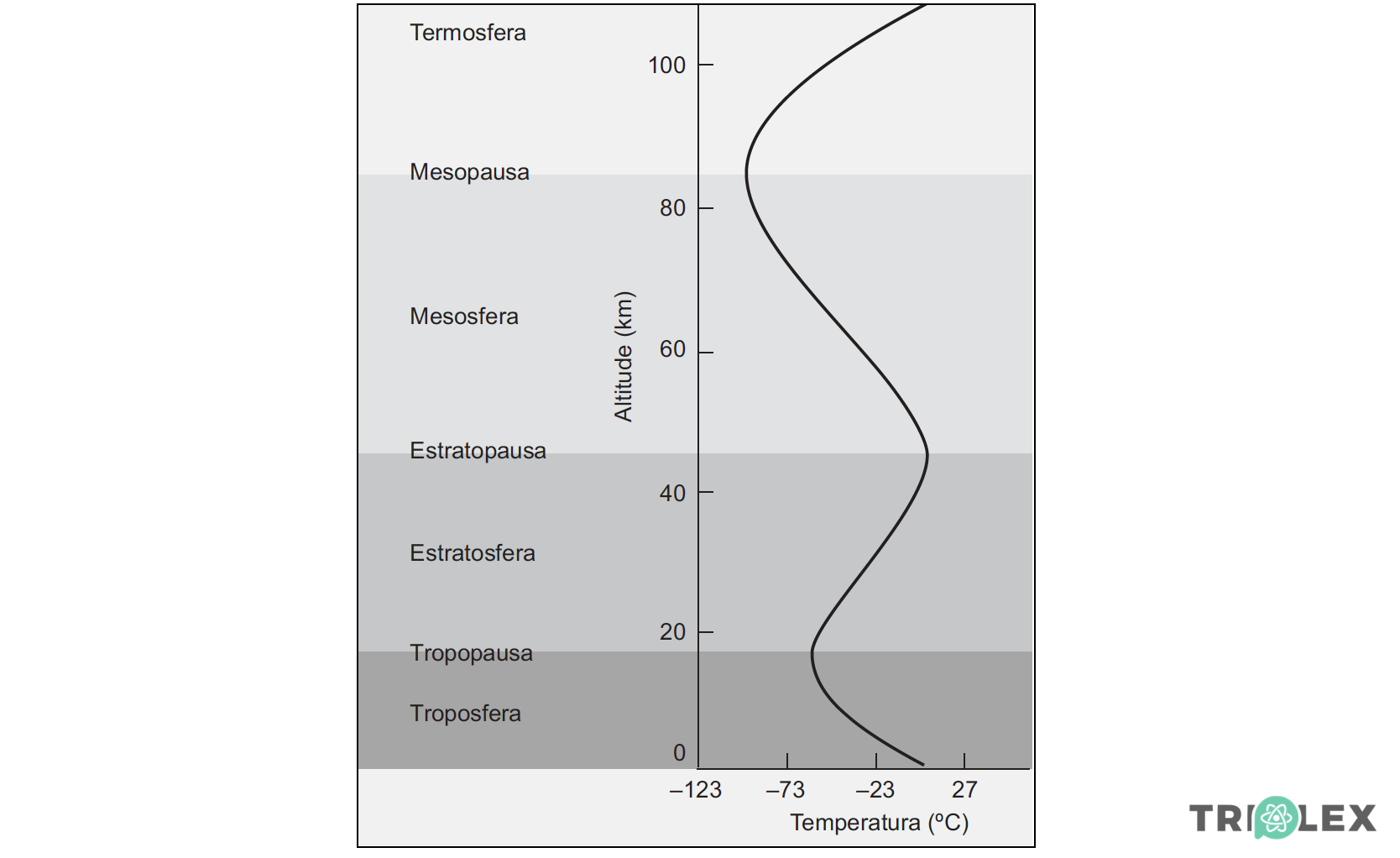
A camada inferior da atmosfera é designada por troposfera. Nesta camada, a temperatura diminui com o aumento de altitude. Aproximadamente entre 11 km e 16 km de altitude, situa-se a tropopausa, uma zona em que a temperatura permanece constante e perto de – 55 ºC. A cerca de 16 km de altitude, inicia-se a estratosfera.
Nesta camada, a temperatura aumenta, até atingir cerca de 0 ºC na estratopausa, aproximadamente a 45 km acima do nível do mar. Acima dessa altitude, na mesosfera, a temperatura torna a diminuir, até se atingir a mesopausa.
Em seguida, na termosfera, a temperatura aumenta e, a altitudes muito elevadas, pode ser superior a 1000 ºC. Contudo, os astronautas n.o s.o reduzidos a cinzas quando saem dos space shuttles, porque a essa altitude as moléculas que existem são em número muito reduzido.
Adaptado de Atkins, P., Jones, L., CHEMISTRY – Molecules,
Matter, and Change, 3rd edition, W. H. Freeman and Company,
New York, 1997
1.1. Tendo em conta a informação apresentada, escreva um texto no qual indique:
- em que se baseia a divisão da atmosfera em camadas;
- como varia a temperatura com a altitude, na estratosfera, apresentando uma justificação para essa variação;
- como varia, de uma forma geral, a densidade da atmosfera com a altitude.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Transmitir indica que se deixa atravessar significativamente pela radiação.
⇒ A divisão da atmosfera em camadas tem por base o perfil de variação da temperatura com a altitude.
⇒ As camadas da atmosfera são definidas a partir de pontos mínimos e máximos da variação da temperatura com a altitude.
⇒ Na estratosfera a temperatura aumenta com a altitude. A principal razão para o aumento de temperatura é a formação de ozono, O3, a partir de O2 e átomos O, resultantes da absorção de radiação ultravioleta pelas moléculas O2.
⇒ A reacção de formação de ozono é fortemente exotérmica.
⇒ De um modo geral, a densidade da atmosfera diminui com a altitude.
⇒ À medida que aumenta a altitude, os gases na atmosfera tornam-se cada vez mais rarefeitos e, portanto, o número de partículas por unidade de volume diminui.
A resposta deve contemplar os seguintes tópicos:
⇒ A divisão da atmosfera em camadas baseia-se na existência de pontos de inflexão na curva que traduz a relação da temperatura com a altitude.
⇒ Nessa camada, a temperatura aumenta com a altitude, porque ocorre libertação de energia em algumas das reacções químicas em que intervém o ozono.
⇒ De um modo geral, a densidade da atmosfera diminui com a altitude.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

1.2. Fazendo o balanço energético da Terra, igualando a potência da radiação solar absorvida pela superfície da Terra e pela atmosfera à potência da radiação por estas emitida, a temperatura média à superfície da Terra seria cerca de –18 ºC.
No entanto, a temperatura média à superfície da Terra é aproximadamente 15 ºC.
Indique qual é o efeito que explica esta diferença.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Efeito de estufa
⇒ Uma parte da radiação infravermelha emitida pela superfície da Terra é absorvida pelas nuvens e outros gases, e reemitida novamente para a superfície, originando o aquecimento das camadas mais baixas da atmosfera.
- Efeito de estufa …………. 8 pontos
2. O monóxido de carbono, CO, e o dióxido de carbono, CO2, são gases que existem na atmosfera, provenientes de fontes naturais (fogos florestais, emissões vulcânicas) e de fontes antropogénicas (combustões domésticas e industriais, escapes de veículos motorizados).
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)

Seleccione a alternativa que contém os termos que devem substituir as letras (a) e (b), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
A ligação carbono–oxigénio na molécula CO2 tem __(_a_)__ energia e __(_b_)__ comprimento do que a ligação carbono–oxigénio na molécula CO.
(A) … maior … maior …
(B) … menor … maior …
(C) … menor … menor …
(D) … maior … menor …
- Opção (B)
⇒ A formação de uma ligação química envolve libertação de energia – a energia de ligação.
⇒ Quanto mais forte for a ligação, mais energia será necessária para a quebrar. Quanto maior for o número de electrões partilhados numa ligação química menor será a distância média entre os núcleos dos átomos que estabelecem a ligação, e mais forte será a ligação.
⇒ Como os átomos envolvidos nas ligações das duas moléculas são os mesmos, o comprimento da ligação dupla é maior do que o comprimento da ligação tripla.
⇒ A um maior comprimento de ligação corresponde uma menor energia de ligação.
- Opção (B)…………. 8 pontos
2.2. Um dos modos de avaliar o grau de toxicidade de uma substância é através do valor da respectiva DL50, normalmente expressa em mg de substância por kg de massa corporal.
Por inalação, verifica-se que o CO é mais tóxico do que o CO2.
Com base na definição de DL50, indique, justificando, qual é a relação (maior, igual ou menor) entre o valor de DL50 para o CO e para o CO2.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (B)
⇒ DL50 (Dose Letal) é a dose de uma substância necessária para provocar a morte de 50% dos indivíduos de uma determinada população.
⇒ Expressa-se em miligramas de substância por quilograma de massa corporal do indivíduo.
⇒ Quanto menor for a dose letal de uma substância, para uma determinada espécie, maior será a sua toxicidade.
A resposta deve contemplar os seguintes tópicos:
⇒ O valor de DL50 para o CO é menor do que o valor de DL50 para o CO2.
⇒ Quanto menor for a dose letal por kg de massa corporal, mais tóxica é a substância.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
2.3. Em termos médios, a % (V/V) do CO2 na atmosfera é 0,035%. Outra maneira de indicar essa concentração é em ppmV (partes por milhão em volume).
Seleccione a alternativa que corresponde a essa concentração, expressa em ppmV.
(A) 3,5 x 10–2
(B) 3,5 x 10–1
(C) 3,5 x 102
(D) 3,5 x 104
- Opção (C)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 1 (Massa e tamanho dos átomos)
2.4. Seleccione a alternativa que corresponde ao número de átomos existente em 22,0 g de dióxido de carbono, CO2.
(A) 3,01 x 1023
(B) 6,02 x 1023
(C) 9,03 x 1023
(D) 1,20 x 1024
- Opção (C)…………. 8 pontos
3. Considere as configurações electrónicas dos átomos dos elementos P, Q, R, e S (as letras não correspondem aos símbolos químicos reais desses elementos), no estado fundamental.
P – [Ne] 3s1
Q – 1s2 2s2 2p5
R – 1s2 2s2 2p6 3s2
S – [Ar] 4s1
3.1. Uma orbital atómica é caracterizada por um conjunto de três números quânticos (n, l, m).
Seleccione a alternativa que corresponde ao conjunto de números quânticos que caracteriza uma das orbitais completamente preenchidas do átomo do elemento P, no estado fundamental.
(A) (3, 0, 0)
(B) (2, 0, 1)
(C) (3, 1, –1)
(D) (2, 1, 0)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (D)
⇒ O elemento P apresenta no estado fundamental a configuração electrónica: 1s2 2s2 2p6 3s1.
⇒ Esta configuração contém dois níveis de energia (n = 1 e n = 2) completamente preenchidos, assim como as respectivas orbitais: 1s, 2s e 2p.
⇒Estas são caracterizadas pelos seguintes conjuntos de números quânticos:
- 1s→ (1,0,0)
- 2s→ (2, 0, 0)
- 2p→ (2, 1, 0); (2, 1, 1); (2, 1, -1)
- Opção (D)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
3.2. Tendo em conta as configurações electrónicas dos átomos dos elementos P, R e S, seleccione a alternativa que corresponde à ordenação correcta dos valores das respectivas energias de ionização, Ei.
(A) Ei (P) < Ei (R) < Ei (S)
(B) Ei (S) < Ei (P) < Ei (R)
(C) Ei (S) < Ei (R) < Ei (P)
(D) Ei (P) < Ei (S) < Ei (R)
- Opção (B)
⇒ Energia de ionização é a energia mínima necessária para extrair um electrão ao átomo no estado fundamental.
⇒ Verifica-se que, de um modo geral, a energia de ionização diminui ao longo do grupo e aumenta ao longo do período.
⇒ Os elementos P e S pertencem ao mesmo grupo (1), pois têm o mesmo número de electrões de valência (um).
⇒ O electrão de valência do elemento S é mais energético do que o do elemento P: o número quântico principal n para o electrão de valência do elemento S é maior, logo este está mais afastado do núcleo e, por isso, é menos atraído. Assim, é necessário menor energia para o remover (Ei (S) < Ei (P)).
⇒ Os elementos P e R pertencem ao mesmo período (3.º), pois os seus electrões estão distribuídos pelo mesmo número de níveis de energia.
⇒ Para os elementos do mesmo período, à medida que a carga nuclear aumenta os electrões vão sendo mais atraídos, pelo que a energia necessária para os remover aumenta (Ei (P) < Ei (R)).
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3.3. Seleccione a alternativa que contém, respectivamente, as configurações electrónicas dos iões Q– e R2+, no estado fundamental.
(A) 1s2 2s2 2p6 e 1s2 2s2 2p6
(B) 1s2 2s2 2p4 e 1s2 2s2 2p6 3s2 3p2
(C) 1s2 2s2 2p4 e 1s2 2s2 2p6
(D) 1s2 2s2 2p6 e 1s2 2s2 2p6 3s2 3p2
- Opção (A)
⇒ O elemento Q adquire maior estabilidade, recebendo um electrão que lhe irá completar o nível de valência.
⇒ Q transforma-se no anião Q–, ao qual corresponde a configuração electrónica 1s2 2s2 2p6.
⇒ O elemento R adquire máxima estabilidade perdendo os dois electrões de valência e transformando-se no catião R2+, ao qual corresponde a configuração 1s2 2s2 2p6.
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
3.4. Seleccione a alternativa que corresponde é fórmula química do composto constituído pelos iões Q– e R2+.
(A) R2Q
(B) RQ2
(C) R2Q3
(D) R3Q2
- Opção (B)
⇒ Na escrita de fórmulas químicas de compostos iónicos, coloca-se primeiro o símbolo do catião e depois o do anião, de modo que a soma das cargas elétricas seja nula.
- Opção (B)…………. 8 pontos
4. A importância do papel do Sol na evolução da vida terrestre é desde há muito reconhecida.
Na figura 2 está esquematizado um balan.o energético da Terra.
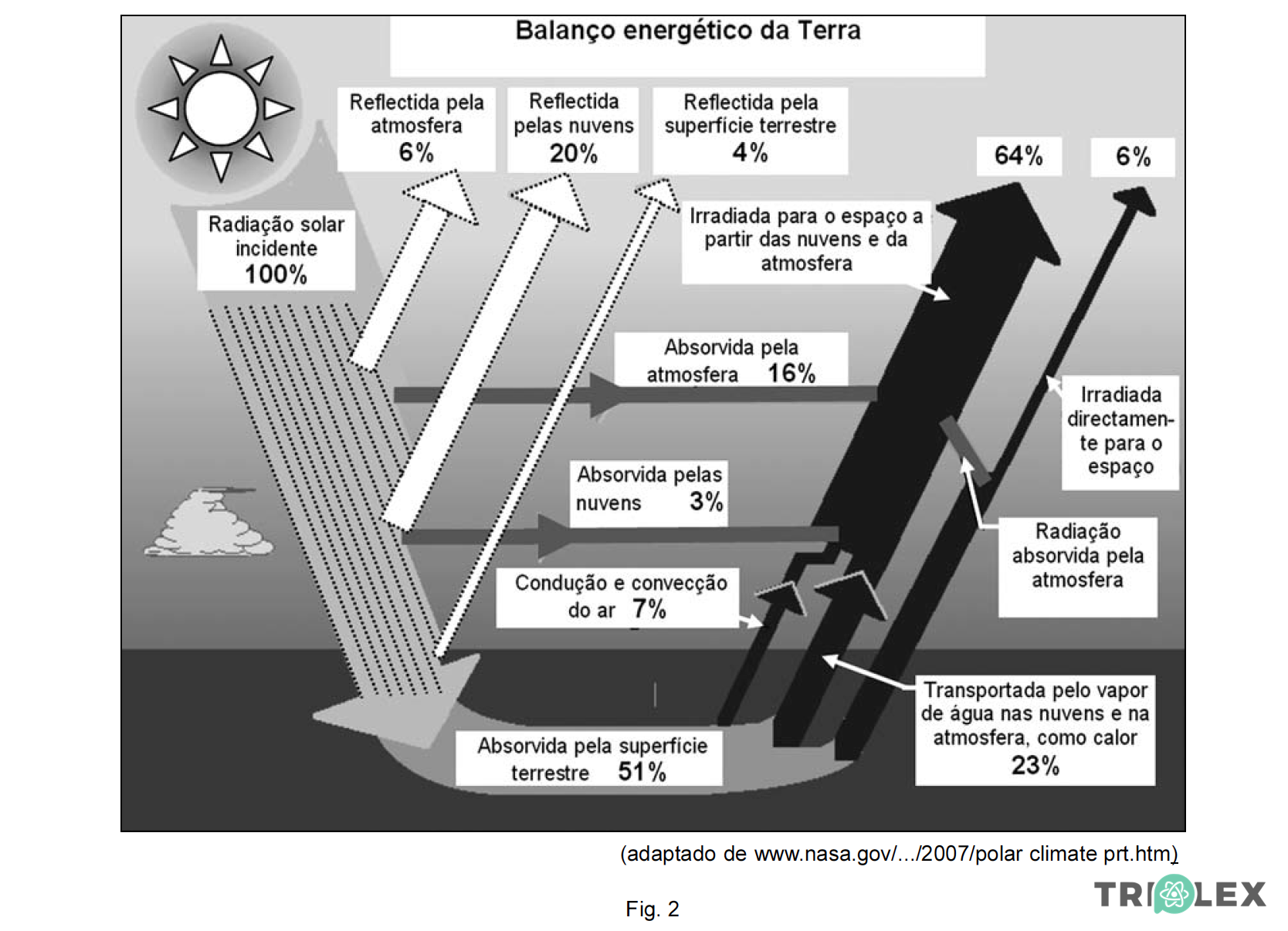 Classifique como verdadeira (V) ou falsa (F), cada uma das afirmações seguintes.
Classifique como verdadeira (V) ou falsa (F), cada uma das afirmações seguintes.
(A) A percentagem da radiação solar incidente que é reflectida é maior do que a que é absorvida pela atmosfera e pelas nuvens.
(B) A radiação solar que atinge a superfície da Terra situa-se apenas na zona visível do espectro electromagnético.
(C) A percentagem da radiação solar absorvida pela atmosfera é superior à reflectida por ela.
(D) A intensidade máxima da radiação emitida pela Terra ocorre na zona do visível do espectro electromagnético.
(E) A intensidade máxima da radiação emitida pelo Sol ocorre na zona do infravermelho do espectro electromagnético.
(F) Aproximadamente metade da radiação solar incidente é absorvida pela superfície terrestre.
(G) Uma parte da radiação solar incidente é absorvida pela atmosfera, sendo a restante radiação totalmente absorvida pela superfície terrestre.
(H) Da radiação solar que atinge o planeta, 30% é reflectida para o espaço.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Verdadeiras – (A), (C), (F) e (H)
- Falsas – (B), (D), (E) e (G)
⇒ (A) Verdadeira.
Refletida = 26%, absorvida = 19%;
⇒ (B) Falsa.
Também nas zonas do IV e UV;
⇒ (C) Verdadeira.
Absorvida = 16%, refletida = 6%;
⇒ (D) Falsa.
Na zona do IV;
⇒ (E) Verdadeira.
Na zona do visível;
⇒ (F) Falsa.
Absorvida = 51%;
⇒ (G) Falsa.
Absorvida pela atmosfera = 16%, absorvida pela superfície = 51%;
⇒ (H) Verdadeira.
Total refletida = 30%.
5. Considere um sistema termodinâmico fechado no qual ocorreu um processo em que se verificaram trocas de energia entre o sistema e a sua vizinhança, sob a forma de calor, de trabalho e de radiação.
Nesse processo, a energia interna do sistema manteve-se constante, tendo o sistema transferido para a sua vizinhança 700 J sob a forma de trabalho e 300 J sob a forma de radiação.
Calcule a energia transferida, sob a forma de calor, e refira o sentido (do sistema para a vizinhança ou da vizinhança para o sistema) dessa transferência.
Apresente todas as etapas de resolução.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ U = constante ⇒ ΔU = 0
⇒ W= – 700 J (o sinal é negativo pois o sistema cede trabalho ao exterior…)
⇒ R= – 300 J (o sinal é negativo pois o sistema transfere a radiação para o exterior…)
⇒ ΔU = W+ Q+ R ⇒ 0 = (– 700) + Q+ (– 300) ⇔ Q= + 1000 J
⇒ A energia transferida sob a forma de calor é + 1000 J. O calor é transferido da vizinhança para o sistema.
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula a energia transferida sob a forma de calor (Q = +1000 J).
⇒ Refere o sentido da transferência (da vizinhança para o sistema).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
- 10ºano – Física – A.l. – 3.2 – Capacidade térmica mássica
6. Para determinar a capacidade térmica mássica do alumínio, formaram-se três grupos de alunos, tendo cada grupo trabalhado com um bloco de alumínio com 500 g de massa, colocado numa caixa isoladora (figura 3).

Cada bloco tem duas cavidades, numa das quais se colocou um termómetro, e na outra uma resistência eléctrica de 60 W de potência, ligada a uma fonte de alimentação.
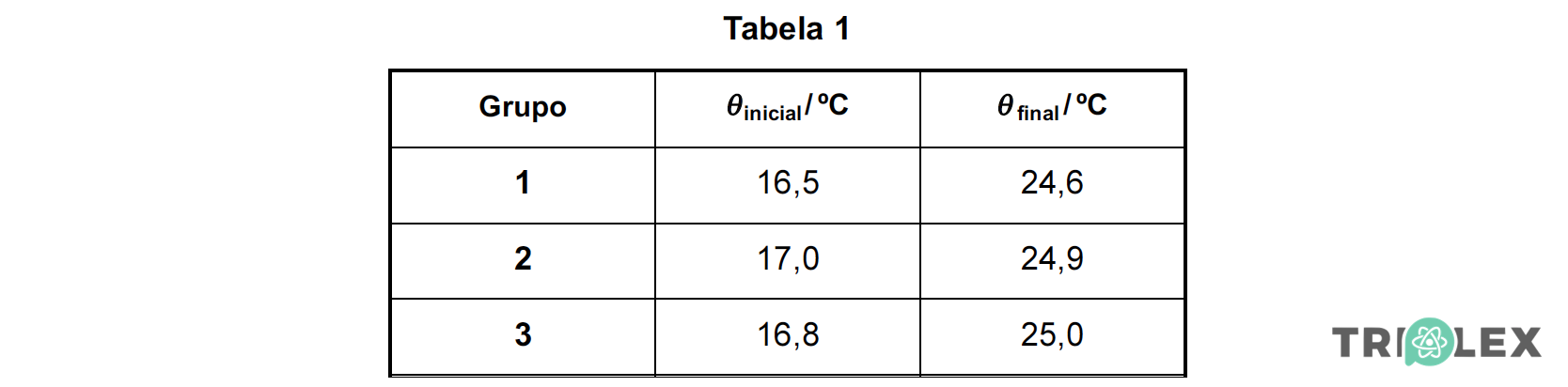
Cada grupo mediu a temperatura inicial do bloco, θinicial. Após a fonte de alimentação ter estado ligada durante 60,0 s, cada grupo mediu a temperatura final do bloco, θ final. Os valores medidos estão registados na tabela 1.
Admita que toda a energia fornecida pela resistência eléctrica é transferida para o bloco de alumínio.
Com base nos dados da tabela 1, calcule o valor mais provável da capacidade térmica mássica do alumínio.
Apresente todas as etapas de resolução.
- Opção (B)
- m = 500 g = 500 x 10-3 kg
- Peléct = 60 W
- Δt = 60,0 s
- 3,60 x 103 = 500 x 10-3 x c1 x (24,6 – 16,5) ⇔ c1 = 889 J kg-1 ºC-1
- 3,60 x 103 = 500 x 10-3 x c2 x (24,9 – 17,0) ⇔ c2 = 911 J kg-1 ºC-1
- 3,60 x 103 = 500 x 10-3 x c3 x (25,0 – 16,8) ⇔ c3 = 878 J kg-1 ºC-1

⇒ O valor mais provável da capacidade térmica mássica do alumínio é, aproximadamente, 8,9 x 102 J kg– 1 ºC-1.
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula a energia fornecida a cada bloco (E = 3,60 x 103 J).
⇒ Calcula para os valores experimentais de cada grupo, a capacidade térmica mássica do alumínio. (c1 = 889 J kg–1 ºC–1; c2 = 911 J kg–1 ºC–1 ; c3 = 878 J kg–1 ºC–1).
⇒ Calcula o valor mais provável da capacidade térmica mássica do alumínio (c = 8,9 x 102 J kg–1 ºC–1).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

7. Um crescente número de pessoas procura as saunas por razões de saúde, de lazer e de bem-estar.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
7.1. Numa sauna, a temperatura constante, uma pessoa sentada num banco de madeira encosta-se a um prego de ferro mal cravado na parede.
Essa pessoa tem a sensação de que o prego está mais quente do que a madeira, e esta está mais quente do que o ar.
Seleccione a alternativa que traduz a situa..o descrita.
(A) A temperatura do prego de ferro é superior à temperatura da madeira.
(B) O ar é melhor condutor térmico do que a madeira.
(C) A temperatura do ar é superior à temperatura da madeira.
(D) O ferro é melhor condutor térmico do que a madeira.
- Opção (D)
⇒ Materiais diferentes, nas mesmas condições, apresentam diferentes condutividades térmicas.
⇒ Os metais são bons condutores térmicos (altas condutividades térmicas), enquanto o ar e a madeira são maus condutores térmicos (baixas condutividades térmicas).
⇒ O melhor condutor térmico é o prego de ferro, depois a madeira e, por último, o ar.
⇒ O prego de ferro, a madeira e o ar encontram-se à mesma temperatura, pois estão em equilíbrio térmico.
- Opção (D)…………. 8 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
7.2. Identifique o principal processo de transferência de energia, que permite o aquecimento rápido de todo o ar da sauna, quando se liga um aquecedor apropriado.
- Convecção
⇒ A convecção ocorre unicamente em fluidos (gases ou líquidos) e caracteriza-se pelo facto de o calor ser transferido pelo movimento ascendente e descendente de partes do próprio fluido.
⇒ Em geral, as partes mais quentes sobem e as mais frias descem, pois as mais quentes são menos densas. Estes movimentos do fluido designam-se por correntes de convecção.
⇒ Quando se liga um aquecedor, a massa de ar mais próxima da fonte térmica aquece primeiro que a restante, aumentando de volume e ficando menos densa.
⇒ A restante massa de ar, a uma temperatura mais baixa, logo mais densa, tende a ocupar a zona inferior da sauna, levando a fracção mais quente a subir. Formam-se assim as correntes de convecção responsáveis pelo aquecimento rápido e homogéneo de todo o ar da sauna.
- Convecção …………. 8 pontos
7.3. Quando se planeou a construção da sauna, um dos objectivos era que a temperatura da sauna diminuísse o mais lentamente possível depois de se desligar o aquecedor.
Seleccione a alternativa que contém os termos que devem substituir as letras (a) e (b), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
Esse objectivo pode ser alcançado __(_a_)__ a espessura das paredes e escolhendo um material, para a construção das paredes, com __(_b_)__ condutividade térmica.
(A) … aumentando … alta …
(B) … diminuindo … baixa …
(C) … aumentando … baixa …
(D) … diminuindo … alta …
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)

⇒ Para que a temperatura da sala diminuísse o mais lentamente possível depois de se desligar o aquecedor, ou seja, para que a quantidade de calor transferido por unidade de tempo seja a mais baixa possível, deve-se aumentar a espessura, l, das paredes, pois a corrente térmica é tanto mais baixa quanto maior for a espessura e quanto mais baixa for a condutividade térmica do material, k, das paredes.
- Opção (C)…………. 8 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
7.4. As toalhas utilizadas na sauna são colocadas num cesto, que é arrastado horizontalmente 2,0 m por acção de uma força F, de intensidade 45 N, na direcção do movimento.
Admitindo que entre o cesto e o solo existe uma força de atrito Fa, de intensidade 40 N, calcule o trabalho realizado pela resultante das forças aplicadas no cesto.
Apresente todas as etapas de resolução.
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula o módulo da resultante das forças (Fres = 5,0 N).
⇒ Calcula o trabalho realizado por essa força (ω = 10 J).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
FIM




