2012 – 2ª Fase – Prova Escrita de Física e Química A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: 2.ª Fase – 2012
Grupo I
Qualquer que seja a temperatura a que se encontre, um corpo emite sempre radiação eletromagnética, devido aos movimentos de agitação térmica das partículas que o constituem.
O espectro da radiação térmica emitida por um corpo é um espectro contínuo em que o comprimento de onda da radiação de máxima intensidade emitida depende da temperatura a que o corpo se encontra: à medida que a temperatura, T, do corpo aumenta, o comprimento de onda ao qual ocorre a emissão de radiação de máxima intensidade, λmáxima, diminui proporcionalmente.
A taxa temporal de emissão de energia de um corpo, sob a forma de radiação térmica, a partir da sua superfície, é proporcional à quarta potência da temperatura absoluta da superfície do corpo, dependendo também da sua área superficial e de uma constante chamada emissividade.
Ao mesmo tempo que emite, um corpo também absorve radiação eletromagnética da sua vizinhança. Quando um corpo está em equilíbrio com a sua vizinhança, emite e absorve energia, como radiação, à mesma taxa temporal.
R. A. Serway, J. W. Jewett, Jr., Princípios de Física, vol. II,
Pioneira Thomson Learning, 2004 (adaptado)
1. A Figura 1 apresenta uma parte do gráfico da intensidade da radiação emitida por um corpo, a uma determinada temperatura, em função do comprimento de onda.

À temperatura considerada, o corpo emite
(A) apenas radiação visível.
(B) radiação de máxima intensidade no visível.
(C) apenas radiação ultravioleta.
(D) radiação de máxima intensidade no ultravioleta.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (D)
⇒ À temperatura considerada, o corpo emite um espetro contínuo de comprimentos de onda, encontrando-se a radiação de máxima intensidade para comprimentos de onda menores do que o violeta, ou seja, na zona do ultravioleta.
- Opção (D)…………. 5 pontos
2. Traduza por uma expressão matemática a lei enunciada no final do segundo parágrafo do texto.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ De acordo com o referido no final no segundo par grafo do texto: “… medida que a temperatura, T, do corpo aumenta, o comprimento de onda ao qual ocorre a emissão de radiação de máxima intensidade, λmáxima, diminui proporcionalmente”, conclui-se que o comprimento de onda da radiação de máxima intensidade é inversamente proporcional à temperatura, logo a expressão que pode traduzir esta relação é λmáxima T = constante.
- λmáxima x T = constante ou equivalente …………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3. Qual é a unidade do Sistema Internacional em que se exprime a taxa temporal de emissão de energia de um corpo?
- watt [ou joule por segundo]
⇒ A taxa temporal de emissão de energia corresponde à energia emitida por unidade de tempo que, em termos das unidades SI, deverá ser expressa em joule por segundo, isto é, em watt.
- Watt …………. 5 pontos
4. Se a temperatura absoluta da superfície de um corpo aumentar duas vezes, a taxa temporal de emissão de energia do corpo, sob a forma de radiação térmica, a partir da sua superfície, aumentará
(A) duas vezes.
(B) quatro vezes.
(C) oito vezes.
(D) dezasseis vezes.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (D)…………. 5 pontos
5. A Terra emite e absorve radiação a uma taxa temporal _____, pelo que a temperatura média da sua superfície _____.
(A) igual … varia
(B) diferente … varia
(C) igual … não varia
(D) diferente … não varia
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
⇒ A Terra está em equilíbrio térmico com a sua vizinhança, portanto, emite e absorve energia, como radiação, à mesma taxa temporal, mantendo uma temperatura média constante à sua superfície.
- Opção (C)…………. 5 pontos
Grupo II
A composição do gás natural depende, entre outros fatores, da localização do reservatório subterrâneo a partir do qual se faz a sua extração.
No entanto, o gás natural é sempre maioritariamente constituído por metano, CH4 (g), embora possa conter outros gases, como, por exemplo, metilbutano, dióxido de carbono, vapor de água e sulfureto de hidrogénio.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1. Considere que se extrai, de um determinado reservatório subterrâneo, gás natural contendo 70%, em volume, de metano.
Determine o número de moléculas de metano que existem numa amostra de 5,0 dm3 do gás natural, nas condições normais de pressão e de temperatura.
Apresente todas as etapas de resolução.
⇒ Cálculo do volume de metano (CH4), em condições normais de pressão e de temperatura (PTN), numa amostra de 5,0 dm3 de gás natural:

⇒ Cálculo da quantidade de metano:
- n(CH4) = V/Vm = 3,50/22,4 = 0,156 mol
⇒ Determinação do número de moléculas de metano:
- N(CH4) = n(CH4) x NA = 0,156 x 6,02 x 1023 = 9,4 x 1022
- A resolução deve apresentar as seguintes etapas:
A) Cálculo da quantidade de metano que existe na amostra do gás natural, nas condições normais de pressão e de temperatura (n = 1,56 x 10-1 mol).
B) Cálculo do número de moléculas de metano que existem na amostra do gás natural (N = 9,4 x 1022).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2. Qual das fórmulas de estrutura seguintes pode representar a molécula de metilbutano?

- Opção (A)
⇒ Na fórmula de estrutura representada por (A), a cadeia mais longa contém 4 átomos de carbono e um substituinte metil.
⇒ As fórmulas (C) e (D) representam o pentano; a fórmula (B) o 2,2-dimetilpropano.
- Opção (A)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
3. Explique porque é que a geometria da molécula de dióxido de carbono, CO2, é linear.
⇒ Nas ligações que se estabelecem no CO2 o carbono é o átomo central e forma ligações duplas com cada oxigénio.
⇒ Como o carbono e o oxigénio têm, respetivamente, 4 e 6 eletrões de valência, não há eletrões não ligantes no átomo central carbono.
⇒ Há dois pares de eletrões não ligantes em cada oxigénio mas o que determina a geometria a minimização da energia das repulsões entre os pares de eletrões não ligantes no átomo central, a qual corresponde a um maior afastamento dos eletrões, o que neste caso significa uma geometria linear.
- A resposta deve apresentar os seguintes tópicos:
A) Na molécula de dióxido de carbono, não existem pares de eletrões [de valência] não ligantes no átomo central.
B) Para minimizar as repulsões que se estabelecem entre os pares de eletrões ligantes, a molécula de dióxido de carbono assume uma geometria linear.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
4. As moléculas de água, H2O, e de sulfureto de hidrogénio, H2S, apresentam geometria semelhante.
Preveja, justificando com base nas posições relativas dos elementos oxigénio e enxofre na tabela periódica, qual das ligações, H – O ou H – S, terá maior comprimento, na respetiva molécula.
⇒ O enxofre e o oxigénio encontram-se no mesmo grupo da tabela periódica (grupo 16).
⇒ No grupo o enxofre encontra-se a seguir ao oxigénio.
⇒ O raio atómico em cada grupo aumenta com o número atómico, por isso o enxofre tem maior raio atómico do que o oxigénio.
⇒ Os átomos de oxigénio e de enxofre ligam-se a átomos do mesmo elemento (hidrogénio).
⇒ O maior raio do átomo do enxofre deverá, previsivelmente, implicar um maior comprimento da ligação com o átomo de hidrogénio.
- A resposta deve apresentar os seguintes tópicos:
A) Como o oxigénio antecede o enxofre no mesmo grupo da tabela periódica [e como o raio atómico tende a aumentar ao longo do grupo,] o átomo de enxofre terá maior raio do que o átomo de oxigénio.
B) O átomo de oxigénio e o átomo de enxofre estão ligados [nas moléculas H2O e H2S, respetivamente,] a átomos do mesmo elemento.
C) É, assim, de prever que a ligação H – S [na molécula H2S] tenha maior comprimento do que a ligação H – O [na molécula H2O].
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

Grupo III
O ácido sulfídrico, H2S (aq), é um ácido diprótico muito fraco, cuja ionização global em água ocorre em duas etapas sucessivas.
A primeira etapa da ionização ocorre em muito maior extensão do que a segunda e pode ser traduzida por
H2S (aq) + H2O (l) ⇋ HS– (aq) + H3O+ (aq)
A constante de acidez do H2S (aq), definida para a reação anterior, é 1,32 x 10-7, a 25 ºC.- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1. Considere 250,0 cm3 de uma solução de ácido sulfídrico cujo pH, a 25 ºC, é 3,94.
Determine a quantidade de ácido sulfídrico não ionizado que existe naquele volume de solução, considerando apenas a contribuição da reação acima indicada para a ionização do ácido em água.
Apresente todas as etapas de resolução.
⇒ Cálculo da concentração do ião hidrónio:
- [H3O+] = 10-pH = 10-3,94 = 1,148 x 10-4 mol dm-3
⇒ Cálculo da concentração do ácido sulfídrico não ionizado:
⇒ considera-se apenas a contribuição do ácido para a concentração hidrogeniónica, o que significa que [HS–] = [H3O+]
⇒ utilizando a expressão da constante de acidez do ácido sulfídrico obtém-se
⇒ Determinação da quantidade de ácido sulfídrico:
- n = c x V = 9,984 x 102 x 0,2500 = 2,50 x 10-2 mol
- A resolução deve apresentar as seguintes etapas:
A) Cálculo da concentração de ácido sulfídrico não ionizado ([H2S] = 9,984 x 10-2 mol dm-3).
B) Cálculo da quantidade de ácido sulfídrico não ionizado que existe em 250,0 cm3 de solução (n = 2,50 x 10-2 mol).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2. O ião sulfureto, S2- (aq), é a base conjugada da espécie HS– (aq) na reação que corresponde à segunda etapa da ionização do ácido sulfídrico em água.
A reação entre o ião S2- (aq) e a água pode ser traduzida por
(A) S2- (aq) + H2O (l) ⇋ H2S (aq) + 2 H3O+ (aq)
(B) S2- (aq) + 2 H2O (l) ⇋ H2S (aq) + 2 OH– (aq)
(C) S2- (aq) + H2O (l) ⇋ H2S (aq) + 2 OH– (aq)
(D) S2- (aq) + 2 H2O (l) ⇋ H2S (aq) + 2 H3O+ (aq)
- Opção (B)
⇒ A equação (B) traduz corretamente a reação ácido-base ocorrida, verificando-se conservação de massa e de carga.
⇒ As equações (A) e (D) não estão corretas porque não estão certas quanto às massas e quanto às cargas e a equação (C) não está certa quanto às massas.
- Opção (B)…………. 5 pontos
Grupo IV
1. O etanol, C2H5OH (M = 46,08 g mol-1), pode reagir com o cloro, Cl2 (M= 70,90 g mol-1), formando-se um composto orgânico denominado cloral, CCl3CHO (M = 147,38 g mol-1), e cloreto de hidrogénio, HCl(g).
A reação pode ser traduzida por
C2H5OH (l) + 4 Cl2 (g) → CCl3CHO (l) + 5 HCl (g)
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
1.1. Considere que se fez reagir 3,0 mol de etanol com 10,0 mol de cloro.
Identifique, justificando, o reagente limitante.
⇒ A estequiometria da reação mostra que com cada 1 mol de etanol, C2H5OH, que reage, reagem 4 mol de cloro, Cl2, ou seja, numa proporção de 1:4.
⇒ Para reagirem com 3 mol de etanol seriam necessárias 12 mol de cloro.
⇒ O reagente limitante é o cloro porque só existem 10 mol disponíveis.
- A resposta deve apresentar os seguintes tópicos:
A) A quantidade de cloro é inferior à quantidade estequiométrica.
ou
A quantidade de cloro é inferior à quantidade necessária para fazer reagir completamente 3,0 mol de etanol.
ou
equivalente.
B) Assim, o cloro é o reagente limitante.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
1.2. Determine, numa outra situação, a massa de etanol que é necessário fazer reagir para se obter, na prática, 1,5 kg de cloral, admitindo que aquela reação apresenta um rendimento médio de 30%.
Apresente todas as etapas de resolução.
 ⇒ Cálculo da quantidade de cloral que se obteria se o rendimento fosse 100%:
⇒ Cálculo da quantidade de cloral que se obteria se o rendimento fosse 100%:
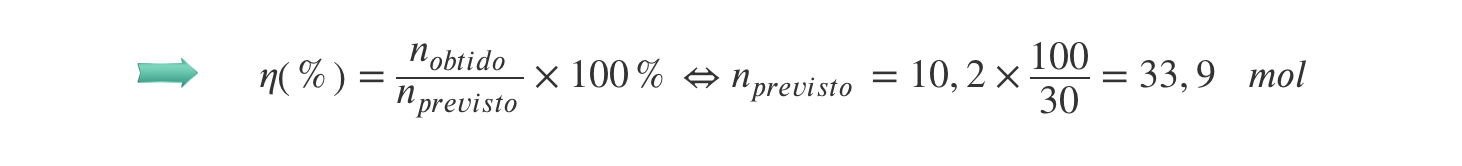
⇒ Cálculo da massa de etanol que é necessário fazer reagir:
⇒ de acordo com a proporção estequiométrica, a quantidade de etanol que reage é igual à de cloral que se deveria formar, logo n(C2H5HO) = 33,9 mol
⇒ m(C2H5HO) = n(C2H5HO) x M(C2H5HO) = 33,9 x 46,08 = 1,6 x 103 g- A resolução deve apresentar as seguintes etapas:
A) Cálculo da massa de cloral que se obteria se o rendimento da reação fosse 100% (m = 5,00 kg) ou equivalente.
B) Cálculo da massa de etanol que é necessário fazer reagir (m = 1,6 kg).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
2. Considere a reação traduzida por
Cl2 (g) + 2 Na (s) → 2 NaCl (s)
Nesta reação, o cloro atua como
(A) oxidante, oxidando-se.
(B) oxidante, reduzindo-se.
(C) redutor, reduzindo-se.
(D) redutor, oxidando-se.
- Opção (B)
⇒ O Cl2 atua como oxidante pois o número de oxidação dos átomos de cloro diminui de 0, em Cl2, para -1 no ião Cl – (cada átomo capta um eletrão; a molécula capta dois eletrões, sendo reduzida).
⇒ A molécula de cloro, ao sofrer redução, oxida o sódio, atuando, portanto, como oxidante.
- Opção (B)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
3. Considere que a energia necessária para dissociar uma mole de moléculas de Cl2 (g) é 242,7 kJ.
A variação de energia associada à formação de duas moles de átomos de cloro, em fase gasosa, a partir de uma mole de Cl2 (g) é
(A) + (2 × 242,7) kJ
(B) – (2 × 242,7) kJ
(C) + 242,7 kJ
(D) – 242,7 kJ
- Opção (C)
⇒ Para dissociar 1 mol de moléculas de Cl2 é fornecida a energia de 242,7 kJ e são originadas duas moles de átomos de Cl.
⇒ A variação de energia é +242,7 kJ.
- Opção (C)…………. 5 pontos
4. Considere átomos de cloro no estado fundamental.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
4.1. Num átomo de cloro, no estado fundamental, existem, no total,
(A) cinco eletrões de valência distribuídos por três orbitais.
(B) cinco eletrões de valência distribuídos por duas orbitais.
(C) sete eletrões de valência distribuídos por duas orbitais.
(D) sete eletrões de valência distribuídos por quatro orbitais.
- Opção (D)
⇒ O átomo de cloro pertence ao 3º período e ao grupo 17. Logo, no estado fundamental, tem 7 eletrões de valência em orbitais de número quântico principal igual a 3.
⇒ A sua configuração eletrónica de valência será 3s2 3p5. Como existem três orbitais p (3px, 3py e 3pz) conclui-se que duas orbitais ficam preenchidas e uma fica semipreenchida, por exemplo, na configuração 3px2, 3py2 e 3pz1.
Conclui-se que os 7 eletrões de valência se distribuem por 4 orbitais: a orbital 3s e as três orbitais 3p.
- Opção (D)…………. 5 pontos
4.2. Uma das orbitais de valência mais energéticas de um átomo de cloro, no estado fundamental, pode ser caracterizada pelo conjunto de números quânticos
(A) (3, 1, 0)
(B) (3, 0, 1)
(C) (3, 0, 0)
(D) (3, 1, 2)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (A)
⇒ As orbitais de valência mais energéticas do átomo de cloro, no estado fundamental, são orbitais do subnível 3p, a que só podem corresponder os números quânticos: n = 3, l = 1 e m = -1, 0, 1.
⇒ As opções (B) e (C) estão incorretas porque se trata de orbitais s, de energia menor do que orbitais p.
⇒ A opção (D) está incorreta porque o número quântico magnético não pode, neste caso, tomar o valor 2 (pode ser -1, 0 e +1).
- Opção (A)…………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
4.3. Como se designa a energia mínima necessária para remover um eletrão de um átomo de cloro, isolado e em fase gasosa, no estado fundamental?
- Energia de ionização [de um átomo de cloro] …………. 5 pontos
Grupo V
Um pequeno objeto de papel, abandonado de uma certa altura, cai verticalmente até ao solo, segundo uma trajetória retilínea, coincidente com o eixo Oy de um referencial unidimensional.
Admita que o objeto de papel pode ser representado pelo seu centro de massa (modelo da partícula material).
1. Considere, numa primeira situação, que o objeto de papel cai no ar.
Na Figura 2, está representado o gráfico da componente escalar, segundo o eixo Oy, da posição, y, do objeto de papel em função do tempo, t. Os dados registados foram adquiridos com um sensor de movimento.

- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.1. Qual é o esboço do gráfico que pode representar a distância percorrida pelo objeto de papel durante o intervalo de tempo em que os dados foram registados?

- Opção (B)
⇒ A distância percorrida é uma grandeza sempre positiva.
⇒ Inicialmente é nula mas vai aumentando à medida que o objeto se move.
⇒ Quando o papel atinge o solo a distância percorrida não aumenta mais, permanecendo com um valor constante.
- Opção (B)…………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.2. Em qual dos esquemas seguintes estão corretamente representadas, para o intervalo de tempo [0,90; 1,30] s, as forças que atuam no objeto de papel?

- Opção (C)
⇒ Do gráfico representado na figura 2, verifica-se que no intervalo de tempo [0,90; 1,30] s a variação da posição do objeto varia linearmente com o tempo, donde se conclui que a velocidade é constante (igual ao declive da reta que traduz y = f(t) no intervalo de tempo [0,55 ; 1,45] s).
⇒ Como a velocidade é constante, então a resultante das forças que atuam sobre o objeto é nula, logo a for a de resistência do ar é simétrica da força gravítica (mesma intensidade e mesma direção, mas sentido oposto).
- Opção (C)…………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1.3. Admita que a massa do objeto de papel é 0,23 g.
Calcule a energia dissipada pelo sistema objeto de papel + Terra no intervalo de tempo [0,90; 1,30] s.
Apresente todas as etapas de resolução.
⇒ A energia dissipada traduz-se numa diminuição de energia mecânica do sistema objeto de papel + Terra.
⇒ No intervalo de tempo considerado a posição varia linearmente com o tempo, o que significa que a velocidade do objeto de papel permanece constante.
Assim, a variação de energia cinética é nula.
⇒ Cálculo da variação de energia potencial gravítica:
- ΔEp = m g Δh = m g Δy = 0,23 x 10-3 x 10 x ( 0,20 – 0,76 ) = -1,29 x 103 J
Como a variação de energia mecânica é igual à soma da variação de energia cinética com a variação de energia potencial, conclui-se que a variação de energia mecânica é igual à variação de energia potencial:
- ΔEm = ΔEc + ΔEp = 0 + (-1,29 x 10-3) = -1,29 x 10-3 J
⇒ Conclui-se que a energia dissipada é 1,3 x 10-3 J
- A resolução deve apresentar as seguintes etapas:
A) Determinação da variação da energia cinética do objeto de papel no intervalo de tempo considerado (ΔEc = 0).
ou
Determinação do trabalho realizado pela força gravítica, que atua no objeto de papel, no intervalo de tempo considerado (WFgravítica = 1,29 x 10-3 J).
B) Determinação da variação da energia potencial gravítica do sistema objeto de papel + Terra no intervalo de tempo considerado (ΔEp = -1,29 x 10-3 J).
ou
Determinação do trabalho realizado pela força de resistência do ar, que atua no objeto de papel, no intervalo de tempo considerado (WFresistência do ar = -1,29 x 10-3 J).
C) Determinação da energia dissipada pelo sistema objeto de papel + Terra no intervalo de tempo considerado (Ed = 1,3 x 10-3 J).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
2. Considere agora, numa segunda situação, que o objeto de papel, abandonado da mesma altura, tem um movimento de queda livre.
Admita que o eixo Oy do referencial tem origem no solo e sentido positivo de baixo para cima.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.1. Apresente o esboço do gráfico da componente escalar, segundo o eixo Oy, da posição, y, do objeto de papel em função do tempo, t, desde o instante em que é abandonado até chegar ao solo.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.2. A equação v(t ) da componente escalar, segundo o eixo Oy, da velocidade, vy, do objeto de papel é
(A) vy = 10 t
(B) vy = -10 t
(C) vy = 1,20 – 10 t
(D) vy = 1,20 + 10 t
- Opção (B)
⇒ O papel inicia o movimento com velocidade nula e a aceleração é a da gravidade que aponta para baixo (sentido negativo de acordo com a convenção escolhida):
- vy = voy – gt = 0 – 10t = – 10t
- Opção (B)…………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.3. Qual das expressões seguintes permite calcular o tempo, em segundos (s), que o objeto de papel demorará a chegar ao solo se a altura da qual é abandonado se reduzir a metade?

- Opção (D)…………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2.4. Admita que, em simultâneo com o objeto de papel, se abandona da mesma altura uma esfera metálica de maior massa.
Se o objeto de papel e a esfera metálica caírem livremente, a esfera chegará ao solo com velocidade de
(A) igual módulo e energia cinética maior.
(B) igual módulo e energia cinética igual.
(C) maior módulo e energia cinética igual.
(D) maior módulo e energia cinética maior.
- Opção (A)
⇒ A aceleração da gravidade não depende da massa do corpo, logo como caem ambos da mesma altura atingem o solo com a mesma velocidade.
⇒ A energia cinética aumenta com a massa do corpo, assim a esfera metálica terá, para a mesma velocidade, maior energia cinética.
- Opção (A)…………. 5 pontos
Grupo VI
Com o objetivo de determinar experimentalmente a velocidade de propagação do som no ar, um grupo de alunos fez uma montagem semelhante à representada na Figura 3, na qual utilizou um osciloscópio, um gerador de sinais, um microfone, um altifalante com suporte e fios de ligação.

Os alunos começaram por ligar o gerador de sinais ao osciloscópio para produzir um sinal elétrico que registaram no osciloscópio.
Ligaram depois o altifalante ao gerador de sinais e o microfone ao osciloscópio, tendo o cuidado de alinhar sempre o altifalante e o microfone, no decorrer das experiências que realizaram.
O valor tabelado da velocidade de propagação do som no ar, nas condições em que foram realizadas as experiências, é 342,3 m s-1.
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
- 11ºano – Física – A.l. – 2.2 – Velocidade de propagação do som
1. Indique a razão pela qual os alunos ligaram o altifalante ao gerador de sinais e a razão pela qual ligaram o microfone ao osciloscópio.
⇒ A ligação do altifalante ao gerador de sinais faz-se para ser produzido um sinal sonoro, como resultado da conversão do sinal elétrico que o gerador produz, e a ligação do microfone ao osciloscópio serve para ser produzido um sinal elétrico, correspondente ao sinal sonoro, que poder ser analisado visualmente no ecrã.
- A resposta deve apresentar os seguintes tópicos:
A) Os alunos ligaram o altifalante ao gerador de sinais para que o sinal elétrico [produzido por este] fosse convertido num sinal sonoro.
B) Os alunos ligaram o microfone ao osciloscópio para que o sinal elétrico[, resultante da conversão do sinal sonoro no microfone,] fosse registado no osciloscópio.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

2. Os alunos mantiveram o altifalante e o microfone à mesma distância um do outro.
A Figura 4 representa o ecrã do osciloscópio onde estão registados os sinais obtidos no decorrer da experiência.

- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
2.1. Os sinais registados no ecrã do osciloscópio apresentam
(A) igual amplitude e igual frequência.
(B) igual amplitude e diferente frequência.
(C) diferente amplitude e diferente frequência.
(D) diferente amplitude e igual frequência.
- Opção (D)
⇒ No ecrã visualizam-se o mesmo número de períodos de ambos os sinais, logo, têm frequências iguais.
⇒ Admitindo que as escalas verticais de ambos os canais do osciloscópio são iguais, o que tem um pico de maior valor tem maior amplitude.
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
- 11ºano – Física – A.l. – 2.2 – Velocidade de propagação do som
2.2. Quanto tempo demorou o sinal sonoro a percorrer a distância entre o altifalante e o microfone?
(A) 10 ms
(B) 2 ms
(C) 1 ms
(D) 0,5 ms
- Opção (D)
⇒ O desfasamento temporal dos picos dos dois sinais, lido no eixo das abcissas, é igual a metade de uma divisão.
⇒ Como o tempo correspondente a cada divisão é de 1 ms, conclui-se que o tempo que o sinal sonoro demorou a percorrer a distância entre o altifalante e o microfone é de 1 ms/2 = 5 ,0 ms
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
- 11ºano – Física – A.l. – 2.2 – Velocidade de propagação do som
3. Os alunos afastaram depois gradualmente o microfone do altifalante e mediram, para cada distância entre estes, o tempo que o sinal sonoro demorava a percorrer essa distância.
Os valores obtidos estão registados na tabela seguinte.

Determine o erro relativo, em percentagem, do valor experimental da velocidade de propagação do som no ar.
Comece por obter o valor experimental da velocidade de propagação do som no ar, em metro por segundo (m s–1), a partir do declive da reta que melhor se ajusta ao conjunto de valores apresentados na tabela (utilize a calculadora gráfica).
Apresente todas as etapas de resolução.
⇒ Equação da reta de ajuste ao gráfico da distância (d expressa em metros) entre o microfone e o altifalante em função do tempo (t expresso em segundos):
- d = 324,0 t + 1,2 x 10-2 ⇒ d ≈ 324,0 t

⇒ Como d = vt conclui-se que o valor experimental da velocidade de propagação do som no ar é vexperimental = 324,0 ms-1
⇒ Determinação do erro relativo:
- A resolução deve apresentar as seguintes etapas:
A) Cálculo do valor experimental da velocidade de propagação do som no ar (v = 324,0 m s-1).
B) Cálculo do erro relativo, em percentagem, do valor experimental da velocidade de propagação do som no ar (5,35%).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos.
FIM




