2012 – Teste Intermédio – 10ºAno
Voltar a: Física e Química
- Prova Escrita de Física e Química A – Versão 1
- Prova: Teste Intermédio – 10ºAno – 2012
- Duração do Teste: 90 minutos | 30.05.2012
Grupo I
O ozono, O3, encontra-se na estratosfera, formando a chamada camada de ozono, que se estende por vários quilómetros de altitude.
Na estratosfera, a interação da radiação ultravioleta B (UV-B) com as moléculas de oxigénio dá origem à formação de radicais livres (átomos) de oxigénio. São estes radicais que, reagindo com outras moléculas de oxigénio, na estratosfera, produzem o ozono.
Por seu lado, as moléculas de ozono também interagem com a radiação UV-B, na estratosfera, dissociando-se.
Se não houvesse interferência de outras espécies químicas presentes na estratosfera, a concentração de ozono nesta camada da atmosfera permaneceria aproximadamente constante – a formação e a decomposição deste gás ocorreriam à mesma velocidade.
No entanto, alguns radicais livres também presentes na estratosfera, nomeadamente os radicais livres (átomos) de cloro, reagem com o ozono, que passa a decompor-se a uma velocidade superior à velocidade a que se forma. Como resultado da ação destes radicais livres, ocorre, assim, uma diminuição da concentração de ozono na estratosfera, fenómeno que é habitualmente designado por «buraco do ozono».
Maria Teresa Escoval, A Ação da Química na Nossa Vida, Editorial Presença, 2010 (adaptado)
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
1. Escreva as equações químicas que traduzem as reações referidas no segundo parágrafo do texto.
- O2 (g) → O (g) + O (g)
- O2 (g) + O (g) → O3 (g)
⇒ O2 (g) → O (g) + O (g)
⇒ O2 (g) + O (g) → O3 (g) —————————– 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
2. A reação dos radicais livres de oxigénio com as moléculas de oxigénio, na estratosfera, envolve a libertação de cerca de 105 kJ por cada mole de moléculas de ozono que se formam.
A variação de energia, em joule (J), associada à formação de uma molécula de ozono, poderá ser traduzida pela expressão
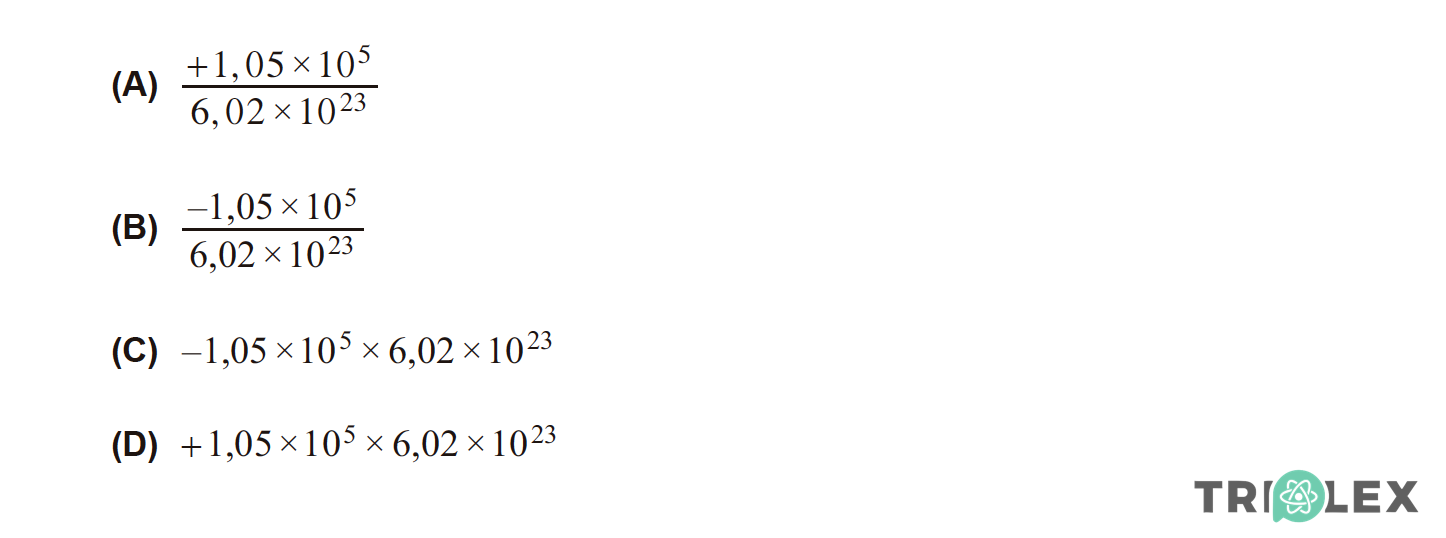
- Opção (B)…………. 8 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
3. Explique porque é que as moléculas de oxigénio e de ozono constituem filtros da radiação UV-B na estratosfera.
⇒ As moléculas de dioxigénio e de ozono da estratosfera constituem filtros de radiação UV-B porque absorvem grande parte deste tipo de radiações provenientes do Sol
O2 (g) + UV-B → 2 O (g)
O3 (g) + UV-B → O2 (g) + O (g)
⇒ moderando a sua chegada à troposfera e à superfície da Terra.
- A resposta deve apresentar os seguintes tópicos:
A) As moléculas de oxigénio e de ozono absorvem grande parte da radiação UV-B que chega à estratosfera.
B) [Ao absorverem a radiação] aquelas moléculas impedem a passagem da radiação UV-B para a troposfera e/ou a sua chegada à superfície terrestre.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
4. Os CFC (clorofluorocarbonetos) são compostos que, interagindo com a radiação UV-B, constituem a principal fonte de radicais livres de cloro na estratosfera.
Nas moléculas de CFC que chegam à estratosfera, verifica-se assim a quebra das ligações C–Cl, mais fracas, não ocorrendo, no entanto, a quebra das ligações C–F, mais fortes.
Indique o motivo que justifica que a quebra das ligações C–F não ocorra.
⇒ Não ocorre quebra das ligações C–F porque a energia transportada pelas radiações UV-B não é suficiente para partir as ligações C–F, mais fortes que as ligações C–Cl.
- A energia da radiação UV-B não é suficiente para quebrar as ligações C – F. ————— 8 pontos
Grupo II
Muitos dos CFC são derivados do metano, CH4, um hidrocarboneto saturado cujas moléculas são constituídas por átomos de carbono e de hidrogénio.
À temperatura e à pressão ambientes, o metano é um gás.
- 10ºano – Química – Domínio 1 – subdomínio 1 (Massa e tamanho dos átomos)
1. Determine a quantidade total, em mol, de átomos existente numa amostra de 20,0 g de metano, CH4(g).
Apresente todas as etapas de resolução.
- A resolução deve apresentar as seguintes etapas:
A) Cálculo da quantidade de metano existente na amostra (n = 1,246 mol).
B) Cálculo da quantidade total de átomos existente na amostra (n = 6,23 mol).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos*.
* Descritores e desvalorizações apresentados no primeiro quadro da dos Critérios Gerais de Classificação.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2. As moléculas de metano apresentam geometria tetraédrica.
Nestas moléculas,
(A) não existem eletrões de valência não ligantes, e existem, no total, oito eletrões ligantes.
(B) existem eletrões de valência não ligantes, e existem, no total, quatro eletrões ligantes.
(C) não existem eletrões de valência não ligantes, e existem, no total, quatro eletrões ligantes.
(D) existem eletrões de valência não ligantes, e existem, no total, oito eletrões ligantes.
- Opção (A)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3. No átomo de carbono no estado fundamental, os eletrões de valência encontram-se distribuídos por
(A) uma orbital.
(B) duas orbitais.
(C) três orbitais.
(D) quatro orbitais.
- Opção (C)
⇒ A configuração eletrónica de valência do átomo de carbono, 6C, no estado fundamental, 2s2 2px1 2py1 mostra 4 eletrões de valência distribuídos por uma orbital s e duas orbitais p.
⇒ A opção (A) é falsa, pois uma orbital fica completamente preenchida com dois eletrões pelo que não pode conter os quatro eletrões de valência do átomo de carbono;
⇒ A opção (B) é falsa por não respeitar a regra de Hund no preenchimento de orbitais;
⇒ A opção (D) é falsa por não respeitar o princípio de energia mínima de preenchimento de orbitais.
- Opção (C)…………. 8 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
4. Na Figura 1, está representado um diagrama de níveis de energia do átomo de hidrogénio.
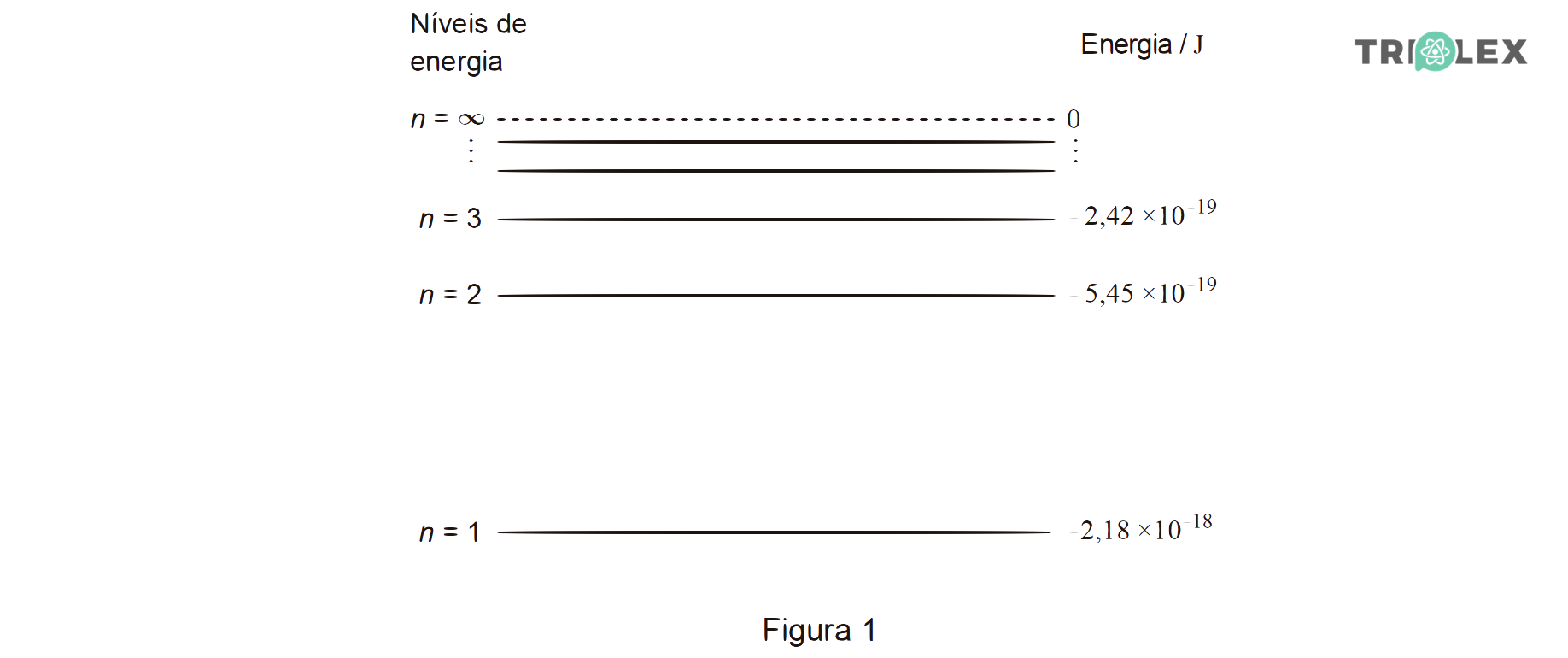
A Figura 2 representa parte do espectro de emissão do átomo de hidrogénio, na região do visível.
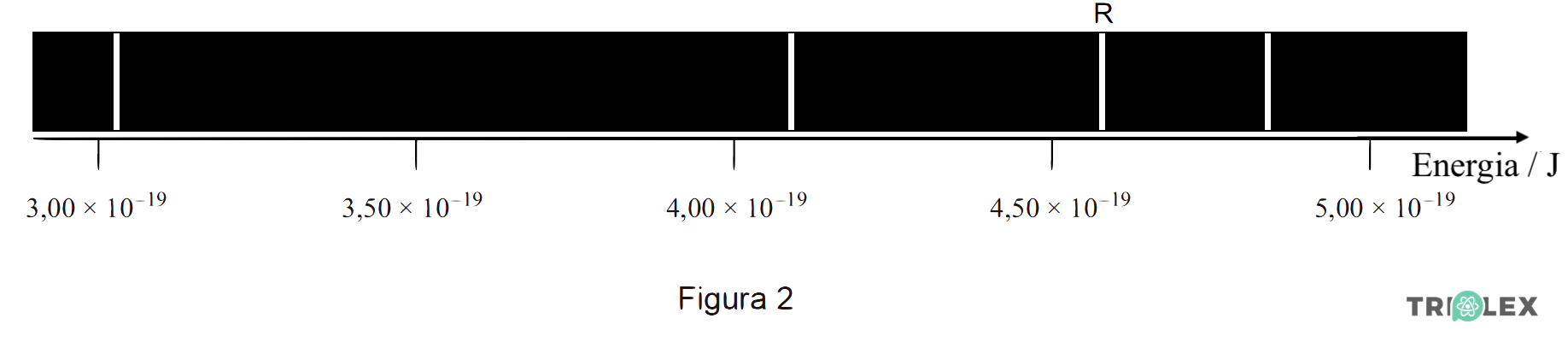
Calcule, para a transição eletrónica que origina a risca assinalada pela letra R na Figura 2, a energia do nível em que o eletrão se encontrava inicialmente.
Apresente todas as etapas de resolução.
⇒ A energia da radiação emitida correspondente à risca R tem de ser calculada por interpolação no desenho, atendendo a que 0,50 x 10-19 J correspondem a 30 mm sobre o papel da prova.
⇒ A risca localiza-se a cerca de 5 mm (0,08 x 10-19 J) acima de 4,50 x 10-19, ou seja, a 4,58 x 10-19 J.
⇒ Como se trata do espetro de emissão do átomo de hidrogénio na região do visível, a transição eletrónica que origina a risca assinalada pela letra R ocorre de um nível energético mais elevado para o 1.º estado excitado (n = 2).
⇒ Sendo X a energia do nível em que o eletrão se encontrava inicialmente e – 5,45 x 10-19 J a energia do 1.º estado excitado, virá:
- Energia da radiação emitida = X – E2 ⇔ 4,58 x 10-19 J = X – (- 5,45 x 10-19 J) ⇔ X = – 8,70 x 10-20 J
- A resolução deve apresentar as seguintes etapas:
A) Determinação da energia da radiação emitida na transição eletrónica considerada (E = 4,58 x 10-19 J).
B) Determinação da energia do nível em que o eletrão se encontrava inicialmente (E = – 8,7 x 10-20 J).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos*.
* Descritores e desvalorizações apresentados no primeiro quadro dos Critérios Gerais de Classificação.
Nota – A resposta deve ser classificada tendo em conta as dimensões que a figura apresenta após impressão.
Grupo III
Com o objetivo de determinar experimentalmente a temperatura de fusão do naftaleno, alguns grupos de alunos efetuaram várias medições.
O valor tabelado da temperatura de fusão do naftaleno, nas condições em que foram realizadas as medições, é 80,0 ºC.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
- 11ºano – Física – A.l. – Medições
1. Depois de efetuadas as medições pelos grupos de alunos, a medida da temperatura de fusão do naftaleno, expressa em função do valor mais provável e da incerteza relativa, foi 81,1 ºC ± 1,1 %.
Determine o intervalo de valores no qual estará contido o valor experimental da temperatura de fusão do naftaleno.
Apresente todas as etapas de resolução.
- Incerteza relativa = 1,1% ⇔ Incerteza absoluta = (1,1%) x 81,1 ºC = 0,89 ºC
⇒ Intervalo de valores no qual estar contido o valor experimental, com certa probabilidade:
- (81,1 – 0,89) ºC = 80,2 ºC e (81,1 + 0,89) ºC = 82,0 ºC, ou seja, [80,2 ºC; 82,0 ºC].
- A resolução deve apresentar as seguintes etapas:
A) Cálculo da incerteza absoluta associada à medida da temperatura de fusão do naftaleno ( ± 0,9 ºC).
B) Determinação do intervalo de valores no qual estará contido o valor experimental da temperatura de fusão do naftaleno ([80,2 ; 82,0] ºC).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos*.
* Descritores e desvalorizações apresentados no primeiro quadro dos Critérios Gerais de Classificação.
Nota – A resposta deve ser classificada tendo em conta as dimensões que a figura apresenta após impressão.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
- 11ºano – Física – A.l. – Medições
2. Dois grupos de alunos, Grupo 1 e Grupo 2, realizaram três ensaios, nas mesmas condições, nos quais mediram os valores de temperatura de fusão, θf, do naftaleno, que se encontram registados na tabela seguinte.

Pode concluir-se, a partir da informação dada, que os valores medidos pelo Grupo 1, comparados com os valores medidos pelo Grupo 2, são
(A) mais exatos e mais precisos.
(B) mais exatos e menos precisos.
(C) menos exatos e menos precisos.
(D) menos exatos e mais precisos.
- Opção (B)
⇒ O valor médio das temperaturas lidas pelo grupo 1 aproxima-se mais do valor real (maior exatidão), embora os desvios das medições sejam mais afastados do valor médio (menor precisão)
- Opção (B)…………. 8 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3. Considere que se forneceu energia a uma amostra pura de naftaleno no estado sólido, inicialmente à temperatura ambiente, até esta fundir completamente.
Qual é o esboço do gráfico que pode representar a temperatura do naftaleno, em função do tempo, para a situação descrita?

- Opção (A)
⇒ O gráfico representado pela letra (A) representa o aumento da temperatura durante o aquecimento da amostra desde a temperatura ambiente até à temperatura de fusão (80 ºC) seguido da constância de temperatura durante a fusão.
- Opção (A)…………. 8 pontos
Grupo IV
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1. Utilizou-se uma resistência de aquecimento de 200 W para aquecer uma amostra de 500 g de água, tendo a temperatura da amostra aumentado 27 ºC.
Considere que o rendimento do processo de aquecimento foi 70%.
Determine o intervalo de tempo que foi necessário para o aquecimento da amostra de água.
Apresente todas as etapas de resolução.
c (capacidade térmica mássica da água) = 4,18 × 103 J kg–1 ºC–1- Pelét. = 200 W;
- m = 500 g = 0,500 kg;
- Δθ = 27 ºC
- η = 70% = 0,70;
- c = 4,18 x 103 J kg-1 ºC-1
- Δt = ?

⇒ A energia útil, energia utilizada no aquecimento da amostra de água, durante o intervalo de tempo Δt, é:
- Eútil = Pútil Δt, que também é dada pela relação Eútil = m c Δθ concluindo-se que:
- Pútil Δt = m c Δθ ⇔ 140 x Δt = 0,500 x 4,18 x 103 x 27 ⇔ Δt = 4,0 x 102 s
- A resolução deve apresentar as seguintes etapas:
A) Cálculo da energia necessária ao aquecimento da amostra de água (E = 5,64 x 104 J).
B) Cálculo da energia fornecida pela resistência de aquecimento (E = 8,06 x 104 J).
C) Cálculo do intervalo de tempo que foi necessário para o aquecimento da amostra de água (Δt = 4,0 x 102 s).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos*.
* Descritores e desvalorizações apresentados no primeiro quadro dos Critérios Gerais de Classificação.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
2. A água, colocada numa cafeteira, pode também ser aquecida num fogão a gás.
Identifique o principal processo de transferência de energia, como calor, que permite o aquecimento de toda a água contida na cafeteira e descreva o modo como essa transferência ocorre.
⇒ O principal processo de transferência de energia como calor responsável pelo aquecimento de toda a água (um fluido) contida na cafeteira é o processo de convecção.
⇒ A água que está em contacto com a base da cafeteira ao aquecer fica menos densa e sobe, dando origem a uma corrente ascendente, quente, que, durante a subida, irá ceder energia à água que se encontra a temperatura inferior.
Assim, durante a subida arrefece, fica mais densa, e pela ação da gravidade desce, dando origem a uma corrente descendente fria.
⇒ Essas correntes de convecção, ascendentes quentes e descendentes frias, que se repetem ciclicamente e em simultâneo, são as responsáveis pelo aquecimento de toda a água contida na cafeteira.
- A resposta deve apresentar as seguintes tópicos:
A) O principal processo de transferência de energia, como calor, que permite o aquecimento de toda a água contida na cafeteira é a convecção.
B) A água que se encontra mais abaixo na cafeteira aquece, tornando-se menos densa, o que dá origem a uma corrente quente ascendente. Esta água, ao subir, arrefece, tornando-se mais densa, o que dá origem a uma corrente fria descendente.
C) As correntes quentes ascendentes e as correntes frias descendentes, repetindo-se, em simultâneo, ao longo do tempo, permitem o aquecimento de toda a água contida na cafeteira.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
* Descritores e desvalorizações apresentados no primeiro quadro da dos Critérios Gerais de Classificação.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3. Quando se pretende manter a temperatura de uma amostra de água aproximadamente constante, pode utilizar-se uma garrafa térmica, tal como a representada na Figura 3.
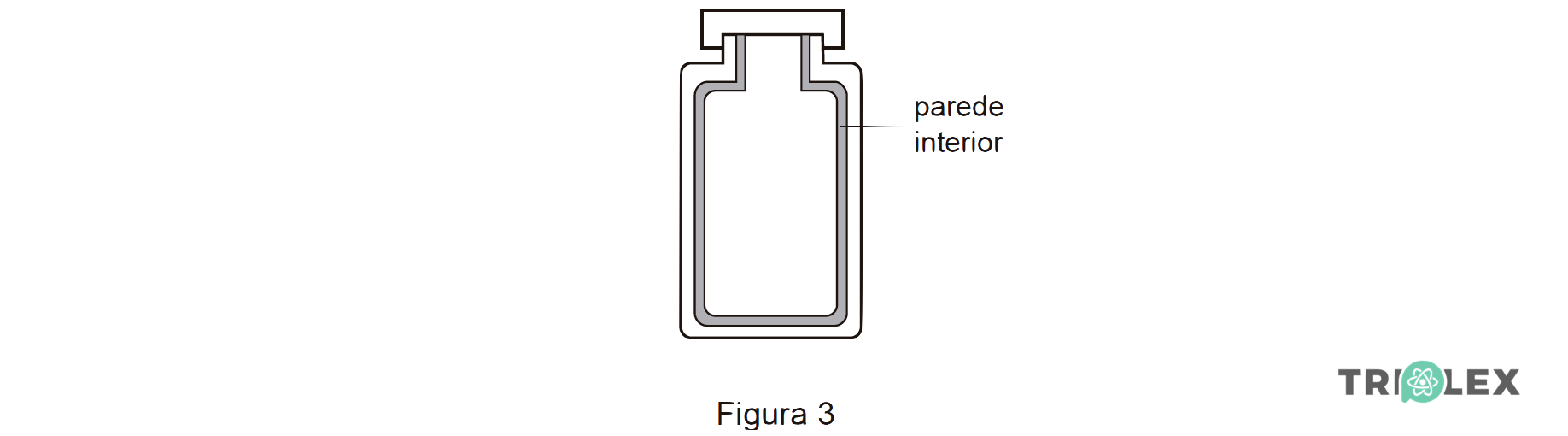
Indique, justificando, duas características que a parede interior da garrafa térmica deve apresentar.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ A parede interior da garrafa térmica deve ser espelhada, de modo a refletir preferencialmente a radiação térmica, minimizando assim as perdas de energia por radiação e ser feita de um material mau condutor de calor (baixa condutividade térmica) e/ou deve ser dupla, de modo a minimizar as perdas de energia como calor por condução.
- A resposta deve apresentar dois dos seguintes tópicos:
A) A parede interior da garrafa térmica deve ser espelhada, para minimizar a transferência de energia por radiação.
B) A parede interior da garrafa térmica deve ser feita de um material que seja um mau condutor térmico, para minimizar a transferência de energia [, como calor,] por condução.
C) A parede interior da garrafa térmica deve ser dupla, [com ar ou vácuo no seu interior] para minimizar a transferência de energia [, como calor,] por condução.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
4. A capacidade térmica mássica do azeite é cerca de metade da capacidade térmica mássica da água.
Se for fornecida a mesma energia a uma amostra de 200 g de azeite e a uma amostra de 100 g de água, a variação de temperatura da amostra de azeite será, aproximadamente,
(A) igual à variação de temperatura da amostra de água.
(B) o dobro da variação de temperatura da amostra de água.
(C) metade da variação de temperatura da amostra de água.
(D) um quarto da variação de temperatura da amostra de água.
- Opção (A)
⇒ cazeite = 0,5 cágua;
⇒ Eazeite = Eágua;
⇒ mazeite = 200 g;
⇒ mágua = 100 g
Como Eazeite = Eágua, então:
mazeite cazeite ΔTazeite = mágua cágua ΔTágua ⇔
⇒ 200 x 0,5 cágua ΔTazeite = 100 x cágua ΔTágua ⇔
⇔ 100 x cágua ΔTazeite = 100 x cágua ΔTágua ⇔
⇔ ΔTazeite = ΔTágua
- A variação de temperatura de ambas as amostras é a mesma.
- Opção (A)…………. 8 pontos
Grupo V
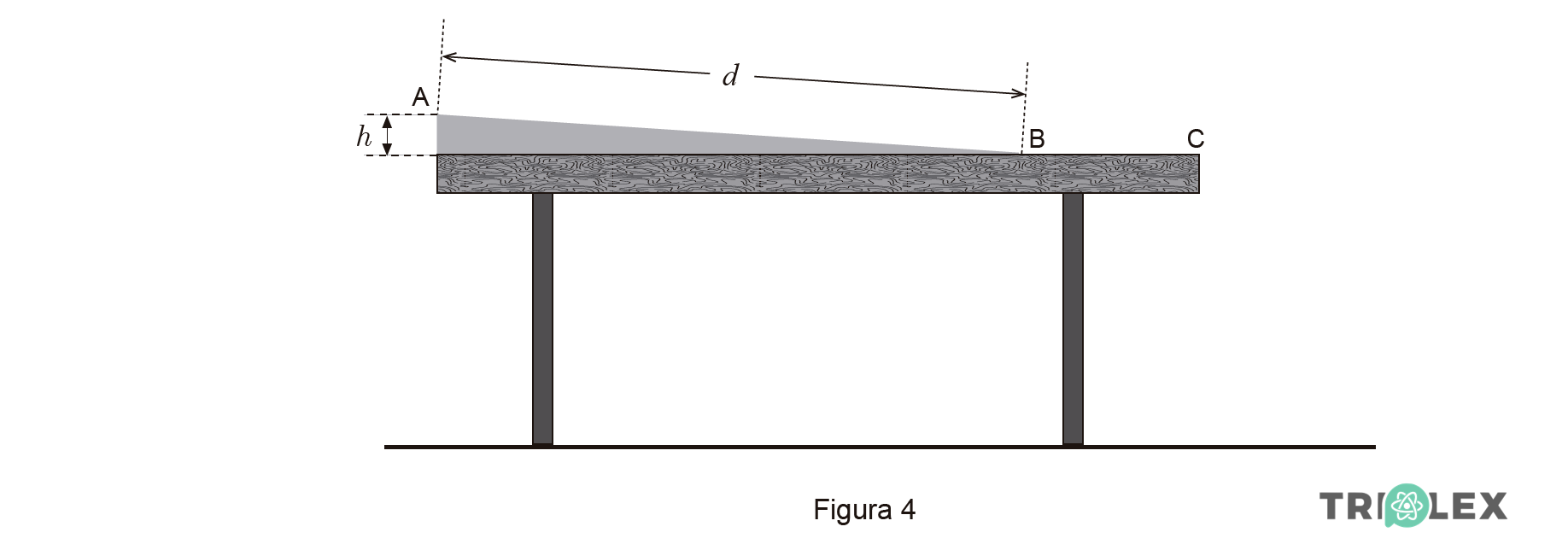
A Figura 4 (que não está à escala) representa uma calha inclinada, montada sobre uma mesa.
Um pequeno paralelepípedo de madeira, de massa m, é abandonado na posição A, situada a uma altura h em relação ao tampo da mesa. O paralelepípedo percorre a distância d sobre a calha, chegando à posição B com velocidade de módulo vB. Em seguida, desliza sobre o tampo da mesa, entre as posições B e C, caindo depois para o solo.
Considere desprezáveis todas as forças dissipativas e admita que o paralelepípedo pode ser representado pelo seu centro de massa (modelo da partícula material).
Considere o solo como nível de referência da energia potencial gravítica.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1. No deslocamento entre as posições A e B, o trabalho realizado pela força gravítica que atua no paralelepípedo pode ser calculado pela expressão
(A) W = m g d
(B) W = -m g d
(C) W = m g h
(D) W = -m g h
- Opção (C)
⇒ O trabalho realizado pela for a gravítica, for a conservativa, entre as posições A e B simétrico da variação de energia potencial entre estas posições.
- WFg = – ΔEp ⇔ WFg = – m g (hB – hA) ⇔ WFg = – m g (0 – h) ⇔ WFg = m g h
- Opção (C)…………. 8 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2. No deslocamento entre as posições A e B, a soma dos trabalhos realizados pelas forças que atuam no paralelepípedo pode ser calculada pela expressão

- Opção (D)
⇒ Para determinar o trabalho realizado pelas forças que atuam sobre o paralelepípedo ou pela resultante das forças que sobre ele atuam, no percurso de A a B, recorre-se à Lei do Trabalho-Energia ou Teorema da Energia Cinética:
- WFR = ΔEc
Como EcA = 0 J, então:
- WFR = EcB ⇔ WFR = ½ m v2B
- Opção (D)…………. 8 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
3. Apresente o esboço do gráfico que pode representar a energia mecânica, Em, do sistema paralelepípedo + Terra, em função do tempo, t, para o movimento do paralelepípedo desde a posição A até chegar ao solo.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
4. Considere que a altura do tampo da mesa em relação ao solo é 80 cm e que o paralelepípedo chega ao solo com velocidade de módulo 4,5 ms-1.
Determine a altura h, representada na Figura 4, a que a posição A se encontra em relação ao tampo da mesa.
Apresente todas as etapas de resolução.
- hC = 80 cm = 0,80 m;
- vsolo = v = 4,5 m s-1;
- g = 10 m s-2;
- vA = 0 m s-1
- h = ?
⇒ Como as forças dissipativas são desprezíveis em todo o percurso, há conservação da energia mecânica entre A e o solo:
- EmA = Em ⇔ EcA + EpA = Ec + Ep
⇒ Como o paralelepípedo é abandonado no ponto A, a sua velocidade nesta posição, vA, nula, bem como a sua energia cinética, EcA, e como a origem do referencial é o solo, a energia potencial gravítica do sistema paralelepípedo + Terra nesta posição é nula.
Assim: Mas,
Mas,
- h = hA – hC ⇒ h = 1,01 – 0,80 = 2,1 x 10-1 m
- A resolução deve apresentar as seguintes etapas:
A) Cálculo da energia mecânica do sistema paralelepípedo + Terra (Em = 10,1 m J).
B) Cálculo da altura a que a posição A se encontra em relação ao tampo da mesa (h = 2,1 x 10-1 m).
A resposta a este item deve ser enquadrada num dos níveis de desempenho relacionados com a consecução das etapas, de acordo com a tabela seguinte.

A classificação a atribuir à resposta resulta da pontuação decorrente do enquadramento num dos níveis de desempenho atrás descritos, à qual podem ser subtraídos pontos, de acordo com o enquadramento nos níveis de desempenho relacionados com o tipo de erros cometidos*.
* Descritores e desvalorizações apresentados no primeiro quadro dos Critérios Gerais de Classificação.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
5. Se, em vez do paralelepípedo de madeira, se abandonasse na posição A um outro paralelepípedo do mesmo tamanho mas de maior massa, este chegaria ao solo com
(A) maior energia mecânica.
(B) maior velocidade.
(C) menor energia mecânica.
(D) menor velocidade.
- Opção (A)
⇒ De acordo com o referido no item 4. a energia mecânica do paralelepípedo ao chegar ao solo é :
- Em = EmA ⇔ Em = EpA ⇔ Em = m g hA
⇒ Assim, aumentando a massa do paralelepípedo e mantendo todas as outras condições, a energia mecânica com que atinge o solo aumenta.
- Opção (A)…………. 8 pontos
FIM