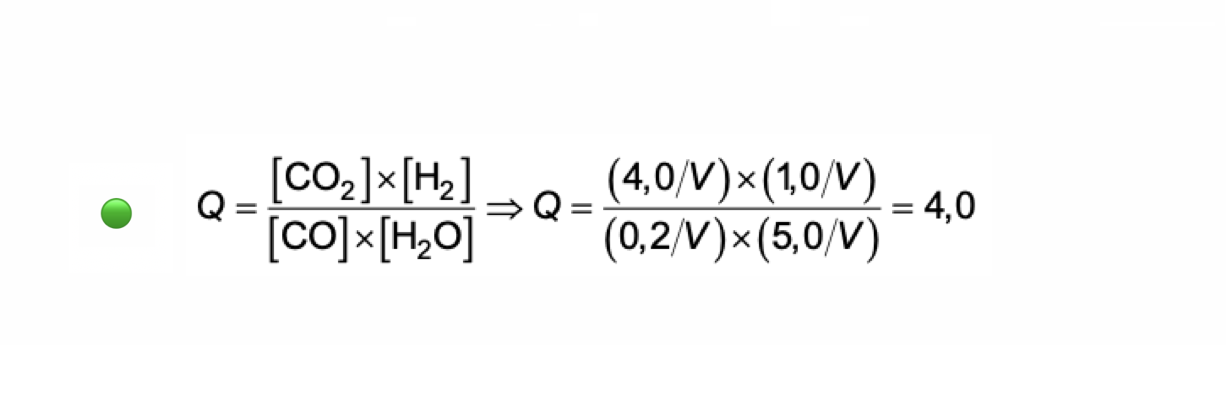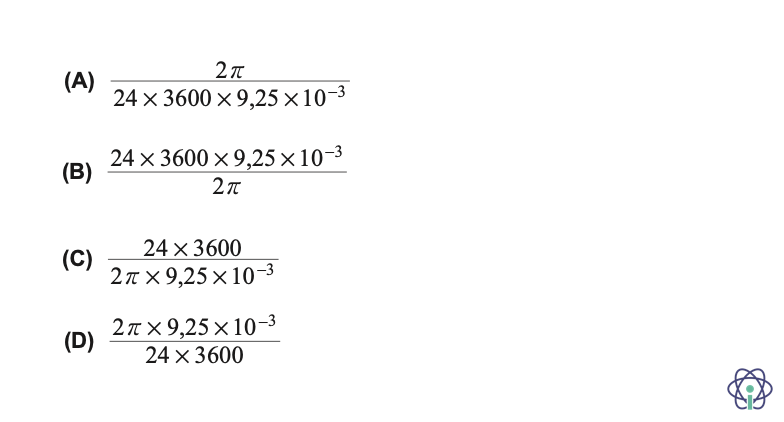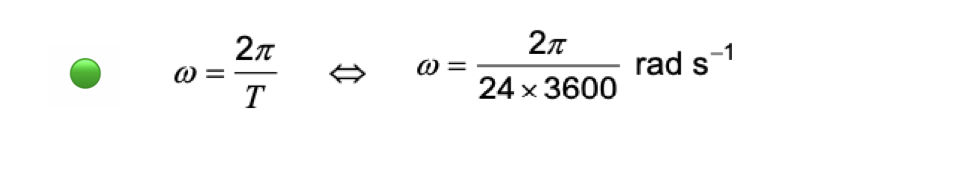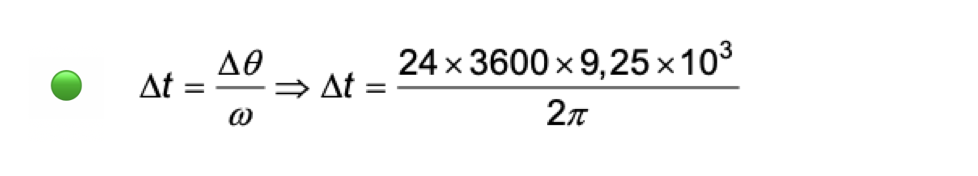Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: Época Especial – 2025
A prova inclui 15 itens, devidamente identificados no enunciado, cujas respostas contribuem obrigatoriamente para a classificação final.
Dos restantes 8 itens da prova, apenas contribuem para a classificação final os 4 itens cujas respostas obtenham melhor pontuação.
1. Portugal integra, desde 1979, um programa internacional de recolha de amostras de ar para análise dos gases com efeito de estufa.
De entre esses gases, destacam-se o dióxido de carbono, CO2 , o metano, CH4 , o monóxido de carbono, CO, e o óxido de dinitrogénio, N2O.
1.1. Considere que, no local de recolha, o ar é homogéneo e que as amostras são representativas do ar circundante.
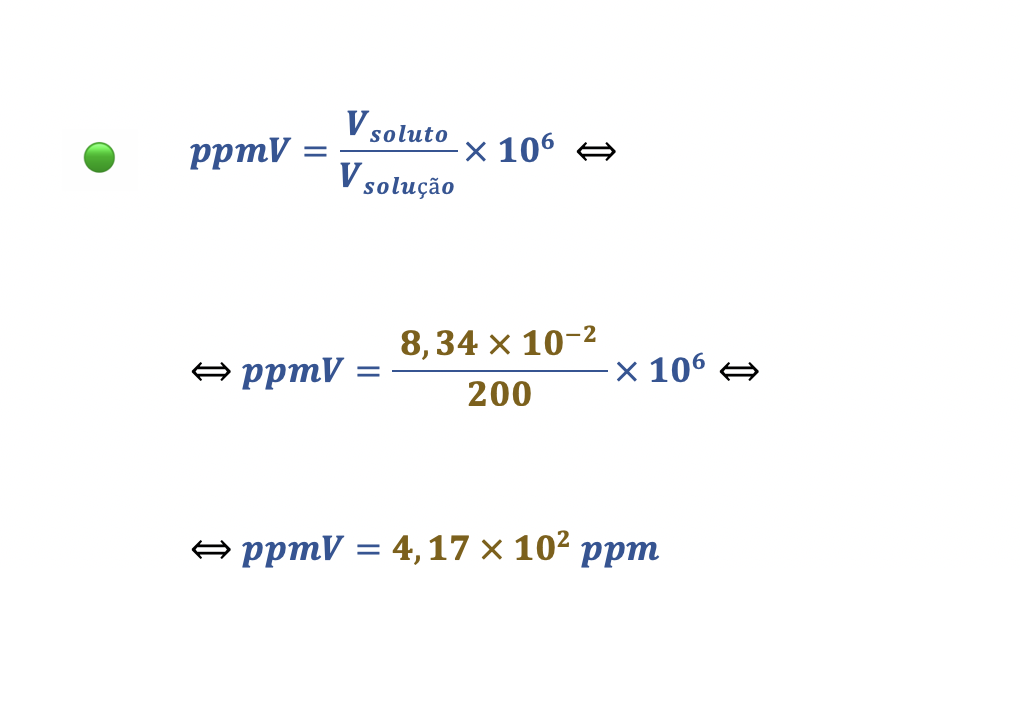
Numa amostra de 200 cm3 de ar seco, existem 8,34 x 10-2 cm3 de CO2.
O teor de CO2 nessa amostra é _______ e é _______ ao teor de CO2 no ar circundante, nas mesmas condições de pressão e de temperatura.
(A) 4,17 x 102 ppm (em volume) … inferior
(B) 4,17 x 102 ppm (em volume) … igual
(C) 4,17 x 10-4 ppm (em volume) … igual
(D) 4,17 x 10-4 ppm (em volume) … inferior
- Opção (B) ……………. 10 pontos
1.2. Considere dois recipientes iguais, fechados, um deles contendo CH4 (M = 16,05 g mol-1) e o outro contendo CO (M = 28,01 g mol-1), ambos no estado gasoso e nas mesmas condições de pressão e de temperatura.
Dentro dos dois recipientes, o número de moléculas é
(A) igual, e a massa de gás também é igual.
(B) diferente, mas a massa de gás é igual.
(C) igual, mas a massa de gás é diferente.
(D) diferente, e a massa de gás também é diferente.
- Opção (C)
🛑 De acordo com a Lei de Avogadro, “volumes iguais de gases diferentes, medidos nas mesmas condições de pressão e de temperatura, contêm o mesmo número de partículas”.
🛑 O número de moléculas nos dois recipientes é igual.
❇️ Como as massas molares dos dois gases, CH4 e CO , são diferentes, e m = n x M , para a mesma quantidade de gás, n , a massa de gás dos dois recipientes é diferente.
- Opção (C) ……………. 10 pontos
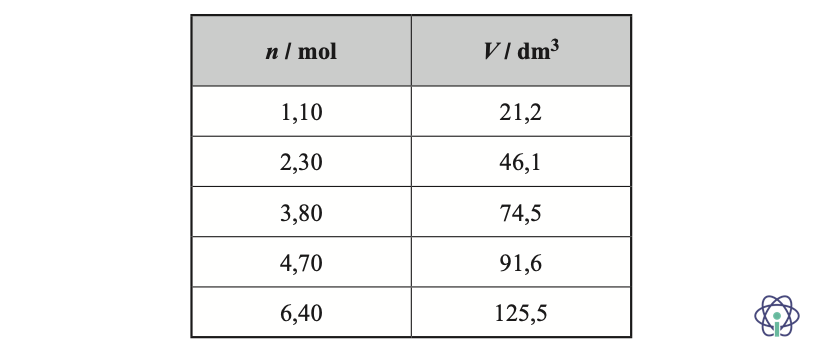
1.3. Na tabela, apresentam-se diferentes quantidades, n, de N2O (g) e os respetivos volumes, V, medidos nas mesmas condições de pressão e de temperatura.
Averigue, justificando, se o N2O (g) se encontra nas condições normais de pressão e de temperatura (condições PTN).
Na resposta, comece por apresentar a equação da reta de ajuste obtida.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
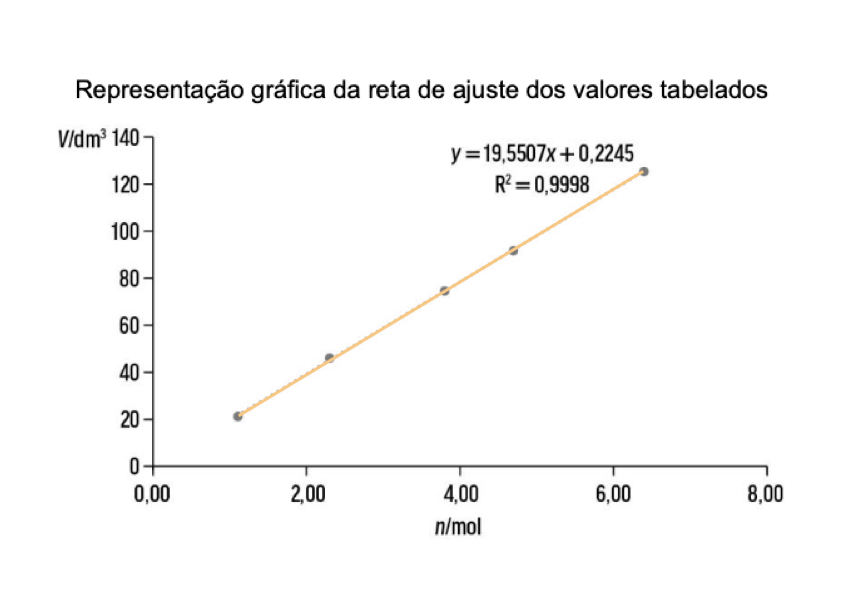
🛑 Recorrendo à calculadora gráfica, a equação da reta de ajuste ao gráfico V = f (n) é:
V = 19,6 n + 0,2 (SI)
🛑 V = n x Vm , o declive da reta, 19,6 dm3 mol−1, corresponde ao volume molar de N2O (g) nas condições de pressão e temperatura da experiência.
🛑 O N2O (g) não se encontra nas condições PTN porque o valor encontrado, Vmolar = 19,6 dm3 /mol, é diferente de Vmolar = 22,4 dm3 (volume ocupado por uma mole de qualquer gás ideal nas condições PTN ).
❇️ Não se encontra nas condições PTN
Elementos de resposta:
⇒ a equação da reta de ajuste ao gráfico [V = f (n) ] é V = 19,6 n + 0,2 (SI) (ver notas 1 e 2);
⇒ o volume molar do N2O (g) obtido a partir da reta de ajuste é 19,6 dm3 mol-1;
⇒ o N2O (g) não se encontra em condições PTN, porque 19,6 dm3 mol-1 é diferente de 22,4 dm3 mol-1 (ver nota 3).
Notas:
1. A apresentação de n = f (V ) (n = 0,0511V – 0,01)(SI)) não implica qualquer desvalorização.
2. Na equação da reta de ajuste, a omissão da ordenada na origem não implica qualquer desvalorização.
3. A omissão das unidades no volume molar deve ser equiparada a falhas na linguagem científica.
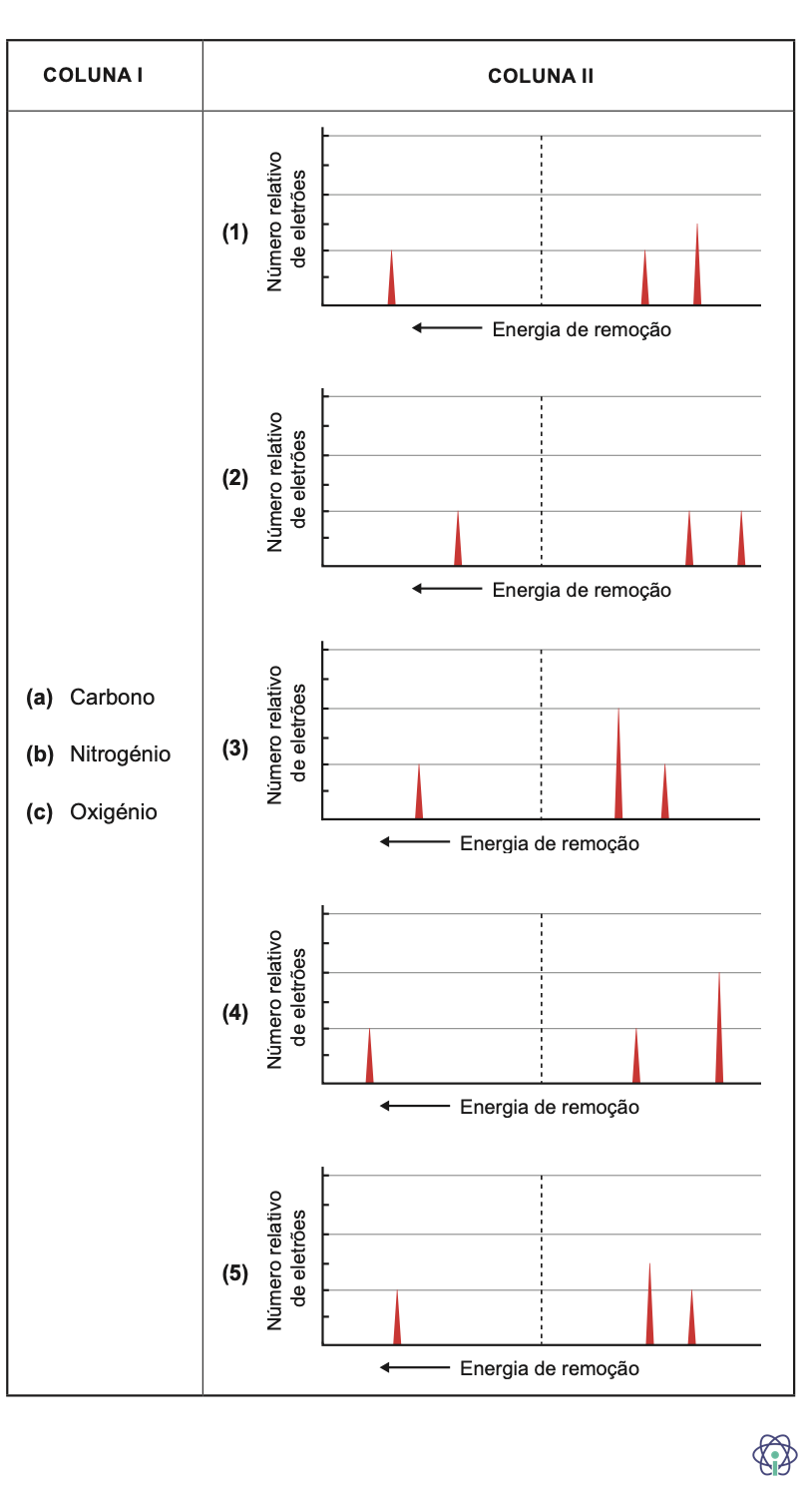
1.4. Associe cada um dos átomos, no estado fundamental, apresentados na Coluna I, ao esboço do espectro fotoeletrónico correspondente, apresentado na Coluna II.
Escreva, na folha de respostas, cada letra da Coluna I seguida do número correspondente da Coluna II.
A cada letra corresponde apenas um número.
⇒ (a) – (2)
⇒ (b) – (1)
⇒ (c) – (4)
🛑 No espetro fotoeletrónico de um elemento são indicadas as respetivas energias de remoção.
🛑 Os eletrões com maior valor de energia de remoção são aqueles que ocupam níveis de menor energia.
🛑 Cada pico corresponde a um valor diferente de energia de remoção, e as correspondentes intensidades do sinal, altura do pico, correspondem ao número relativo de eletrões.
De acordo com as configurações eletrónicas, no estado fundamental, de cada um dos átomos:
- 6C − 1s2 2s2 2p2
- 7N − 1s2 2s2 2p3
- 8O − 1s2 2s2 2p4
verifica-se que todos estes átomos têm três valores de energia de remoção: um com valor muito maior, correspondente aos eletrões do nível 1 (com dois eletrões), e dois outros valores, sendo um destes correspondente aos eletrões do subnível 2s (com dois eletrões) e outro, com menor valor, correspondente aos eletrões do subnível 2p (com dois, três e quatro eletrões, respetivamente).
🛑 Os espetros fotoeletrónicos destes elementos têm, todos, três picos:
- no caso do átomo de carbono, o número relativo de eletrões dos respetivos subníveis é 2 : 2 : 2 , o que corresponde ao esquema (2).
- no caso do átomo de nitrogénio, o número relativo de eletrões dos respetivos subníveis é 2 : 2 : 3 , o que corresponde ao esquema (1).
- no caso do átomo de oxigénio, o número relativo de eletrões dos respetivos subníveis é 2 : 2 : 4 , o que corresponde ao esquema (4).
2. O metano, CH4 (g), tem um potencial de efeito de estufa muito superior ao do dióxido de carbono.
Por esse motivo, em aterros sanitários ou em refinarias de petróleo, é preferível realizar a sua combustão, originando a libertação de dióxido de carbono.
A reação de combustão pode ser traduzida por
CH4 (g) + 2 O2 (g) → CO2 (g) + 2 H2O (g)
2.1. Num recipiente fechado, foram inseridas 2 mol de CH4 e 3 mol de O2 .
Nestas condições, e considerando a reação completa, o reagente limitante é o
(A) CH4, obtendo-se 1 mol de H2O.
(B) CH4, obtendo-se 4 mol de H2O.
(C) O2, obtendo-se 2 mol de H2O.
(D) O2, obtendo-se 3 mol de H2O.
- Opção (D)
🛑 De acordo com a estequiometria da reação, 1 (CH4) : 2 (O2), pode concluir-se que, considerando a reação completa, 2 mol de CH4 reagiriam com 4 mol de O2 .
🛑 Como só foram inseridas 3 mol de O2 , conclui-se que o reagente limitante é o dioxigénio.
🛑 Comparando as frações:
o dioxigénio é o reagente limitante
- O produto obtido numa reação é determinado a partir do reagente limitante.
❇️ De acordo com a estequiometria da reação, 1 (O2) : 1 (H2O), considerando a reação completa, a partir de 3 mol de O2, obter-se-iam 3 mol de H2O.
- Opção (D) ……………. 10 pontos
2.2. A energia libertada na combustão de 40,0 g de CH4 (g) (M = 16,05 g mol-1) permitiu aquecer até 35,0 ºC uma amostra de água inicialmente a 10,0 ºC.
Admita que a combustão foi realizada a pressão constante, com excesso de O2 (g) e com um rendimento de 100% em todos os processos envolvidos.
Considere as energias de ligação médias apresentadas na tabela seguinte.
Determine a massa da amostra de água que foi aquecida.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 A energia libertada ou absorvida, quando ocorre uma reação, resulta de um balanço entre a energia absorvida pelo sistema (positiva) para quebrar as ligações dos reagentes e a energia libertada (negativa) na formação das ligações dos produtos.
- ΔH = [4 x E (C − H) + 2 x ( E (O = O)] − [2 x E (C = O) + 4 x E (O − H)] ⇔ ΔH = [4 x 414 + 2 x 490] − [2 x 799 + 4 x 460] ⇔ ΔH = 2636 – 3438 = – 802 kJ mol-1
🔶 ΔH < 0 ⇒ reação exotérmica
🔶 n = m / M ⇔ n = 40,0 / 16,05 ⇔ n = 2,492 mol
- Sendo a energia libertada na combustão de 1,00 mol de metano 802 kJ , na combustão de 2,492 mol de metano libertam-se 2,492 mol x 802 kJ/mol = 1999 kJ
🛑 Como a energia libertada na combustão do metano permitiu aquecer a amostra de água de 10,0 ºC a 35,0 ºC:
🔶 Q = m x c x ΔT ⇔ 1999 x 103 = m x 4,18 x 103 x (35,0 – 10,0) ⇔ m = 19,1 kg
❇️ A massa da amostra de água aquecida foi 19,1 kg
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a energia que se liberta na combustão de 1 mol de CH4 (802 kJ ) ………. 3 pontos
⇒ Calcula a energia que se liberta na combustão de 40,0 g de CH4 ( 1999 kJ) ………. 3 pontos
⇒ Calcula a massa da amostra de água ( 91,1 kg ) ………. 6 pontos
3. A reação entre o monóxido de carbono, CO, e a água, em fase gasosa, permite obter di-hidrogénio, num equilíbrio traduzido por
CO (g) + H2O (g) ⇋ CO2 (g) + H2 (g) ΔH < 0 e Kc = 1,8 (à temperatura T )
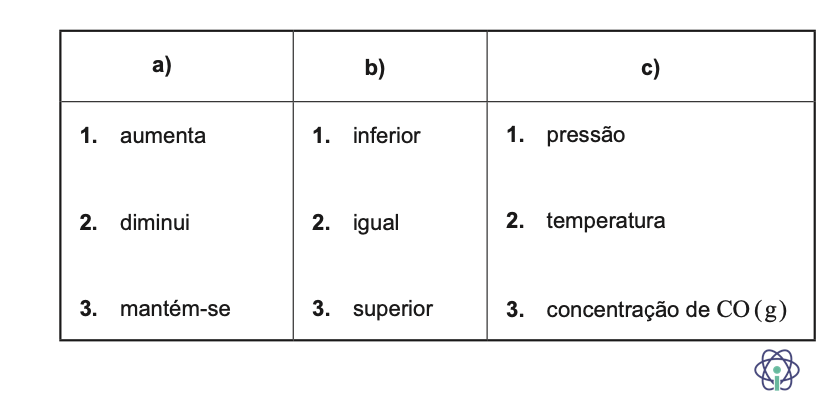
3.1. Complete o texto seguinte, selecionando a opção correta para cada espaço.
Escreva, na folha de respostas, cada uma das letras seguida do número que corresponde à opção selecionada.
Num reator vazio, fechado e indeformável, introduziram-se CO (g) e H2O (g). Até ser atingido o equilíbrio químico, a concentração dos reagentes ____(a)____ , e a velocidade da reação direta é____(b)____ à velocidade da reação inversa. A reação direta é favorecida pela diminuição da ____(c)____ .
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
⇒ (a) – (2)
⇒ (b) – (3)
⇒ (c) – (2)
🛑 Como, num reator vazio, fechado e indeformável, se introduziram inicialmente apenas CO (g) e H2O (g), reagentes da reação, até ser atingido o equilíbrio químico, a concentração dos reagentes diminui, e a velocidade da reação direta é superior à velocidade da reação inversa.
🛑 À medida que o tempo passa, a velocidade da reação no sentido direto vai diminuindo, porque as concentrações dos reagentes também vão diminuindo. A velocidade da reação no sentido inverso vai aumentando, devido ao aumento da concentração dos produtos da reação. Após atingido o estado de equilíbrio, as velocidades das reações direta e inversa são iguais.
🛑 Como ΔH < 0 , a reação é exotérmica no sentido direto. De acordo com o Princípio de Le Châtelier, as reações exotérmicas são favorecidas pela diminuição de temperatura, que faz evoluir a reação no sentido direto, aumentando a constante de equilíbrio.
🛑 Note-se que, como todos os componentes são gasosos e não há variação do número total de moles de partículas na passagem de reagentes a produtos, a diminuição da pressão não altera o estado de equilíbrio. De acordo com o Princípio de Le Châtelier, com a diminuição da concentração de CO (g), seria favorecida a reação inversa.
3.2. Considere que, num reator fechado e indeformável, de volume V, mantido à temperatura T, existem, num determinado instante, 0,2 mol de CO (g), 5,0 mol de H2O (g), 4,0 mol de CO2 (g) e 1,0 mol de H2 (g).
Desde esse instante, e até se atingir o equilíbrio químico, todos os constituintes do sistema reacional alteraram a sua quantidade em 0,15 mol.
Determine a quantidade de CO (g) no reator quando se atinge o equilíbrio. Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 Informações fornecidas:
⇒ Kc = 1,8
🛑 Identificação do sentido em que ocorre a reação até atingir o equilíbrio:
- Como Q > Kc , para se atingir o equilíbrio, a reação evolui no sentido inverso.
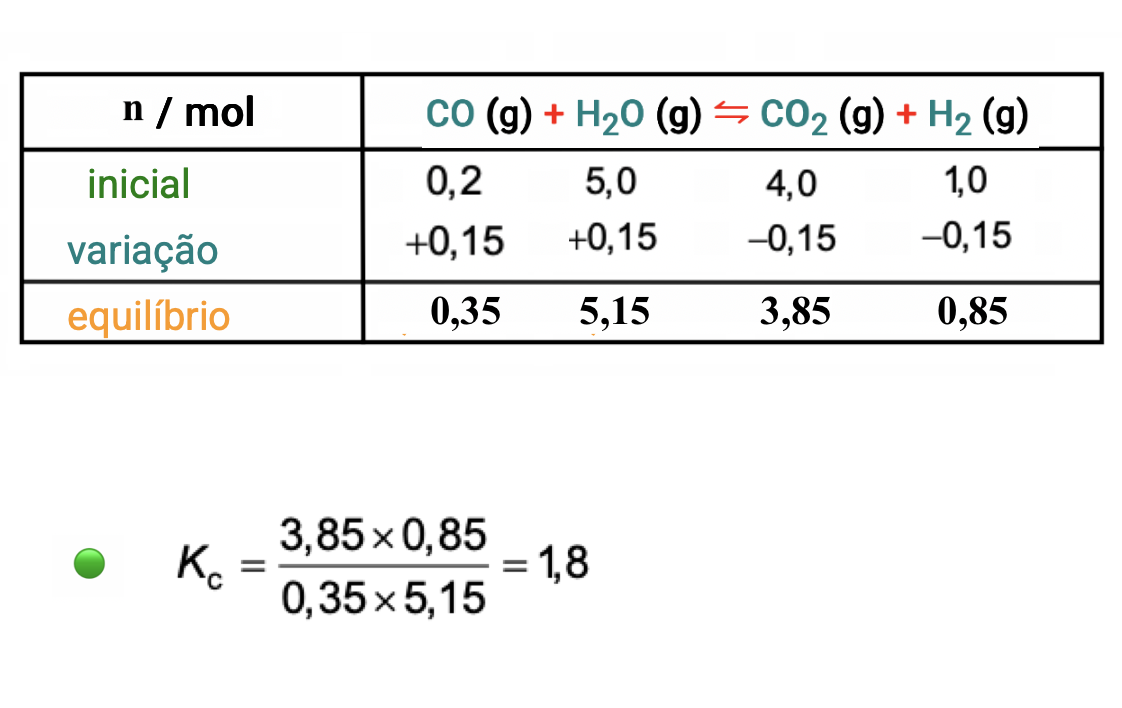
🛑 Quantidades de CO (g) quando se atinge o equilíbrio:
❇️ A quantidade de CO (g) no reator, quando se atinge o equilíbrio, é 0,35 mol.
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula o quociente da reação (4,00 ) ………. 4 pontos
⇒ Reconhece que a reação evolui no sentido inverso ( Q > Kc) ………. 4 pontos
⇒ Calcula a quantidade de CO (g) no equilíbrio ( 0,35 mol ) ………. 4 pontos
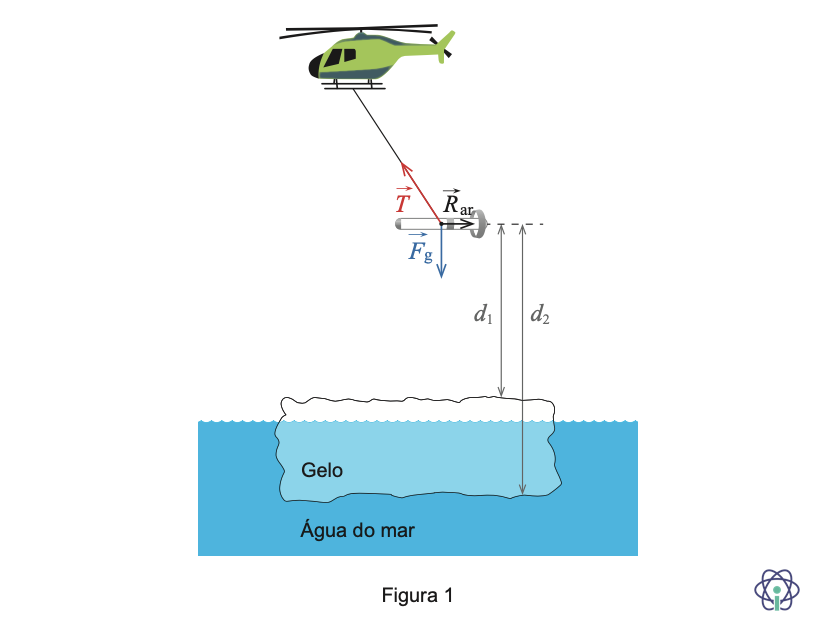
4. O EM-Bird é um dispositivo usado para medir a espessura do gelo marinho, fornecendo dados que possibilitam a monitorização de um dos efeitos do aquecimento global.
Na Figura 1, que não se encontra à escala, estão representados o EM-Bird, suspenso de um helicóptero que voa horizontalmente, a baixa altitude, as forças nele aplicadas e as distâncias do dispositivo à superfície e à base do gelo, d1 e d2 , respetivamente.
4.1. Considere que, no EM-Bird, atuam três forças constantes: a força gravítica, Fg , a tensão exercida pelo cabo, T , e a resistência do ar, Rar.
No deslocamento horizontal do EM-Bird, realiza(m) trabalho nulo a(s) força(s)
(A) Fg e Rar.
(B) Fg.
(C) T.
(D) T e Rar.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (B) ……………. 10 pontos
4.2. Para um determinado local, considere que:
– a distância d1 é obtida a partir da emissão, pelo EM-Bird, de um pulso de luz laser que é refletido na superfície do gelo marinho e recebido, pelo EM-Bird, 6,08 x 10-8 s após a sua emissão.
– a distância d2 , de 11,32 m, é obtida a partir de um sensor eletromagnético.
Qual é a espessura do gelo marinho nesse local?
(A) 2,20 m
(B) 3,46 m
(C) 6,92 m
(D) 9,12 m
- Opção (A)
🛑 O pulso de luz, que permite calcular d1, percorre a distância 2 d1, no intervalo de tempo 6,08 x 10−8 s , com velocidade constante c = 3,00 x 108 m s−1.
🔶 d = c x Δt ⇔ 2 d1 = 3,00 x 108 x 6,08 x 10-8 ⇔ d1 = 9,12 m
❇️ A espessura do gelo marinho será:
🔶 d2 – d1 = 11,32 – 9,12 ⇔ d2 – d1 = 2,20 m
- Opção (A) ……………. 10 pontos
4.3. O processo de medição da distância do EM-Bird à base do gelo marinho baseia-se no facto de a água do mar, no estado líquido, ser boa condutora elétrica, ao contrário do que acontece com o gelo e com o ar.
A água do mar conduz a corrente elétrica, por conter ________ , apresentando uma resistência elétrica ________ .
(A) eletrões livres … elevada
(B) iões em solução … elevada
(C) eletrões livres … baixa
(D) iões em solução … baixa
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (D) ……………. 10 pontos
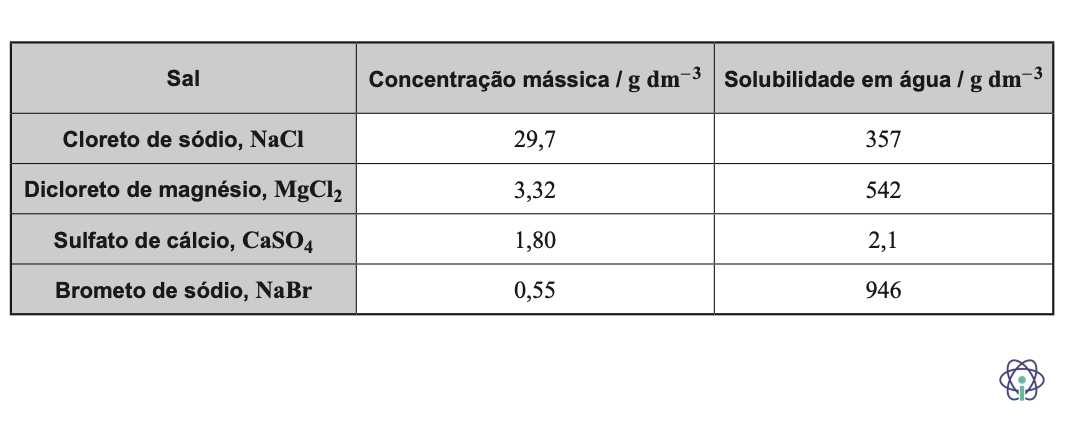
5. A água do mar contém vários sais dissolvidos.
Para simular uma água do mar, preparou-se, em laboratório, uma solução contendo quatro sais.
Na tabela, estão registadas a concentração mássica e a solubilidade em água, a 25 ºC, desses sais.
5.1. Qual é o primeiro sal a precipitar durante a evaporação de uma amostra dessa solução?
(A) NaCl
(B) MgCl2
(C) CaSO4
(D) NaBr
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (C) ……………. 10 pontos
5.2. O ião magnésio pode ser extraído da água do mar mediante a sua precipitação sob a forma de di-hidróxido de magnésio, Mg(OH)2 (s), estabelecendo-se um equilíbrio que pode ser traduzido por
Mg(OH)2 (s) ⇋ Mg2+ (aq ) + 2 OH– (aq )
Preveja, justificando, como varia a solubilidade do Mg(OH)2 (s) com a diminuição do pH, a temperatura constante.
Apresente um texto bem estruturado e utilize linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 De acordo com a definição de pH , pH = – log [H3O+] , a diminuição de pH , a temperatura constante, conduz a um aumento da concentração de H+ (aq) ou H3O+ (aq).
🛑 A temperatura constante, Kw = [H3O+] x [OH–] se mantém, o aumento da concentração de H3O+ provoca uma diminuição da concentração de OH–.
🛑 De acordo com o Princípio de Le Châtelier, a diminuição da concentração de OH− faz evoluir o sistema em equilíbrio, traduzido pela equação em causa, no sentido de se formar mais OH− , ou seja, no sentido direto.
❇️ A diminuição do pH, a temperatura constante, conduz a um aumento da solubilidade do hidróxido de magnésio, Mg(OH)2 .
6. Os raios são descargas elétricas que ocorrem na atmosfera durante as trovoadas.
6.1. Considere que, quando se estabelece uma diferença de potencial de 3,0 x 107 V entre uma nuvem e a superfície da Terra, se forma um raio, de potência 1,0 x 1012 W, constituído por eletrões que se deslocam da nuvem para a Terra e que demoram 0,10 s a atravessar uma dada secção reta da sua superfície.
A carga do eletrão é 1,6 x 10-19 C.
Determine a ordem de grandeza do número de eletrões que atravessam a superfície da Terra nesta descarga elétrica.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 A corrente elétrica, I , estabelecida entre a nuvem e a superfície terrestre, é a quantidade de carga elétrica, Q , que na unidade de tempo atinge a superfície da Terra, e é:
- I = Q / Δt
🛑 A diferença de potencial, U :
- U = E / Q ⇔ E = U Q ⇔ E = U I Δt
🛑 A potência elétrica P = E / Δt ⇔ P = U I , e a potência elétrica do raio formado igual a
- P = U I ⇔ 1,0 x 1012 = 3,0 x 107 x I ⇔ I = 3,33 x 104 A
🛑 A carga elétrica transportada pelo raio é:
- I = Q / Δt ⇔ Q = 3,33 x 104 x 0,10 ⇔ Q = 3,33 x 103 C
🛑 Calculo do N ( número de eletrões que atingem a superfície da Terra):
🔶 Q = N x qe ⇔ 3,33 x 103 = N x 1,6 x 10-19 ⇔ N = 2,1 x 1022 eletrões
❇️ A ordem de grandeza do número de eletrões é 1022
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a corrente elétrica (3,33 x 104 A) ………. 4 pontos
⇒ Calcula a carga transportada pelo raio (3,33 x 10-12 mol) ………. 4 pontos
⇒ Obtém a ordem de grandeza do número de eletrões que atravessam a superfície da Terra ( 1022 ) (ver nota) ………. 4 pontos
Nota: A apresentação do resultado 2,1 x 1022 sem que a ordem de grandeza seja especificada implica uma desvalorização de dois pontos.
6.2. Um raio atinge a superfície da Terra nas proximidades de um armazém.
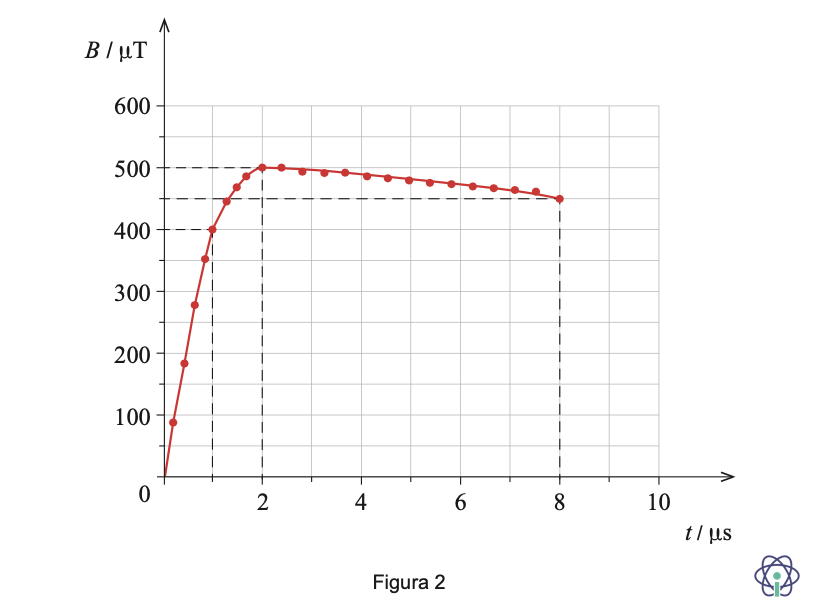
O módulo do campo magnético, B, medido no interior do armazém em função do tempo, t, está representado no gráfico da Figura 2.
Admita que parte da instalação elétrica do armazém pode ser equiparada a uma espira retangularbcom 18 m2 de área e que o campo magnético é perpendicular ao plano dessa espira.
Considere os intervalos de tempo [0; 1] μs, [1; 2] μs e [2; 8] μs.
Determine o módulo da força eletromotriz induzida nessa espira, no intervalo de tempo em que esta é máxima, começando por identificar esse intervalo.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Identifica o intervalo de tempo em que o módulo da força eletromotriz é máximo ([0 ; 1] μs) ………. 4 pontos
⇒ Calcula a variação de fluxo magnético no intervalo de tempo [0 ; 1] μs (7,20 x 10-3 Wb) ………. 4 pontos
⇒ Calcula o módulo da força eletromotriz induzida no intervalo de tempo [0; 1] μs (7,2 x 103 V ) ………. 4 pontos
7. Uma gota de água, com um volume de 4,2 x 10-3 cm3, cai verticalmente de uma nuvem que se encontra a 1700 m do solo, sofrendo a ação do peso e da resistência do ar, acabando por atingir uma velocidade terminal de módulo 7,0 m s-1.
Considere que, nas condições verificadas durante a queda, a massa volúmica da água é 1,0 g cm-3 e que a gota de água pode ser representada pelo seu centro de massa (modelo da partícula material).
7.1. O movimento da gota de água, antes e depois de atingir a velocidade terminal, é, respetivamente,
(A) uniformemente acelerado e uniforme.
(B) acelerado e uniforme.
(C) uniformemente acelerado e retardado.
(D) acelerado e retardado.
- Opção (B)
🛑 Durante a queda vertical, a gota de água está submetida à ação da força gravítica, constante de sentido descendente, e da resistência do ar, ascendente, de módulo variável, pois aumenta com o aumento de velocidade até atingir a intensidade da força gravítica.
🛑 Até atingir a velocidade terminal, o movimento da gota de água é acelerado, pois a resultante das forças tem sentido descendente e é variável (diminui).
❇️ Após atingir a velocidade terminal, a resultante das forças é nula e, consequentemente, a gota adquire movimento uniforme.
- Opção (B) ……………. 10 pontos
7.2. No instante em que a gota de água atinge a velocidade terminal, a resistência do ar tem
(A) sentido de cima para baixo e intensidade 4,1 x 10-5 N.
(B) sentido de cima para baixo e intensidade 4,2 x 10-3 N .
(C) sentido de baixo para cima e intensidade 4,2 x 10-3 N .
(D) sentido de baixo para cima e intensidade 4,1 x 10-5 N.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (D)
🛑 A resistência do ar tem sentido oposto ao do movimento, isto é, o sentido ascendente, de baixo para cima.
🛑 A velocidade terminal é atingida quando a força de resistência do ar tem a mesma intensidade da força gravítica.
🔶 ρ = m / V
🔶 Rar = Fg ⇔ Rar = mg ⇔ Rar = ρ m V ⇔ Rar = ρ m V ⇔ Rar = 1,0 x 103 x 4,2 x 10-9 x 9,8 ⇔ Rar = 4,1 x 10-5 N
- Opção (D) ……………. 10 pontos
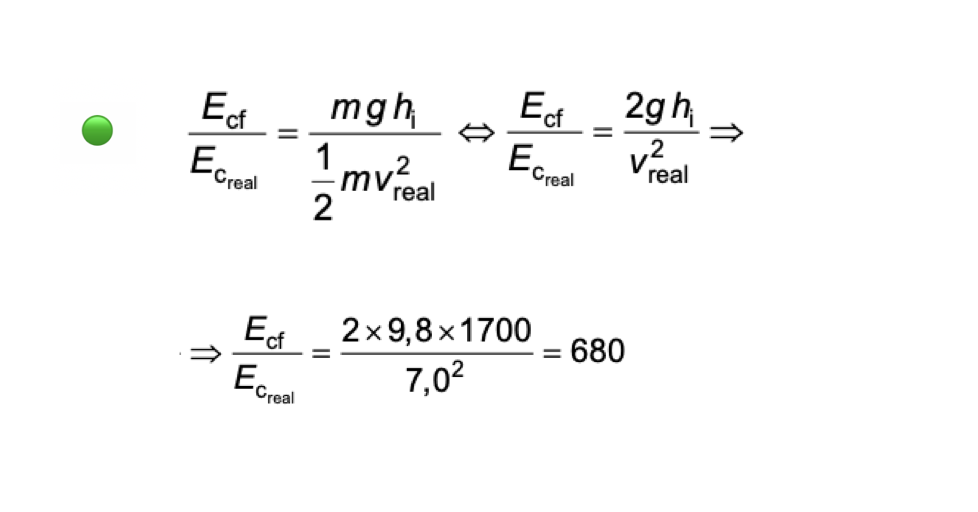
7.3. Se a gota caísse, da mesma altura, sem resistência do ar, comparativamente à situação real, a sua energia cinética no instante imediatamente anterior a atingir o solo seria
(A) 680 vezes superior.
(B) 680 vezes inferior.
(C) 26 vezes superior.
(D) 26 vezes inferior.
- Opção (A)
🛑 Sendo a resistência do ar uma força dissipativa, se a gota caísse, da mesma altura, na ausência desta força, a energia cinética no instante imediatamente anterior a atingir o solo seria superior em relação ao valor atingido na situação real.
- Na situação real, Ec = ½ mv2real
❇️ Considerando a resistência do ar desprezável, há conservação de energia mecânica:
- Opção (A) ……………. 10 pontos
8. Numa aula laboratorial, pretende-se que os alunos efetuem medições de massas e de volumes e, posteriormente, determinem o número de iões hidróxido, OH–, numa gota de água.
8.1. Na Figura 3, apresentam-se os instrumentos usados por um grupo de alunos, dos quais apenas a bureta tem inscrita a indicação do fabricante relativa à sua sensibilidade.
As medidas registadas pelos alunos foram
- m = (5,934 ± 0,005) g
- V = (6,00 ± 0,05) cm3
Que medidas estão corretamente registadas?
(A) Apenas a medida da massa.
(B) Apenas a medida do volume.
(C) Ambas as medidas.
(D) Nenhuma das medidas.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (D)
🛑 Como a balança usada é um aparelho digital (com valores descontínuos num mostrador), a incerteza de uma medida é o menor valor lido nessa balança (salto entre dois valores na escala), o menor valor lido é 1 mg (0,001 g) e não 5 mg .
❇️ A medida correta será (5,934 ± 0,001) g
🛑 Como a bureta usada tem inscrita a indicação do fabricante relativa à sua sensibilidade (tolerância), é esse o valor a considerar. Neste caso, é ± 0,030 mL e não 0,05 mL, pelo que também está incorreto o registo da medida do volume.
❇️ A medida correta será (6,00 ± 0,030) cm3
- Opção (D) ……………. 10 pontos
8.2. Outro grupo de alunos mediu um volume de 5,92 cm3 para 120 gotas de água pura, à temperatura de 25 ºC.
A autoionização da água pode ser traduzida por
2 H2O (l) ⇋ H3O+ (aq ) + OH– (aq )
Determine o número de iões OH– existentes, em média, numa gota de água pura.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 Informações fornecidas:
⇒ Produto iónico da água a 25ºC : Kw = 1,012 x 10-14
⇒ Volume de 120 gotas de água a 25ºC : 5,92 cm3
🛑 De acordo com a estequiometria da reação da autoionização da água : 1 (H3O+) : 1 (OH–)
🔶 Kw = [H3O+] x [OH–] ⇔ Kw = [OH–]2 ⇔ [OH–] = 1,006 x 10-7 mol dm-3
🛑 A quantidade de iões OH– existentes em 5,92 cm3 (120 gotas) de água é:
🔶 c = n / V ⇔ n = 5,92 x 10-3 x 1,006 x 10-7 ⇔ n = 5,956 x 10-10 mol dm-3
🛑 A quantidade de iões OH– existentes numa gota de água é:
🔶 5,956 x 10-10 / 120 = 4,963 x 10-12 mol
❇️ O número de iões OH– existentes, em média, numa gota de água pura:
🔶 N = n x NA ⇔ N = 4,963 x 10-12 x 6,02 x 1023 ⇔ N = 2,99 x 1012 iões OH–
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a concentração do ião OH– (1,006 x 10-7 mol dm-3) ………. 4 pontos
⇒ Calcula a quantidade de iões OH– numa gota de água (4,963 x 10-12 mol)
ou
Calcula a quantidade de iões OH– em 120 gotas de água (5,956 x 10-10 mol) ………. 4 pontos
⇒ Calcula o número de iões OH– numa gota de água (2,99 x 10-12 ) ………. 4 pontos
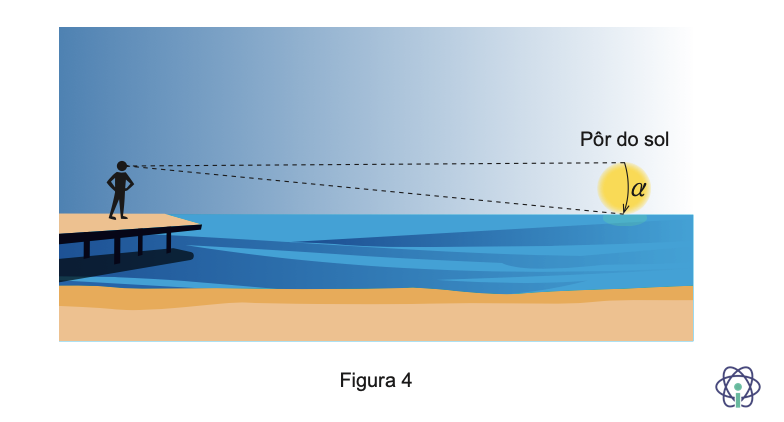
9. Na Figura 4, representa-se uma praia a partir da qual um indivíduo observa o pôr do sol.
9.1. O tamanho aparente do Sol pode ser quantificado por um ângulo representado por a na Figura 4.
Considere que o disco solar tem um tamanho aparente, a, de 9,25 x 10-3 rad e que a Terra efetua uma rotação completa em 24 horas com velocidade angular constante.
Qual das expressões seguintes permite calcular, em segundos, o tempo que, em média, decorre desde que o Sol «toca» o horizonte até «desaparecer» completamente?
- Opção (B) ……………. 10 pontos
9.2. Nas tardes quentes de verão, na praia, o ar tem um movimento ascendente sobre a areia e descendente sobre o mar, verificando-se um movimento de ar superficial do mar para a terra ‒ a brisa marítima.
Compare, justificando, as capacidades térmicas mássicas da areia da praia e da água do mar, tendo em consideração o sentido das correntes de convecção estabelecidas.
Considere que a energia absorvida, por unidade de tempo e por unidade de massa, é igual para a areia e para a água do mar.
Apresente um texto bem estruturado e utilize linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 Dado que a energia absorvida, por unidade de tempo e por unidade de massa, é igual para a areia e para a água do mar, e dado que a temperatura da areia é superior à temperatura da água do mar, então o ar sobre a areia está a uma temperatura superior à temperatura do ar sobre a água do mar, logo a capacidade térmica mássica da areia é inferior à da água do mar (E = m c Δθ ) .
Elementos de resposta:
⇒ o ar sobre a areia da praia tem um movimento ascendente, porque é menos denso, por estar a uma temperatura superior [à temperatura do ar que não contacta com a areia];
⇒ [o ar sobre a areia está a uma temperatura superior] pois contacta com a superfície da areia da praia que está a uma temperatura superior à temperatura da água do mar;
⇒ a areia da praia atinge uma temperatura superior [à temperatura da água do mar, no mesmo intervalo de tempo,] por ter menor capacidade térmica mássica.
9.3. A velocidade de propagação da luz na atmosfera é ligeiramente inferior à velocidade de propagação da luz no vazio.
Por este motivo, quando observamos o pôr do sol, vemos o Sol numa posição diferente daquela em que o veríamos se não existisse atmosfera.
Esta diferença justifica-se pelo fenómeno ótico da
(A) refração da luz.
(B) dispersão da luz.
(C) reflexão da luz.
(D) absorção da luz.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (A)
🛑 A direção de propagação da luz altera-se quando esta atravessa a superfície de separação de dois meios óticos com índices de refração diferentes, resultantes da luz se propagar com diferentes velocidade (var < vvazio).
🛑 Este fenómeno ótico designa-se por refração da luz.
❇️ Ao observarmos o pôr do sol, vemo-lo numa posição diferente daquela em que o veríamos se não existisse atmosfera.
- Opção (A) ……………. 10 pontos
FIM