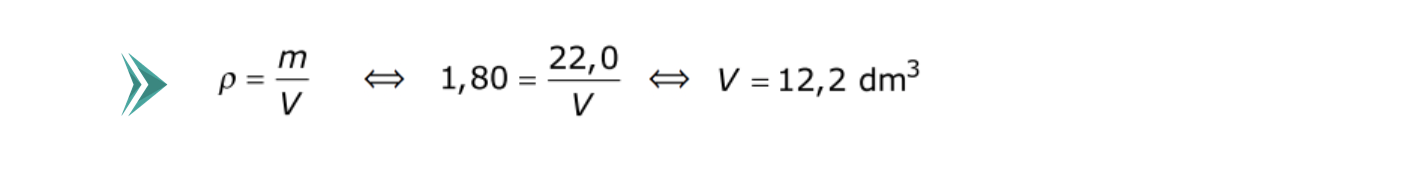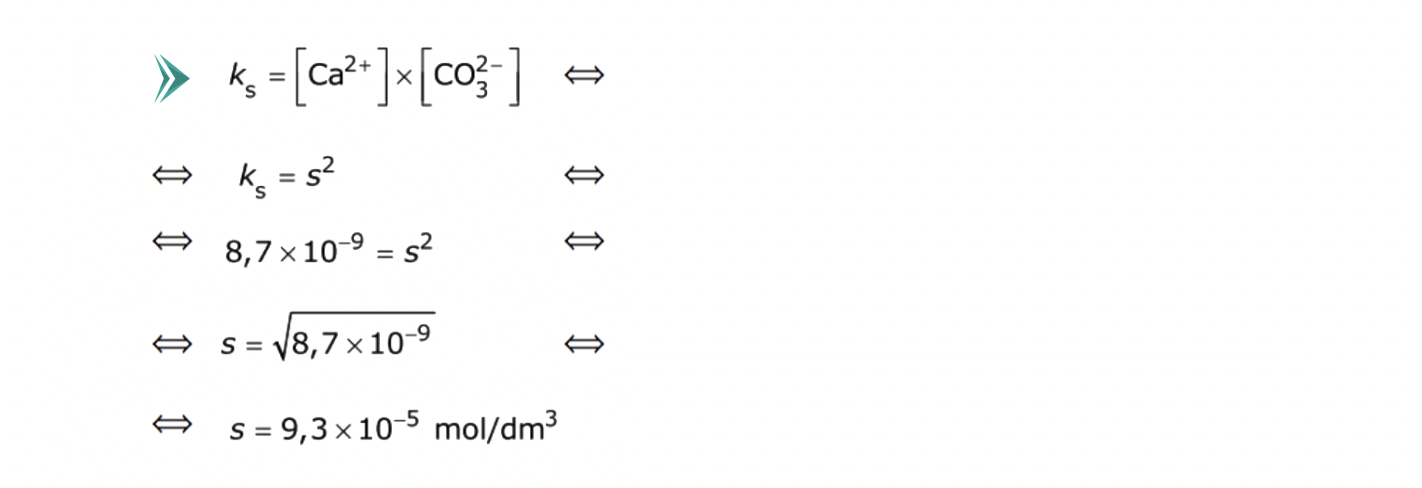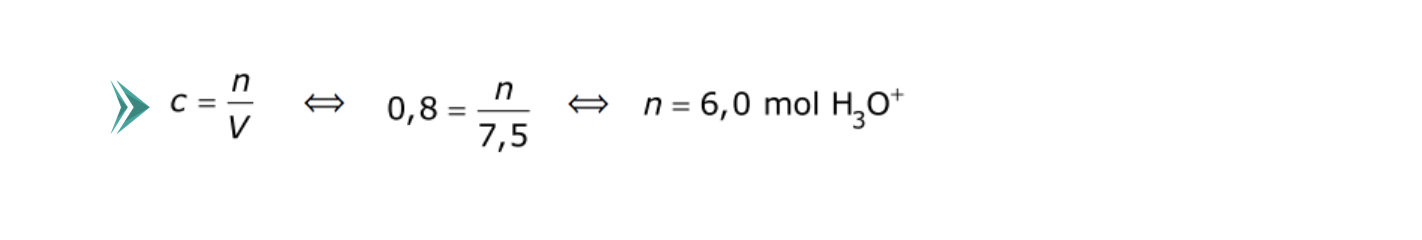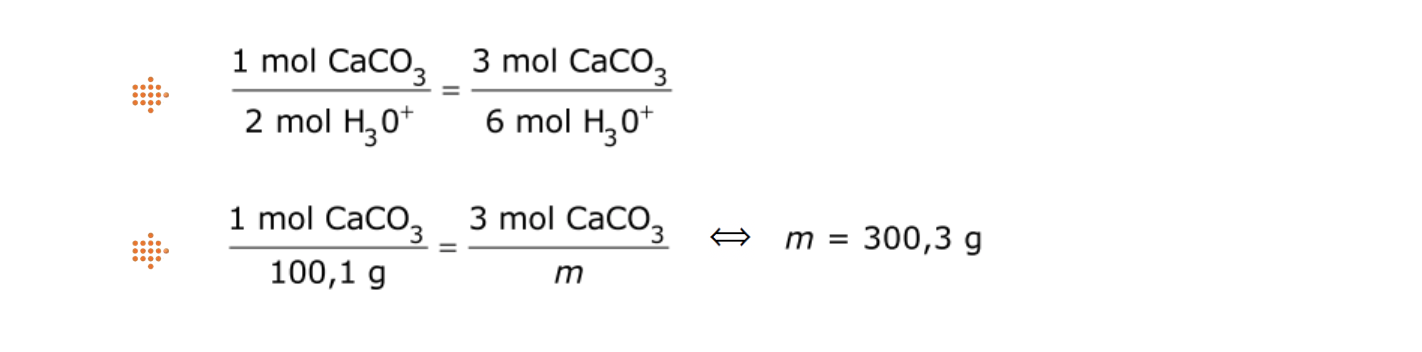2010 – 2ª Fase – Prova Escrita de Física e Química A
Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: 2.ª Fase – 2010
A vida dos organismos marinhos com concha enfrenta uma nova ameaça: o aumento do nível de dióxido de carbono (CO2) atmosférico.
Os oceanos absorvem naturalmente parte do CO2 emitido para a atmosfera, dissolvendo-o nas suas águas.
Uma vez em solução, o CO2 reage, tornando a água do mar, atualmente a um pH de cerca de 8,1, menos alcalina.
Como se continua a emitir enormes quantidades daquele gás, o impacto começa a notar-se – os cientistas mediram já um aumento de acidez de cerca de 30% na água do mar e prevêem um aumento de 100 a 150% até 2100.
O aumento de acidez é acompanhado por uma diminuição da concentração de iões carbonato em solução.
Assim, muitos organismos marinhos, que dependem do carbonato da água do mar para construírem as suas conchas e outras componentes duras, perderão a capacidade de construir ou de manter essas estruturas vitais.
J.S. Holland, «A ameaça ácida», National Geographic Portugal, Novembro 2007 (adaptado)
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1.1. Refira, com base no texto, um fator que ameaça a vida dos organismos marinhos com concha e que é devido ao aumento da concentração de CO2 dissolvido na água do mar.
⇒ Um factor que ameaça a vida dos organismos marinhos é a diminuição da concentração dos iões carbonato, em resultado do aumento da acidez da água do mar.
- Aumento da acidez da água do mar ou diminuição da concentração de iões carbonato em solução. …………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1.2. Selecione a única opção que permite obter uma afirmação correta.
Entendendo por acidez de uma solução a concentração hidrogeniónica ([H3O+]) total existente nessa solução, um aumento de acidez de cerca de 100% na água do mar, em relação ao valor atual, determinará um pH de cerca de…
(A) 4,1
(B) 8,4
(C) 16,2
(D) 7,8
- Opção (D)
⇒ Um aumento de 100% da acidez corresponde a um aumento da concentração de H3O+ para o dobro.
- [H3O+]f = 2 × [H3O+]i
Como:
- [H3O+] = 10–pH ⇒ [H3O+]i = 10–8,1 = 7,94 × 10–9 mol dm-3
- pH = –log [H3O+] ⇒ pH= – log (2 × [H3O+]i) = –log (1,589 × 10–8) = 7,8
⇒ Também se podia escolher correctamente a opção sem fazer cálculos.
⇒ Dois dos valores correspondiam a um aumento de pH, logo a uma diminuição da acidez, o que contradiz a situação, e outro, pH=4, correspondia a uma água do mar muito ácida, o que não faz sentido.
- Opção (D)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.3. Considere que a densidade do CO2 (g), à pressão de 1 atm e à temperatura de 25 ºC, é igual a 1,80 g dm–3.
Calcule o volume ocupado por NA/2 moléculas de CO2 (g) nas condições de pressão e de temperatura referidas, sendo NA a constante de Avogadro.
Apresente todas as etapas de resolução.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Determina o volume molar do CO2 (g), nas condições de pressão e de temperatura referidas (Vm = 24,45 dm3 mol–1).
ou
⇒ Determina a quantidade de CO2 (g) existente em 1 dm3 deste gás, nas condições de pressão e de temperatura referidas (n = 4,090 x 10−2 mol).
⇒ Determina o volume ocupado por NA/2 moléculas de CO2 (g) nas mesmas condições de pressão e de temperatura (V = 12,2 dm3).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
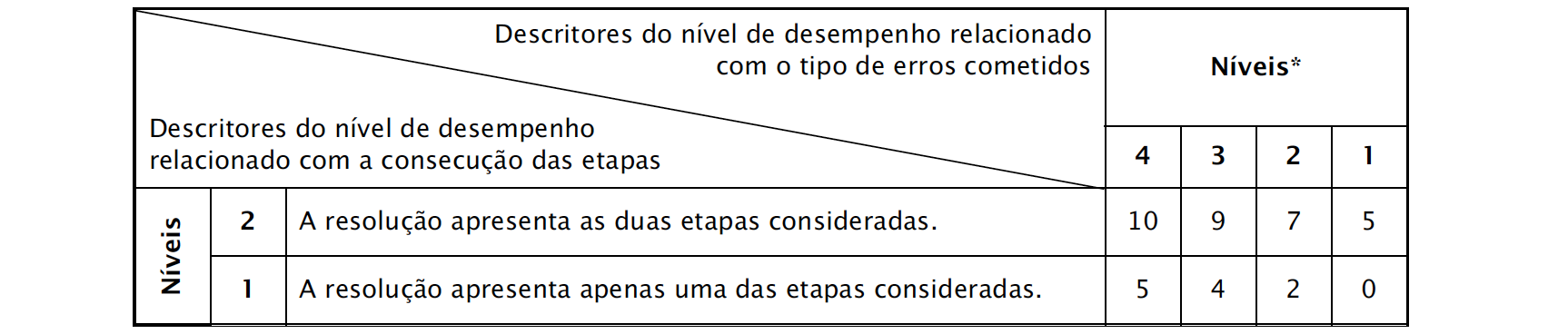
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
1.4. Selecione a única opção que apresenta uma equação química que pode traduzir a reação do dióxido de carbono com a água.
(A) CO2 (g) + 2 H2O (l) ⇋ CO32– (aq) + 2 H3O+ (aq)
(B) CO2 (g) + H2O (l) ⇋ CO32– (aq) + H3O+ (aq)
(C) CO2 (g) + H2O (l) ⇋ HCO3– (aq) + H3O+ (aq)
(D) CO2 (g) + 2 H2O (l) ⇋ HCO3– (aq) + H3O+ (aq)
- Opção (D)
⇒ Apenas na opção D se verifica que o número de átomos de cada elemento nos reagentes é igual ao do número de átomos de cada elemento nos produtos de reacção.
- Opção (D)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
1.5. O carbono, elemento presente nas moléculas de CO2, dá origem a uma grande variedade de compostos orgânicos, nos quais se incluem os hidrocarbonetos saturados, também designados por alcanos.
Selecione a única opção que corresponde à representação correta de uma molécula de propano.
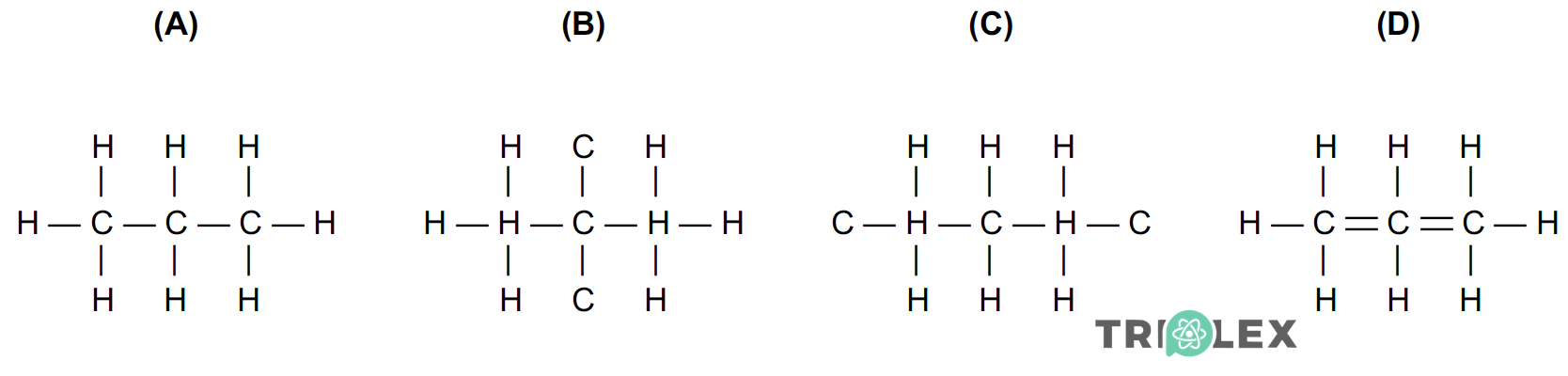
- Opção (A)
⇒ O propano é um composto em que os átomos apenas estabelecem ligações simples.
⇒ O hidrogénio só pode estabelecer uma ligação e o carbono deve ter quatro. Apenas uma opção respeita essa condição.
- Opção (A)…………. 5 pontos
2. As conchas dos organismos marinhos são constituídas, maioritariamente, por carbonato de cálcio, CaCO3.
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
2.1. O carbonato de cálcio resulta de uma reação de precipitação entre os iões cálcio (Ca2+) e os iões carbonato (CO32–) presentes na água.
Entre o precipitado e os iões em solução estabelece-se um equilíbrio que é traduzido por:
CaCO3 (s) ⇋ Ca2+ (aq) + CO32– (aq)
Selecione a única opção que apresenta o valor da solubilidade do carbonato de cálcio em água, à temperatura de 25 ºC, sabendo que a constante de produto de solubilidade deste sal, à mesma temperatura, é 8,7 x 10–9.
(A) 4,4 x 10–9 mol dm–3
(B) 1,7 x 10–8 mol dm–3
(C) 7,6 x 10–17 mol dm–3
(D) 9,3 x 10–5 mol dm–3
- Opção (D)…………. 5 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
2.2. O carbonato de cálcio dissolve-se em meio ácido, devido a uma reacção química que pode ser representada por:
CaCO3 (s) + 2 H3O+ (aq) → Ca2+ (aq) + 3 H2O (l) + CO2 (g)
Considere que se quer fazer reagir um conjunto de conchas marinhas, exclusivamente constituídas por CaCO3 (M = 100,1 g mol–1), com 7,5 dm3 de uma solução aquosa de um ácido forte, cuja concentração hidrogeniónica é 0,80 mol dm–3.
Calcule a massa de conchas que é possível dissolver nas condições referidas.
Apresente todas as etapas de resolução.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Determina a quantidade de H3O+ (aq) existente na solução de ácido forte (n = 6,00 mol).
⇒ Determina a massa de conchas que é possível dissolver (m = 3,0 x 102 g).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
2.3. Escreva a configuração electrónica do átomo de cálcio no estado fundamental.
⇒ 20Ca – 1s2 2s2 2p6 3s2 3p6 4s2
- 1s2 2s2 2p6 3s2 3p6 4s2 …………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
2.4. Justifique a afirmação seguinte, com base nas posições relativas dos elementos cálcio (Ca) e manganês (Mn), na Tabela Periódica.
O raio atómico do cálcio é superior ao raio atómico do manganês.
⇒ O cálcio e o manganésio pertencem ao 4.º período da tabela periódica, mas o cálcio está 2.º grupo e o manganésio no 7.º grupo.
⇒ Ao longo do período a carga nuclear aumenta, pelo que há tendência a haver uma maior força atractiva entre os núcleos e a nuvem electrónica, ocorrendo uma contracção da nuvem electrónica.
⇒ Deste modo, o raio atómico do cálcio deve ser superior ao do manganésio.
- A resposta deve abordar os seguintes tópicos:
⇒ O cálcio precede o manganês no mesmo período da Tabela Periódica.
⇒ Como o raio atómico apresenta tendência para diminuir ao longo de um período, o raio atómico do cálcio é superior ao raio atómico do manganês.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
2.5. Para comparar o poder redutor dos metais manganês (Mn), ferro (Fe), prata (Ag) e chumbo (Pb), adicionou-se um pequeno pedaço de cada um destes metais a várias soluções aquosas, cada uma contendo iões positivos de um desses mesmos metais, em concentrações semelhantes.
A tabela seguinte apresenta os resultados obtidos.
Indique qual dos metais tem menor poder redutor.
- Prata (Ag)
⇒ Se houver reacção entre o metal e o ião presente na solução, o metal reduz o ião.
⇒ Se não houver reacção entre o metal e o ião presente na solução, o metal não se oxida e o ião não se reduz.
⇒ Neste caso o metal tem baixo poder redutor.
- Prata (Ag) …………. 5 pontos
- 10ºano – Física – subdomínio 3
3. A água é a única substância que coexiste na Terra nas três fases (sólida, líquida e gasosa).
3.1. A Figura 1 representa o gráfico teórico que traduz o modo como varia a temperatura, θ, de uma amostra de água, inicialmente em fase sólida, em função da energia fornecida, E, à pressão de 1 atm.

- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.1.1. Indique, justificando com base no gráfico, em que fase (sólida ou líquida) a água apresenta maior capacidade térmica mássica.
⇒ Para a mesma energia fornecida a uma mesma massa, sofre menor elevação de temperatura a que tiver maior capacidade térmica mássica.
⇒ Analisando o gráfico, verifica-se que a amostra na fase sólida, ao absorver energia correspondente a duas divisões faz variar cerca de 30 ºC a temperatura.
⇒ A mesma energia absorvida na fase líquida faz variar a temperatura menos de 20 ºC.
⇒ Então, a capacidade térmica mássica é maior na fase líquida.
- A resposta deve abordar os seguintes tópicos:
⇒ A análise do gráfico apresentado permite concluir que, para se obter uma mesma variação de temperatura, será necessário fornecer mais energia à amostra de água em fase líquida do que amostra de água em fase sólida.
ou
⇒ Nos troços do gráfico correspondentes ao aquecimento da amostra de água, o declive da recta é 1/mc , verificando-se que este declive é menor quando a amostra se encontra em fase líquida.
⇒ Conclui-se, assim, que a água em fase líquida apresenta maior capacidade térmica mássica do que a água em fase sólida.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.1.2. A Figura 2 representa um gráfico que traduz o modo como variou a temperatura de uma amostra de água, inicialmente em fase líquida, em função do tempo de aquecimento, à pressão de 1 atm.

Selecione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correta.
A amostra de água considerada _______ impurezas, uma vez que a ebulição ocorre a uma temperatura, diferente de 100 ºC, que ________ constante ao longo do tempo.
(A) não contém … não se mantém
(B) contém … não se mantém
(C) contém … se mantém
(D) não contém … se mantém
- Opção (B)
⇒ A observação do gráfico permite verificar que a temperatura de ebulição não se mantém constante, o que é uma característica da água com impurezas.
- Opção (B)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
3.2. Identifique a propriedade física considerada quando se afirma que duas amostras de água com a mesma massa, uma na fase sólida e outra na fase líquida, têm volumes diferentes.
⇒ Massa volúmica ou densidade.
- Densidade ou massa volúmica …………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
- 10ºano – Física – A.l. – 3.2 – Capacidade térmica mássica
3.3. A tabela seguinte apresenta os valores da energia que foi necessário fornecer a diversas amostras de água na fase sólida, à temperatura de fusão e a pressão constante, para que elas fundissem completamente.

O gráfico da energia fornecida às amostras de água, em função da massa dessas amostras, permite determinar a energia necessária à fusão de uma unidade de massa de água.
Obtenha o valor dessa energia, expresso em J kg–1, a partir da equação da reta que melhor se ajusta ao conjunto de valores apresentado na tabela.
Utilize a calculadora gráfica.
Apresente o resultado com três algarismos significativos.
⇒ Colocar nas listas da máquina de calcular os valores:
⇒ Utilizar, na parte estatística, a função de regressão linear (obtenção da equação da recta que melhor se ajusta aos pontos).
A equação obtida é :
- y = ax + b
⇒ a = 3,4066 x 105
⇒ b = 3,0497
ou seja:
- E = 3,4066 × 105 m + 3,0497
⇒ A energia por unidade de massa é 3,4066 × 105 JKg.
Como era exigida a apresentação de apenas três algarismos significativos, 3,41 × 105 JKg–1.
- 3,41 x 105 J kg-1 …………. 5 pontos
3.4. As paredes dos igloos, abrigos tradicionalmente usados pelos esquimós, são feitas de blocos de gelo ou de neve compacta.
Se, num igloo, o gelo fosse substituído por betão, a espessura da parede do igloo deveria ser maior, para que, considerando uma mesma diferença de temperatura entre as faces interior e exterior dessa parede, a energia transferida por unidade de tempo fosse a mesma.
Que conclusão se pode retirar da afirmação anterior?
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ A taxa temporal de transferência de energia, Q/Δt, é inversamente proporcional ao comprimento l, mantendo tudo o resto constante.
⇒ Assim, por exemplo, se l duplicar, para que a taxa Q/Δt, se mantenha, conclui-se que o valor de k, a constante de proporcionalidade designada por condutividade térmica, deve ser maior no betão:

- A condutividade térmica do betão é superior à do gelo …………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
3.5. A velocidade de propagação de uma radiação monocromática na água em fase líquida é cerca de 3/4 da velocidade de propagação dessa radiação no vácuo.
Selecione a única opção que apresenta um valor aproximado do índice de refração da água em fase líquida, para aquela radiação.
(A) 0,75
(B) 1,33
(C) 2,25
(D) 1,20
- Opção (B)…………. 5 pontos
4. O amoníaco, NH3 (g), obtém-se industrialmente através do processo de Haber, podendo a reação de síntese ser representada por:
3 H2 (g) + N2 (g) ⇋ 2 NH3 (g) ΔH = – 92,6 kJ mol–1
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
4.1. Preveja, justificando, como varia a concentração de NH3 (g) quando ocorre um aumento da temperatura do sistema inicialmente em equilíbrio.
⇒ Como ΔH < 0, a reacção directa é exotérmica.
⇒ De acordo com o princípio de Le Chatelier, quando se aumenta a temperatura de um sistema em equilíbrio este evolui no sentido de contrariar esse aumento de temperatura, favorecendo a reacção endotérmica.
⇒ Neste caso, a reacção favorecida é a inversa, que é endotérmica.
⇒ Assim, quando a reacção inversa é favorecida, a concentração de NH3 irá diminuir.
- A resposta deve abordar os seguintes tópicos:
⇒ A reação direta é uma reação exotérmica.
⇒ Quando ocorre um aumento da temperatura do sistema inicialmente em equilíbrio, este evolui, de acordo com o Princípio de Le Châtelier, favorecendo a reacção endotérmica.
⇒ Como a reacção endotérmica é, neste caso, a reacção inversa, a concentração de NH3 (g) deverá diminuir.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
4.2. Seleccione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
Se a reacção de síntese do amoníaco ocorrer em sistema isolado, ______ transferência de energia entre o sistema e o exterior, e a energia interna do sistema _______.
(A) não há … mantém-se
(B) não há … diminui
(C) há … diminui
(D) há … mantém-se
- Opção (A)
⇒ Um sistema isolado não permite troca de energia com o exterior.
- Opção (A)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
4.3. A tabela seguinte apresenta dois valores de energia média de ligação.

Seleccione a única opção que apresenta a expressão que permite estimar a energia envolvida na quebra da ligação tripla (EN≡N) na molécula de azoto, expressa em kJ mol−1.
(A) – 3(436,4) – EN≡N + 6(393) = –92,6
(B) +3(436,4) + EN≡N – 6(393) = –92,6
(C) +3(436,4) + EN≡N – 2(393) = –92,6
(D) – 3(436,4) – EN≡N + 2(393) = –92,6
- Opção (B)
⇒ De acordo com a equação de formação do amoníaco, quebram-se três ligações simples no H2 e uma ligação tripla no N2 para se formarem 2 × 3 = 6 ligações simples no NH3.
⇒ Na formação de ligações liberta-se energia e, para as quebrar, é necessário fornecer essa mesma energia.
⇒ De acordo com a convenção, a energia fornecida é positiva e a libertada é negativa.
- Opção (B)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
4.4. Seleccione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
Na molécula de NH3, existem, no total, ______ electrões de valência não ligantes e ______ electrões de valência ligantes.
(A) três … dois
(B) dois … seis
(C) dois … três
(D) três … seis
- Opção (B)
⇒ Cada ligação do N com o H tem 2 electrões ligantes e existe, de valência, um par não ligante no N.
- Opção (B)…………. 5 pontos
5. As auto-estradas dispõem de diversos dispositivos de segurança, como os postos SOS e as escapatórias destinadas à imobilização de veículos com falhas no sistema de travagem.
Considere que, no item 5.1., o automóvel pode ser representado pelo seu centro de massa (modelo da partícula material).
5.1. Considere um automóvel que, devido a uma falha no sistema de travagem, entra numa escapatória com uma velocidade de módulo 25,0 m s–1.
Admita que a massa do conjunto automóvel + ocupantes é 1,20 x 103 kg .
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
5.1.1. A Figura 3 representa o percurso do automóvel na escapatória, imobilizando-se aquele a uma altura de 4,8 m em relação à base da rampa, após ter percorrido 53,1 m.
A figura não está à escala.

Calcule a intensidade da resultante das forças não conservativas que actuam sobre o automóvel, no percurso considerado.
Admita que essas forças se mantêm constantes e que a sua resultante tem sentido contrário ao do movimento.
Apresente todas as etapas de resolução.
⇒ O trabalho das forças não conservativas é igual à variação de energia mecânica.
- Wfnc = ΔEc + ΔEp
- Wfnc = (Ecf – Eci) + (Epf – Epi) = (0 – ½ m vi2) + (m g h – 0) = – 0,5 × 1,2 × 103 × 252 + 1,2 × 103 × 4,8 = –3,17 × 105 J
- Wfnc = Fnc × d × cos 180º = – Fnc × d ⇔ –3,17 × 105 = Fnc × d ⇔ –3,17 × 105 = – Fnc x 53,1 ⇔ Fnc = 6,0 × 103 N
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Determina a variação da energia mecânica do sistema, no percurso considerado (ΔEm = –3,17 x 105 J).
ou
⇒ Determina a intensidade da resultante das forças que actuam sobre o automóvel, no percurso considerado (FR = 7,06 x 103 N).
⇒ Determina a intensidade da resultante das forças não conservativas que actuam sobre o automóvel, no percurso considerado (F = 6,0 x 103 N).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 10ºano – Física – subdomínio 1 (Energia e movimentos)
5.1.2. Considere que o automóvel entra na escapatória, nas mesmas condições.
Selecione a única opção que permite obter uma afirmação correta.
Se a intensidade das forças dissipativas que atuam sobre o automóvel fosse maior, verificar-se-ia que, desde o início da escapatória até ao ponto em que o automóvel se imobiliza, a variação da energia…
(A) potencial gravítica do sistema automóvel-Terra seria maior.
(B) cinética do automóvel seria maior.
(C) potencial gravítica do sistema automóvel-Terra seria menor.
(D) cinética do automóvel seria menor.
- Opção (C)
⇒ Com forças dissipativas maiores, se o automóvel entrasse nas mesmas condições, a variação de energia cinética até parar seria a mesma, mas imobilizava-se a um nível mais baixo.
- Opção (C)…………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
5.1.3. Suponha que a escapatória não tinha o perfil representado na Figura 3 (situação A), mas tinha o perfil representado na Figura 4 (situação B), e que o automóvel se imobilizava à mesma altura (4,8 m).
A figura não está à escala.

Seleccione a única opção que compara correctamente o trabalho realizado pela força gravítica aplicada no automóvel, desde o início da escapatória até ao ponto em que o automóvel se imobiliza, na situação A, WA, e na situação B, WB.
(A) WA = WB
(B) WA > WB
(C) WA < WB
(D) WA ≥ WB
- Opção (A)
⇒ O trabalho realizado pela força gravítica sobre o automóvel apenas depende da diferença de níveis, que neste caso são iguais.
- Opção (A)…………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
5.2. Nas auto-estradas, os telefones dos postos SOS são alimentados com painéis fotovoltaicos.
Considere um painel fotovoltaico, de área 0,50 m2 e de rendimento médio 10%, colocado num local onde a potência média da radiação solar incidente é 600 W m−2.
Selecione a única opção que permite calcular a potência útil desse painel, expressa em W.

- Opção (D)
⇒ Pu = η × P= η × I × A = I × A × η = 600 × 0,50 × 0,10 W
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
5.3. Em situações de emergência, os automobilistas podem usar a buzina para emitir um sinal sonoro que, ao propagar-se no ar, origina uma onda sonora.
Sabendo que uma onda sonora é uma onda mecânica longitudinal, descreva como ocorre a propagação de um sinal sonoro no ar.
⇒ O sinal sonoro origina compressões e rarefacções sucessivas no ar.
⇒ Essas compressões e rarefacções propagam-se na mesma direcção da propagação do sinal sonoro.
- A resposta deve abordar os seguintes tópicos:
⇒ A propagação de um sinal sonoro ocorre por sucessivas compressões rarefações (ou expansões) de ar, em cada ponto da vizinhança do emissor.
ou
- A propagação de um sinal sonoro ocorre por sucessivas variações de pressão de ar, em cada ponto da vizinhança do emissor.
⇒ Aquelas compressões e rarefações ocorrem na mesma direção em que se dá a propagação do sinal sonoro.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

6. Para investigar se o valor da aceleração da gravidade depende da massa dos corpos em queda livre e da altura de queda, um grupo de alunos usou duas células fotoeléctricas, X e Y, ligadas a um cronómetro digital, e diversas esferas de um mesmo material, mas com diâmetros diferentes.
A Figura 5 representa um esquema da montagem utilizada.

Os alunos começaram por medir, com uma craveira, o diâmetro, d, de cada uma das esferas.
Realizaram, seguidamente, diversos ensaios, para determinarem:
– o tempo que cada esfera demora a percorrer a distância entre as células X e Y, Δtqueda ;
– o tempo que cada esfera demora a passar em frente à célula Y, ΔtY.
Os alunos tiveram o cuidado de largar cada esfera sempre da mesma posição inicial, situada imediatamente acima da célula X, de modo a poderem considerar nula a velocidade com que a esfera passava nessa célula (vX = 0).
6.1. Para uma dada esfera, os alunos obtiveram os valores mais prováveis do diâmetro, d, e do tempo de passagem da esfera pela célula Y, ΔtY :
• d = 2,860 cm
• ΔtY = 12,3 x 10–3 s
Os alunos usaram a expressão
(que se refere a um movimento rectilíneo uniforme) para calcular um valor aproximado da velocidade, vY, com que a esfera passa na célula Y.
- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
- 11ºano – Física – A.l. – 1.1 – Queda livre força gravítica
6.1.1. Explique por que é possível utilizar-se aquela expressão no cálculo do valor aproximado da velocidade vY.
⇒ O diâmetro da esfera é pequeno e o intervalo de tempo que a esfera demora a passar pela célula fotoeléctrica é também pequeno, pelo que se pode afirmar que nesse intervalo de tempo a velocidade da esfera é praticamente constante.
- A resposta deve abordar os seguintes tópicos:
⇒ O tempo de passagem da esfera pela célula Y, ΔtY, é muito pequeno.
⇒ A velocidade da esfera mantém-se, assim, praticamente constante nesse intervalo de tempo.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
- 11ºano – Física – A.l. – 1.1 – Queda livre força gravítica
6.1.2. Os alunos obtiveram, em três ensaios consecutivos, os valores de tempo que a esfera demora a percorrer a distância entre as células X e Y, Δtqueda , apresentados na tabela seguinte.

Calcule o valor experimental da aceleração da gravidade obtido pelos alunos a partir das medidas efectuadas.
Apresente todas as etapas de resolução.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Determina o valor mais provável do tempo que a esfera demora a percorrer a distância entre as células X e Y (Δtqueda = 0,2272 s).
⇒ Determina o valor aproximado da velocidade com que a esfera passa na célula Y (vY = 2,325 m s–1 ).
⇒ Determina o valor experimental da aceleração da gravidade (g = 10,2 m s–2 ).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
- 11ºano – Física – A.l. – 1.1 – Queda livre força gravítica
6.2. A tabela seguinte apresenta alguns dos valores experimentais da aceleração da gravidade, expressos em ms–2, obtidos pelos alunos, utilizando esferas de massas diferentes e alturas de queda diferentes.

Selecione a única opção que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correta.
A partir dos resultados experimentais obtidos, podemos concluir que o valor da aceleração da gravidade ______ da massa dos corpos em queda e que ______ da altura de queda.
(A) depende … depende
(B) depende … não depende
(C) não depende … depende
(D) não depende … não depende
- Opção (D)
⇒ Para as diferentes massas e para diferentes alturas de queda, os valores da aceleração na tabela são aproximadamente os mesmos.
- Opção (D)…………. 5 pontos
FIM