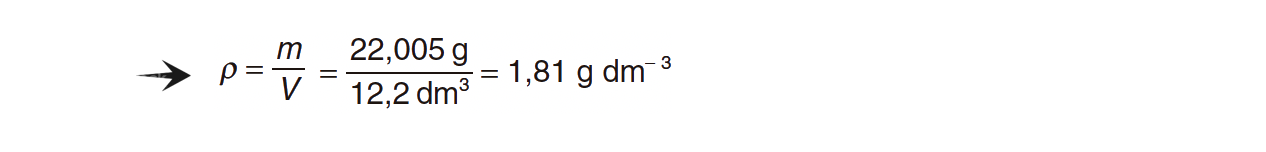2009 – Época Especial – Prova Escrita de Física e Química A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: Época especial – 2009
Grupo I
1. Leia o seguinte texto.Um dia, os homens voltarão à Lua e, provavelmente, construirão aí uma base. Embora na Lua não haja atmosfera apreciável, nem água corrente, nem materiais orgânicos, ela possui, no entanto, alguns recursos que podem ser aproveitados para a sustentação da vida numa base lunar.
Entretanto, será necessário estudar a forma de manter uma base complexa a funcionar num ambiente hostil: a radiação ultravioleta proveniente do Sol incide livremente na superfície lunar, a amplitude térmica é elevadíssima (a temperatura, à superfície, chega a atingir 120 °C, durante o dia, descendo a – 130 °C, à noite) e o campo gravítico lunar é, aproximadamente, um sexto do campo gravítico terrestre (gL = 1/6 gT).
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
1.1. Indique o único facto referido no texto que justifica a elevada amplitude térmica observada na Lua.
⇒ De acordo com o parágrafo 1 do texto, na Lua a atmosfera é praticamente inexistente, o que justifica a elevada amplitude térmica.
- Ausência da atmosfera apreciável …………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.2. Considere um mesmo objecto em queda livre vertical, a partir de posições à mesma altura em relação ao solo, em duas situações distintas: numa situação, próximo da superfície da Lua; e noutra, próximo da superfície da Terra.
Seleccione a única alternativa que relaciona correctamente o tempo de queda desse objecto, próximo da superfície terrestre, tTerra, com o tempo de queda, próximo da superfície da Lua, tLua.

- Opção (C) …………. 5 pontos
1.3. Astronautas de diversas missões Apollo divertiram-se a atirar pequenos objectos, observando a sua trajectória no fraco campo gravítico lunar.
Admita que um desses astronautas lançou, horizontalmente, um pequeno objecto, de uma posição situada a uma altura de 1,40 m em relação ao solo lunar, com uma velocidade inicial de módulo 3,0 m s-1.
Na figura 1, está representada a trajectória desse objecto, assim como um referencial bidimensional, cuja origem se considera situar-se ao nível do solo.
1.3.1. Considere esse referencial e recorra, exclusivamente, às equações que traduzem o movimento, x (t) e y (t).
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
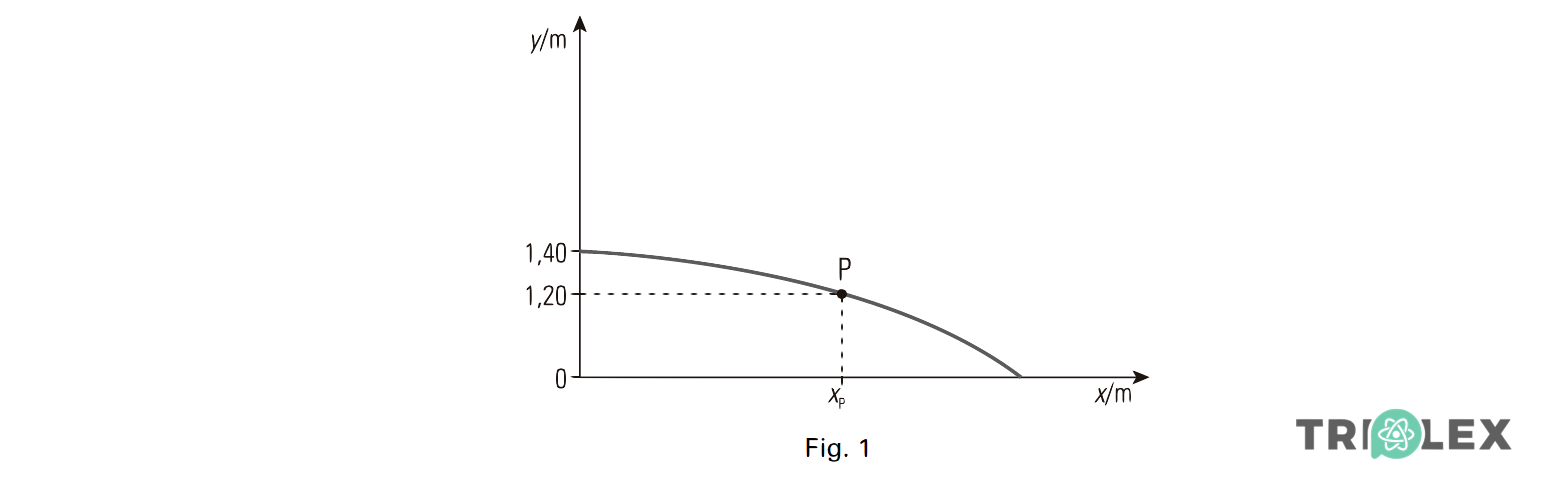
Determine a coordenada xP desse objecto quando este se encontra na posição P, situada a 1,20 m acima do solo.
Apresente todas as etapas de resolução.
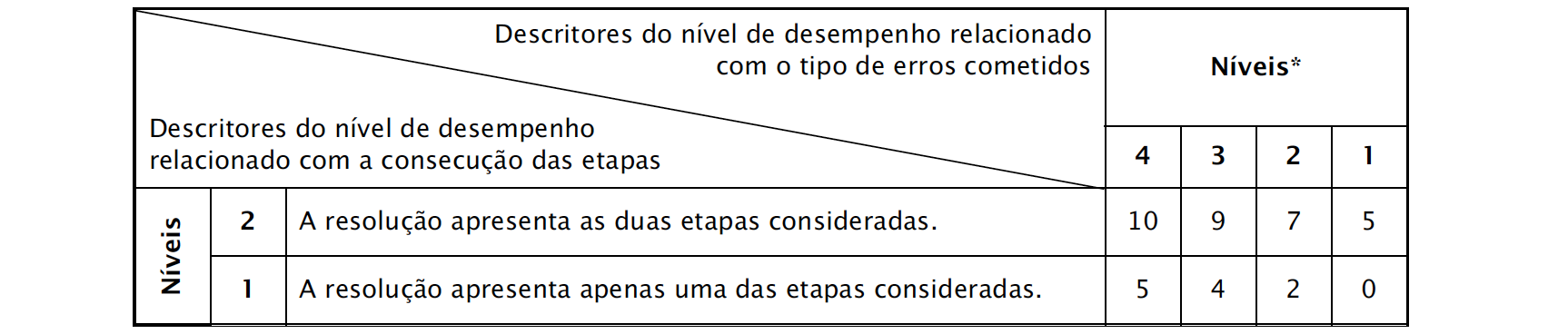
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ De acordo com o referencial apresentado, estabelece as equações x(t) e y(t) (x = 3,0 t e y = 1,40 – 0,83 t 2).
⇒ Utilizando a equação y(t), calcula o tempo que o objecto demora a atingir a posição com coordenada y = 1,20 m (t = 0,491 s).
⇒ Utilizando a equação x(t), calcula a coordenada xP (xP = 1,5 m).
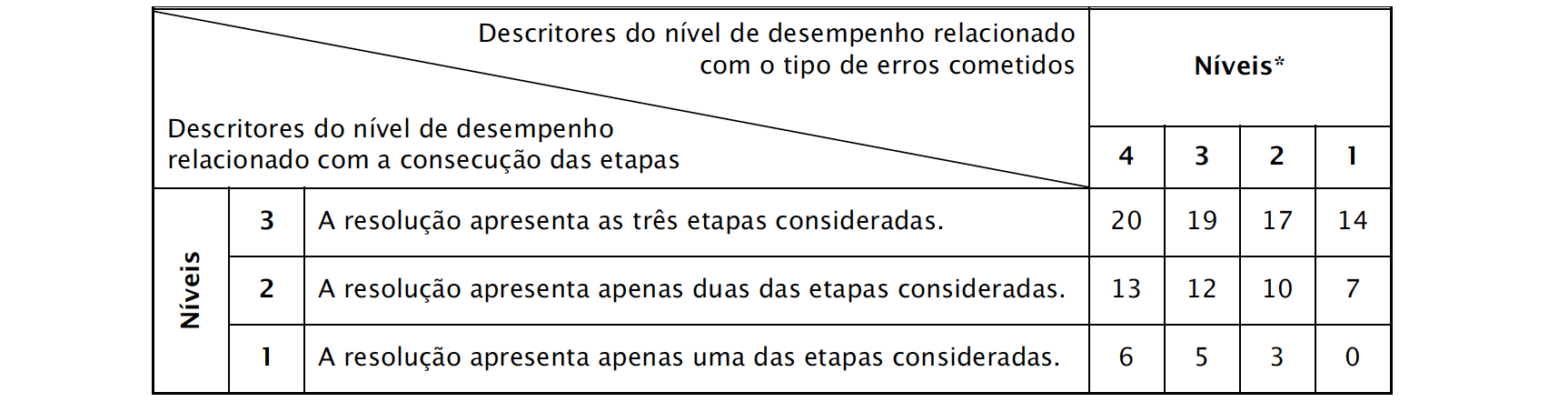
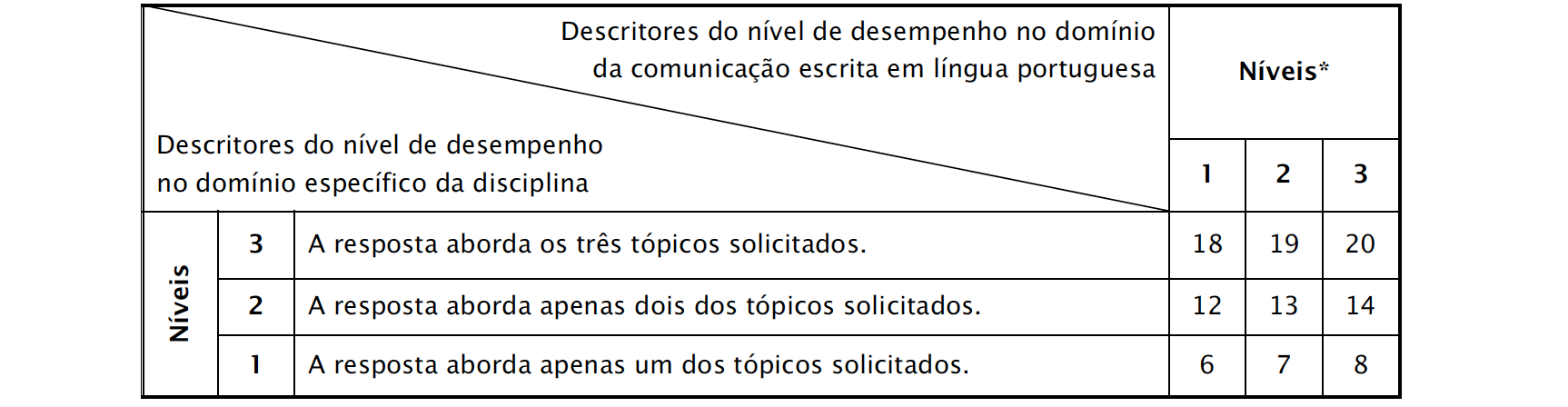
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1.3.2. Seleccione a única alternativa que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
A energia cinética com que o objecto chega ao solo _____ da energia potencial gravítica inicial do sistema objecto + Lua e ______ da energia cinética com que o objecto é lançado.
(A) depende … não depende
(B) depende … depende
(C) não depende … depende
(D) não depende … não depende
- Opção (B)
⇒ Sobre o objeto apenas atua a força gravítica, logo, há conservação da energia mecânica.
Assim:
- Em = Em0 ⇔ Ec + Ep = Ec0 + Ep0
Ao atingir o solo Ep = 0, pois h = 0, então:
- Ec = Ec0 + Ep0
⇒ concluindo-se que a energia cinética com que o objeto atinge o solo depende das energias potencial e cinética iniciais.
- Opção (B)…………. 5 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1.3.3. Em vez de lançar o objecto horizontalmente, o astronauta podia tê-lo lançado verticalmente para cima, a partir da mesma posição inicial.
Justifique a afirmação seguinte.
O trabalho realizado pelo peso do objecto, entre a posição de lançamento e o solo, é o mesmo nas duas situações (lançamento horizontal e lançamento vertical).
⇒ O trabalho realizado pelo peso do objeto apenas depende das posições final e inicial e é simétrico da variação da energia potencial gravítica:
- WP = – ΔEp = – m g (h – ho)
⇒ Quer no lançamento horizontal quer no vertical para cima o objeto é lançado da mesma posição, h0, pelo que em ambas as situações é a mesma. Como a posição final, h, é a mesma, o solo, a energia potencial é nula.
⇒ Pode, pois, concluir-se que em ambas as situações o trabalho realizado pelo peso é o mesmo.
- A resposta deve referir os seguintes elementos:
⇒ O trabalho realizado pelo peso é simétrico da variação da energia potencial gravítica do sistema.
⇒ Como a posição inicial e a final se encontram à mesma altura em relação ao solo, nas duas situações, o sistema sofre a mesma variação de energia potencial, sendo o trabalho realizado pelo peso também igual nas duas situações.
ou
⇒ Como o peso é uma força conservativa, o trabalho por ele realizado só depende da altura das posições inicial e final.
⇒ Como a posição inicial e a final se encontram à mesma altura em relação ao solo, nas duas situações, o trabalho realizado pelo peso é igual, nas duas situações.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
1.4. Seleccione a única alternativa que permite obter uma afirmação correcta.
Um sinal electromagnético enviado da Lua quando esta se encontra a 3,84 x 108 m da Terra atinge o nosso planeta após um intervalo de tempo de…
(A) 0,00 s.
(B) 0,78 s.
(C) 1,28 s.
(D) 2,56 s.
- Opção (C)
⇒ d = 3,84 x 108 m
⇒ c = 3,0 x 108 m s-1
- d = c Δt ⇔ 3,84 x 108 = 3,0 x 108 x Δt ⇔ Δt = 1,28 s
- Opção (C)…………. 5 pontos
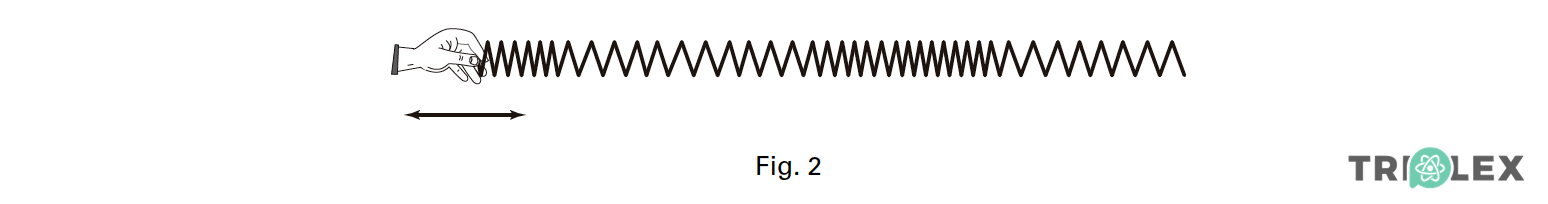
2. A extremidade de uma mola é posta a oscilar horizontalmente, conforme representado na figura 2.
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
- Onda longitudinal
⇒ A onda é longitudinal, pois a propagação da onda dá-se na direção horizontal que coincide com a direção da perturbação.
- A resposta deve referir os seguintes elementos:
⇒ A onda que se propaga na mola é longitudinal.
⇒ As espiras vibram paralelamente à direcção de propagação da onda.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
2.2. Seleccione a única alternativa que permite obter uma afirmação correcta.
Se o movimento da mão for mais rápido, …
(A) o período e a frequência da oscilação aumentam.
(B) o período e a frequência da oscilação diminuem.
(C) o período da oscilação aumenta, mas a frequência diminui.
(D) o período da oscilação diminui, mas a frequência aumenta.
- Opção (D)
⇒ Se o movimento da mão for mais rápido, aumenta a frequência da perturbação.
⇒ Como a frequência da oscilação aumenta, é igual à da perturbação, a fonte, e, dado que o período é inverso da frequência, T = 1/f , então o período diminui.
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
2.3. Considere que o afastamento, y, de uma espira em relação à sua posição de equilíbrio é descrito pela função
y = 0,01 sin (3,3 π t),
na qual as diversas grandezas estão expressas nas respectivas unidades SI.
Seleccione a única alternativa que permite obter uma afirmação correcta.
Numa oscilação completa, a espira percorre uma distância de…
(A) 0,01 m.
(B) 0,02 m.
(C) 0,04 m.
(D) 3,3 m.
- Opção (C)
- y = 0,01 sin (3,3 πt) e y = A sin (ωt)
⇒ Numa oscilação completa t = T e a distância percorrida pela espira (“partícula” em oscilação) é:
- d = 4 A ⇒ d = 4 x 0,01 = 0,04 m
- Opção (C)…………. 5 pontos
3. Para comparar o poder de absorção de energia, sob a forma de radiação, de superfícies diferentes, um grupo de alunos usou uma lâmpada de 100 W e duas latas idênticas, A e B, mas pintadas com tintas diferentes.
Os alunos iluminaram as latas com a lâmpada e registaram a evolução da temperatura do ar contido em cada lata, até a temperatura estabilizar. Com os dados obtidos, construíram o gráfico representado na figura 3.

3.1. Analise a actividade laboratorial realizada pelos alunos, elaborando um texto no qual aborde os seguintes tópicos:
• justificação da utilização, na experiência, de uma lâmpada de potência elevada, em vez de uma lâmpada de baixa potência;
• identificação do material que os alunos tiveram de utilizar para medir os valores necessários à construção do gráfico representado na figura 3;
• discussão da necessidade de as condições iniciais da experiência serem, ou não, semelhantes para as duas latas.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ Quanto mais elevada for a potência elétrica da lâmpada mais elevada é a potência da radiação emitida e consequentemente a potência da radiação incidente nas latas.
⇒ Assim, a diferença de temperatura entre as latas (temperatura ambiente) e a da radiação (Lei de Stefan-Boltzmann) é mais elevada, o que conduzirá a uma variação de temperatura no interior das latas até se atingir o equilíbrio térmico superior à que se verificaria se a potência fosse mais baixa, o que dificultaria a análise de resultados.
⇒ O material utilizado para medir os valores necessários à construção do gráfico representado na figura 3 é: dois termómetros (medir as temperaturas); um cronómetro (medir o tempo).
⇒ As condições iniciais têm de ser as mesmas de modo que a intensidade da radiação incidente sobre cada uma das latas seja igual.
- A resposta deve abordar os seguintes tópicos:
⇒ Na experiência, utilizou-se uma lâmpada de potência elevada, para que o intervalo de tempo que decorre entre o início da experiência e a estabilização da temperatura do ar que se encontra dentro da lata não fosse demasiado longo.
⇒ Para medir os valores necessários à construção do gráfico, os alunos utilizaram um termómetro e um cronómetro ou um sensor de temperatura e um cronómetro ou um sensor de temperatura ligado a um sistema automático de aquisição de dados.
⇒ Para poderem comparar os resultados obtidos com as duas latas, os alunos devem ter partido de condições iniciais semelhantes.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.2. Seleccione a única alternativa que permite obter uma afirmação correcta.
A partir do instante t1 a temperatura do ar no interior da lata A mantém-se constante, porque…
(A) as taxas de absorção e de emissão de energia são nulas.
(B) o módulo da taxa de absorção de energia é superior ao módulo da taxa de emissão.
(C) o módulo da taxa de absorção de energia é inferior ao módulo da taxa de emissão.
(D) os módulos das taxas de absorção e de emissão de energia são iguais.
- Opção (D)
⇒ O equilíbrio térmico é um processo dinâmico, isto é, a temperatura do sistema mantém-se constante quando o módulo da taxa de absorção de radiação é igual à de emissão.
- Opção (D)…………. 5 pontos
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.3. Seleccione a única alternativa que permite obter uma afirmação correcta.
Com base nos resultados experimentais, conclui-se que a superfície da lata A…
(A) absorve melhor a radiação, enquanto a da lata B emite melhor a radiação.
(B) absorve melhor a radiação, enquanto a da lata B reflecte melhor a radiação.
(C) emite melhor a radiação, enquanto a da lata B absorve melhor a radiação.
(D) reflecte melhor a radiação, enquanto a da lata B absorve melhor a radiação.
- Opção (B)
⇒ Da radiação incidente em cada uma das latas uma fração é absorvida e a outra é refletida.
⇒ Da análise do gráfico representado na figura 3 verifica-se que a variação de temperatura no interior da lata A é superior à da lata B, logo, a lata A absorve melhor a radiação incidente, enquanto a B a reflete melhor.
- Opção (B)…………. 5 pontos
4. A cafeína é um composto químico que se encontra, por exemplo, no café, no chocolate e em alguns refrigerantes.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
4.1. Estudos realizados sobre os efeitos da cafeína na saúde dos seres humanos sugerem que, no caso de um adulto saudável, se a dose diária ingerida não ultrapassar 300 mg, o consumo daquele composto não apresenta, em geral, riscos.
Considere o caso de um adulto saudável que beba, diariamente, duas chávenas de café expresso, o que corresponde à ingestão de 60 mg de cafeína, e que consuma, também diariamente, um refrigerante cujo teor em cafeína seja igual a 138,2 mg dm-3.
Calcule o número de latas de 0,33 L desse refrigerante que poderão ser ingeridas por dia, para além dos dois cafés, sem que seja ultrapassado o limite diário acima referido.
Apresente todas as etapas de resolução.
- Opção (D)
⇒ Em duas chávenas de café existem 60 mg de cafeína.
Pode, ainda, ingerir (300 – 60) mg = 240 mg, que correspondem a 1,74 dm3 de refrigerante.
⇒ Como o teor em cafeína é igual a 138,2 mg dm-3, vem:
⇒ contido num pouco mais de cinco latas de 33 mL cada:
⇒ O número de latas de refrigerante que pode ser ingerido é igual a 5.
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Calcula a massa de cafeína contida numa lata de 0,33 L do refrigerante (m = 45,6 mg).
⇒ Calcula o número de latas de 0,33 L do refrigerante que poder o ser ingeridas por dia, para além dos dois cafés (5 latas).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.
4.2. A cafeína é um composto cujas unidades estruturais são constituídas por átomos de carbono, hidrogénio, azoto e oxigénio.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
4.2.1. Seleccione a única alternativa que permite obter uma afirmação correcta.
No estado de energia mínima, os átomos dos elementos carbono, azoto e oxigénio apresentam o mesmo número de…
(A) orbitais s e p totalmente preenchidas.
(B) orbitais p semipreenchidas.
(C) orbitais s totalmente preenchidas.
(D) orbitais p totalmente preenchidas.
- Opção (C)
⇒ Nas configurações eletrónicas:
- 6C – 1s2 2s2 2p2
- 7N – 1s2 2s2 2p3
- 8O – 1s2 2s2 2p4
⇒ só as orbitais s (1s e 2s) estão totalmente preenchidas.
- Opção (C)…………. 5 pontos
4.2.2. Seleccione a única alternativa que refere um conjunto de números quânticos que pode caracterizar um dos electrões mais energéticos do átomo de oxigénio, no estado fundamental.
(A) (2 , 0 , 0 , +½)
(B) (2 , 0 , 1 , -½)
(C) (2 , 1 , -1 , +½)
(D) (2 , -1 , 1 , -½)
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
⇒ Só nesta alternativa se refere um conjunto de números quânticos que caracteriza um eletrão com n = 2 e l = 1 (orbital 2p dos eletrões mais energéticos do oxigénio).
⇒ A alternativa (A) caracteriza um eletrão numa orbital 2s (n = 2 e l = 0) e as alternativas (B) e (D) representam conjuntos impossíveis.
- Opção (C)…………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
4.2.3. Seleccione a única alternativa que contém os termos que preenchem, sequencialmente, os espaços seguintes, de modo a obter uma afirmação correcta.
O carbono e o azoto são elementos que ocupam posições consecutivas no mesmo da Tabela Periódica, sendo de prever que a energia de ionização do carbono seja à energia de ionização do azoto.
(A) período … superior
(B) grupo … superior
(C) grupo … inferior
(D) período … inferior
- Opção (D)
⇒ Os elementos C e N encontram-se no mesmo período da Tabela Periódica.
⇒ Como o carbono antecede o azoto e a energia de ionização apresenta tendência para aumentar ao longo do período, a energia de ionização do carbono é inferior à do azoto.
⇒ As outras alternativas estão incorretas porque:
- (A) a energia de ionização do carbono não é superior à do azoto;
- (B) e (C) o carbono e o azoto não se encontram no mesmo grupo.
- Opção (D)…………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
4.2.4. Indique o valor da energia da radiação emitida na transição electrónica entre os níveis n = 3 e n = 2 do átomo de hidrogénio, com base nos valores de energia desses níveis, respectivamente – 0,24 x 10-18 J e 0,54 x 10-18 J.
⇒ Variação de energia na transição eletrónica do nível n = 3 para n = 2
- ΔE = E2 – E3 = – 0,54 x 10-18 – (– 0,24 x 10-18 ) = – 3,0 x 10-19
⇒ Como a energia é libertada, a sua variação é negativa.
⇒ O valor da energia da radiação emitida é 3,0 x 10-19 J.
- 3,0 x 10-19 J …………. 5 pontos
5. Muitos dos refrigerantes que contêm cafeína são gaseificados por adição de CO2 (g), sob pressão.
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
5.1. Seleccione a única alternativa que permite obter uma afirmação correcta.
Na molécula de CO2, existem…
(A) duas ligações covalentes duplas.
(B) apenas dois pares de electrões não ligantes.
(C) apenas dois pares de electrões ligantes.
(D) duas ligações covalentes simples.
- Opção (A)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
- Geometria linear
⇒ Geometria linear, pois é a que apresenta os dois “pares” eletrónicos em torno do carbono o mais afastados possível e este átomo não contém pares eletrónicos não ligantes.
- Geometria linear …………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
5.3. Sendo NA a Constante de Avogadro, considere que NA/2 moléculas de CO2 (g) (M = 44,01 g mol-1) ocupam um volume igual a 12,2 dm3, à pressão de 1 atm e à temperatura de 25 °C.
Calcule a densidade do CO2 (g), expressa em g dm-3, nessas condições de pressão e de temperatura.
Apresente todas as etapas de resolução.
- A resolução deve apresentar, no m nimo, as seguintes etapas:
⇒ Calcula o volume molar, nas condições de pressão e de temperatura consideradas (Vm = 24,4 dm3).
⇒ Calcula a densidade do CO2 (g), nas mesmas condições de pressão e de temperatura (ρ = 1,80 g dm–3).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
5.4. O dióxido de carbono dissolve-se em água, formando ácido carbónico, H2CO3 (aq) que é um ácido diprótico que, em solução aquosa, se encontra quase totalmente decomposto.
Seleccione a única alternativa que apresenta uma equação química que pode traduzir a reacção global de ionização do ácido carbónico, que existe como tal, em água.
(A) 2 H2CO3 (aq) + H2O (l) ⇋ CO32- (aq) + 2 H3O+ (aq)
(B) H2CO3 (aq) + 2 H2O (l) ⇋ CO32- (aq) + 2 H3O+ (aq)
(C) H2CO3 (aq) + 2 H2O (l) ⇋ HCO3– (aq) + H3O+ (aq)
(D) H2CO3 (aq) + 2 H2O (l) ⇋ 2 HCO3+ (aq) + H3O+ (aq)
- Opção (B)
⇒ Esta alternativa é a única que satisfaz a Lei de Lavoisier e que traduz a reação global de ionização do ácido carbónico.
- Opção (B)…………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
5.5. A dureza total de uma água é um parâmetro normalmente relacionado com as concentrações dos iões cálcio, Ca2+, e dos iões magnésio, Mg2+, nela contidos.
Considere que a dissolução do carbonato de cálcio, CaCO3, por acção de uma água contendo CO2 dissolvido pode ser representada por:
CaCO3 (s) + CO2 (aq) + H2O (l) → Ca2+ (aq) + 2 HCO3– (aq)
Refira, justificando, com base na reacção acima representada, de que modo a presença de uma quantidade apreciável de CO2 dissolvido pode alterar a dureza da mesma água.
⇒ De acordo com o Princípio de Le Chatelier, o aumento de [CO2 (aq)] desloca o equilíbrio no sentido direto, aumentando a [CO2+ ], ou seja, aumentando a dureza da água.
- A resposta deve referir os seguintes elementos:
⇒ Uma quantidade apreciável de CO2 dissolvido implica que o sistema considerado evolua no sentido da reacção directa, o que se traduz num aumento da concentração de Ca2+ (aq).
⇒ O aumento da concentração de Ca2+ (aq) corresponde a um aumento da dureza da água.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

6. O nitrato de amónio, NH4NO3, é um fertilizante azotado, que é usado para obter melhores rendimentos na produção agrícola.
Aquele composto pode ser obtido através de uma reacção química representada por:
NH3 (aq) + HNO3 (aq) → NH4NO3 (aq)
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
6.1. A 20,0 mL de uma solução aquosa de ácido nítrico, HNO3 (aq), de concentração 2,51 x 10-2 mol dm-3, adicionaram-se 20,0 mL de uma solução aquosa de amoníaco, NH3 (aq), contendo 3,00 x 10-4 mol.
Calcule a concentração de nitrato de amónio na solução resultante, admitindo que a reacção acima representada é completa.
Apresente todas as etapas de resolução.
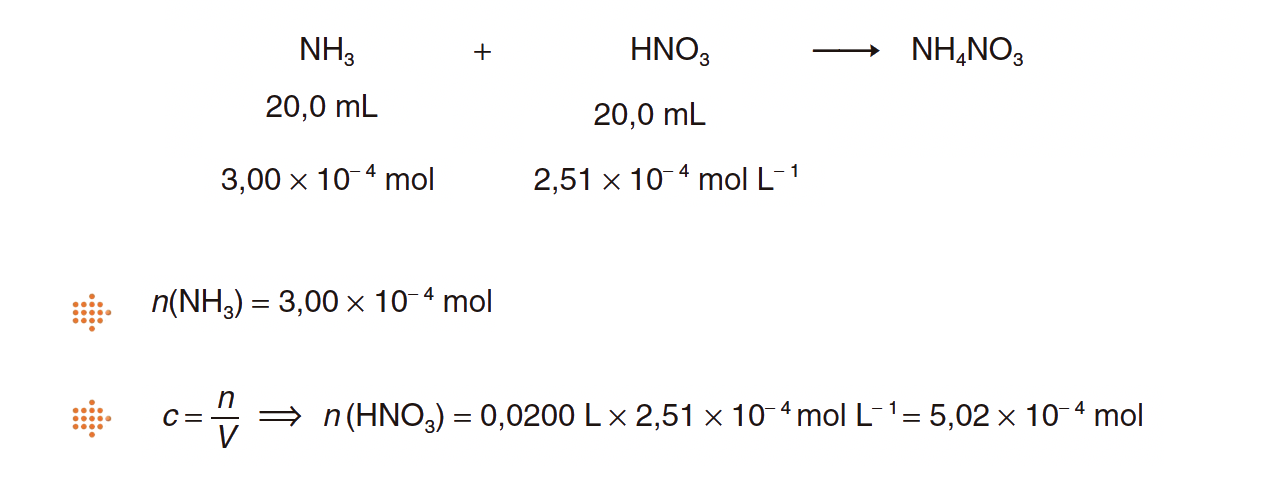
⇒ A equação química mostra que a proporção estequiométrica entre os dois reagentes é de 1:1.
⇒ Como n(NH3) < n(HNO3), o amoníaco está em defeito e, por isso, a quantidade de NH4NO3 formado na reação completa é igual à quantidade de NH3 existente: 3,00 x 10-4 mol.
⇒ A sua concentração é:
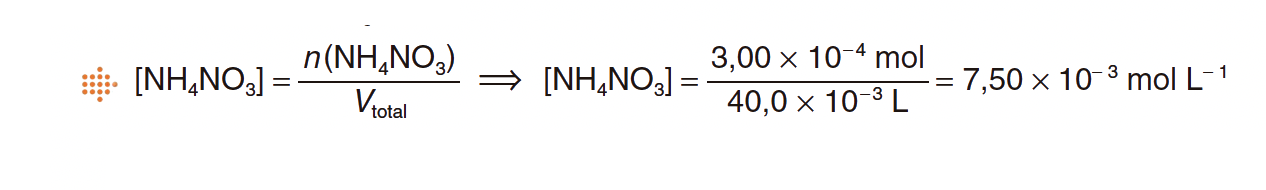
⇒ A concentração de nitrato de amónio na solução resultante é de 7,50 x 10-3 mol L-1
- A resolução deve apresentar, no mínimo, as seguintes etapas:
⇒ Calcula a quantidade de HNO3 (aq) (n = 5,02 x 10–4 mol).
⇒ Calcula a concentração de NH4NO3 (aq) na solução resultante (c = 7,50 x 10–3 mol dm–3), considerando o NH3 (aq) como reagente limitante.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
6.2. O ácido nítrico é um ácido torte, cujo valor de Ka é muito elevado.
Seleccione a única alternativa que refere o valor de pH da solução aquosa de ácido nítrico de concentração 2,51 x 10-2 mol dm-3.
(A) 1,30
(B) 1,60
(C) 5,02
(D) 3,30
- Opção (B)
⇒ Como o ácido nítrico é um ácido forte, em solução aquosa encontra-se quase totalmente ionizado:
HNO3 (aq) + H2O (l) → NO3– (aq) + H3O+ (aq)
⇒ Assim, [H3O+ ] = [HNO3] = 2,51 x 10-2 mol dm-3
⇒ Como pH = – log [H3O+ ], vem pH = – log (2,51 x 10-2) = 1,60.
- Opção (B)…………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
- + 5
⇒ n.o. (N) = + 5 porque (+ 1) + x + 3 (- 2) = 0 conduz a x = + 5 .
⇒ O n.o. do azoto na molécula de HNO3 é igual a + 5.- + 5 …………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
6.4. O amoníaco, NH3, é uma base de Brönsted-Lowry mais forte do que a espécie NO3–.
Seleccione a única alternativa que corresponde a uma afirmação correcta, tendo em conta a informação acima dada.
(A) A espécie NH3 cede iões H+ com mais facilidade do que a espécie NH4+.
(B) A espécie NO3– aceita iões H+ com mais facilidade do que a espécie NH3.
(C) A espécie HNO3 cede iões H+ com mais facilidade do que a espécie NH4+.
(D) A espécie HNO3 aceita iões H+ com mais facilidade do que a espécie NO3–.
- Opção (C)
⇒ porque se NO3¯ é uma base mais fraca que NH3, o ácido HNO3 é mais forte que o ácido NH4+ com mais facilidade que NH4+.
⇒ (A) Falsa
- NH3 em água aceita protões, logo, é um ácido mais fraco que a água; mas o NH4+ em água liberta protões, sendo um ácido mais forte que a água. Assim, o NH3 é um ácido mais fraco que NH4+ e, portanto, não cede protões com mais facilidade.
⇒ (B) Falsa
- Como a espécie NO3– é uma base mais fraca que NH3, tem menos facilidade de aceitar iões H+.
⇒ (D) Falsa
- Embora NO3¯ tenha pouca tendência para aceitar protões, a espécie HNO3, sendo um ácido forte, tem ainda menos tendência e só na presença de ácidos mais fortes aceitaria protões.
- Opção (C)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
6.5. O nitrato de amónio, NH4NO3, é um sal que pode ser utilizado como primeiro socorro no tratamento de determinadas lesões, uma vez que é muito solúvel em água, sendo a sua dissolução um processo endotérmico.
Escreva a equação química que traduz a dissolução do nitrato de amónio em água, considerando que este sal se encontra totalmente dissociado em solução aquosa, e indique como variará a temperatura de uma amostra de água em que ocorra a dissolução desse sal.
- NH4NO3 (s) → NH4+ (aq) + NO3¯ (aq) ΔH> 0
⇒ Se a reação é endotérmica no sentido direto, absorve calor do exterior, baixando a temperatura da água em que se dissolveu.
- A resposta deve referir os seguintes elementos:
NH4NO3 (s) → NH4+ (aq) + NO3– (aq)
⇒ A temperatura de uma amostra de água em que ocorra a dissolução do nitrato de amónio diminuir .
* A omissão da indicação ”H2O” na equação química apresentada não deverá ser penalizada.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte.

FIM