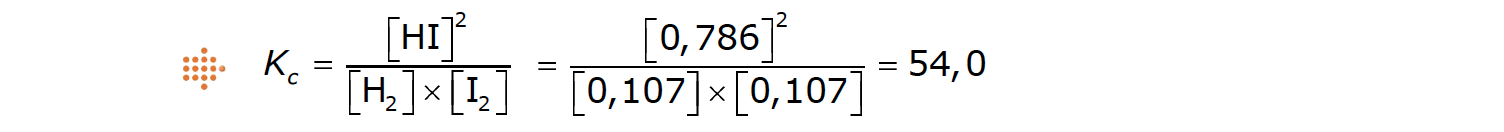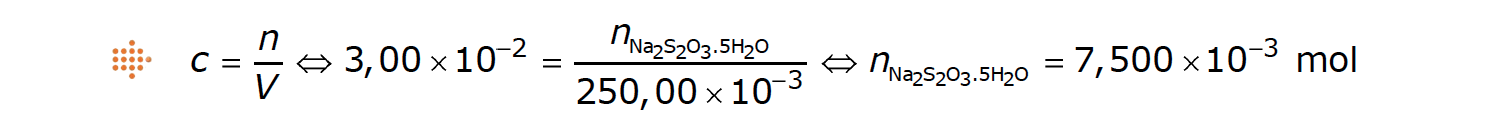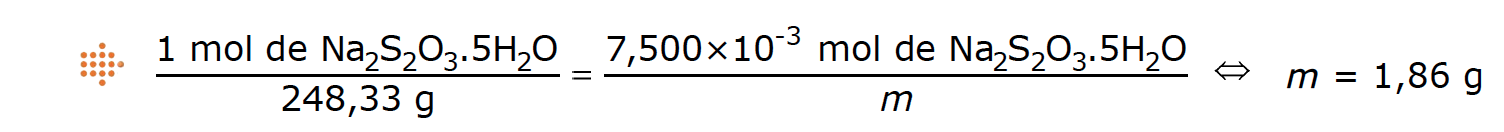2008 – 2ª Fase – Prova Escrita de Física e Química A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: 2.ª Fase – 2008
Quando o astronauta Neil Armstrong pisou pela primeira vez o solo lunar, a 20 de Julho de 1969, entrou num mundo estranho e desolado. Toda a superfície da Lua está coberta por um manto de solo poeirento. Não há céu azul, nuvens, nem fenómenos meteorológicos de espécie alguma, porque ali não existe atmosfera apreciável. O silêncio é total.
Nas análises laboratoriais de rochas e solo trazidos da Lua não foram encontrados água, fósseis nem organismos de qualquer espécie.
A maior parte da luz do Sol que incide na superfície lunar é absorvida, sendo o albedo médio da Lua de apenas 11%. A aceleração da gravidade à superfície da Lua é cerca de 1/6 da que se verifica à superfície da Terra.
Depois da Lua, Vénus é o astro mais brilhante no céu nocturno, uma vez que a espessa camada de nuvens que o envolve reflecte grande quantidade da luz proveniente do Sol. A atmosfera de Vénus é constituída por cerca de 97% de dióxido de carbono e por uma pequena percentagem de azoto, com vestígios de vapor de água, hélio e outros gases. A temperatura à superfície chega a atingir 482 ºC, porque o dióxido de carbono e o vapor de água atmosféricos se deixam atravessar pela luz visível do Sol, mas não deixam escapar a radiação infravermelha emitida pelas rochas da sua superfície.
Dinah Moché, Astronomia, Gradiva, 2002 (adaptado)
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
1.1. Tendo em conta a informação dada no texto, explique por que motivo, na Lua, «o silêncio é total».
⇒ Na Lua o «silêncio é total», porque para haver som é necessário um meio físico para as ondas sonoras (mecânicas) existirem.
- Na Lua não existe atmosfera e, portanto, não existem ondas sonoras.
A resposta deve contemplar os seguintes elementos:
⇒ A Lua não possui atmosfera apreciável.
⇒ Não ocorre propagação do som, uma vez que o som necessita de um meio material para se propagar.
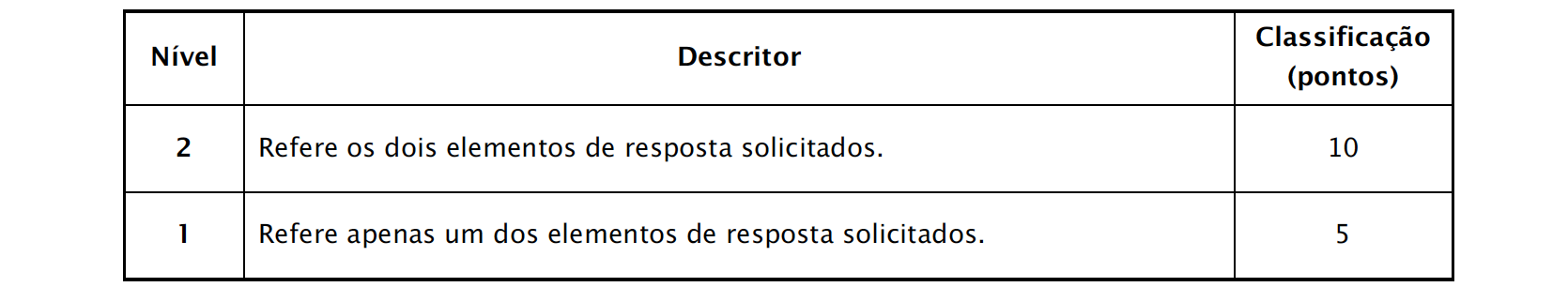
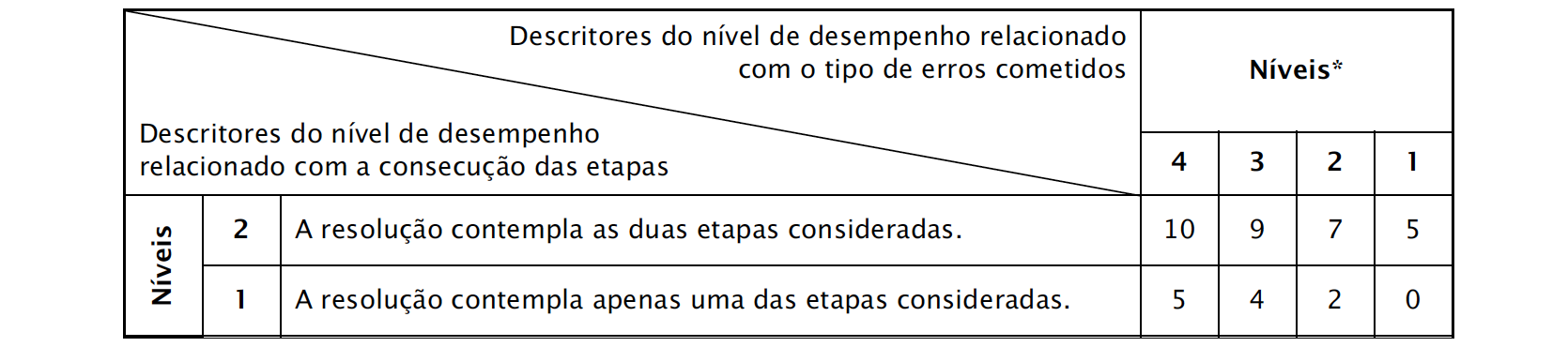
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.2. Identifique o efeito descrito no último período do texto, que também ocorre na atmosfera da Terra, embora em menor extensão.
⇒ O efeito descrito no último parágrafo do texto, responsável pela temperatura à superfície de Vénus e responsável também pela temperatura à superfície da Terra, é o efeito de estufa.
- Efeito de estufa …………. 5 pontos
1.3. Com base na informação apresentada no texto, seleccione a alternativa que contém os termos que devem substituir as letras (a), (b) e (c), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
O albedo da Lua é __ (a) __ ao de Vénus, uma vez que a superfície da Lua ___ (b) __ grande parte da radiação solar incidente e a atmosfera de Vénus __ (c) __ a maior parte dessa radiação.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
(A) … superior … absorve … absorve …
(B) … inferior … absorve … reflecte …
(C) … superior … absorve … reflecte …
(D) … inferior … reflecte … absorve …
- Opção (B)
⇒ No texto pode ler-se «A maior parte da luz do Sol que incide na superfície lunar é absorvida, sendo o albedo médio da Lua de apenas 11%». Por outro lado também se refere para Vénus que «a espessa camada de nuvens que o envolve reflecte grande quantidade da luz proveniente do Sol». Conclui-se que a Lua tem um albedo inferior ao de Vénus, absorve grande parte da radiação solar incidente e que Vénus reflecte muita radiação.
ou
⇒ “O albedo da Lua é inferior ao de Vénus, uma vez que a superfície da Lua absorve grande parte da radiação solar incidente e a atmosfera de Vénus reflecte a maior parte dessa radiação”.
ou
⇒ De acordo com o terceiro parágrafo do texto, “A maior parte da luz que incide na superfície lunar é absorvida, sendo o albedo de apenas 11%” e de acordo com o último parágrafo “… Vénus é o astro mais brilhante no céu noturno, uma vez que a espessa camada de nuvens que o envolve reflete grande quantidade da luz proveniente do Sol”.
- Opção (B)…………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
1.4. Com base na informação apresentada no texto, seleccione a alternativa que compara correctamente a intensidade da força gravítica que actua sobre um mesmo corpo, quando colocado à superfície da Terra, FgTerra, e à superfície da Lua, FgLua.

- Opção (D)
⇒ Se a aceleração da gravidade à superfície da Lua é cerca de 1/6 da que se verifica à superfície da Terra, a força gravítica na Terra, para um mesmo corpo, é seis vezes maior do que na Lua.
ou
⇒ A intensidade da força gravítica que actua num corpo num determinado local é directamente proporcional à intensidade da aceleração da gravidade nesse local. É referido no texto que “a aceleração da gravidade à superfície da Lua é cerca de 1/6 da que se verifica à superfície da Terra”. Sendo assim, também a força gravítica que actua num corpo na superfície da Lua é 1/6 da força gravítica que actua num corpo na superfície da Terra.
ou
⇒ gLua = 1/6 gTerra ⇒ m = massa do corpo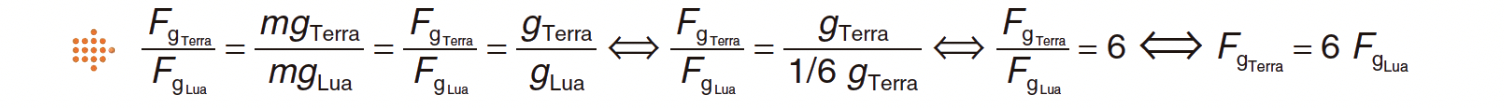
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
1.5. Com base na informação apresentada no texto, seleccione o gráfico que traduz o modo como variam os módulos da velocidade de um corpo em movimento de queda livre vertical, próximo da superfície da Lua, vLua, e próximo da superfície da Terra, vTerra, em função do tempo de queda.

- Opção (B)
⇒ No gráfico v(t) o declive é igual à aceleração. Na Terra a aceleração é maior do que na Lua, logo o declive da recta é maior.
ou
⇒ Sendo a aceleração da gravidade na Terra superior à aceleração da gravidade na Lua, num movimento de queda livre vertical o módulo da velocidade de um corpo aumenta mais rapidamente na Terra do que na Lua.
ou
- VLua = gLuat e VTerra = gTerrat ⇔ VTerra = 6 gLuat
⇒ Para o mesmo tempo de queda, VTerra = 6 VLua, logo o gráfico que melhor traduz como variam os módulos da velocidade de um corpo em movimento de queda livre vertical, próximo da superfície da Lua e próximo da superfície da Terra, em função do tempo de queda é o representado em (B).
- Opção (B)…………. 5 pontos
2. Enquanto os astronautas N. Armstrong e E. Aldrin, da missão Apollo 11, recolhiam amostras na superfície lunar, o seu colega M. Collins permanecia no Módulo de Comando (MC), em órbita à volta da Lua (L), como representado na figura 1 (a figura não está representada à escala).

- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.1. Tendo em conta a situação descrita, seleccione o diagrama que representa correctamente as forças de interacção entre o Módulo de Comando e a Lua.

- Opção (D)
⇒ As forças constituem um par acção-reacção, sendo simétricas.
ou
⇒ As forças constituem um par acção-reacção: têm, por isso, a mesma intensidade e apontam para lados opostos.
ou
⇒ As forças de interação entre o Módulo de Comando e a Lua são um par ação-reação, pelo que têm a mesma direção, a mesma intensidade, sentidos opostos e pontos de aplicação no centro de massa de cada um dos corpos. Estas forças são atrativas.
⇒ O diagrama que representa corretamente as forças de interação entre o Módulo de Comando e a Lua é o (D).
- Opção (D)…………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.2. Considere que o Módulo de Comando (MC) descreveu, com um período de 2,0 h, diversas órbitas circulares, de raio 1,9 × 106 m, sujeito apenas à força gravítica exercida pela Lua.
Relativamente à situação descrita, classifique como verdadeira (V) ou falsa (F) cada uma das afirmações seguintes.
(A) O MC descreveu cada volta completa em 7,2 × 103 s.
(B) A velocidade linear do MC manteve-se constante.
(C) Em 2,0 h o MC percorreu uma distância de 1,9 × 106 m.
(D) O trabalho realizado pela resultante das forças aplicadas no MC foi nulo.
(E) O produto do módulo da velocidade angular do MC pelo período do seu movimento é independente do raio da órbita.
(F) O módulo da velocidade linear do MC depende da sua massa.
(G) O módulo da velocidade angular do MC foi 8,7 × 10–4 rad s–1.
(H) O valor da energia cinética do MC variou ao longo da órbita.
- Verdadeiras : (A), (D), (E), (G)…………. 10 pontos
- Falsas : (B), (C), (F), (H)
⇒ (A) Verdadeira
- 2,0 × 3600 s = 7200 s = 7,2 × 103 s
⇒ (B) Falsa
- A velocidade é tangente à trajectória e como a trajectória é circular está permanentemente a variar. O módulo da velocidade linear é que se mantém constante.
⇒ (C) Falsa
- Distância percorrida numa volta completa = 2 πr = 2 × 3,14 × 1,9 × 106 m = 1,19 × 107 m
⇒ (D) Verdadeira
- O trabalho realizado pela resultante das forças depende do deslocamento do corpo. Num período, o objecto descreve uma orbita completa sendo o seu deslocamento nulo, logo o trabalho da resultante é nulo. O Módulo descreveu as órbitas sujeito apenas à força gravítica. Como esta aponta sempre para o centro da trajectória nunca tem componente na direcção do deslocamento, pelo que não realiza trabalho.
⇒ (E) Verdadeira
- ω = v/r ; T = 2πr/v , logo o ω x T = 2π , sendo por isso independente do raio da órbita
⇒ (F) Falsa
- A velocidade linear do Módulo depende do raio da órbita e da massa da Lua sendo independente da massa do Módulo.
⇒ (G) Verdadeira
ω = 2π/T = 8,7 x 10-4 rad s-1
⇒ (H) Falsa
- O Módulo move-se com movimento circular uniforme, logo o módulo da velocidade é constante. A energia cinética depende da massa do Módulo e do módulo da velocidade que são constantes, por isso a energia cinética é também constante.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2.3. Para recolher amostras na superfície lunar, os astronautas usaram um utensílio de cabo extensível, tal como representado na figura 2.
Imagine que, quando um dos astronautas tentou recolher uma amostra, de massa 200 g, esta deslizou, inadvertidamente, numa zona onde o solo era inclinado, passando na posição A com uma velocidade de módulo igual a 0,50 m s–1 e parando na posição B, tendo percorrido 51 cm entre estas posições.

Nesse percurso, a energia potencial gravítica do sistema amostra + Lua diminuiu 8,16 × 10–2 J.
Calcule a intensidade da força de atrito que actuou sobre a amostra no percurso considerado, admitindo que aquela se manteve constante.
Apresente todas as etapas de resolução.
⇒ A energia potencial gravítica entre A e B diminui 8,16 x 10-2 J, logo a variação de energia potencial gravítica é:
- ΔEpg = – 8,16 x 10-2 J
⇒ No ponto B a velocidade da amostra é nula. A energia cinética em B é, pois, também nula.
⇒ O módulo da velocidade da amostra em A é 0,50 ms-1, a que corresponde a energia cinética de:
- Ec = ½ x m x v2 = 0,5 x 200 x 10-3 x 0,52 = 2,5 x 10-2 J
⇒ A variação de energia cinética entre A e B é:
- ΔEc = EcB – ΔEcA = 0 – 2,5 x 10-2 = -2,5 x 10-2 J
⇒ A variação de energia mecânica depende da variação de energia potencial gravítica e da variação de energia cinética, logo:
- ΔEm = ΔEpg + ΔEc = – 8,16 x 10-2 + (-2,5 x 10-2) = – 1,07 x 10-1 J
⇒ A variação de energia mecânica é igual ao trabalho realizado pelas forças dissipativas:
- WFa = ΔEm = – 1,07 x 10-1 J
- WFa = d x Fa x cos α ⇔ – 1,07 x 10-1 J = 51 x 10-2 x Fa x cos 180º ⇔ Fa = 0,21 N
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula a variação de energia cinética da amostra entre as posições A e B (ΔEc = –2,50 × 10–2 J).
⇒ Calcula a variação da energia mecânica do sistema entre as posições A e B (ΔEm = –1,07 × 10–1 J).
⇒ Identifica a variação da energia mecânica do sistema com o trabalho realizado pela força de atrito e calcula a intensidade da força de atrito (Fa = 0,21 N).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

* Descritores apresentados no segundo quadro da página C/3 dos critérios gerais de classificação.
2.4. Uma vez que na Lua «o silêncio é total», os astronautas comunicavam entre si, mesmo a pequena distância, por meio de ondas electromagnéticas.
Qualquer sinal sonoro, antes de poder ser enviado sob a forma de uma onda electromagnética, deve ser transformado num sinal eléctrico, recorrendo, por exemplo, a um microfone de indução.
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
2.4.1. O funcionamento do microfone de indução baseia-se no fenómeno da indução electromagnética, descoberto por Faraday.
Este fenómeno pode ser evidenciado com um circuito constituído apenas por uma bobina ligada a um aparelho de medida adequado. Verifica-se que esse aparelho de medida detecta a passagem de corrente no circuito, quando se move um íman no interior da bobina (figura ).

Tendo em conta a situação descrita, seleccione a alternativa que completa correctamente a frase seguinte.
Quanto mais rápido é o movimento do íman no interior da bobina, …
(A) … menor é o módulo da força electromotriz induzida, sendo maior a energia que o circuito pode disponibilizar.
(B) … maior é o módulo da força electromotriz induzida, sendo menor a energia que o circuito pode disponibilizar.
(C) … maior é o módulo da força electromotriz induzida, sendo maior a energia que o circuito pode disponibilizar.
(D) … menor é o módulo da força electromotriz induzida, sendo menor a energia que o circuito pode disponibilizar.
- Opção (C)
⇒ Quanto mais rápido for o movimento mais rápida é a variação do fluxo do campo magnético através da área da bobina.
⇒ A lei de Faraday da indução, mostra-nos que também é maior o módulo da força electromotriz induzida; consequentemente, pode ser disponibilizada mais energia.
- Opção (C)…………. 5 pontos
2.4.2. O sinal eléctrico gerado num microfone tem frequências demasiado baixas para ser encaminhado directamente para a antena emissora. Deve, por esse motivo, sofrer um processo de modulação.
Além do sinal eléctrico gerado no microfone, o processo de modulação requer outro sinal. Identifique esse sinal e explique sucintamente em que consiste o processo de modulação.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
⇒ A modulação consiste na utilização de um protocolo que utiliza uma onda de elevada frequência de amplitude constante, a onda portadora, e uma onda que contém a informação. Dessas duas ondas resulta apenas uma. Existem protocolos de modulação em frequência e de modulação em amplitude. Na modulação em amplitude, AM, a amplitude da onda resultante varia de acordo com a amplitude da onda que contém a informação. Na modulação em frequência, o que vai variando é a frequência da onda produzida, depois de incorporadas as duas ondas.
ou
⇒ A emissão das ondas de rádio não é feita com o sinal original porque a sua frequência é muito baixa para poder ser emitida e recebida. O sinal com a informação original é utilizado para modificar as propriedades de uma onda de alta frequência, a onda transportadora. É a onda transportadora que é emitida e depois recebida. A modulação pode ser feita modificando a amplitude da onda transportadora em diferentes intervalos de tempo, modulação em amplitude ou AM, ou modificando a frequência da onda transportadora em diferentes intervalos de tempo, modulação de frequência ou FM.
ou
⇒ No processo de modulação além do sinal elétrico gerado no microfone é necessária uma onda portadora sinusoidal de alta frequência. A modulação consiste na alteração da frequência (FM) ou da amplitude (AM) da onda portadora, por combinação com a onda que contém a informação a transmitir.
A resposta deve contemplar os seguintes elementos:
⇒ O processo de modulação requer também uma onda portadora (ou onda sinusoidal de elevada frequência).
⇒ A modulação consiste na alteração da frequência ou da amplitude da onda portadora, por combinação com a onda que contém a informação a transmitir.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

3. Um sistema químico muito estudado é o que corresponde à reacção entre o hidrogénio gasoso e o vapor de iodo para formar iodeto de hidrogénio, HI.
Esta reacção reversível é traduzida pela seguinte equação química:
H2 (g) + I2⇋ 2 HI (g)
Tal como qualquer outro sistema químico em equilíbrio, também este sistema é capaz de evoluir num sentido ou noutro, devido a algumas alterações que nele se produzam.
3.1. À temperatura de 430 ºC, fez-se reagir 0,500 mol de H2 (g) e 0,500 mol de I2 (g), num recipiente fechado, de capacidade igual a 1,00 L.
A reacção química progrediu, tendo-se estabelecido, num dado instante, uma situação de equilíbrio. Este equilíbrio foi depois perturbado pela adição de HI(g).
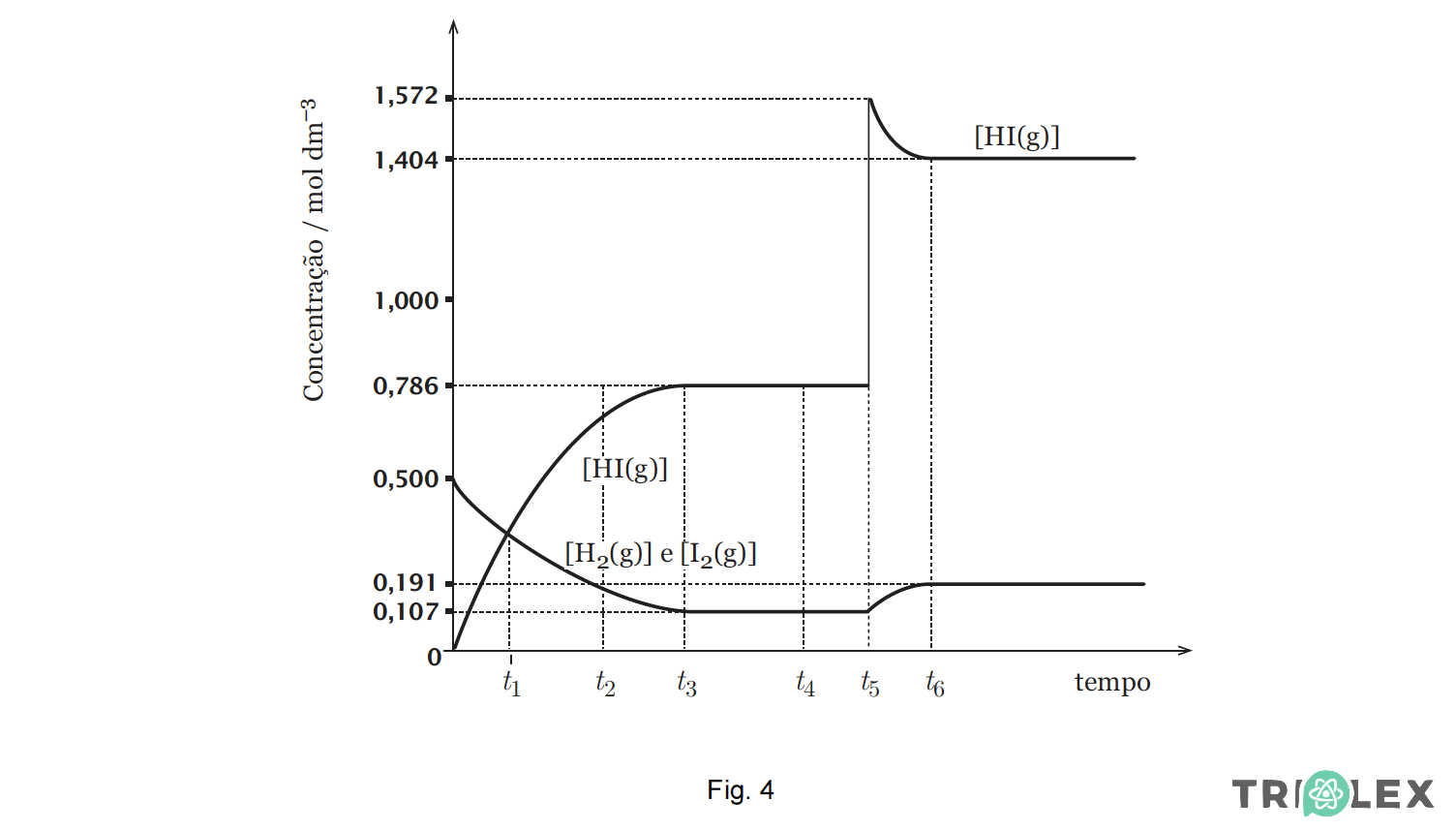
Simulando esta situação experimental, obteve-se o gráfico apresentado na figura 4, que representa a evolução das concentrações dos reagentes e do produto da reacção, ao longo do tempo, à mesma temperatura.
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
3.1.1. Tendo em conta a informação fornecida pelo gráfico, seleccione a alternativa que completa correctamente a frase seguinte.
Os instantes que correspondem ao estabelecimento do equilíbrio inicial, à igualdade das concentrações de reagentes e de produto, e à adição de HI(g), são, respectivamente, …
(A) … t1, t3 e t5
(B) … t3, t1 e t6
(C) … t3, t1 e t5
(D) … t2, t4 e t6
- Opção (C)
⇒ O equilíbrio estabelece-se quando não existe variação das concentrações das espécies envolvidas na reacção, no instante t3. Sempre que existe uma adição de uma espécie o equilíbrio altera-se de forma abrupta, em t5.
ou
⇒ “…t3, t1 e t5”
O equilíbrio inicial surge a partir do instante em que as concentrações estabilizam (instante t3), a igualdade das concentrações de reagente e de produto acontece no instante em que as linhas se cruzam (instante t1), a adição de HI(g) corresponde ao instante em que se verificam as variações bruscas nos valores da concentração (instante t5).
ou
⇒ t3 → estabelecimento do equilíbrio inicial; t1 → estabelecimento da igualdade de concentrações dos reagentes e dos produtos; t5 → momento de adição de HI (g).
- Opção (C)…………. 5 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
3.1.2. Escreva a expressão que traduz a constante de equilíbrio, Kc, da reacção em causa.
Utilizando a informação contida no gráfico, calcule o valor dessa constante, à temperatura referida.
Apresente todas as etapas de resolução.A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Escreve a expressão que traduz a constante de equilíbrio, Kc, da reacção
⇒ Retira, do gráfico, um conjunto coerente de valores de concentração ([H2(g)]e = [I2(g)]e = 0,107 mol dm–3 e [HI(g)]e = 0,786 mol dm–3 ou [H2(g)]e = [I2(g)]e = 0,191 mol dm–3 e [HI(g)]e = 1,404 mol dm–3) e calcula o valor da constante de equilíbrio (Kc = 54,0).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

* Descritores apresentados no segundo quadro da página C/3 dos critérios gerais de classificação.
3.2. O iodeto de hidrogénio, HI(g), é um gás cujas moléculas são constituídas por átomos de hidrogénio e átomos de iodo.
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
3.2.1. Tendo em conta a posição dos elementos iodo e flúor na Tabela Periódica, seleccione a alternativa que completa correctamente a frase seguinte.
O iodo e o flúor apresentam comportamento químico semelhante, porque…
(A) … pertencem ao mesmo período da Tabela Periódica.
(B) … apresentam valores muito baixos de energia de ionização.
(C) … apresentam o mesmo número de electrões de valência.
(D) … apresentam valores muito semelhantes de raio atómico.
- Opção (C)
⇒ O que caracteriza os elementos de um mesmo grupo é terem o mesmo número de electrões de valência. O iodo tem um raio atómico maior do que o flúor, pois está dois períodos abaixo e ambos têm elevadas energias de ionização.
ou
⇒ “O iodo e o flúor apresentam comportamento químico semelhante, porque apresentam o mesmo número de electrões de valência” O iodo e o flúor estão no grupo 17 da T.P., pois apresentam o mesmo número de electrões de valência.
ou
⇒ (A) Falsa.
Os elementos flúor e iodo pertencem a períodos da TP diferentes. Pertencem, respetivamente, aos períodos 2 e 5.
⇒ (B) Falsa.
Apresentam valores elevados de energia de ionização.
⇒ (C) Verdadeira.
O número de eletrões de valência destes elementos é o mesmo: 7. As configurações eletrónicas de valência dos átomos de flúor e de iodo são, respetivamente, 2s2 2p5 e 5s2 5p5.
⇒ (D) Falsa.
Como estes elementos pertencem, respetivamente, aos períodos 2 e 5 da TP, apresentam valores muito diferentes do raio atómico: r (I) > r (F).
- Opção (C)…………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)

Escreva um texto no qual analise o espectro de emissão do átomo de hidrogénio, abordando os seguintes tópicos:
• descrição sucinta do espectro;
• relação entre o aparecimento de uma qualquer risca do espectro e o fenómeno ocorrido no átomo de hidrogénio;
• razão pela qual esse espectro é descontínuo.
⇒ O espectro de emissão é descontínuo, identificando-se riscas em diferentes zonas do espectro electromagnético. Por exemplo, no infravermelho, no visível e no ultravioleta. As riscas aparecem devido à emissão de uma dada radiação, em resultado da transição do electrão do hidrogénio de níveis de maior energia para níveis de menor energia, após ter sido excitado, ou seja, do processo de desexcitação. O espectro é descontínuo porque também o são os níveis de energia. A energia de cada radiação depende da diferença de energia entre os níveis entre os quais se processa a transição.
ou
⇒ O espectro do átomo de hidrogénio apresenta três grupos distintos de riscas, um na zona do infravermelho, outro na zona do visível e outro na zona do ultravioleta. As riscas do espectro correspondem a transições do electrão de níveis de energia mais elevados para níveis de energia mais baixos (processo de desexcitação), com a consequente emissão de radiação correspondente a cada transição. A cada transição do electrão corresponde um valor de energia, que está quantizado, pelo que o espectro é descontínuo.
ou
⇒ – Espetro constituído por três conjuntos de riscas nas zonas do infravermelho, visível e ultravioleta, respetivamente, agrupadas em séries espetrais (não diferenciadas na figura). – Cada risca corresponde à energia libertada numa transição eletrónica descendente entre dois mesmos níveis energéticos dos átomos de hidrogénio excitados. – Como a energia do eletrão no átomo está quantizada, os níveis energéticos dos átomos são descontínuos (só existem níveis separados entre si por quantidades de energia finitas), as diferenças de energia entre esses níveis (que correspondem às energias das radiações que constituem o espetro) também são descontínuas.
⇒ O espectro apresenta um conjunto de riscas no domínio do ultravioleta, outro no domínio do visível e outro no domínio do infravermelho.
⇒ Cada risca corresponde a uma radiação emitida pelo átomo quando o electrão sofre um processo de desexcitação.
⇒ O espectro do átomo de hidrogénio é descontínuo, uma vez que a energia do electrão no átomo está quantizada.
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

* Descritores apresentados no segundo quadro da página C/3 dos critérios gerais de classificação.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
3.2.3. À semelhança do iodeto de hidrogénio, HI (g), também o fluoreto de hidrogénio, HF (g), apresenta elevada solubilidade em água.
O fluoreto de hidrogénio, em solução aquosa, sofre uma reacção de ionização que pode ser traduzida pela seguinte equação química:
HF (aq) + H2O (g) ⇋ F– (aq) + H3O+ (aq)
Seleccione a alternativa que refere as duas espécies que, na reacção acima indicada, se comportam como bases de Brönsted-Lowry.
(A) H2O (l) e F– (aq)
(B) F– (aq) e H3O+ (aq)
(C) HF (aq) e F– (aq)
(D) HF (aq) e H2O (l)
- Opção (A)
⇒ Uma espécie comporta-se como base se aceitar um H+. H2O comporta-se como base ao passar a H3O+, e também F– , ao passar a HF.
ou
⇒ Uma base de Brönsted-Lowry é uma espécie que tem tendência para receber protões. Observando a equação, essas espécies são a água (H2O), que recebe o protão (ião H+) do fluoreto de hidrogénio (HF), e o ião fluoreto (F–), que é a base conjugada do fluoreto de hidrogénio. O ião F– tem tendência a receber protões da água segundo a equação F– (aq) + H2O (l) ⇋ HF (aq) + OH– (aq).
ou
⇒ (A) Verdadeira.
As espécies H2O (l) e F– (aq) captam um protão na transformação direta e inversa, respetivamente: H2O → H3O+ e F– → HF .
⇒ (B) Falsa.
Só F– (aq) é base de Brönsted-Lowry.
⇒ (C) Falsa.
Ver (B).
⇒ (D) Falsa.
Só H2O (l) se comporta como base de Brönsted-Lowry. H3O+ (aq) e HF (aq) são ácidos de Brönsted-Lowry.
- Opção (A)…………. 5 pontos
4. A preparação de soluções aquosas de uma dada concentração é uma actividade muito comum, quando se trabalha num laboratório químico.
No decurso de um trabalho laboratorial, um grupo de alunos preparou, com rigor, 250,00 cm3 de uma solução aquosa, por pesagem de uma substância sólida.
4.1. Na figura está representado um balão volumétrico calibrado de 250 mL, semelhante ao utilizado pelos alunos na preparação da solução.
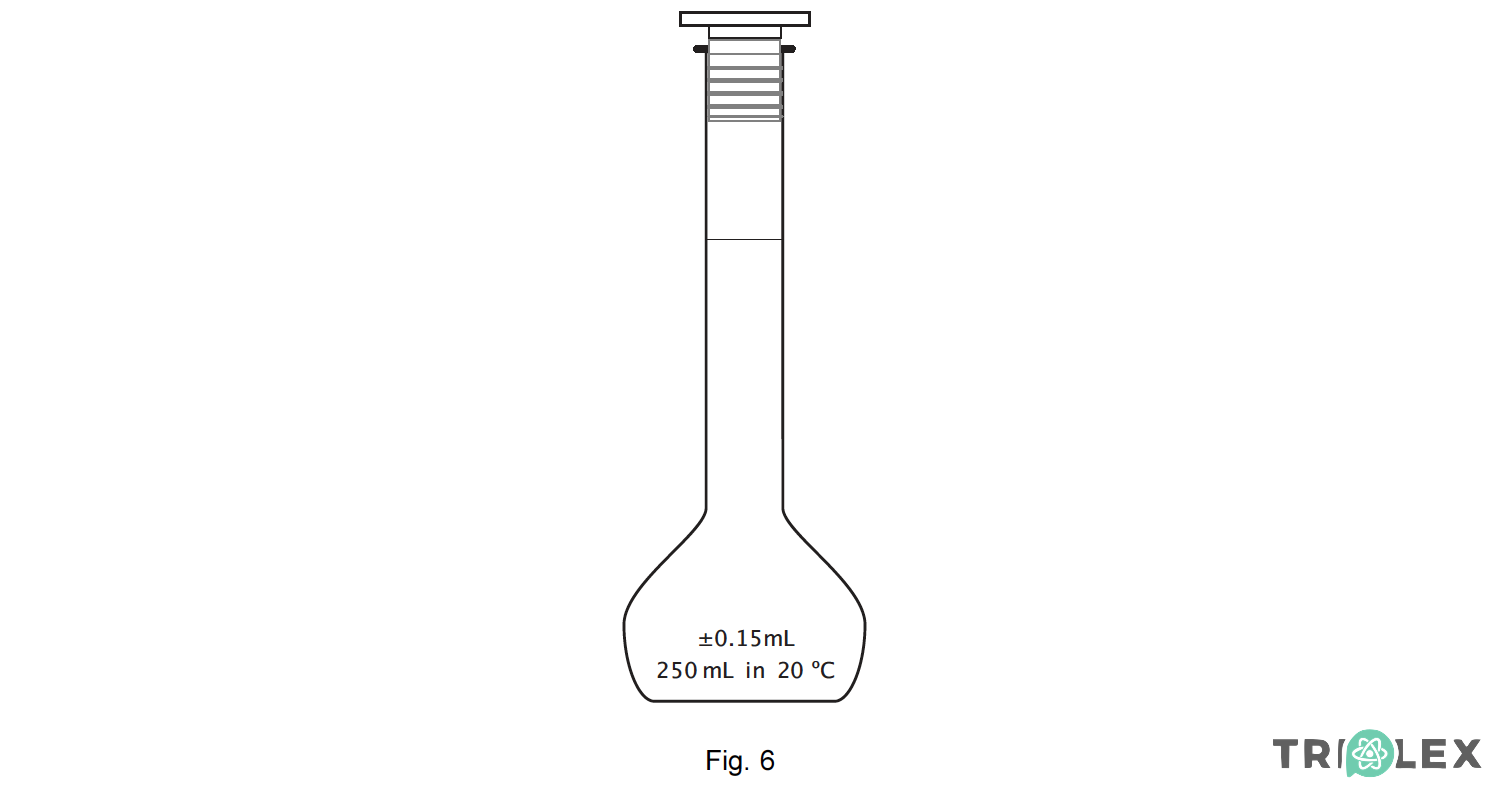
No balão estão indicadas a sua capacidade, a incerteza associada à sua calibração e a temperatura à qual esta foi efectuada.
No colo do balão está marcado um traço de referência em todo o perímetro.
- A.l. – Medições
4.1.1. Tendo em conta as indicações registadas no balão volumétrico, indique o intervalo de valores no qual estará contido o volume de líquido a ser medido com este balão, à temperatura de 20 oC.
- 249,85 mL < V < 250,15 mL
ou
⇒ A incerteza associada à calibração é de 0,15 mL. O volume de líquido contido no balão estará entre V = 200 – 0,15 = 249,85 cm3 e V = 200 + 0,15 = 250,15 cm3.ou
⇒ V = 250 ± 0,15 mL logo, 249,85 mL ≤ V ≤ 250,15 mL- 249,85 cm3 ≤ V ≤ 250,15 cm3 …………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
- A.l. – Medições
4.1.2. Os alunos deverão ter alguns cuidados ao efectuarem a leitura do nível de líquido no colo do balão, de modo a medirem correctamente o volume de solução aquosa preparada.
Seleccione a alternativa que corresponde à condição correcta de medição.
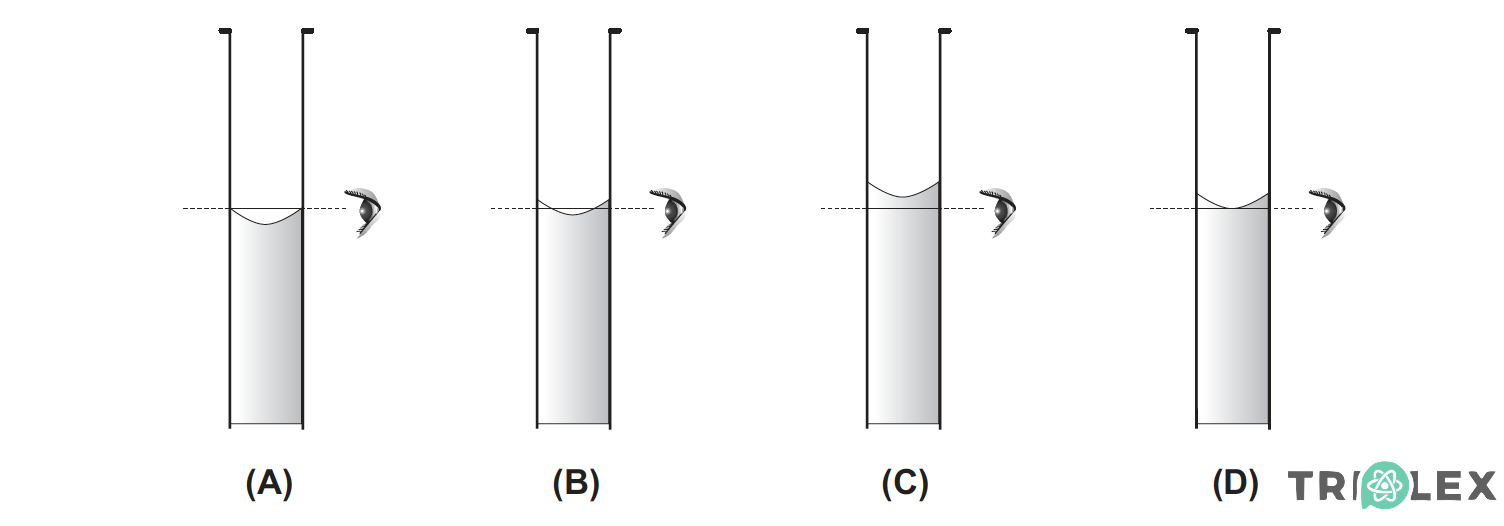
- Opção (D)
ou
⇒ Quando um líquido forma um menisco côncavo, como o representado na figura, a leitura deve ser feita de modo que os olhos se situem ao mesmo nível da parte inferior do menisco e olhem na direção tangente a esta parte do menisco. Esta condição verifica-se unicamente na medição correspondente à alternativa (D).- Opção (D)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
4.2. O grupo de alunos teve que preparar, com rigor, 250,00 cm3 de solução de tiossulfato de sódio penta-hidratado, Na2S2O3 • 5 H2O(aq) (M = 248,22 g mol–1), de concentração 3,00 × 10–2 mol dm–3, por pesagem do soluto sólido.
Calcule a massa de tiossulfato de sódio penta-hidratado que foi necessário pesar, de modo a preparar a solução pretendida.
Apresente todas as etapas de resolução.
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula a quantidade de soluto que existirá em 250,00 cm3 de solução (n = 7,500 × 10–3 mol).
⇒ Calcula a massa de tiossulfato de sódio penta-hidratado correspondente (m = 1,86 g).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:
* Descritores apresentados no segundo quadro da página C/3 dos critérios gerais de classificação.
4.3. Considere que os alunos prepararam ainda, com rigor, 50,00 cm3 de uma solução de concentração 6,00 × 10–3 mol dm–3, por diluição da solução 3,00 × 10–2 mol dm–3 de tiossulfato de sódio penta-hidratado.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
4.3.1. Seleccione a alternativa que permite calcular correctamente o volume, expresso em cm3, da solução mais concentrada, que os alunos tiveram que medir, de modo a prepararem a solução pretendida.
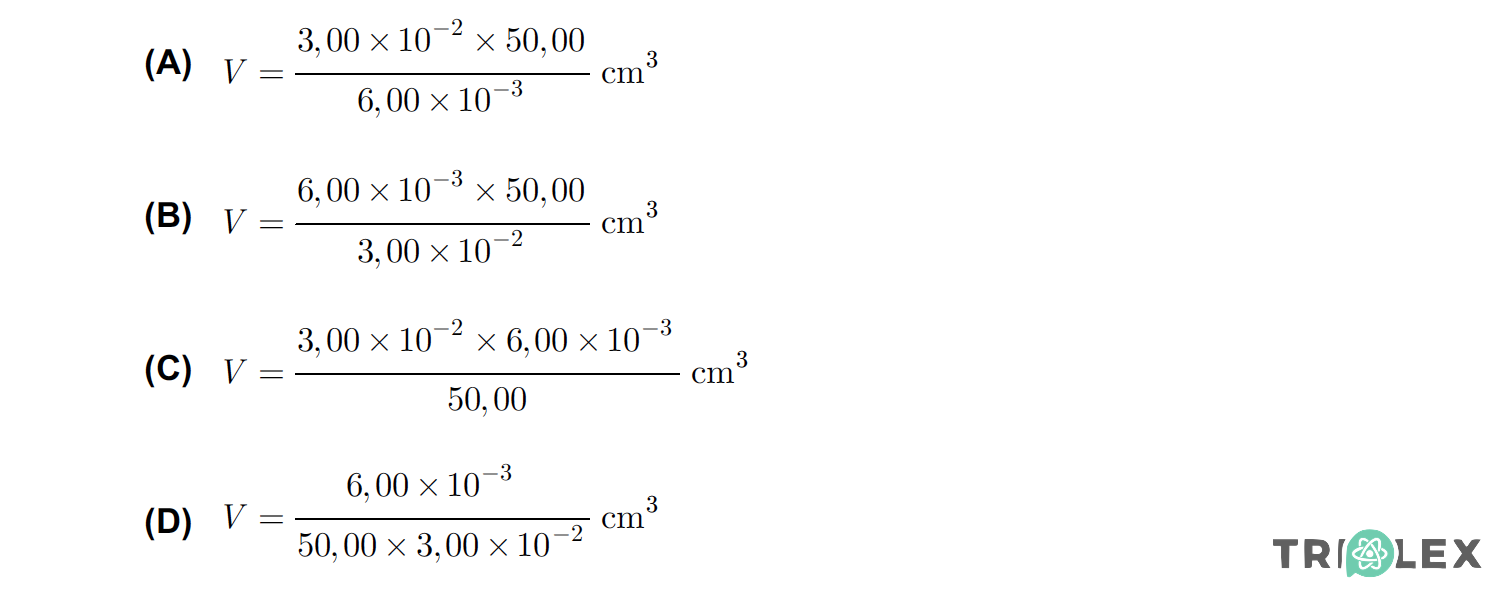
- Opção (B)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
4.3.2. Para medirem o volume da solução mais concentrada, os alunos utilizaram material de laboratório adequado.
Seleccione a alternativa que refere o tipo de instrumento de medição de volumes de líquidos que deverá ter sido utilizado naquela medição.
(A) Balão de Erlenmeyer
(B) Proveta
(C) Pipeta
(D) Gobelé
- Opção (C)
⇒ Sempre que se prepara uma solução, deve ser usado o instrumento que permita uma medida mais rigorosa: a pipeta.
- Opção (C)…………. 5 pontos
5. A água consegue dissolver, em extensão apreciável, um elevado número de substâncias. O cloreto de sódio, NaCl, é exemplo de uma substância muito solúvel em água.
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
5.1. Considerando que a solubilidade do NaCl em água, a 25 oC, é igual a 36,0 g NaCl/100 g H2O, seleccione a opção que contém os termos que devem substituir as letras (a) e (b), respectivamente, de modo a tornar verdadeira a afirmação seguinte.
Adicionando 90,0g de NaCl (s) a 250g de água, a 25 oC, obtém-se uma solução ___ (a) ___ naquele composto, ___ (b) __ sólido depositado no fundo do recipiente.
(A) … saturada … sem …
(B) … insaturada … sem …
(C) … saturada … com …
(D) … insaturada … com …
- Opção (A)
⇒ Como s (NaCl) = 36,0 g NaCl/100 g H2O, a 25 ºC, a quantidade máxima de soluto (expressa em gramas) que é possível dissolver em 250,0 g de água, a 25 ºC, é exatamente 90,0 g.
⇒ Obter-se-ia, então, uma solução saturada em NaCL, sem sólido depositado no fundo do recipiente.
- Opção (A)…………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
5.2. Em solução aquosa, o ácido clorídrico, HCl (aq), reage com o hidróxido de sódio, NaOH (aq).
Esta reacção pode ser traduzida pela seguinte equação química:
HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l)
Considere que se fez reagir 25,0 cm3 de ácido clorídrico, de concentração 0,100 mol dm–3, com um determinado volume de uma solução aquosa de hidróxido de sódio, contendo 1,0 × 10–3 mol de NaOH.
Calcule o pH da solução resultante, sabendo que o volume total desta solução é 35,0 cm3.
Apresente todas as etapas de resolução.
O ácido clorídrico, por ser um ácido forte, ioniza-se completamente em solução aquosa originando iões Cl– e H3O+.
A quantidade química de iões H3O+ presentes na solução inicial é:
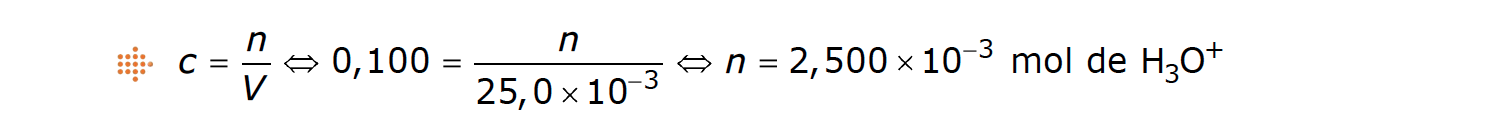
Sendo o NaOH uma base forte, encontra-se completamente dissociada em iões Na+ e iões OH–.
⇒ A quantidade química de iões OH– adicionada é assim igual a 1,0 x 10-3 mol.
Sendo a reacção entre H3O+ e OH– uma reacção completa,
n(H3O+ que reage) = n(OH– adicionados)
⇒ A quantidade de H3O+ que permanece em solução é:
- n = 2,500 x 10-3 – 1,0 x 10-3 = 1,50 x 10-3 mol
A concentração da nova solução é:
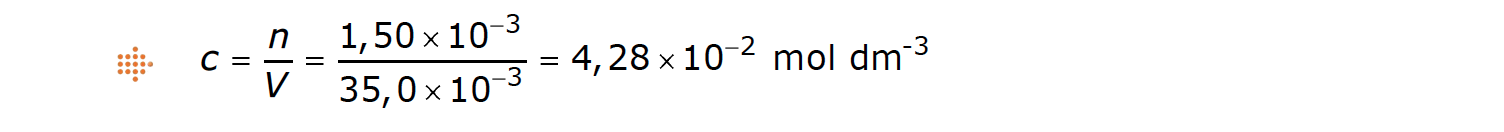 ⇒ pH = – log [ H3O+] = – log 4,28 x 10-2 = 1,4
⇒ pH = – log [ H3O+] = – log 4,28 x 10-2 = 1,4
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒ Calcula a quantidade de H3O+ que existe na solução ácida inicial (n = 2,500 × 10–3 mol).
⇒ Calcula a quantidade de H3O+ que fica em solução depois da adição da solução básica (n = 1,50 × 10–3 mol).
⇒ Calcula a concentração hidrogeniónica na solução resultante e o correspondente valor de pH (1,4).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

* Descritores apresentados no segundo quadro da página C/3 dos critérios gerais de classificação.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
6. As transferências de energia podem ser realizadas com maior ou menor rendimento, consoante as condições em que ocorrem.
Na figura está representado um gerador, que produz corrente eléctrica sempre que se deixa cair o corpo C. Admita que a corrente eléctrica assim produzida é utilizada para aquecer um bloco de prata, de massa 600 g, nas condições da figura.

Considere que a temperatura do bloco de prata aumenta 0,80 oC quando o corpo C, de massa 8,0 kg, cai 2,00 m. Calcule o rendimento do processo global de transferência de energia.
Apresente todas as etapas de resolução.
c (capacidade térmica mássica da prata) = 2,34 × 102 J kg–1oC–1.
A resolução deve apresentar, no mínimo, as seguintes etapas, para ser considerada correcta:
⇒Calcula a energia cedida pelo corpo C durante a queda (E = 1,60 × 102 J).
⇒Calcula a energia absorvida pelo bloco de prata (Eu = 1,12 × 102 J).
⇒Calcula o rendimento do processo (η = 70%).
A classificação da resposta a este item é feita em função do enquadramento da mesma num dos níveis de desempenho, de acordo com a tabela seguinte:

* Descritores apresentados no segundo quadro da página C/3 dos critérios gerais de classificação.
FIM