2021 – 1ªFase – Prova Escrita de FQ A
Voltar a: Física e Química
- Prova Escrita de Física e Química A – versão 1
- Prova 715: 1.ª Fase – 2021
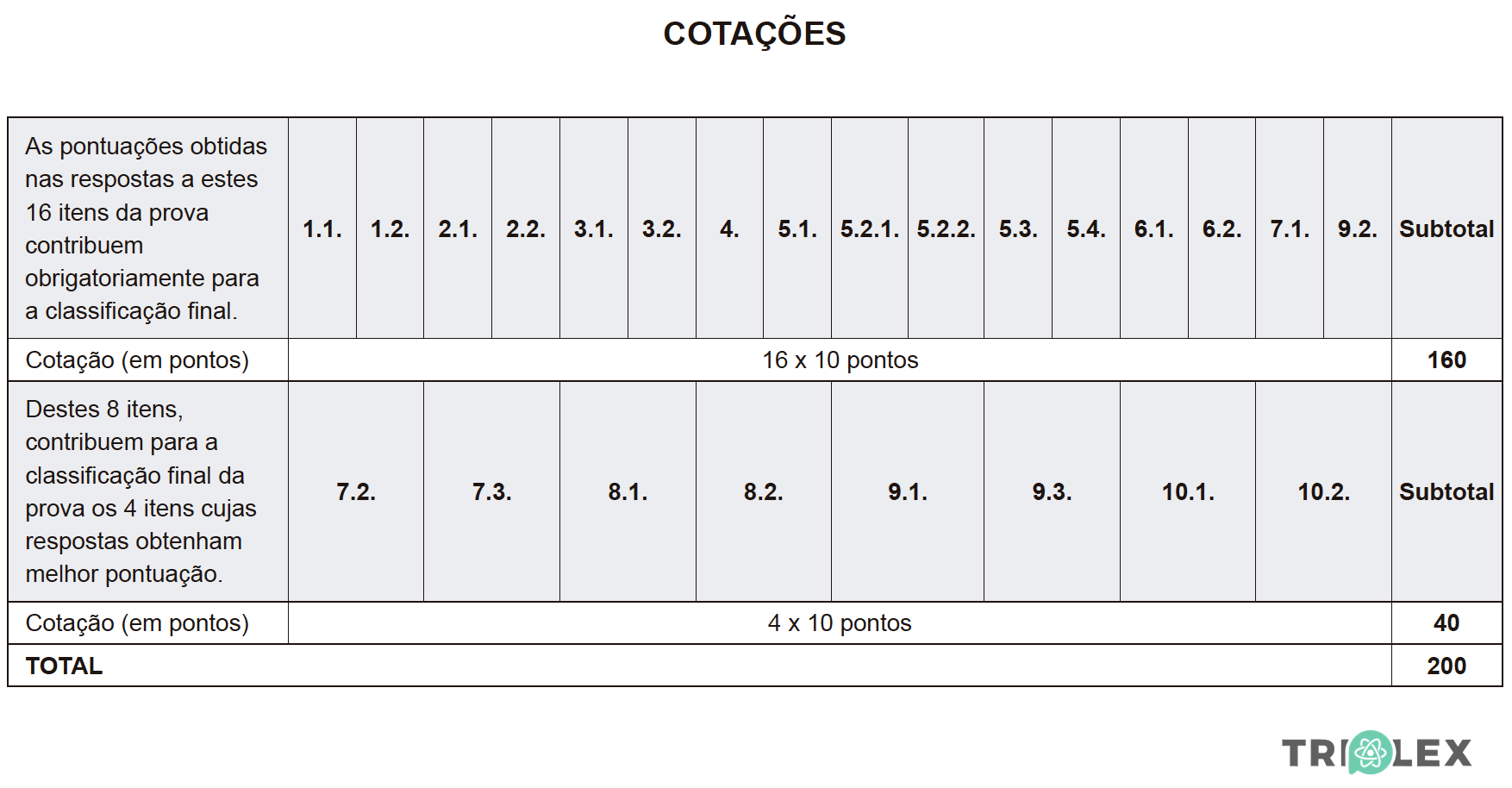
A prova inclui 16 itens, devidamente identificados no enunciado, cujas respostas contribuem obrigatoriamente para a classificação final.
Dos restantes 8 itens da prova, apenas contribuem para a classificação final os 4 itens cujas respostas obtenham melhor pontuação.
1. Em meados do século XIX, James Joule estabeleceu a equivalência entre trabalho e calor, comparando a energia transferida como trabalho, necessária para obter um determinado aumento de temperatura numa amostra de água, com a energia transferida como calor para obter o mesmo efeito.
Joule utilizou um dispositivo semelhante ao esquematizado na Figura 1, no qual dois discos de chumbo (D1 e D2) eram elevados a uma determinada altura.
Quando os discos caíam, faziam rodar um sistema de pás mergulhado na água contida num recipiente.
O movimento rotativo das pás provocava a agitação da água, o que conduzia a um aumento da sua temperatura.

A massa total dos discos era 26,3 kg e a massa da água contida no recipiente era 6,04 kg.
A partir dos resultados obtidos numa série de experiências, Joule verificou que, após 20 quedas sucessivas de uma mesma altura de 1,60 m, o aumento de temperatura da água era, em média, 0,313 ºC.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1.1. Admita que, naquela série de experiências, o aumento da energia interna da água foi, em média, 95,2% da diminuição da energia potencial gravítica do sistema discos + Terra que resultou das 20 quedas sucessivas dos discos.
Considere que, no local onde foram realizadas as experiências, o módulo da aceleração gravítica era 9,81 m s-2.
Determine, a partir dos resultados de Joule, a capacidade térmica mássica da água.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Cálculo da variação de energia potencial gravítica do sistema discos + Terra nas 20 quedas dos discos:
- Δ𝐸pg = 𝑚 𝑔 (ℎ − ℎ0) × 20, em que se considera ℎ = 0 m e ℎ0 = 1,60 m
- Δ𝐸pg = 26,3 kg × 9,81 m s−2 × (−1,60 m) × 20 ⇔ Δ𝐸pg = −8256 J
⇒ Cálculo da variação de energia interna da amostra de água contida no recipiente:
- Δ𝐸int = 0,952 × |Δ𝐸pg| ⟶ Δ𝐸int = 0,952 × 8256 J ⇔ Δ𝐸int = 7860 J
⇒ Cálculo da capacidade térmica mássica da água:
Considerando que só há variação de temperatura, Δ𝑡 = 0,313 ℃, da amostra de água, a variação de energia interna é dada por:
- Δ𝐸int = 𝑚 × 𝑐 × Δ𝑡
em que 𝑚 é a massa da amostra de água e 𝑐 a capacidade térmica mássica da água.
Substituindo, vem:
- 7860 J = 6,04 kg × 𝑐 × 0,313 ℃ ⇔ 𝑐 = 4,16 × 103 J kg−1 ℃−1
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a diminuição da energia potencial gravítica do sistema discos + Terra numa queda dos discos (4,128 x 102 J)
ou
- Calcula a diminuição da energia potencial gravítica do sistema discos + Terra para 20 quedas dos discos (8,256 x 103 J) ………… 2 pontos
⇒ Calcula o aumento da energia interna da água (7,860 x 103 J) ……….. 4 pontos
⇒ Calcula a capacidade térmica mássica da água (4,16 x 103 J kg-1 ºC-1 ) ……. 4 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1.2. Considere que, durante uma parte do percurso, os discos caíram com velocidade constante.
Qual foi a soma dos trabalhos realizados pelas forças que atuaram nos discos, nessa parte do percurso?
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ A soma dos trabalhos realizados pelas forças que atuaram nos discos na parte do percurso em que os discos caíram com velocidade constante é nula.
Notas:
⇒ Se numa parte do percurso a velocidade é constante, nessa parte do percurso a energia cinética dos discos é constante, ou seja, a variação de energia cinética dos discos é nula.
⇒ Considerando o Teorema da Energia Cinética, segundo o qual o somatório dos trabalhos é igual à variação de energia cinética, conclui-se que o somatório dos trabalhos é nulo.
Ou
⇒ A aceleração dos discos animados de movimento de translação, no intervalo de tempo em que a sua velocidade é constante, é nula.
O que significa que a resultante das forças também é nula, não realizando por isso trabalho.
- Indica o valor solicitado (zero) —– 10 pontos
2. Um LED (Light Emitting Diode) é um dispositivo que emite luz com elevada eficiência.
Na Figura 2, representa-se o gráfico da corrente elétrica, I, num LED, em função da diferença de potencial elétrico, U, nos seus terminais (curva característica do LED).

Para se obter a curva característica do LED, montou-se um circuito no qual o LED se encontrava ligado em série a um reóstato e a uma pilha ideal (pilha cuja resistência interna pode ser considerada nula) de forçaa eletromotriz 4,50 V.
Nesse circuito, introduziram-se ainda dois aparelhos de medida adequados.
- 10ºano – Física – subdomínio 2 (Energia e fenómenos elétricos)
2.1. Qual dos esquemas seguintes representa o circuito que permite obter a curva característica do LED?

A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (B)

Notas:
⇒ Na Figura 2 do enunciado da prova, representa-se o gráfico da corrente elétrica, 𝐼, num LED, em função da diferença de potencial elétrico, 𝑈, nos seus terminais, pelo que o voltímetro tem de ser ligado aos terminais do LED.
- Opção (B) ……………. 10 pontos
- 10ºano – Física – subdomínio 2 (Energia e fenómenos elétricos)
2.2. Caso os terminais do LED tivessem sido ligados diretamente à pilha, a corrente elétrica seria superior à que o LED suporta e este acabaria por se queimar. Ao introduzir-se o reóstato em série no circuito, a corrente elétrica no LED pode ser controlada.
Determine qual deverá ser o valor da resistência elétrica mínima introduzida pelo reóstato, para que a corrente elétrica no LED não exceda 20 mA.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Leitura a partir do gráfico da diferença de potencial elétrico nos terminais do LED quando a corrente elétrica que o atravessa é de 20,0 mA:
- O gráfico mostra que, quando a corrente elétrica no LED é de 20,0 mA, a diferença de potencial elétrico nos seus terminais é de 1,950 V (máximo da diferença de potencial elétrico em “condições de segurança”).
⇒ Cálculo do valor mínimo para a diferença de potencial elétrico nos terminais do reóstato, em condições de segurança:
- Considerando o esquema do circuito elétrico usado para obter a curva característica do LED, conclui-se que a diferença de potencial elétrico nos terminais da pilha, 𝑈, é igual à soma da diferença de potencial nos terminais do LED, 𝑈LED, com a diferença de potencial nos terminais do reóstato, 𝑈reóstato.

- Considerando que a pilha é ideal (a resistência interna da pilha, 𝑟, é considerada nula), a diferença de potencial elétrico nos terminais da pilha, 𝑈=𝜀−𝑟 𝐼, é igual à sua força eletromotriz, 𝜀.
Assim,
- 𝑈 = 𝑈LED + 𝑈reóstato ⟶ 4,50 V = 1,950 V + 𝑈reóstato ⇔ 𝑈reóstato = 2,55 V
⇒ Cálculo do valor mínimo da resistência elétrica introduzida pelo reóstato, 𝑅reóstato_mín, em condições de segurança:
- Usando a equação de definição de resistência elétrica, tem-se:
𝑅reóstato_min = 𝑈reóstato/𝐼máx = 2,55 V / 20×10−3 A ⇔ 𝑅reóstato_min = 1,3 × 102 Ω
Nota:
⇒ No limite das “condições de segurança”, a resistência elétrica do material semicondutor do LED é:
- 𝑅LED_mín = 𝑈LED_máx/𝐼máx = 1,950 V/ 20×10−3 A = 98 Ω
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Obtém, a partir do gráfico, a diferença de potencial nos terminais do LED para uma corrente elétrica de 20 mA (1,95 V) ………… 2 pontos
⇒ Calcula a diferença de potencial elétrico mínima nos terminais do reóstato (2,55 V) ……. 4 pontos
⇒ Calcula o valor da resistência elétrica mínima introduzida pelo reóstato (1,3 x 102 Ω) ……. 4 pontos
3. Em 1849, Hippolyte Fizeau mediu a velocidade da luz no ar com base na experiência esquematizada na Figura 3 (que não está à escala).
Nessa experiência, um feixe de luz passava numa ranhura, na periferia de uma roda dentada, e era, a seguir, refletido num espelho colocado a uma distância de 8,63 km da roda.
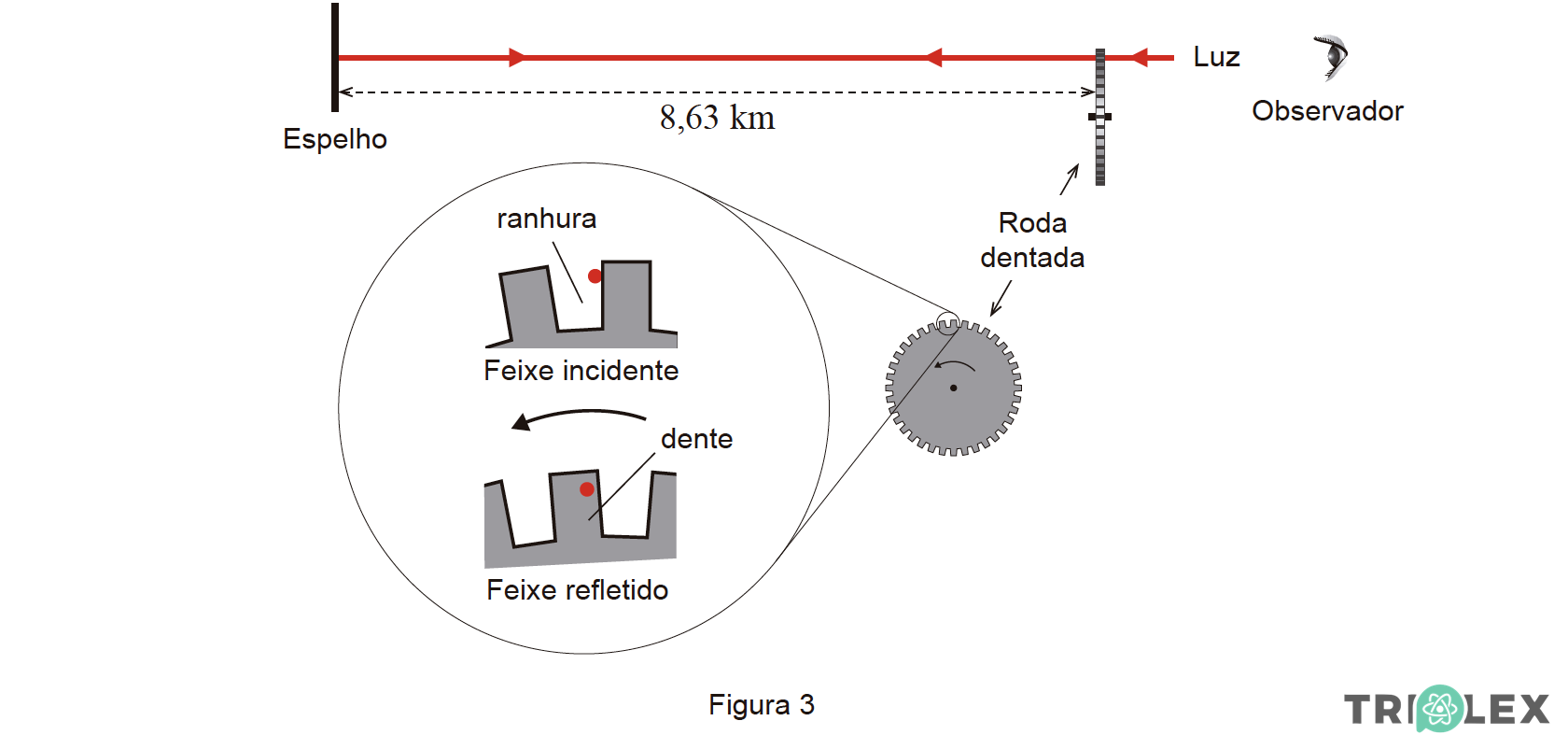
Com a roda parada, o feixe refletido no espelho voltava a passar na mesma ranhura.
Com a roda a girar com uma frequência de 12,6 Hz, o feixe refletido no espelho não voltava a passar pela ranhura, incidindo no dente imediatamente a seguir, deixando de ser detetado pelo observador.
Nestas condições, a roda descrevia um ângulo de 0,250º desde o instante em que o feixe incidente passava pela ranhura até ao instante em que o feixe refletido incidia no dente.
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
3.1. Determine a velocidade da luz no ar, tal como é obtida a partir da experiência descrita.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Cálculo da distância percorrida, 𝑑, pelo feixe de luz:
- 𝑑 = 2 × 𝑑roda−espelho = 2 × 8,63 × 103 m = 1,726 × 104 m
⇒ Cálculo do intervalo de tempo desde o instante em que o feixe incidente passava pela ranhura até ao instante em que o feixe refletido incidia no dente:
- 360°/(1/12,6 s) = 0,250°/ Δ𝑡 ⇔ Δ𝑡 = 5,511 × 10−5 s
⇒ Cálculo da velocidade de propagação da luz no ar, tal como é obtida a partir da experiência descrita:
- 𝑐 = 𝑑/Δ𝑡 = 1,726 × 104 m / 5,511×10−5 s = 3,13 × 108 m s−1
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula o intervalo de tempo desde a passagem da luz pela ranhura até incidir no dente imediatamente a seguir da roda (5,512 x 10-5 s) ………… 5 pontos
⇒ Calcula a velocidade da luz no ar, obtida a partir da experiência descrita (3,13 x 108 m s-1 ) …………. 5 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
3.2. Considere a roda dentada a girar e dois pontos da roda a diferentes distâncias do centro.
Os módulos das velocidades desses pontos são ______ e os módulos das suas velocidades angulares são ______.
(A) iguais … iguais
(B) iguais … diferentes
(C) diferentes … iguais
(D) diferentes … diferentes
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (C)
⇒ Os módulos das velocidades desses pontos são diferentes e os módulos das suas velocidades angulares são iguais.
 Notas:
Notas:
⇒ Considerem-se os pontos X e P da roda dentada. Qualquer um dos pontos descreve uma volta completa em torno do eixo de rotação no mesmo intervalo de tempo. Assim, a velocidade angular de X é igual à velocidade angular de P.
⇒ Porque a distância de X ao eixo de rotação é maior do que a distância de P a esse eixo, em intervalos de tempo iguais, a distância percorrida por X é maior do que a distância percorrida por P. Logo, o ponto X move-se mais rapidamente, pelo que o módulo da sua velocidade é maior do que o módulo da velocidade de P.
- Opção (C) ……………. 10 pontos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
- 11ºano – Física – A.l. – 3.1 – Ondas: absorção, reflexão, refração
4. Fez-se incidir um feixe de luz laser, que se propagava no ar, numa lâmina de um vidro, segundo cinco ângulos de incidência, αinc.
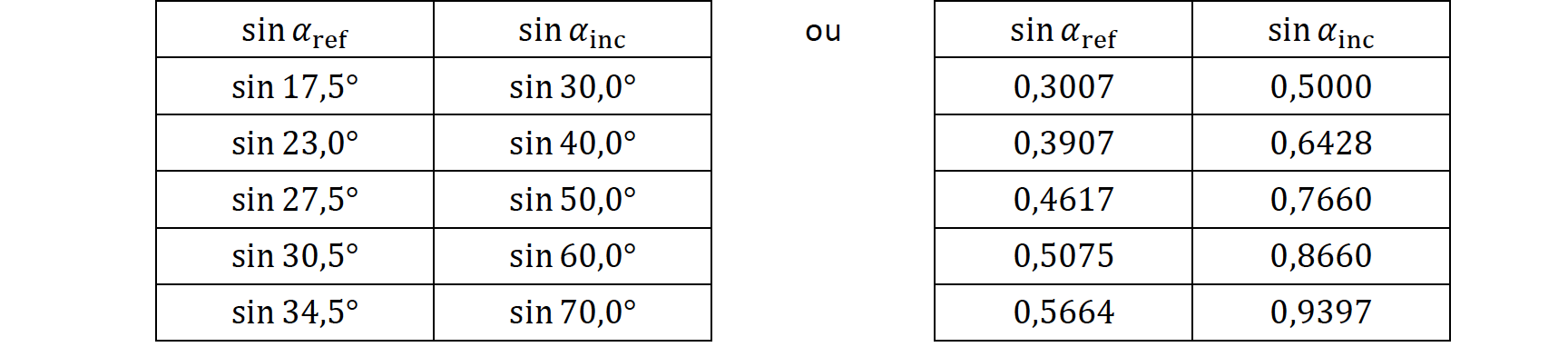
Para cada ângulo de incidência, mediu-se o correspondente ângulo de refração, αref. As amplitudes dos ângulos αinc e αref a estão registadas na tabela.
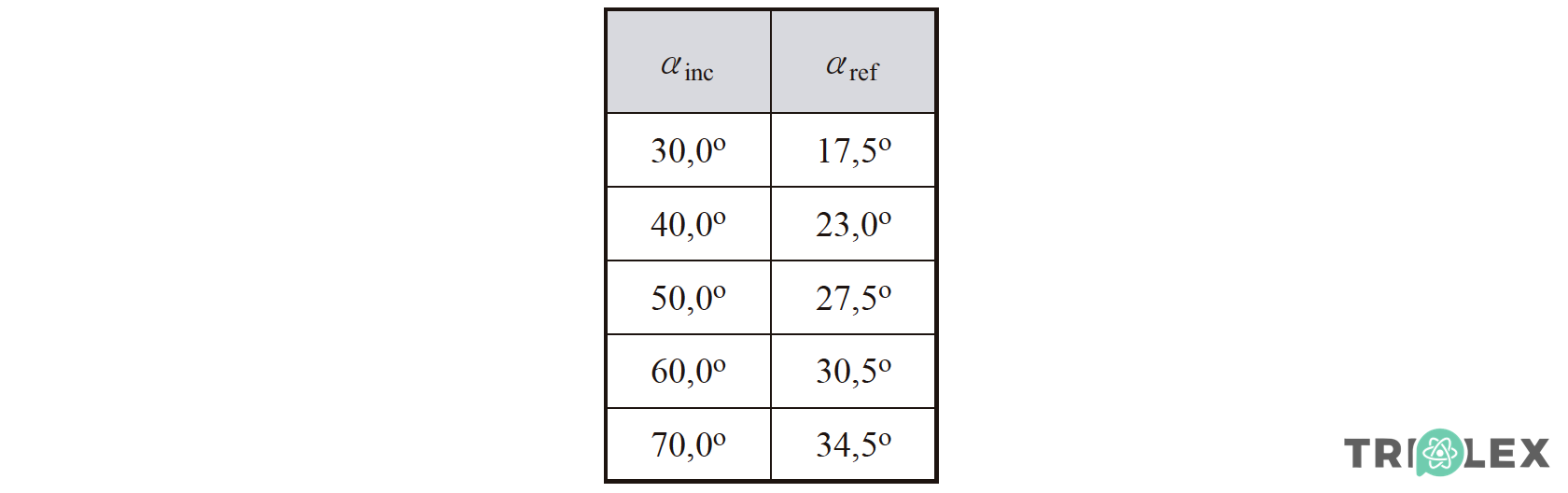
Determine o índice de refração daquele vidro.
Na resposta, apresente:
– uma tabela com os valores a utilizar na construção do gráfico, identificando as variáveis consideradas;
– a equação da reta de ajuste a um gráfico adequado;
– o cálculo do valor solicitado, a partir da equação da reta de ajuste.
Apresente todos os cálculos efetuados e o resultado com três algarismos significativos.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Uso da expressão da Lei de Snell-Descartes:
- 𝑛ar sin 𝛼inc = 𝑛vidro sin 𝛼ref ⇔ sin 𝛼inc = 𝑛vidro sin 𝛼ref (Equação 1)
ou
- sin 𝛼ref = (1 /𝑛vidro ) sin 𝛼inc (Equação 2)
⇒ Apresentação de uma tabela com os valores a utilizar na construção de um gráfico adequado à determinação do índice de refração:
- Tabela sin 𝛼ref =𝑓 (sin 𝛼inc)1 (correspondente ao gráfico sin 𝛼ref =𝑓 ( sin 𝛼inc))
ou
- Tabela sin 𝛼inc =𝑓 (sin 𝛼ref ) (correspondente ao gráfico sin 𝛼inc =𝑓 (sin 𝛼ref ))
⇒ Apresentação da equação da reta de ajuste ao gráfico2
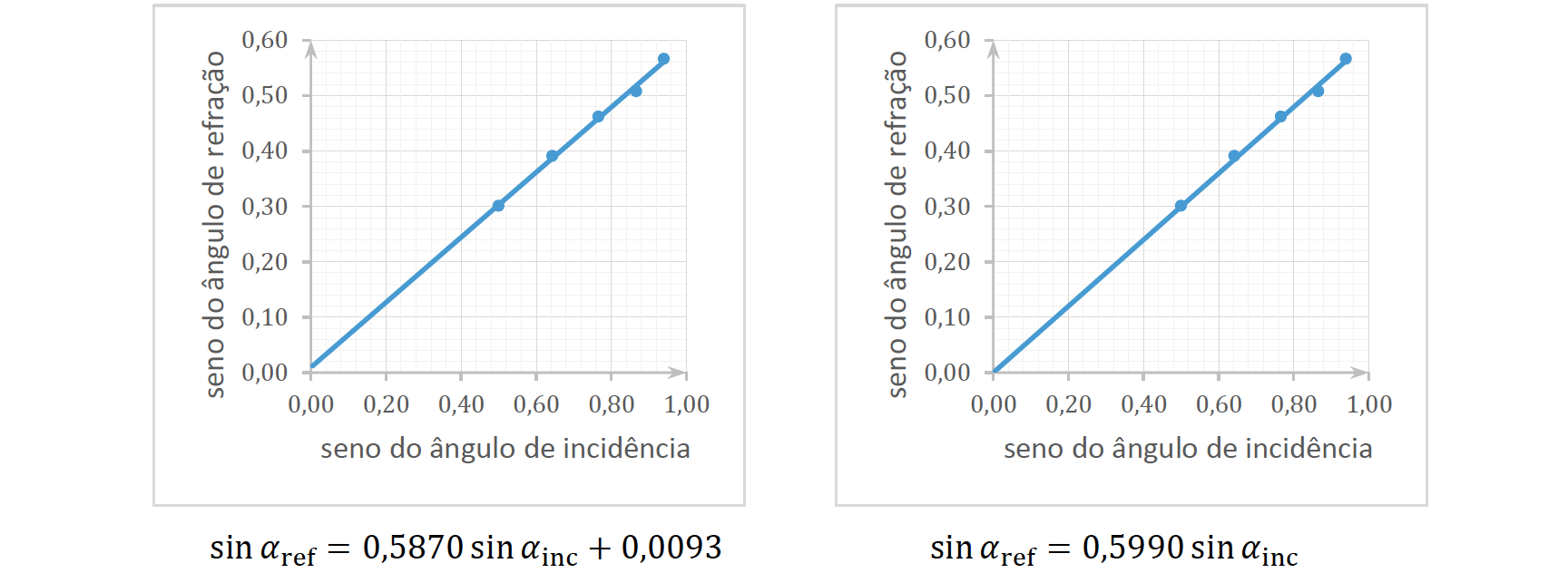
- Obtida a partir do gráfico sin 𝛼ref =𝑓 (sin 𝛼inc)
ou
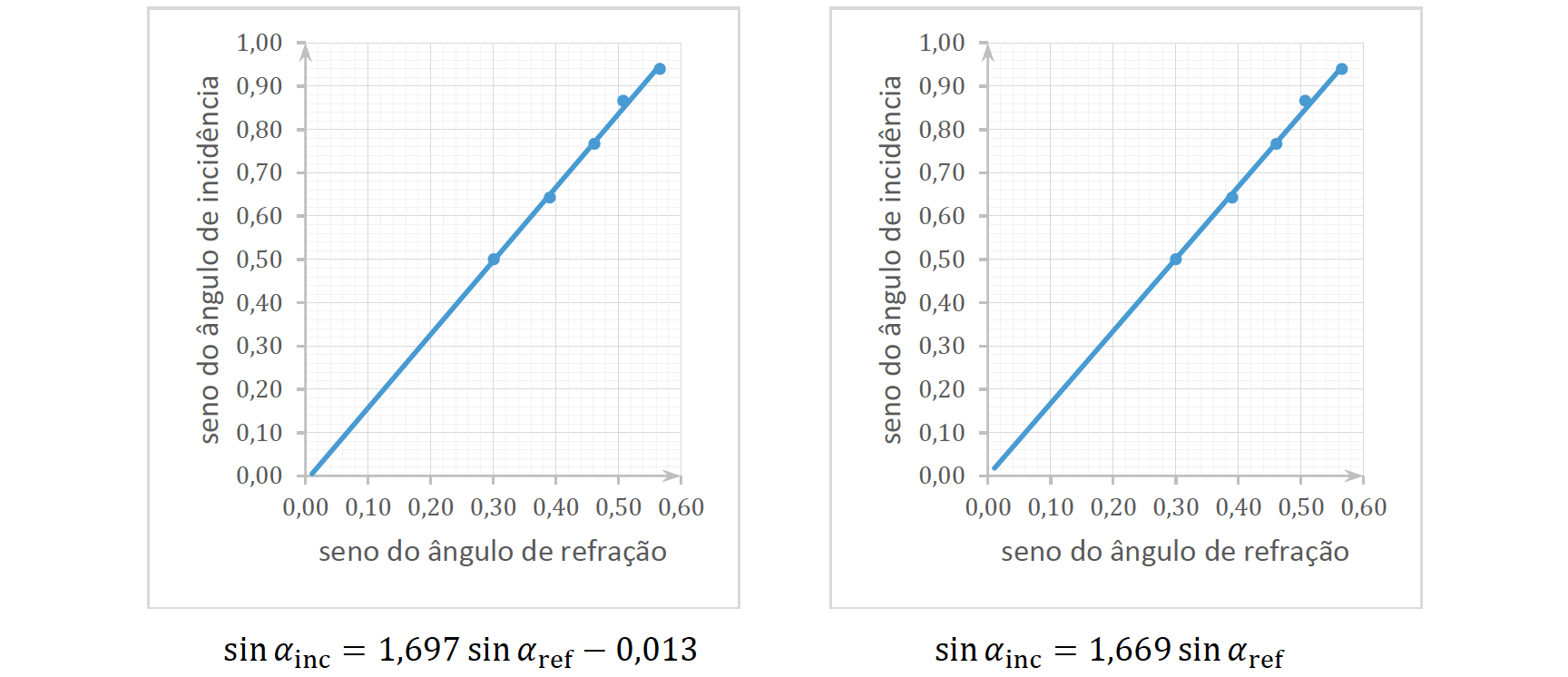
- Obtida a partir do gráfico sin 𝛼inc =𝑓 (sin 𝛼ref )
⇒ Apresentação da equação da reta de ajuste ao gráfico3
Considerando a Equação 1, conclui-se que o índice de refração é numericamente igual ao declive da reta de ajuste cuja equação é:
- sin 𝛼inc = 1,697 sin 𝛼ref – 0,013 ⇔ 𝑛vidro = 1,70
- sin 𝛼inc = 1,669 sin 𝛼ref ⇔ 𝑛vidro = 1,67
Considerando a Equação 2, conclui-se que o índice de refração é numericamente igual ao inverso do declive da reta de ajuste cuja equação é:
- sin 𝛼ref = 0,5870 sin 𝛼inc + 0,0093 ⇔ 𝑛vidro = 1,70
- sin 𝛼ref = 0,5990 sin 𝛼inc ⇔ 𝑛vidro = 1,67
Notas:
⇒ 1 sin 𝛼ref (ou o ângulo de refração, 𝛼ref) é a variável dependente, o que corresponde à situação experimental.
⇒ 2 A lei a que se pretende ajustar os resultados experimentais é da forma 𝑦=𝑚 𝑥 e deveria ser esse o ajuste feito. No entanto, as calculadoras gráficas permitem apenas a opção de ajustar a retas com ordenada não nula na origem, 𝑦=𝑚 𝑥+𝑏. Como o declive da reta de ajuste é diferente para os diferentes ajustes, apresentam-se ambas as soluções.
Contudo, uma ordenada na origem não nula pode refletir a existência de um erro sistemático.
⇒ 3 Idem
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Apresenta uma tabela com os valores sin αinc e sin αref a utilizar na construção do gráfico ……….. 5 pontos
⇒ Apresenta a equação da reta de ajuste ao gráfico sin αref = f(sin αinc )
- sin αref = 0,587 sin αinc + 0,009 (ver nota)
ou
Apresenta a equação da reta de ajuste ao gráfico sin αinc = f(sin αref )
- sin αinc = 1,697 sin αref – 0,013 (ver nota) ……….. 5 pontos
⇒ Calcula o índice de refração do vidro considerado (1,70) ……… 5 pontos
Nota: Na equação da reta de ajuste, a omissão da ordenada na origem não implica qualquer desvalorização.5. O pentacloreto de fósforo, PCl5, pode decompor-se, em fase gasosa, originando tricloreto de fósforo, PCl3 , e cloro, Cl2.
Esta reação pode ser traduzida porPCl5 (g) ⇋ PCl3 (g) + Cl2 (g)
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
5.1. Considere que a variação de entalpia associada à decomposição de 1 mol de PCl5 (g) é 88 kJ.
A energia média da ligação P – Cl na molécula PCl5 é 257 kJ mol-1, e a energia média da ligação Cl – Cl na molécula Cl2 é 243 kJ mol-1 .
Conclua, a partir das energias fornecidas, se a ligação P – Cl é, em média, mais forte na molécula PCl5 ou na molécula PCl3 .
Mostre como chegou à conclusão solicitada, apresentando todos os cálculos.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Como é necessário fornecer energia para ocorrer a decomposição, em fase gasosa, do pentacloreto de fósforo, PCℓ5 , a reação é endotérmica. Por isso, ΔH > 0 .
Para calcular a energia da ligação P − Cℓ na molécula PCℓ3, pode fazer-se o balanço entre a energia posta em jogo na decomposição do PCℓ5 , ΔHr, a energia absorvida na rutura de ligações e a energia libertada na formação das novas ligações.
⇒ Energias envolvidas:
Seja x kJ/mol a energia de ligação P − Cℓ em PCℓ3
Variação de entalpia associada à reação de decomposição de
- 1 mol de PCℓ5 (g) : ΔHr = + 88 kJ/mol
Energia absorvida na dissociação de uma mol de ligações
- P − Cℓ em PCℓ5 = 257 kJ/mol
Energia libertada na formação de uma mol de ligações
- Cℓ − Cℓ = 243 kJ/mol
⇒ Nas ligações que se partem e que se formam, atendendo a que, por convenção, a energia absorvida pelo sistema é positiva e a energia libertada é negativa.
Energia absorvida para romper ligações nas moléculas reagentes:
- 5 x 257 = 1285 kJ/mol
Energia libertada ao formar ligações nas moléculas resultantes:
- − (3 x + 243) kJ/mol
⇒ Balanço energético:
- 1285 − (3 x + 243) = 88 ⇔ 1285 − 88 = 3 x + 243 ⇔ 954 = 3 x ⇔ x = 318 kJ/mol
Como 318 kJ/mol > 257 kJ/mol ⇔ Elig P − Cℓ em PCℓ3 > Elig P − Cℓ em PCℓ5 .
⇒ Como quanto maior for a energia de ligação mais forte é a ligação, a ligação P − Cℓ em PCℓ3 é mais forte do que em PCℓ5 .
- Elementos de resposta:
⇒ cálculo da energia da ligação P – Cl na molécula PCl3 com base na diferença entre a energia envolvida na rutura de ligações químicas e a energia envolvida na formação de ligações químicas (318 kJ mol-1);
⇒ identificação da ligação mais forte com base na associação entre uma maior energia de ligação e uma ligação mais forte (P – Cl na molécula PCl3).

5.2. Um reator de volume variável contém, inicialmente, apenas 3,00 mol de PCl5 (g) e 0,80 mol de PCl3 (g).
O sistema atinge o equilíbrio à temperatura T. Considere que o volume do reator é 2,5 dm3 e que não reagiu 90% da quantidade inicial de PCl5 (g).
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
5.2.1. Determine a constante de equilíbrio, Kc , da reação de decomposição considerada, à temperatura T.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
PCℓ5 (g) ⇌ PCℓ3 (g) + Cℓ2 (g)
- n (PCℓ5)inicial = 3,00 mol
- n (Cℓ2)inicial = 0 mol
- n (PCℓ3)inicial = 0,80 mol
⇒ Como não reagiu 90% da quantidade inicial de PCℓ5 , o rendimento, η , é de 10% .
⇒ Atendendo às proporções estequiométricas 1 : 1 : 1 e ao rendimento de 10% , as quantidades no estado de equilíbrio são:
- n (PCℓ5)e = 3,00 − 0,10 x 3,00 = 2,70 mol
- n (Cℓ2)e = 0,10 x 3,00 = 0,30 mol
- n (PCℓ3)e = 0,80 + 0,10 x 3,00 = 1,10 mol
⇒ Como o volume do reator é de 2,5 dm3 , as concentrações no estado de equilíbrio são:
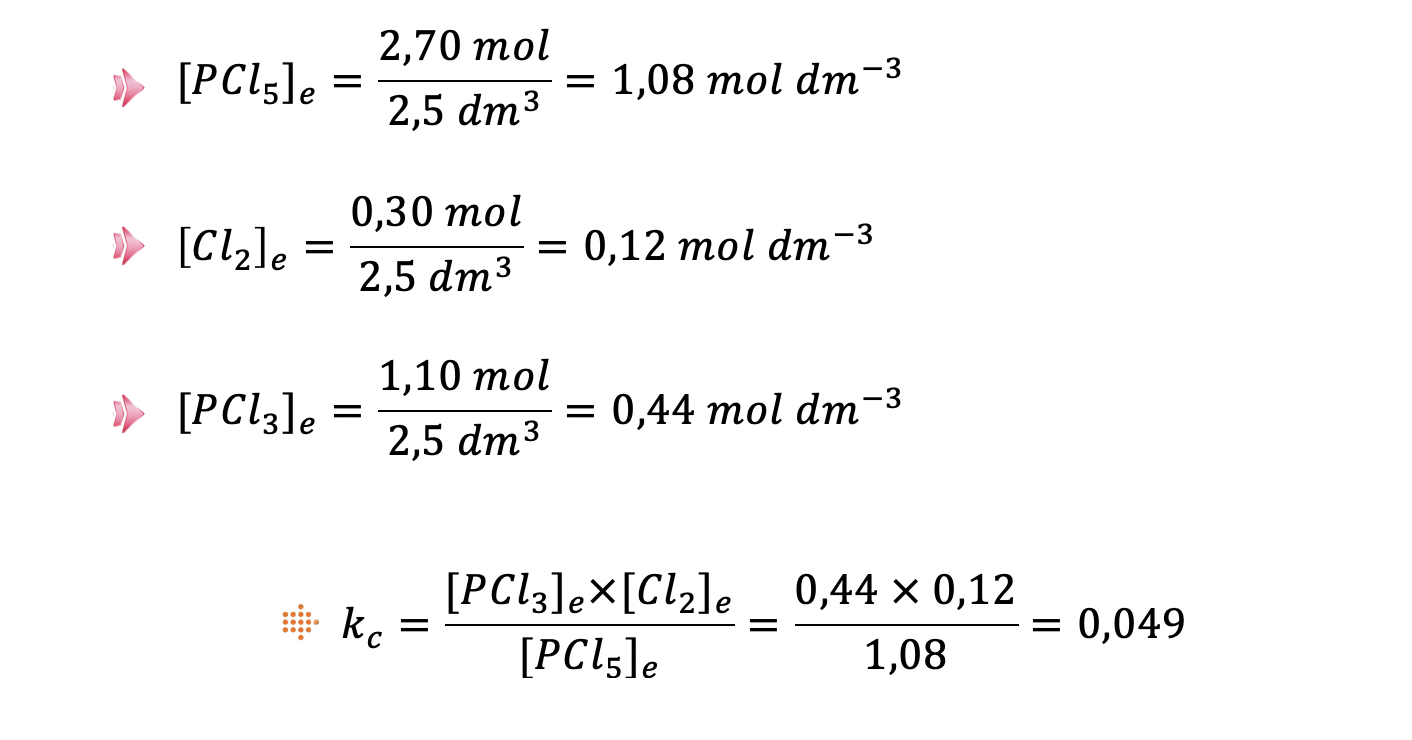
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a quantidade de Cl2 (g) no estado de equilíbrio (0,30 mol) ………. 3 pontos
⇒ Calcula a quantidade de PCl3 (g) no estado de equilíbrio (1,10 mol) …… 3 pontos
⇒ Calcula a constante de equilíbrio, Kc , da reação de decomposição considerada, à temperatura T (4,9 x 10-2 ) ……… 4 pontos
- 11ºano – Química – Domínio 1 – subdomínio 2 (Equilíbrio químico)
5.2.2. Considere que, estando o sistema em equilíbrio, se provoca uma diminuição do volume do reator, à temperatura T.
Preveja, fundamentando, como variará a quantidade de PCl5.
Escreva um texto estruturado, utilizando linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Diminuindo o volume do reator, aumenta a pressão exercida pelo sistema.
⇒ De acordo com o Princípio de Le Châtelier, o sistema reage contrariando esse aumento, evoluindo no sentido em que o sistema forma um menor número de partículas no estado gasoso, ou seja, evolui no sentido inverso, provocando, assim, um aumento da quantidade de PCℓ5 .
ou
⇒ Diminuindo o volume do reator, aumenta a concentração das três substâncias gasosas.
- Consequentemente, ocorre um aumento do quociente da reação.
⇒ Por exemplo, diminuindo, o volume do reator para 2,0 dm3 :
⇒ A temperatura constante, T, a Kc mantém-se.
⇒ Para que a razão
- se mantenha igual a Kc, isto é, para repor o equilíbrio, o sistema reage contrariando esse aumento do quociente da reação, ou seja, evolui no sentido inverso, provocando, assim, um aumento da quantidade de PCℓ5 .
- Elementos de resposta:
⇒ diminuição de volume, consequente aumento de pressão e favorecimento da reação que origina menor quantidade de moléculas;
ou
- diminuição de volume, consequente aumento das concentrações de reagentes e de produtos de reação e aumento do quociente de reação;
⇒ favorecimento da reação inversa e aumento da quantidade de PCl5 .

- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
5.3. Represente a molécula de cloro na notação de Lewis.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ A configuração eletrónica do átomo de cloro no estado fundamental é:
- 17Cℓ − 1s2 2s2 2p6 3s2 3p5
⇒ Cada átomo de cloro tem sete eletrões de valência, que são os que participam na ligação entre átomos.
⇒ Para que os dois átomos em Cℓ2 fiquem rodeados por oito eletrões (estrutura de gás nobre), é necessário que seja compartilhado um só dupleto, formando uma ligação covalente simples:
⇒ Assim, na molécula Cℓ2 há sete pares eletrónicos de valência: um compartilhado (2 eletrões ligantes) e seis não compartilhados (12 eletrões não ligantes).
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
5.4. Considere átomos de fósforo e de cloro no estado fundamental.
Prevê-se que, no átomo de fósforo, os eletrões de valência sejam, em média, _____ atraídos pelo respetivo núcleo e que o raio atómico do cloro seja ______.
(A) mais … menor
(B) mais … maior
(C) menos … maior
(D) menos … menor
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (D)
⇒ Os elementos cloro e fósforo estão localizados na Tabela Periódica no 3º período e nos grupos 17 e 15, respetivamente.
⇒ Embora o número de eletrões no cloro (17) seja superior ao número de eletrões no fósforo (15), o número de níveis de energia é o mesmo (3), pelo que a blindagem nuclear praticamente a mesma.
⇒ A carga nuclear do tomo de cloro (+ 17) é, porém, superior à carga nuclear do átomo de fósforo (+ 15) , o que provoca um aumento da força atrativa núcleo- eletrões, que é mais forte do que as repulsões entre os eletrões, ligeiramente superior nos átomos de cloro.
⇒ Assim, prevê-se que, no átomo de fósforo, os eletrões de valência sejam, em média, menos atraídos pelo respetivo núcleo e, consequentemente, que o raio atómico do cloro, cujos eletrões estão mais fortemente atraídos para o núcleo, seja menor.
- Opção (D) ……………. 10 pontos
6. Dissolveu-se amoníaco, NH3 (g), em água, tendo-se obtido uma solução de concentração 2,27 mol dm-3 e de densidade 0,98 g cm-3 , a 25 ºC.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
6.1. Determine o número de moléculas de água que existem em 250 cm3 de solução.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
⇒ Como c = n/V , a quantidade de amoníaco existente em 250 cm3 da solução considerada é dada por:
- n = c x V = 2,27 mol dm−3 x 0,250 dm3 = 0,5675 mol
⇒ Como n = m/M, a massa de amoníaco em 250 cm3 da solução considerada será:
- m = n x M = 0,5675 mol x 17,04 g/mol = 9,670 g
⇒ Como ρsolução = m/V, a massa de 250 cm3 da solução considerada será:
- msolução = ρ x V = 0,98 x 250 cm3 = 245 g
⇒ A massa de água existente nos 250 cm3 da solução considerada será:
- m (H2O) = m (solução) − m (NH3) = 245 g − 9,670 g = 235,3 g
⇒ A quantidade de água existente nos 250 cm3 da solução é:
- n (H2O) = 235,3 /18,02 = 13,06 mol
⇒ Como o número de moléculas, N = n x NA , o número de moléculas de água nos 250 cm3 da solução considerada será:
- N = 13,06 x 6,02 x 1023 ⇔ N = 7,9 x 1024 moléculas
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a massa de amoníaco em 250 cm3 da solução considerada (9,670 g) ……. 2 pontos
⇒ Calcula a massa de água no volume da solução considerada (235,3 g) ……. 4 pontos
⇒ Calcula o número de moléculas de água que existem no volume da solução considerada (7,9 x 1024 moléculas) ……. 4 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
6.2. O amoníaco, NH3 (aq), é uma base fraca, cuja ionização em água pode ser traduzida por
NH3 (aq) + H2O (l) ⇋ NH4 + (aq) + OH– (aq)
Adicionando algumas gotas de um ácido forte concentrado a um dado volume da solução de amoníaco, a concentração de OH– (aq)
(A) diminui e a concentração de NH4+ (aq) aumenta.
(B) aumenta e a concentração de NH4 + (aq) diminui.
(C) aumenta e a concentração de NH4 + (aq) aumenta.
(D) diminui e a concentração de NH4 + (aq) diminui.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (A)
⇒ O ácido forte adicionado reagirá com os aniões hidróxido (formando água) diminuindo, assim, a sua concentração na solução:
H+ (aq) + OH− (aq) → H2O (ℓ)
⇒ Para restabelecer o equilíbrio de ionização do amoníaco em água, a reação avançará no sentido direto, aumentado assim a concentração de catião amónio, NH4+ (aq).
- Opção (A) ……………. 10 pontos
7. O ácido sulfúrico, H2SO4 (aq), ioniza-se de acordo com as reações traduzidas por
(1) H2SO4 (aq) + H2O (l) → HSO4– (aq ) + H3O+ (aq) Ka1 elevado
(2) HSO4– (aq) + H2O (l) ⇋ SO42- (aq) + H3O+ (aq) Ka2 = 1,0 x 10-2 , a 25 ºC
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
7.1. Numa solução de H2SO4 (aq) 1,00 x 10-2 mol dm-3 , a 25 ºC, a concentração de H3O+ (aq) é
(A) superior à concentração de SO42- (aq), sendo o pH da solução 2,0.
(B) superior à concentração de SO42- (aq), sendo o pH da solução inferior a 2,0.
(C) igual à concentração de SO42- (aq), sendo o pH da solução 2,0.
(D) igual à concentração de SO42- (aq), sendo o pH da solução inferior a 2,0.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (B)
⇒ Como a solução é diluída (1,00 x 10−2 mol dm−3) , a reação traduzida pela equação (1) uma protólise muito extensa (Ka1 elevado) originando HSO4− (aq) e H3O+ (aq) com concentrações praticamente iguais à concentração inicial de H2SO4, 1,00 x 10−2 mol dm−3 .
⇒ Como a segunda protólise, traduzida pela equação (2) é incompleta, as concentrações de SO42− (aq) e H3O+ (aq) são inferiores à concentração de HSO4− (aq) resultante da primeira reação.
⇒ Como pH = − log [H3O+ (aq)] , o pH da solução será inferior a 2,0
- Opção (B) ……………. 10 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
7.2. O ácido conjugado da espécie SO42- (aq) é a espécie
(A) HSO4– (aq), comportando-se a água como base apenas na reação (1).
(B) HSO4– (aq), comportando-se a água como base nas reações (1) e (2).
(C) H2SO4 (aq), comportando-se a água como base nas reações (1) e (2).
(D) H2SO4 (aq), comportando-se a água como base apenas na reação (1).
- Opção (B)
⇒ Como um par conjugado ácido-base é o conjunto de duas partículas que diferem entre si em um H+ , o ácido conjugado da espécie SO42− (aq) é a espécie HSO4− (aq) .
⇒ Como, de acordo com a teoria protónica de Brönsted-Lowry, base é a espécie química aceitadora de iões H+ , a água comporta-se como base quer na primeira reação, quer na segunda reação.
- Opção (B) ……………. 10 pontos
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
7.3. A reação do ácido sulfúrico com o magnésio pode ser traduzida por
H2SO4 (aq ) + Mg (s) → H2 (g) + MgSO4 (aq)
Nesta reação, o ião H+
(A) oxida-se, sendo o magnésio a espécie redutora.
(B) reduz-se, sendo o magnésio a espécie oxidante.
(C) oxida-se, sendo o magnésio a espécie oxidante.
(D) reduz-se, sendo o magnésio a espécie redutora.
- Opção (D)
⇒ Os números de oxidação do hidrogénio são + 1 na espécie reagente H2SO4 e zero (0) na espécie H2 .
⇒ Os números de oxidação do magnésio são zero (0) na espécie reagente Mg e + 2 na espécie MgSO4 .
⇒ Como, nesta reação, o número de oxidação do hidrogénio diminui, o ião H+ reduz-se (capta eletrões), atuando como oxidante.
⇒ Como o número de oxidação do magnésio aumenta, o magnésio liberta eletrões, sofrendo oxidação e atuando como espécie redutora.
- Opção (D) ……………. 10 pontos
8. Os componentes maioritários do ar são o nitrogénio, N2 (g), e o oxigénio, O2 (g).
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
8.1. Considere uma amostra de N2 (g) e uma amostra de O2 (g), com massas iguais.
Nas mesmas condições de pressão e de temperatura, pode concluir-se que os volumes das amostras são ______ e que o número de moléculas de cada uma das amostras é ______ .
(A) iguais … igual
(B) iguais … diferente
(C) diferentes … igual
(D) diferentes … diferente
- Opção (D)
⇒ Como as massas molares do nitrogénio, N2 (g) e do oxigénio, O2 (g) são diferentes e n = m/M, massas iguais das duas amostras contém quantidades de matéria diferentes.
⇒ Como, de acordo com a lei de Avogadro, nas mesmas condições de pressão e temperatura, os volumes são proporcionais as quantidades de matéria dos gases, sendo as quantidades de matéria diferentes, também os volumes das amostras são diferentes e o número de moléculas de cada uma das amostras é diferente.
- Opção (D) ……………. 10 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
8.2. Os eletrões do átomo de nitrogénio no estado fundamental distribuem-se por
(A) três orbitais, sendo os eletrões da orbital 1s os de menor energia.
(B) cinco orbitais, sendo os eletrões da orbital 1s os de menor energia.
(C) três orbitais, sendo os eletrões das orbitais 2p os de menor energia.
(D) cinco orbitais, sendo os eletrões das orbitais 2p os de menor energia.
- Opção (B)
⇒ A configuração eletrónica do átomo de nitrogénio no estado fundamental é:
- N − 1s2 2s2 2px1 2py1 2pz1
⇒ De acordo com esta configuração, os 7 eletrões do átomo de nitrogénio, no estado fundamental, distribuem-se por cinco orbitais (1s, 2s, 2px , 2py e 2pz) , sendo os eletrões da orbital 1s os de menor energia.
- Opção (B) ……………. 10 pontos
9. Na Figura 4 (que não está à escala), representa-se parte do percurso de um corpo que foi lançaado da posição A, no instante t = 0,0 s, passando pela posição B, ao fim de 1,0 s, e atingindo a posição C, no instante t = 1,5 s.

Considere que o corpo pode ser representado pelo seu centro de massa (modelo da partícula material).
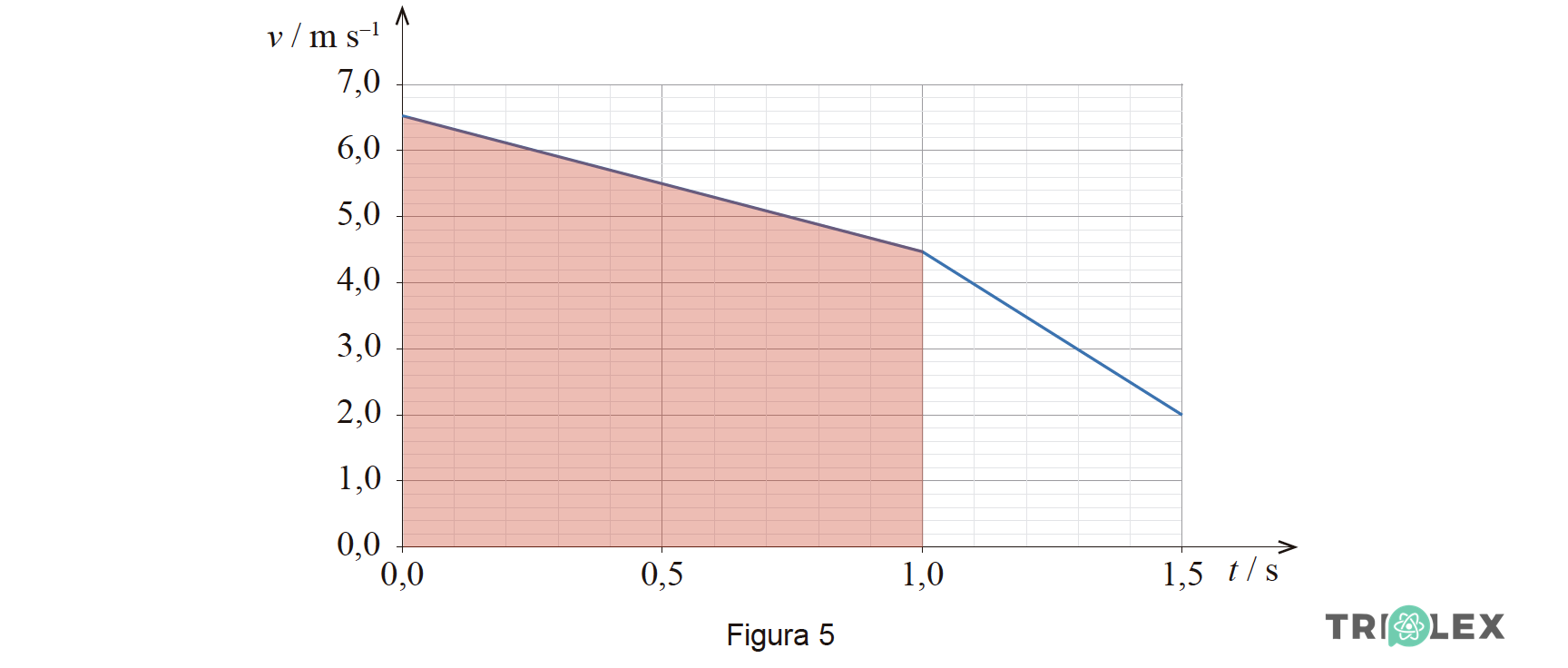
Na Figura 5, apresenta-se o gráfico do módulo da velocidade, v, do corpo em função do tempo, t.

- 11ºano – Física – Domínio 1 – subdomínio 1 (Tempo, posição e velocidade)
9.1. Qual é a distância entre as posições A e B?
(A) 5,5 m
(B) 4,5 m
(C) 6,5 m
(D) 7,5 m
- Opção (A) ……………. 10 pontos
- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
9.2. Qual dos diagramas pode representar, numa mesma escala, as forças que atuam no corpo, na subida da rampa, entre as posições B e C?
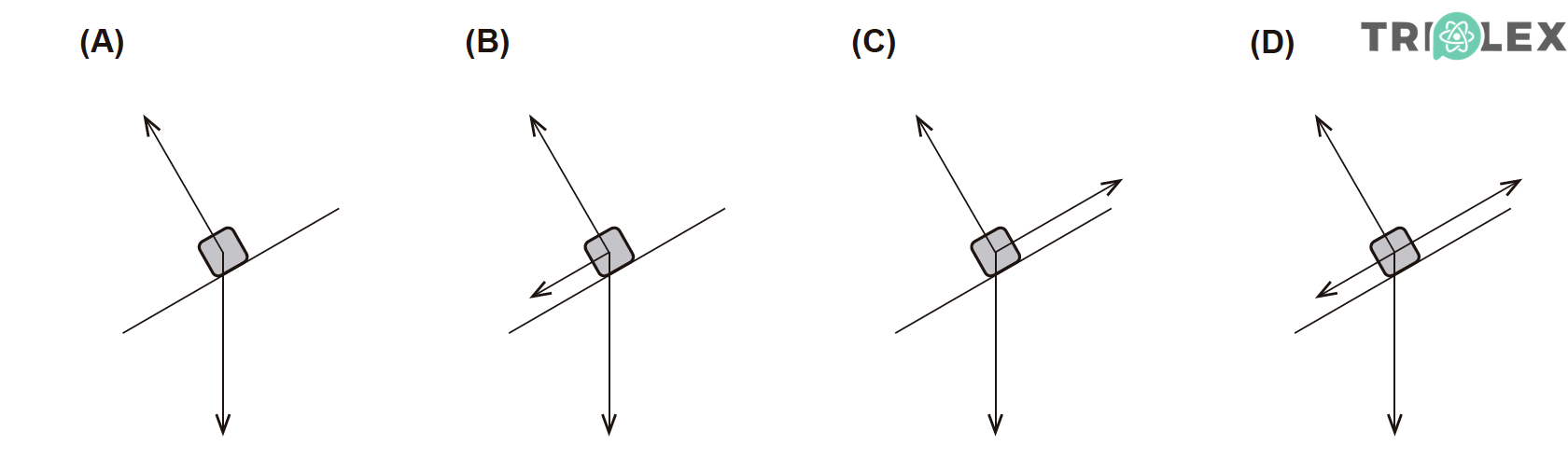
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova.
- Opção (A)
⇒ O diagrama que pode representar, numa mesma escala, as forças que atuam no corpo, na subida da rampa, entre as posições B e C é:
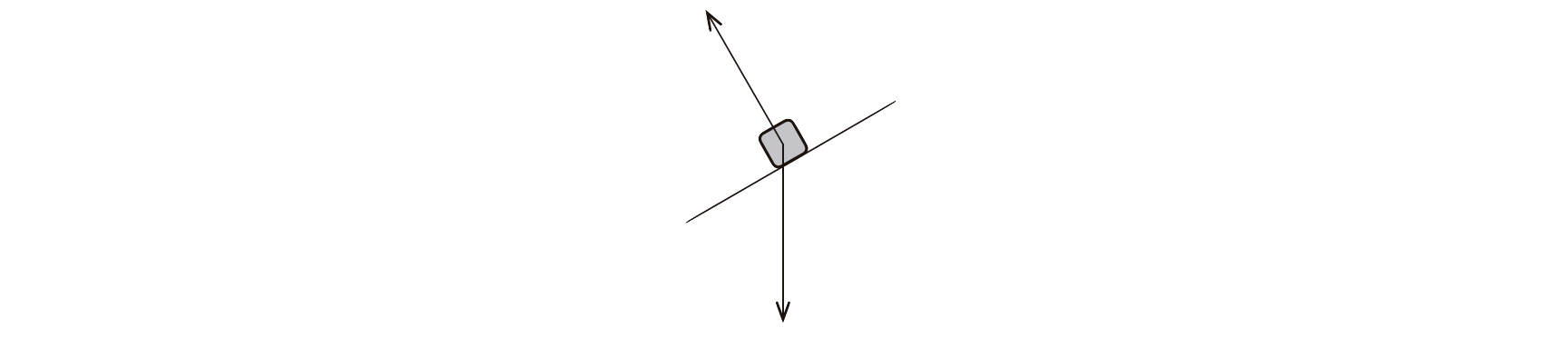 Notas:
Notas:
⇒ Na ausência de atrito, a resultante das forças que atuam sobre um corpo, considerado uma partícula, que se move ao longo de uma rampa com inclinação de 30°, sujeito apenas à força gravítica e à reação normal, é igual à componente da força gravítica na direção paralela à rampa.
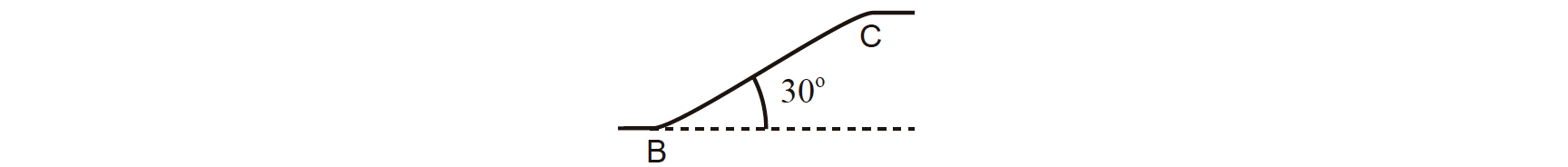
- Assim, 𝑚 𝑎 = 𝑚 𝑔 sin 30° ⇔ 𝑎 = 𝑔 sin30°
O que significa que o corpo se move com uma aceleração cujo módulo é, aproximadamente, 5,0 m s−2.
⇒ Por outro lado, a componente escalar da aceleração é numericamente igual ao declive da reta tangente ao gráfico 𝑣 =𝑓(𝑡) correspondente ao percurso entre as posições B e C (reta a vermelho).

- Esse declive é dado por: (4,5 − 2,0)/ (1,5 − 1,0) = −5,0
O que significa que o corpo se move com uma aceleração cujo módulo é, aproximadamente, 5,0 ms−2.
⇒ Conclui-se, assim, que a variação de velocidade entre B e C se deve apenas à ação da força gravítica.
⇒ Se a escala para representar as forças é a mesma, de acordo com a representação em B, temos a força de atrito praticamente igual à componente da força gravítica na direção paralela à rampa (conforme se pode constatar usando uma régua), o que conduziria a uma componente escalar da aceleração de aproximadamente −10,0 m s−2.

- Opção (A) ……………. 10 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
9.3. Considere:
⇒ ΔEc a variação de energia cinética do corpo;
⇒ ΔEpg a variação de energia potencial gravítica do sistema corpo + Terra;
⇒ ∑Wi a soma dos trabalhos realizados pelas forças que atuam no corpo;
⇒ WFg o trabalho realizado pela força gravítica que atua no corpo.
Pode afirmar-se que no percurso do corpo entre as posições A e C
(A) |ΔEc| < |ΔEpg| e |∑Wi| < |WFg|
(B) |ΔEc| < |ΔEpg| e |∑Wi| > |WFg|
(C) |ΔEc| > |ΔEpg| e |∑Wi| < |WFg|
(D) |ΔEc| > |ΔEpg| e |∑Wi| > |WFg|
- Opção (D)

⇒ No percurso de A até B, 𝑊𝐹⃗gA→B = 0 J;
- no percurso de B até C, 𝑊𝐹⃗gB→C = −(𝐸pgC − 𝐸pgB) < 0 J.
Logo, no percurso de A até C, 𝑊𝐹⃗gA→C = −(𝐸pgC − 𝐸pgB ), ou seja, 𝑊𝐹⃗gA→C = −Δ𝐸pg
⇒ No percurso de B até C, a diminuição de energia cinética é no mínimo igual ao aumento da energia potencial gravítica nesse percurso;
- no percurso de A até B, o módulo da velocidade diminui, pelo que há diminuição de energia cinética também nesse percurso.
Logo, no percurso de A até C, |Δ𝐸c| > |Δ𝐸pg|
⇒ Havendo diminuição da energia cinética no percurso de A até B, o trabalho realizado pela resultante das forças nesse percurso é negativo.
Como o trabalho realizado pela força gravítica no percurso de B até C também é negativo, conclui-se que |Σ𝑊|>|𝑊𝐹⃗g|.
- Opção (D) ……………. 10 pontos
10. Dois microfones idênticos, ligados a um osciloscópio, foram colocados à mesma distância de um altifalante.
A Figura 6 apresenta os sinais I e II, visualizados no ecrã do osciloscópio, quando a base de tempo foi regulada para 0,5 ms por divisão e o amplificador vertical foi regulado para 0,5 V por divisão (para os dois sinais).

- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
- 11ºano – Física – A.l. – 2.1 – Características do som
10.1. A frequência do sinal I é ______ e a amplitude desse sinal é ______ amplitude do sinal II.
(A) 3,0 x 102 Hz … igual
(B) 3,3 x 103 Hz … igual
(C) 3,0 x 102 Hz … inferior
(D) 3,3 x 103 Hz … inferior
- Opção (A)
⇒ A frequência do sinal I é 3,0×102 Hz e a amplitude desse sinal é igual à amplitude do sinal II.
Notas:
⇒ O intervalo de tempo referente ao sinal apresentado no ecrã do osciloscópio corresponde a um período e meio.
Como a base de tempo está regulada para 0,5 ms/DIV, pode concluir-se que
- 0,5 × 10−3 s/DIV × 10 DIV = 1,5 × 𝛵 ⇔ 𝛵 = 5 × 10−3 s/ 1,5
⇒ Sendo a frequência por definição o inverso do período, vem:
- 𝑓 = 1/𝛵 = 1,5 / 5 × 10−3 s ⇔ 𝑓 = 3,0 × 102 Hz
⇒ Observando a imagem do ecrã do osciloscópio, pode concluir- -se que a distância pico a pico do sinal I é aproximadamente igual à do sinal II, pelo que se pode afirmar que a amplitude do sinal I é igual à do sinal II, o que corresponde ao esperado, pois os dois microfones foram colocados à mesma distância de um altifalante.
- Opção (A) ……………. 10 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
- 11ºano – Física – A.l. – 2.1 – Características do som
10.2. O microfone que originava o sinal II foi afastado do altifalante de uma distância igual a um quarto do comprimento de onda da onda sonora produzida pelo altifalante.
Qual das opções seguintes apresenta os sinais que seriam observados no ecrã do osciloscópio, após o ajuste do sinal II ao ecrã do osciloscópio?

- Opção (C)
A SPF concluiu que nenhum dos gráficos está correto, porque o afastamento do microfone que originava o sinal II de um quarto de comprimento de onda implica que este deveria estar atrasado de um quarto de período relativamente ao sinal I, isto é, o pico do sinal II deveria aparecer à direita do pico do sinal I.
Estando o microfone que originava o sinal II mais longe, o sinal nele detetado num certo instante é um sinal emitido pelo altifalante antes do sinal que está nesse mesmo instante a ser detetado pelo outro microfone. É esta a razão para o desfasamento. Além disso, há atenuação do sinal II que está bem refletida na opção C.
- Opção (C) ……………. 10 pontos
FIM






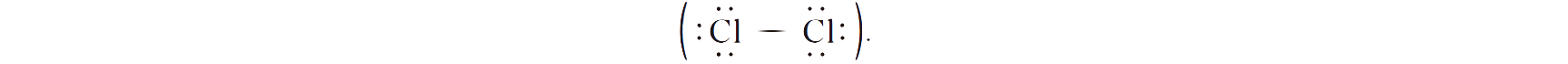
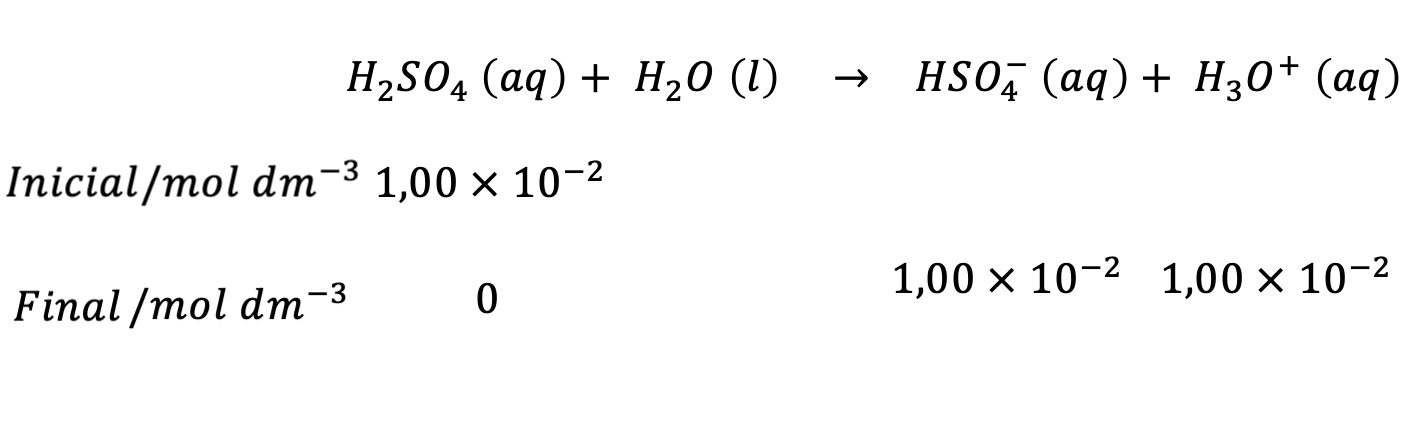
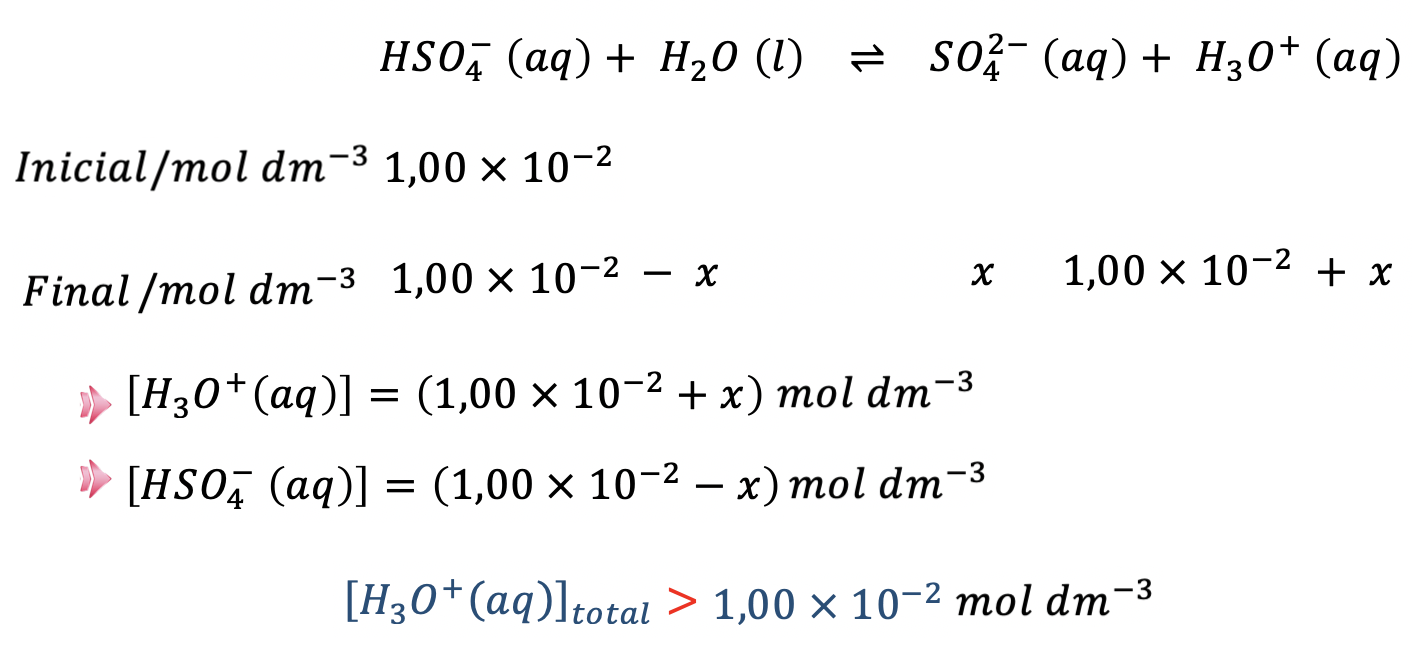

Foi uma agradavel surpresa – e de grande utilidade- ter encontrado este site.
Sou uma avó ( com 76 anos) a estudar pata ajudar o neto a ter notas para poder entrar na Faculdade …
Fico grata
Maria Augusta
Não foi muito fácil, exame 2024 é amanhã..