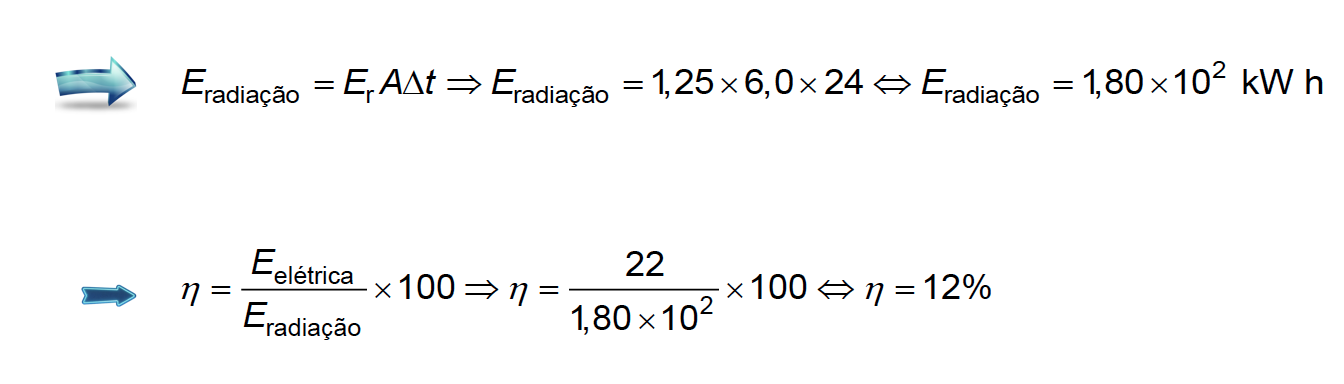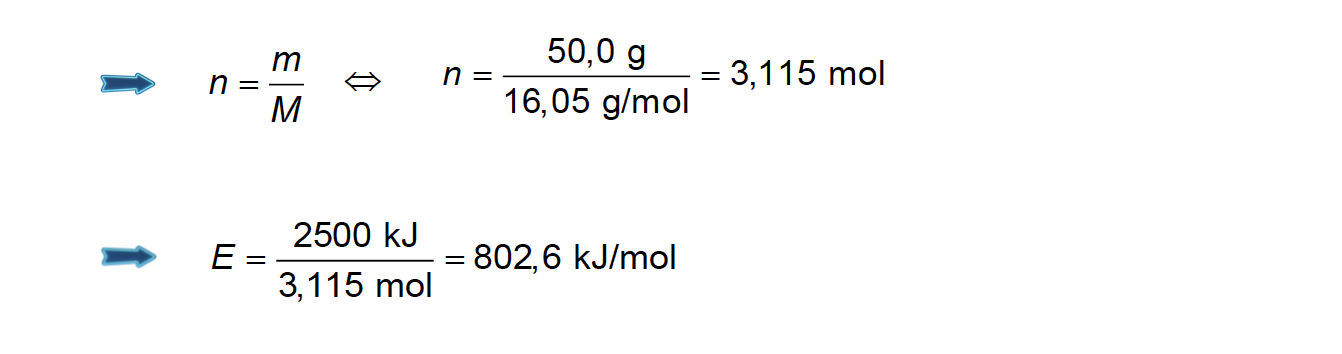2021 – Época Especial – Prova Escrita de FQ A
Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: Época especial – 2021
A prova inclui 16 itens, devidamente identificados no enunciado, cujas respostas contribuem obrigatoriamente para a classificação final.
Dos restantes 8 itens da prova, apenas contribuem para a classificação final os 4 itens cujas respostas obtenham melhor pontuação.
1. Os ácidos orgânicos apresentam um grupo funcional característico.
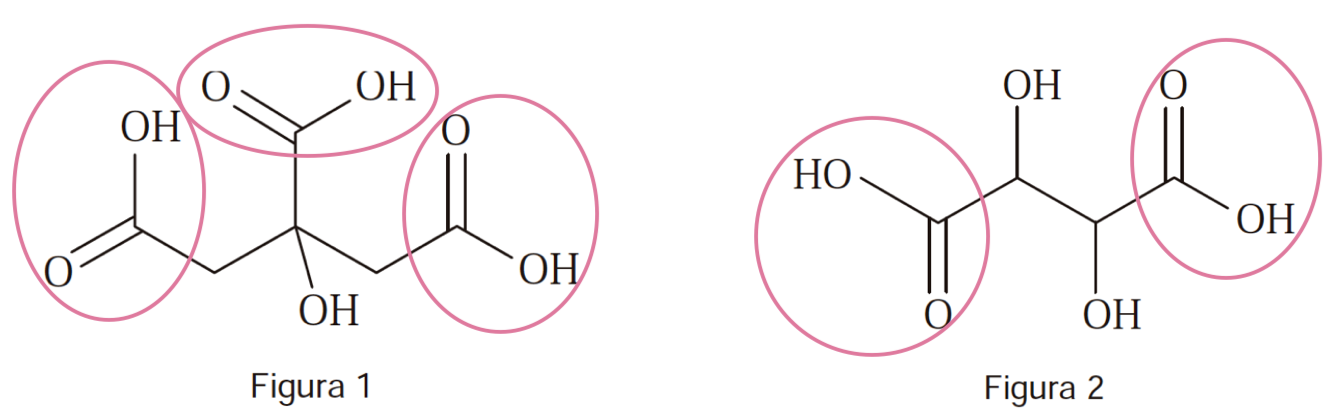
O ácido cítrico, C6H8O7 (M = 192,14 g mol-1), cuja fórmula de estrutura da molécula se representa na Figura 1, é uma substância presente nos citrinos.

- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
1.1. A molécula de ácido tartárico, C4H6O6 , presente no vinho, tem a fórmula de estrutura representada na Figura 2.
Nas moléculas de ácido cítrico e de ácido tartárico existem, respetivamente,
(A) dois e três grupos funcionais carboxilo.
(B) quatro e dois grupos funcionais hidroxilo.
(C) um e quatro grupos funcionais hidroxilo.
(D) três e dois grupos funcionais carboxilo.
- Opção (D) ……………. 10 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1.2. Um sumo de limão, de massa volúmica 1,03 g cm-3, contém 4,71%, em massa, de ácido cítrico.
Determine a quantidade de ácido cítrico que existe em 75,0 cm3 desse sumo.
Apresente todos os cálculos efetuados.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a massa de ácido cítrico no sumo (3,638 g) …….. 6 pontos
⇒ Calcula a quantidade de ácido cítrico no sumo (1,89 x 10-2 mol) …….. 4 pontos
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
1.3. A reação entre o ácido cítrico e o hidrogenocarbonato de sódio, NaHCO3 (aq ), pode ser traduzida por
C6H8O7 (aq ) + 3 NaHCO3 (aq ) → 3 H2O ( l ) + 3 CO2 ( g ) + Na3C6H5O7 (aq )
Considere que se adicionam 80 mL de NaHCO3 (aq), de concentração 0,50 mol dm-3, a 30 mL de C6H8O7 (aq ), com a mesma concentração, e se recolhem 3,6 x 10-2 mol de CO2 (g).
O rendimento da reação é
(A) 65%
(B) 90%
(C) 80%
(D) 30%
⇒ Calculo das quantidades dos reagentes nas soluções iniciais:
⇒ Os reagentes reagem nas proporções de 1 : 3, o reagente limitante é o hidrogenocarbonato de sódio.
⇒ De acordo com a proporção estequiométrica entre o reagente limitante (o hidrogenocarbonato de sódio) e o produto recolhido considerado (dióxido de carbono), que é 3 : 3 ou 1 : 1, obter-se-ia, no máximo, 0,040 mol deste gás, ou seja, se o rendimento da reação fosse 100%:
- Opção (B) ……………. 10 pontos
1.4. O ácido fosfórico, H3PO4 (aq ), é um ácido que, tal como o ácido cítrico, sofre em água ionizações sucessivas.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1.4.1. Considere uma solução aquosa de ácido fosfórico e uma solução aquosa de ácido cítrico com a mesma concentração, a uma dada temperatura, T.
A constante de acidez definida para a primeira ionização de H3PO4 (aq ) é cerca de dez vezes maior do que a constante de acidez definida para a primeira ionização de C6H8O7 (aq ), à temperatura T.
Conclua, fundamentando, em qual das soluções será maior a concentração de OH– (aq ), considerando apenas a contribuição da primeira ionização daqueles ácidos em água.
Escreva um texto estruturado, utilizando linguagem científica adequada.
⇒ Quanto maior for a constante de acidez, maior é a extensão da reação de ionização do ácido em água, mais forte é o ácido e, portanto, maior é a concentração de H3O+ (aq).
⇒ Como a constante de acidez definida para a primeira ionização é maior para o ácido fosfórico do que para o ácido cítrico e as concentrações das soluções aquosas são iguais, conclui-se que o grau de ionização do ácido fosfórico nessa solução será maior e, portanto, esta terá maior concentração de iões H3O+ .
⇒ Como a constante de autoprotólise da água é constante a uma dada temperatura, T, a uma maior concentração de iões corresponderá uma menor concentração de iões OH–.
- A solução de ácido cítrico terá maior concentração de iões OH–.
- Elementos de resposta:
⇒ reconhecimento de que a uma maior concentração de OH– (aq) corresponde uma menor concentração de H3O+(aq) [com base no facto de Kw ser constante];
⇒ reconhecimento de que a concentração de H3O+ (aq) é menor na solução de ácido cítrico, com base na relação entre as constantes de acidez definidas para a primeira ionização e a extensão dessa ionização;
⇒ conclusão de que a concentração de OH– (aq) é maior na solução de ácido cítrico.
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1.4.2. A primeira ionização do ácido fosfórico em água pode ser traduzida por
H3PO4 (aq ) + H2O (l) H2PO4– (aq) + H3O+ (aq )
Escreva as fórmulas químicas das duas espécies que resultam da segunda ionização do ácido fosfórico em água.
⇒ A segunda ionização do ácido fosfórico em água é traduzida por:
H2PO4– (aq ) + H2O (l) HPO42- (aq) + H3O+ (aq )
⇒ Formam-se, portanto, os iões com as fórmulas (HPO42- e H3O+)
- Apresenta as duas fórmulas químicas solicitadas (HPO42- e H3O+) ……………. 10 pontos
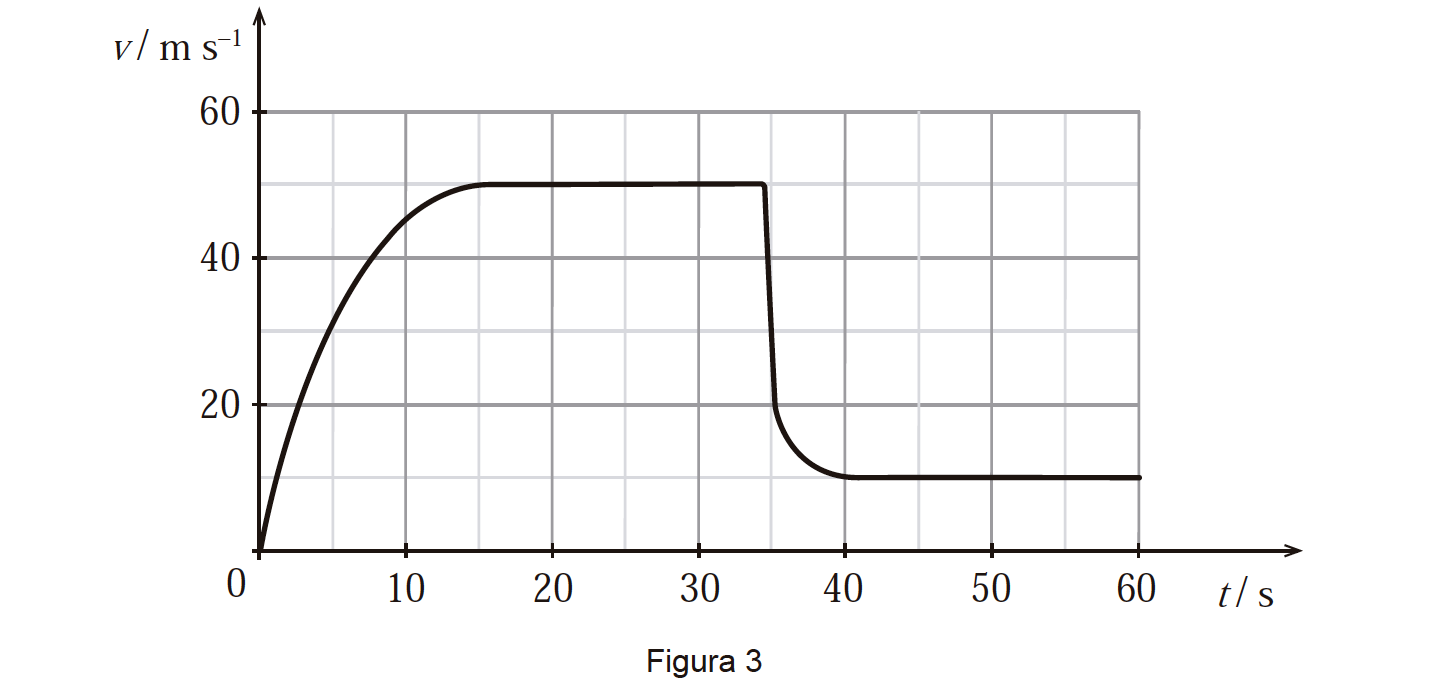
2. Na Figura 3, apresenta-se o gráfico da componente escalar da velocidade, v , de um paraquedista (sistema paraquedista + paraquedas), em função do tempo, t , nos primeiros 60 s do seu movimento de descida, na vertical.
Considere um referencial Oy vertical e admita que o paraquedista pode ser representado pelo seu centro de massa (modelo da partícula material).
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
2.1. Qual dos esboços de gráfico seguintes pode representar a componente escalar da posição, y , do paraquedista, em relação ao referencial Oy , em função do tempo, t , no intervalo de tempo [0; 30]s ?
- Opção (B)
⇒ Da análise do enunciado e do gráfico v = f (t) representado na Figura 3, verifica-se que o referencial Oy, vertical, está orientado no sentido descendente, logo a componente escalar da posição, y, aumenta ao longo do tempo.
⇒ A componente escalar da velocidade aumenta de 0 s até cerca de 15 s, movimento retilíneo acelerado, e mantém-se constante até 30 s, movimento retilíneo uniforme.
⇒ A curva y = f (t) apresenta a concavidade para cima (movimento retilíneo acelerado), seguida de um aumento retilíneo (movimento retilíneo uniforme).
- Opção (B) ……………. 10 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
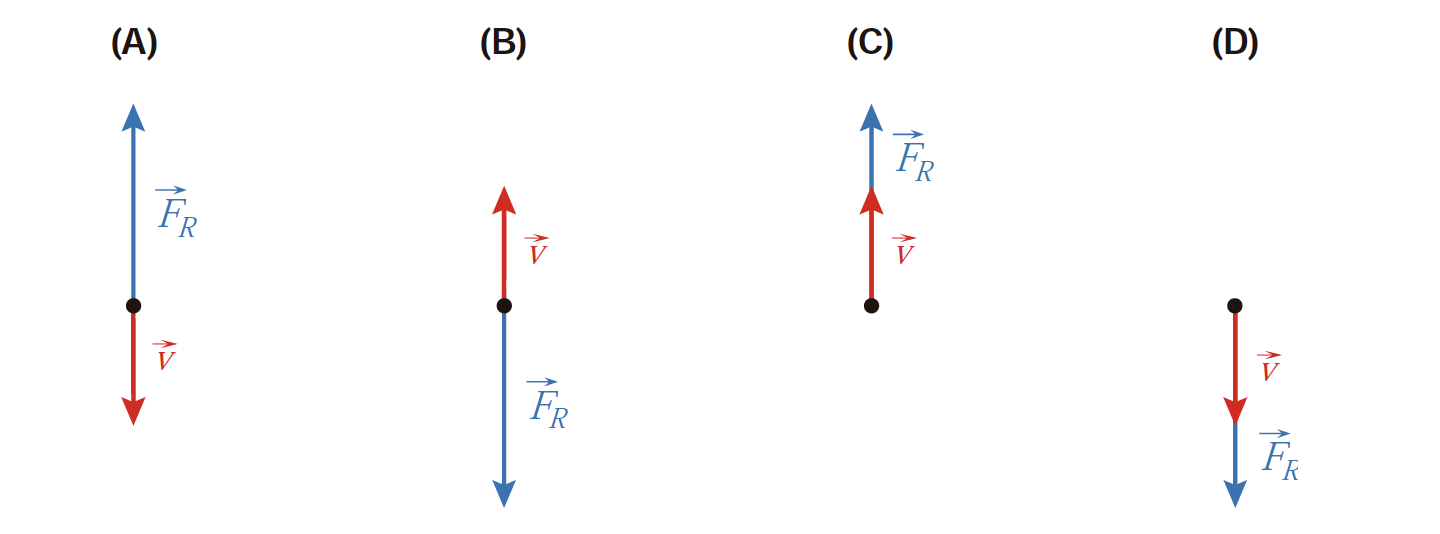
2.2. Qual das opções pode representar a velocidade, v , do paraquedista e a resultante das forças, FR , que nele atuam no instante t = 35 s ?
- Opção (A)
⇒ Durante todo o movimento, o sentido é o descendente, logo a velocidade tem este sentido.
⇒ A partir do instante 35 s e até ao instante 40 s, o movimento é retilíneo e retardado (a componente escalar da velocidade diminui – Figura 3 do enunciado), pelo que a resultante das forças, Fr, que atua sobre o sistema tem sentido ascendente.
- Opção (A) ……………. 10 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2.3. O módulo do trabalho, |WRar,1| , realizado pela resistência do ar no intervalo de tempo [ 20; 30] s é cinco vezes superior ao módulo do trabalho, |WRar,2| , realizado pela resistência do ar no intervalo de tempo [50; 60] s .
Comprove a veracidade desta afirmação.
Explicite o seu raciocínio.
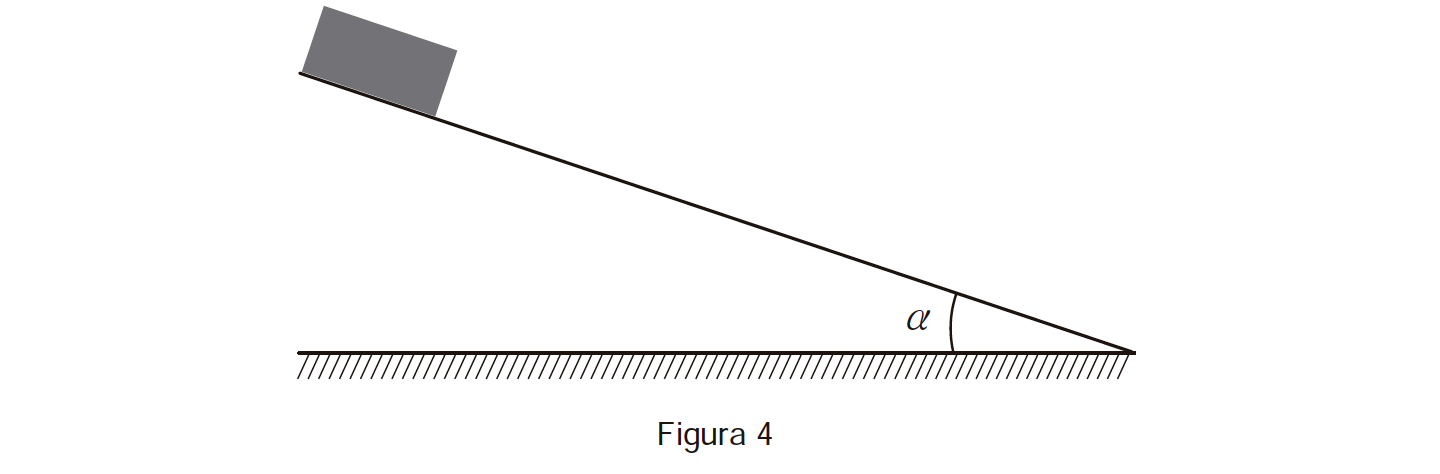
3. Um corpo foi abandonado sobre um plano com uma dada inclinação, α , de acordo com a Figura 4 (que não está à escala).
Admita que o corpo pode ser representado pelo seu centro de massa (modelo da partícula material).
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
- 10ºano – Física – A.l. – 1.1 – Movimento num plano inclinado
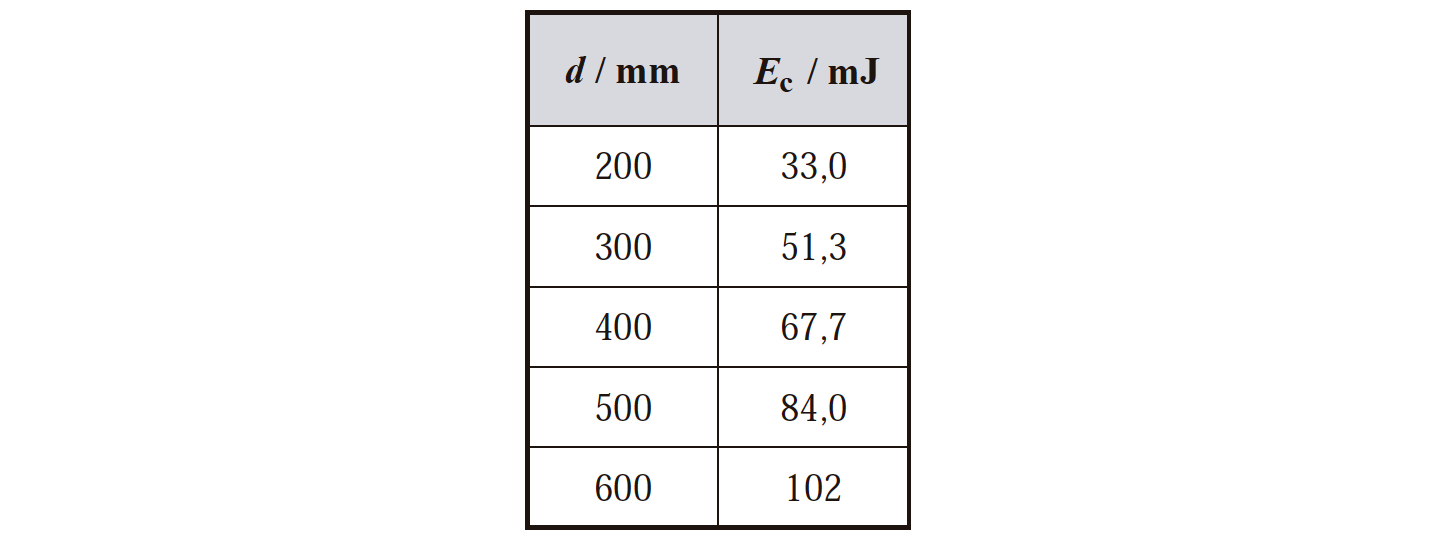
3.1. Numa série de ensaios, o corpo, de massa 189,2 g , foi abandonado de cinco posições diferentes.
Admita que a resultante das forças que nele atuam é constante.
Na tabela, estão registadas as distâncias, d, percorridas pelo corpo sobre o plano inclinado e as energias cinéticas, Ec , do corpo, ao percorrer aquelas distâncias.
Determine o módulo da aceleração do corpo.
Na resposta:
– deduza uma expressão que mostre uma relação linear de Ec em função de d;
– apresente a equação da reta de ajuste ao gráfico deEc em função de d;
– calcule o valor solicitado com três algarismos significativos, a partir da equação da reta de ajuste.
Apresente todos os cálculos efetuados.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Deduz uma expressão que relaciona Ec com d (Ec = Fr d) …….. 3 pontos
⇒ Obtém a equação da reta de ajuste ao gráfico Ec = f (d) ( Ec = 0,1707 d – 6,800 x 10-4 (SI)) (ver notas 1 e 2) …….. 3 pontos
⇒ Calcula o módulo da aceleração do corpo (0,904 m s-2) …….. 4 pontos
Notas:
1. Na equação da reta de ajuste, a omissão da ordenada na origem não implica qualquer desvalorização.
2. A ordem das etapas 1 e 2 é arbitrária.
- 11ºano – Física – Domínio 1 – subdomínio 2 (Interações e os seus efeitos)
3.2. Na ausência de forças dissipativas, a expressão que permite calcular a inclinação do plano é
- Opção (C) ……………. 10 pontos
- 11ºano – Física – Domínio 2 – subdomínio 1 (Sinais e ondas)
4. Considere uma onda transversal e sinusoidal que se propaga num lago onde se encontra uma boia de sinalização, B.
Na Figura 5 (que não está à escala), representa-se uma porção da superfície da água do lago, num dado instante, ti , e um referencial xOy.
Admita que a onda se propaga no sentido positivo do eixo Ox com velocidade constante.
Qual dos esboços de gráfico seguintes pode representar a componente escalar da posição da boia de sinalização, yB , segundo o eixo Oy, em função do tempo, t , considerando ti o instante inicial?
- Opção (A)
⇒ Da Figura, verifica-se que a boia no instante ti se encontra na posição de equilíbrio (y = 0).
⇒ No instante ti, a partícula que se encontra no eixo dos tem elongação máxima negativa, pelo que, no instante ti + T/4, passa na posição y = 0 ; assim, a porção da água do lago para este instante é a representada (a tracejado) na figura seguinte:
⇒ Nesta figura, verifica-se que a boia se encontra na elongação máxima negativa.
- Opção (A) ……………. 10 pontos
5. Muitos satélites movimentam-se em órbitas aproximadamente circulares e estão equipados com painéis fotovoltaicos que produzem a energia necessária ao seu funcionamento.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
5.1. Um satélite geoestacionário possui painéis fotovoltaicos cuja área total é 6,0 m2.
Considere que a irradiância solar média é 1,25 kW m-2 e que, ao fim de uma órbita, a energia elétrica produzida pelos painéis é 22 kW h.
O rendimento médio dos painéis fotovoltaicos será
(A) 49%
(B) 34%
(C) 24%
(D) 12%
- Opção (D) ……………. 10 pontos
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
5.2. Considere dois satélites, A e B, que se movem em torno da Terra.
Se o raio da órbita de A for quatro vezes maior do que o raio da órbita de B, a velocidade de A será
(A) quatro vezes maior do que a velocidade de B.
(B) quatro vezes menor do que a velocidade de B.
(C) duas vezes menor do que a velocidade de B.
(D) duas vezes maior do que a velocidade de B.
- Opção (C) ……………. 10 pontos
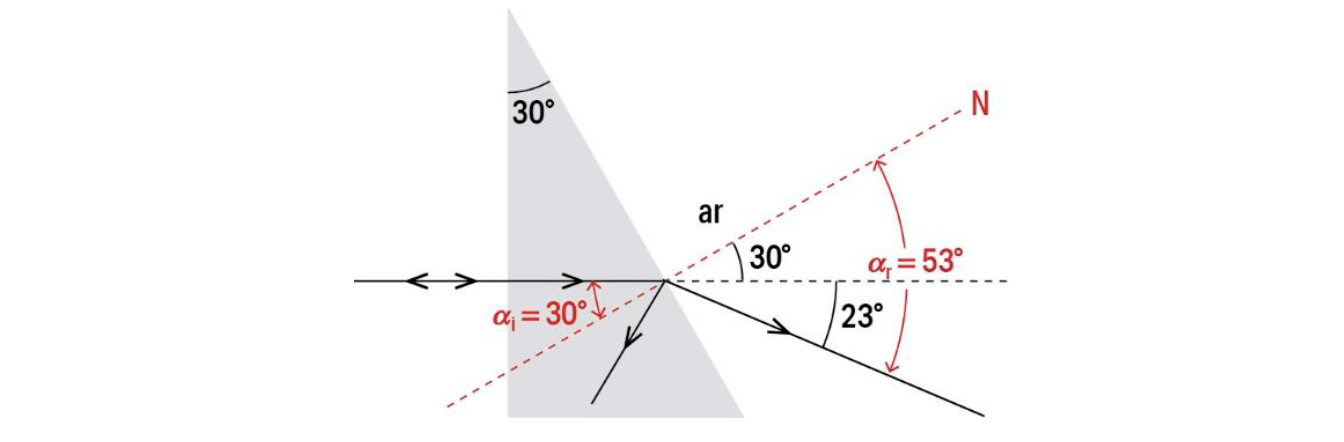
6. Na Figura 6 (que não está à escala), representa-se a secção transversal de um prisma de vidro e parte do trajeto de um feixe fino de luz laser, de frequência 4,74 x 1014 Hz, que, ao propagar-se no ar, incide numa das faces desse prisma.
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
6.1. A potência do feixe de luz incidente na superfície de separação ar-vidro é _____ à potência do feixe de luz refletida nessa superfície, e as velocidades desses feixes de luz são _____.
(A) superior … iguais
(B) igual … diferentes
(C) superior … diferentes
(D) igual … iguais
- Opção (A)
⇒ A potência da luz refletida na superfície de separação ar-vidro é inferior à da luz incidente, pois uma parte desta atravessa (é refratada) o vidro.
⇒ A velocidade de propagação só depende do meio de propagação.
⇒ Como o ar é o meio de propagação do feixe incidente e do refletido, esta mantém-se.
- Opção (A) ……………. 10 pontos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
6.2. Determine o comprimento de onda da luz laser no vidro.
Apresente todos os cálculos efetuados.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula o índice de refração do vidro constituinte do prisma (1,597) …….. 4 pontos
⇒ Calcula o módulo da velocidade de propagação da luz no vidro constituinte do prisma (1,878 x 108 m s-1) …….. 3 pontos
⇒ Calcula o comprimento de onda da luz no vidro (3,96 x 10-7 m) …….. 3 pontos
7. Na Figura 7, está esquematizado um circuito elétrico com os seguintes componentes:
• uma pilha, de força eletromotriz 9,0 V e resistência interna 1,5 Ω;
• três componentes puramente resistivos (R1, R2 e R3), com a mesma resistência elétrica;
• um amperímetro ideal;
• um interruptor.

- 10ºano – Física – subdomínio 2 (Energia e fenómenos elétricos)
7.1. Qual a diferença de potencial elétrico entre os pontos P e Q quando o interruptor está aberto?
⇒ Quando o interruptor está aberto, a diferença de potencial lida num voltímetro ligado aos pontos P e Q é igual à diferença de potencial entre os terminais da pilha, isto é, igual à sua força eletromotriz:
- UPilha = ε – ri I ⇔ UPilha = ε
⇒ Assim, a diferença de potencial referida é igual a 9,0 V.
- Apresenta o valor solicitado (9,0 V).
Nota ‒ A ausência de unidade não implica qualquer desvalorização.
- 10ºano – Física – subdomínio 2 (Energia e fenómenos elétricos)
7.2. Com o interruptor fechado, o amperímetro regista 0,25 A.
Determine a potência total dissipada nos três componentes puramente resistivos.
Apresente todos os cálculos efetuados.
⇒ O amperímetro está ligado a R3, regista 0,25 A.
⇒ R1 e R3 (iguais) estão ligadas em paralelo, então a corrente elétrica que atravessa R2 também é igual a 0,25 A.
⇒ R1 está ligada em série com R2 e R3, a corrente que a atravessa é igual a 0,50 A (0,25 A + 0,25 A), logo a corrente debitada pela pilha para o circuito é igual a 0,50 A.
⇒ A potência dissipada em R1, R2 e R3 é igual à potência debitada pela pilha ao circuito:
- UPilha = ε – ri I ⇔ UPilha = 9,0 – 1,5 x 0,50 = 8,25 V
- PPilha = UPilha I ⇔ PPilha = 8,25 x 0,5 = 4,1 W
⇒ A potência dissipada nos três componentes, R1, R2 e R3, é igual a 4,1 W.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a corrente elétrica fornecida pela pilha (0,50 A) …….. 3 pontos
⇒ Calcula a diferença de potencial elétrico nos terminais da pilha (8,25 V) …….. 4 pontos
⇒ Calcula a potência total dissipada nos três componentes puramente resistivos (4,1 W) …….. 3 pontos
- 10ºano – Química – Domínio 1 – subdomínio 3 (Tabela periódica)
8. Considere o átomo de carbono e o átomo de oxigénio no estado fundamental.
Compare a energia dos eletrões de valência mais energéticos do átomo de carbono com a energia dos eletrões de valência mais energéticos do átomo de oxigénio.
Explicite o seu raciocínio.
⇒ Num átomo, os eletrões de valência mais energéticos são os que ocupam o nível de energia mais elevado e que, portanto, precisam de receber menos energia para serem removidos do átomo.
⇒ Os elementos carbono (6C) e oxigénio (8O) estão localizados, na Tabela Periódica, no 2.º período e nos grupos 14 e 16, respetivamente.
⇒ As configurações eletrónicas destes átomos no estado fundamental são, respetivamente, 1s2 2s2 2p2 e 1s2 2s2 2p4.
⇒ Os eletrões de valência mais energéticos do átomo de carbono e do átomo de oxigénio são os do subnível 2p.
⇒ Embora o número de eletrões no átomo de carbono (6) seja inferior ao número de eletrões no átomo de oxigénio (8), o número de níveis de energia é o mesmo (2), pelo que a blindagem nuclear (repulsão por eletrões internos) é aproximadamente a mesma.
⇒ A carga nuclear do átomo de oxigénio (+8) é, porém, superior à carga nuclear do átomo de carbono (+6), o que provoca, para o oxigénio, uma maior atração entre o núcleo e os eletrões de valência mais energéticos.
- A energia de ionização do oxigénio é maior do que a energia de ionização do carbono.
⇒ Prevê-se que, no átomo de carbono, os eletrões de valência mais energéticos sejam, em média, menos atraídos pelo respetivo núcleo e, consequentemente, tenham maior energia potencial do que os eletrões de valência mais energéticos do oxigénio, que estão mais fortemente atraídos para o núcleo.
- A energia dos eletrões de valência mais energéticos do átomo de carbono, no estado fundamental, é maior do que a energia dos eletrões de valência mais energéticos do átomo de oxigénio, no estado fundamental.
- Elementos de resposta:
⇒ reconhecimento de que os eletrões de valência mais energéticos têm uma menor energia de ionização;
⇒ reconhecimento de que a energia de ionização do oxigénio é maior do que a energia de ionização do carbono, com base no aumento predominante da carga nuclear ao longo de um mesmo período ou na tendência de aumento da energia de ionização ao longo de um mesmo período;
⇒ reconhecimento de que a energia dos eletrões de valência mais energéticos do átomo de oxigénio é menor do que a energia dos eletrões de valência mais energéticos do átomo de carbono.
9. O metano é um composto constituído por átomos de hidrogénio e de carbono.
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
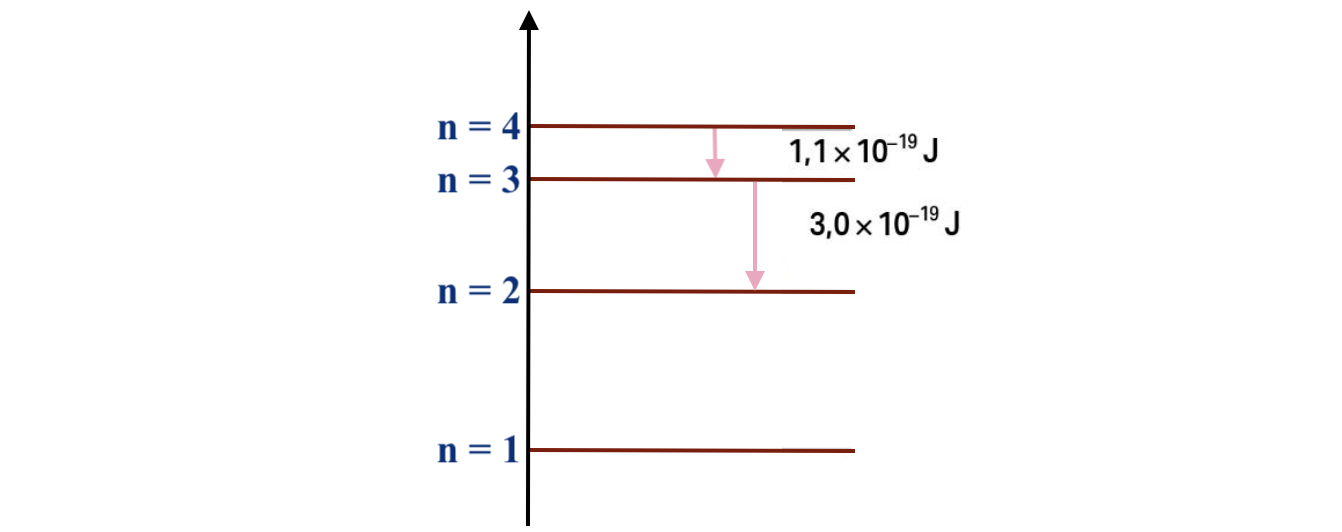
9.1. No espectro de emissão do átomo de hidrogénio, as energias dos fotões correspondentes às transições de menor energia para os níveis n = 2 e n = 3 são 3,0 x 10-19 J e 1,1 x 10-19 J , respetivamente.
Assim, pode concluir-se que a diferença de energia entre os níveis
(A) n = 3 e n = 2 é 1,9 x 10-19 J
(B) n = 4 e n = 3 é 1,9 x 10-19 J
(C) n = 4 e n = 2 é 4,1 x 10-19 J
(D) n = 3 e n = 1 é 4,1 x 10-19 J
- Opção (C)
⇒ A diferença de energia entre os níveis n = 4 e n = 2 é igual à soma das diferenças de energia entre os níveis n = 4 e n = 3 e entre os níveis n = 3 e n = 2, ou seja , (4,1 x 10-19 J).
⇒ A energia dos fotões correspondentes à transição de menor energia para o nível n = 2 é igual à diferença de energia entre os níveis e n = 3 e n = 2 (3,0 x 10-19 J).
⇒ A energia dos fotões correspondentes à transição de menor energia para o nível n = 3 é igual à diferença de energia entre os níveis n =4 e n = 3 (1,1 x 10-19 J).
- Não há dados para concluir sobre a energia de transição entre os níveis n = 3 e n = 1, mas será bem maior do que 4,1 x 10-19 J, pois a diferença de energia entre os níveis n = 2 e n = 1 será maior do que 3,0 x 10-19 J.
- Opção (C) ……………. 10 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
9.2. A combustão do metano pode ser traduzida por
CH4 (g) + 2 O2 (g) → CO2 ( g ) + 2 H2O (g)
A energia libertada na combustão de 50,0 g de CH4 é 2500 kJ.
Considere as energias de ligação médias apresentadas na tabela.
Determine, em kJ mol-1, a energia média de dissociação da molécula de O2 .
Apresente todos os cálculos efetuados.
⇒ Calculo da variação de entalpia associada à reação de combustão do metano:
⇒ A energia libertada ou absorvida numa reação química resulta de um balanço entre a energia absorvida na rutura das ligações entre os átomos dos reagentes e a energia libertada na formação das novas ligações. Por convenção, a energia absorvida pelo sistema é positiva e a energia libertada é negativa.
⇒ Para determinar a energia de dissociação da molécula de O2, pode recorrer-se a este balanço energético:
- A energia de dissociação é numericamente igual à energia de ligação, Ediss (O = O) = 490 kJ/mol, ou seja, a energia necessária para dissociar de é 1 mol de O2 é 490 kJ.
- Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a energia que se liberta na combustão de 1 mol de CH4 (802,6 kJ) …….. 4 pontos
⇒ Calcula a energia envolvida na formação das ligações de 1 mol de CO2 e de 2 mol de H2O (3438 kJ)…….. 3 pontos
⇒ Calcula a energia necessária para dissociar 1 mol de O2 (490 kJ) …….. 3 pontos
10. Em 1811, Amedeo Avogadro publicou um artigo em que admitia que volumes iguais de gases diferentes, nas mesmas condições de pressão e de temperatura, continham o mesmo número de moléculas.
Na Figura 8, representam-se quatro recipientes iguais (com o mesmo volume e a mesma massa).
Posteriormente, encheram-se estes recipientes com gases, identificados pelas respetivas fórmulas químicas, nas mesmas condições de pressão e de temperatura.
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
10.1. O número total de átomos contidos nos recipientes é igual em
(A) 1 e 2.
(B) 2 e 4.
(C) 2 e 3.
(D) 3 e 4.
- Opção (A)
⇒ De acordo com a Lei de Avogadro, se os quatro recipientes têm o mesmo volume (capacidade), nas mesmas condições de pressão e de temperatura, conterão igual número de moléculas dos gases com que foram enchidos, N.
Recipiente 4 : → Número de átomos de He (gás monoatómico) será N.
Recipiente 3 : → Número de átomos de CO2 (gás triatómico) será 3N.
Recipiente 2 : → Número de átomos de O2 (gás diatómico) será 2N.
Recipiente 1: → Número de átomos de N2 e O2 (gases diatómico) será 2N.
- Opção (A) ……………. 10 pontos
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
10.2. Selecione a opção que ordena os recipientes 1, 2 e 3, tendo em conta os respetivos gases, por ordem crescente das suas massas.
(A) 2 < 3 < 1
(B) 1 < 2 < 3
(C) 1 < 3 < 2
(D) 2 < 1 < 3
- Opção (B)
⇒ Se os quatro recipientes têm o mesmo volume (capacidade), nas mesmas condições de pressão e de temperatura, conterão quantidades iguais dos gases com que foram enchidos, n.
⇒ A massa de gás contido em cada um dos recipientes será:
- n = m/M
Recipiente 4 : (He) m4 = n x 4,00 = n x 4,0 g
Recipiente 3 : (CO2) m3 = n x 44,01 = n x 44,01 g
Recipiente 2 : (O2) m2 = n x 32,00 = n x 32,00 g
Recipiente 1: (N2 e O2) n x 28,02 < m1 < n x 32,00
⇒ Assim, m1 < m2 < m3
- Opção (B) ……………. 10 pontos
11. Os metais podem sofrer corrosão.
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
11.1. Em canalizações que contenham chumbo pode, a partir de PbCl2 , formar-se um óxido de chumbo de fórmula química PbO2 .
Nesta transformação, a variação do número de oxidação do chumbo é
(A) -2
(B) -1
(C) +1
(D) +2
- Opção (D)
⇒ n.o. (Pb) em PbCl2 :
- x + 2 x (-1) = 0 ⇔ x = + 2
⇒ n.o. (Pb) em PbO2 :
- x + 2 x (-2) = 0 ⇔ x = + 4
⇒ Numa reação em que a espécie PbCl2 origina a espécie PbO2, o número de oxidação do elemento Pb aumenta.
⇒ Variação do seu número de oxidação:
- Δn.o. (Pb) = +4 – (+2) = +2
- Opção (D) ……………. 10 pontos
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
11.2. Uma placa de cobre, Cu (s), e uma placa de zinco, Zn (s), foram mergulhadas numa solução contendo iões Pb2+ (aq), tendo-se verificado que, passado algum tempo, apenas a placa de zinco tinha sofrido corrosão.
Pode concluir-se que
(A) o poder redutor do Pb (s) é inferior ao do Cu (s).
(B) o poder redutor do Zn (s) é inferior ao do Pb (s).
(C) o poder oxidante do Zn2+ (aq) é inferior ao do Cu2+ (aq).
(D) o poder oxidante do Pb2+ (aq) é inferior ao do Zn2+ (aq).
- Opção (C)
⇒ Se, quando se mergulha uma placa de zinco, Zn (s), numa solução contendo iões Pb2- (aq), a placa de zinco sofre corrosão.
- Zn (s) + Pb2+ (aq) → Zn2+ (aq) + Pb (s). (I)
⇒ Reação é espontânea no sentido direto; o zinco tem mais tendência para se oxidar do que o chumbo, ou seja, o poder redutor do Zn (s) é superior ao do Pb (s).
⇒ O poder oxidante do Pb2+ (aq) é superior ao do Zn2+ (aq).
⇒ Quando se mergulha uma placa de cobre, Cu (s), numa solução contendo iões Pb2+ (aq), verifica-se que não ocorre qualquer reação.
⇒ A reação espontânea ocorreria em sentido inverso:
- Pb (s) + Cu2+ (aq) → Pb2+ (aq) + Cu (s) (II)
⇒ O poder redutor do Cu (s) é inferior ao do Pb (s), o poder oxidante do Pb2+ (aq) é inferior ao do Cu2+ (aq).
⇒ Como, de acordo com a reação (I), se viu que o poder oxidante do PB2+ (aq) é superior ao do Zn2+ (aq) , conclui-se que o poder oxidante do Zn2+ (aq) é inferior ao do Pb2+ (aq), que, por sua vez, é inferior ao do Cu2+ (aq).
- Opção (C) ……………. 10 pontos
FIM








 H2PO4– (aq) + H3O+ (aq )
H2PO4– (aq) + H3O+ (aq )