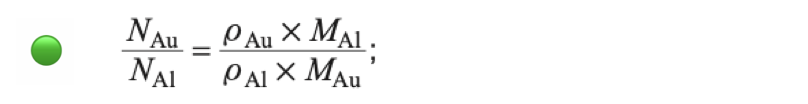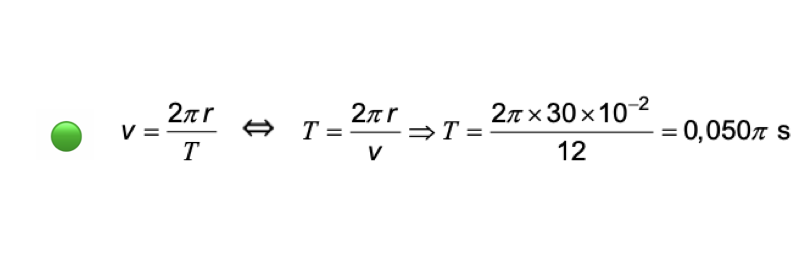Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: 2.ª Fase – 2025
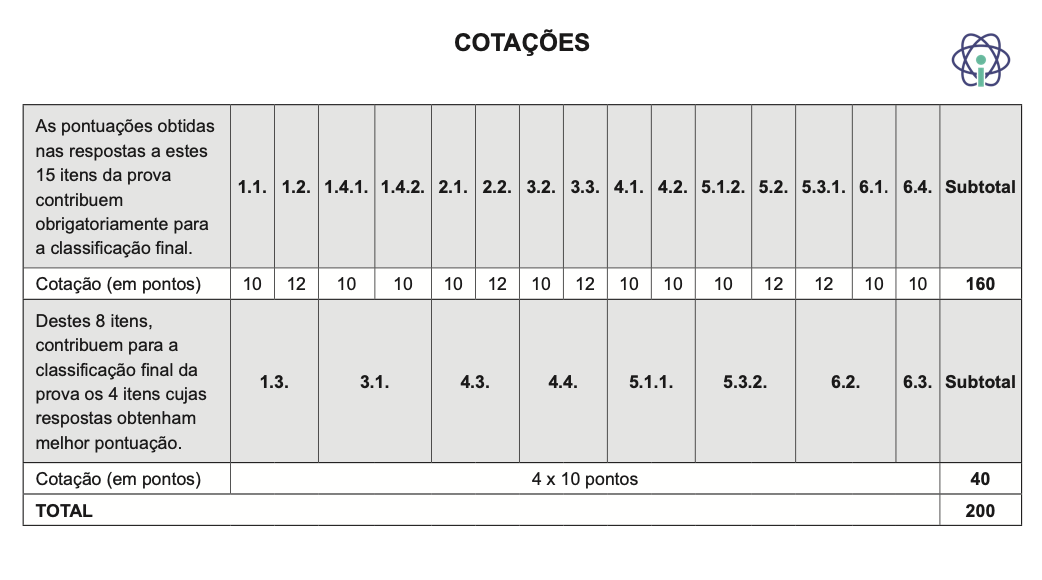
A prova inclui 15 itens, devidamente identificados no enunciado, cujas respostas contribuem obrigatoriamente para a classificação final.
Dos restantes 8 itens da prova, apenas contribuem para a classificação final os 4 itens cujas respostas obtenham melhor pontuação.
1. Os telescópios espaciais, que orbitam a Terra ou o Sol, permitem observar o espaço longínquo em diferentes comprimentos de onda.
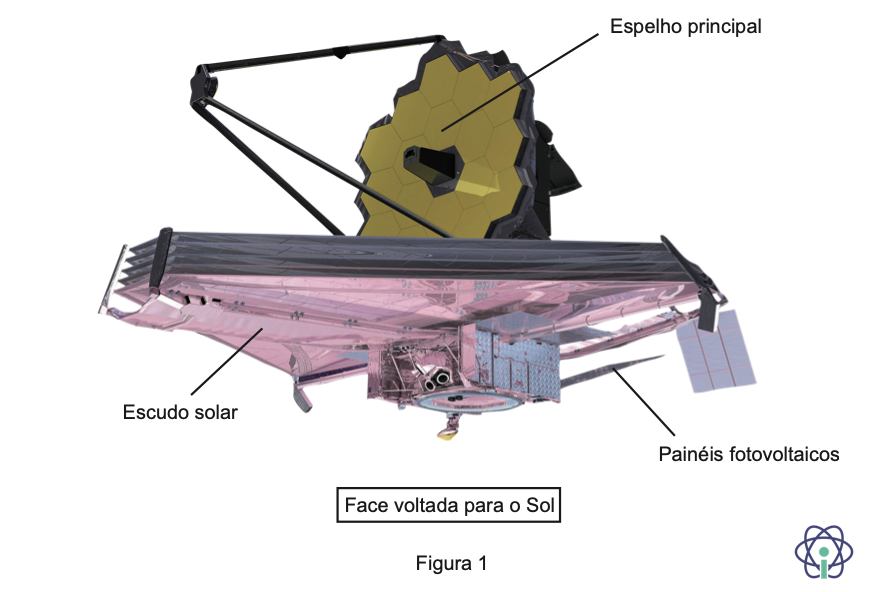
Na Figura 1, está representado o Telescópio Espacial James Webb (cuja sigla corrente, JWST, designa o seu nome original, em inglês, James Webb Space Telescope), podendo observar-se o espelho principal, o escudo solar e os painéis fotovoltaicos.
1.1. O JWST opera, essencialmente, na região do infravermelho, ao contrário do Telescópio Espacial Hubble, que opera na região do visível.
Comparativamente às radiações detetadas pelo Hubble, o JWST pode detetar radiações de
(A) menor comprimento de onda e maior energia por fotão.
(B) menor comprimento de onda e menor energia por fotão.
(C) maior comprimento de onda e maior energia por fotão.
(D) maior comprimento de onda e menor energia por fotão.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (D)
🛑 A energia e, portanto, a frequência da radiação visível é superior à energia da radiação infravermelha (IV).
🛑 Sendo a velocidade da radiação eletromagnética no vazio uma constante, o comprimento de onda das radiações (𝜆)é inversamente proporcional à sua frequência, ou seja, as radiações visíveis têm 𝜆 inferiores aos das radiações IV.
🛑 Uma vez que o telescópio JWST opera, essencialmente, na região do IV, ele detetará radiações de maior comprimento de onda, mas menor energia por fotão que o telescópio espacial Hubble, que opera na região do visível.
❇️ Maior comprimento de onda e menor energia por fotão.
- Opção (D) ……………. 10 pontos
1.2. O escudo solar do JWST impede que a luz proveniente do Sol, da Terra e da Lua atinja alguns dos seus equipamentos, permitindo que estes se mantenham à temperatura adequada ao seu funcionamento.
Complete o texto seguinte, selecionando a opção correta para cada espaço.
Escreva, na folha de respostas, cada uma das letras seguida do número que corresponde à opção selecionada.
A função do escudo solar do JWST é ___(a)___ a energia que é transferida do Sol, da Terra e da Lua por ___(b)___ . Este telescópio já conseguiu identificar várias substâncias no Universo, entre as quais hidrocarbonetos saturados, como, por exemplo, ___(c)___ , e substâncias constituídas por moléculas apolares, como, por exemplo, ___(d)___ .
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
⇒ (a) – (2)
⇒ (b) – (1)
⇒ (c) – (3)
⇒ (d) – (1)
🛑 Se a função do escudo solar é impedir que a luz proveniente do Sol, Terra e Lua atinjam alguns dos equipamentos do JWST, o escudo deverá refletir a energia que lhe é transferida por estes astros por radiação.
🛑 Dos hidrocarbonetos indicados, o único que é saturado (ligações C − C simples) é o C2H6.
🛑 Das substâncias identificadas pelo telescópio, a única molécula apolar é o CH4.
1.3. Os painéis fotovoltaicos do JWST produzem energia elétrica.
A potência gerada por estes painéis aumenta com _______ do ângulo entre os raios solares incidentes e a normal ao plano do painel fotovoltaico e é calculada pela expressão _______, em que U representa a diferença de potencial elétrico aos terminais do painel e I representa a corrente elétrica que o atravessa.
(A) a diminuição … U x I 2
(B) a diminuição … U x I
(C) o aumento … U x I 2
(D) o aumento … U x I
- Opção (B) ……………. 10 pontos
1.4. Enquanto nos espelhos comuns, na Terra, se utiliza, como superfície refletora, o alumínio, Al, o espelho principal do JWST é revestido por uma camada de ouro, Au.
1.4.1. Compare o número de átomos de ouro com o número de átomos de alumínio necessários para revestir espelhos de área igual com uma camada metálica de espessura igual.
Considere as massas volúmicas do ouro e do alumínio, respetivamente, ρAu = 19,3 g cm-3 e ρAl = 2,7 g cm-3.
Na sua resposta, estabeleça a razão entre o número de átomos de ouro e o número de átomos de alumínio, arredondada às unidades.
Mostre como chegou ao resultado solicitado.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 Informações fornecidas:
⇒ M(Au) = 196,97 g mol-1
⇒ ρ(Au) = 19,3 g cm-3
⇒ M(Al) = 26,98 g mol-1
⇒ ρ(Al) = 2,7 g cm-3
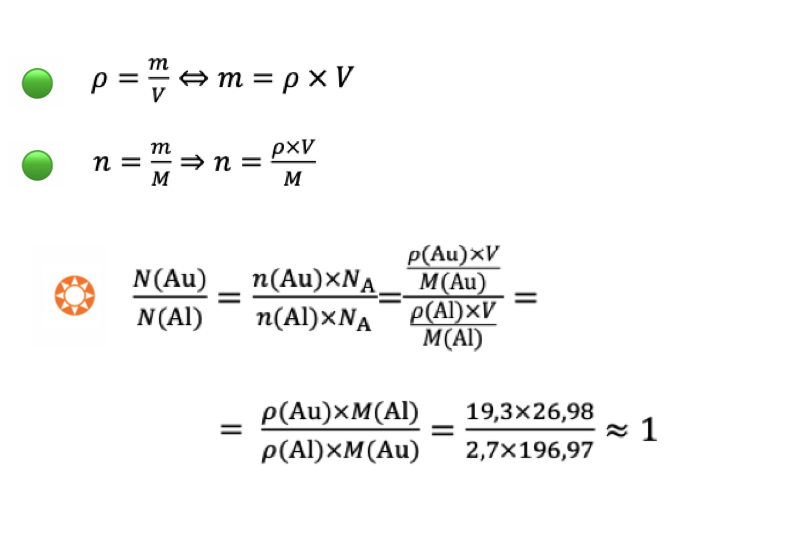
🛑 Se os espelhos têm igual área e igual espessura da camada metálica, os átomos que fazem o seu revestimento distribuem-se, necessariamente, pelo mesmo volume (VAu = VAl = V) :
❇️ N(Au) = N(Al)
1.4.2. Na Terra, a superfície refletora de alumínio dos espelhos é protegida por um vidro que impede o contacto do metal com o ar, evitando a sua deterioração.
A reação do alumínio com o dioxigénio do ar pode ser traduzida pela equação
4 Al (s) + 3 O2 (g) → 2 Al2O3 (s)
Nesta reação, o alumínio é o
(A) redutor, e o seu número de oxidação aumenta.
(B) redutor, e o seu número de oxidação diminui.
(C) oxidante, e o seu número de oxidação aumenta.
(D) oxidante, e o seu número de oxidação diminui.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (A)
🛑 Na equação química apresentada o número de oxidação (n.o.) do alumínio passa de 0, em Al(s), para +3, em Al2O3 (s), ou seja ∆n.o. = +3 − 0 = +3.
🛑 O alumínio sofre uma oxidação, por perda de eletrões e, consequente, com o aumento do seu n.o.
❇️ O alumínio é, pois, um redutor (ou agente redutor).
- Opção (A) ……………. 10 pontos
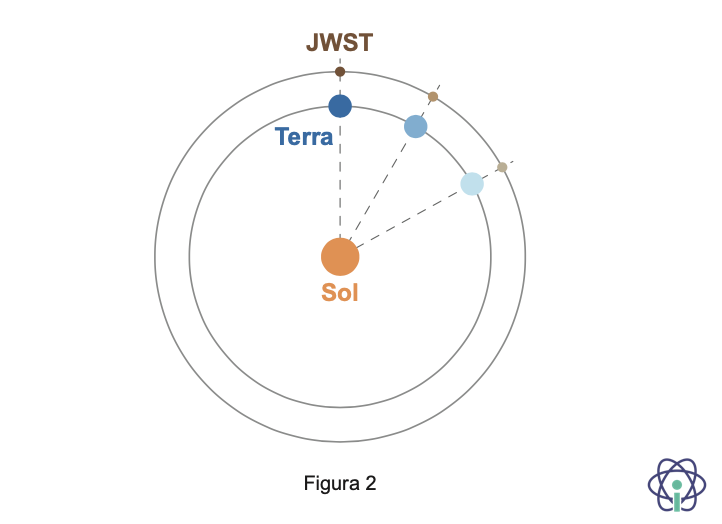
2. Na Figura 2, que não está à escala, está representado o movimento do Telescópio Espacial James Webb (JWST) em torno do Sol, numa região exterior à órbita da Terra.
A localização nesta região particular permite que o telescópio acompanhe a Terra no seu movimento de translação.
Considere que a Terra e o JWST realizam órbitas circulares em torno do Sol e que podem ser representados pelo seu centro de massa (modelo da partícula material).
2.1. Qual dos diagramas seguintes, que não se encontram à escala, pode representar a resultante das forças, FR, que atuam na Terra e a aceleração, a , da Terra durante o seu movimento em torno do Sol?
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (A)
🛑 O JWST executa o seu movimento de translação segundo uma trajetória circular e com módulo da velocidade constante (movimento circular e uniforme) pelo que, a resultante das forças sobre ele aplicadas é perpendicular à velocidade em cada ponto.
🛑 Tal fará com que a direção da força resultante assuma, em cada ponto, a direção radial e o sentido centrípeto (aponta para o centro da trajetória).
❇️ Pela Lei Fundamental da Dinâmica, e dado que a massa é sempre um escalar positivo, a direção e o sentido da aceleração são sempre iguais à direção e ao sentido da resultante das forças que lhe deu origem.
- Opção (A) ……………. 10 pontos
2.2. Determine o período de translação do JWST, em dias, tendo em conta o efeito da ação conjunta das forças gravíticas exercidas pelo Sol e pela Terra no telescópio.
Considere que:
– a massa do JWST é 6200 kg;
– a massa da Terra é 5,97 x 1024 kg;
– o módulo da força gravítica que o Sol exerce no JWST é 36,03 N; – a distância entre o Sol e a Terra é 1,496 x 1011 m;
– a distância entre o JWST e a Terra é 1,50 x 109 m.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 O telescópio JWST encontra-se sob a ação da força gravítica exercida pelo Sol (36,03 N) e da força gravítica exercida pela Terra, cuja magnitude poderá ser calculada pela Lei da Gravitação Universal:
🛑 Dado que a força gravítica exercida pelo Sol e a força gravítica exercida pela Terra no telescópio JWST têm, a cada instante, a mesma direção e sentido, produzirão uma força resultante 𝐹 de magnitude 36,03 N + 1,097 N = 37,13 N
Aplicando-se a Lei fundamental da Dinâmica e dado que se trata de um movimento circular e uniforme:
❇️ Se o período orbital da Terra em torno do Sol é de 365 dias, igual valor terá o período de translação do JWST.
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a intensidade da força de atração gravitacional entre a Terra e o JWST (1,097 N) ………. 4 pontos
⇒ Calcula a intensidade da resultante das forças de atração gravitacional aplicadas no JWST (37,13 N) ………. 3 pontos
⇒ Calcula o período de translação do JWST (365 dias) ………. 5 pontos
3. Suponha que um automóvel com motor de combustão se encontra estacionado e que, num dado momento, o seu sistema de ignição é acionado.
3.1. O sistema de ignição do motor do automóvel possui uma bobina, ligada ao eixo do motor, com 20 000 espiras, cada uma de área 1,25 x 10-3 m2.
Quando o sistema é acionado, produz-se uma variação do módulo do campo magnético de 1,0 T durante um milissegundo. Considere que a direção do campo magnético se mantém perpendicular ao plano das espiras.
O módulo da força eletromotriz induzida nos terminais da bobina, quando o sistema de ignição é acionado, é
(A) 2,5 x 104 V e aumentaria se o número de espiras diminuísse.
(B) 2,5 x 104 V e aumentaria se o número de espiras aumentasse.
(C) 2,5 x 101 V e aumentaria se o número de espiras diminuísse.
(D) 2,5 x 101 V e aumentaria se o número de espiras aumentasse.
- Opção (B)
🛑 Cálculo do módulo da variação do fluxo magnético (|Δ𝛷|) total da bobina
🔶 |Δ𝛷| = N x |ΔB| x Aespira x cos 0º ⇔ |Δ𝛷| = 20 000 x 1,0 x 1,120 x 10-2 x 1 ⇔ |Δ𝛷| = 25 Wb
🛑 Cálculo do módulo da força eletromotriz induzida, 𝜀i:
🔶 |εi| = |ΔΦ| / Δt ⇔ |εi| = 25 / 1 x 10-3 ⇔ |εi| = 2,5 x 104 V
❇️ Se o número de espiras, N, aumentar, o módulo da força eletromotriz induzida também aumentará, pois o módulo da força eletromotriz induzida é diretamente proporcional ao módulo da variação do fluxo magnético na bobina que, por sua vez, é diretamente proporcional ao número de espiras.
- Opção (B) ……………. 10 pontos
3.2. Os elementos principais da bateria de chumbo-ácido, usada no automóvel, são placas de chumbo imersas em ácido sulfúrico.
Na Figura 3, estão representados dois voltímetros e a bateria do automóvel que inclui uma associação de seis células idênticas ligadas em série.
Quando a bateria está desligada, a diferença de potencial elétrico aos seus terminais é 12,00 V, sendo 2,00 V aos terminais de cada célula. Quando o automóvel está em funcionamento, a corrente elétrica gerada pela bateria é 40,0 A, e a diferença de potencial elétrico aos seus terminais é 9,00 V.
Qual é a resistência interna da célula 1?
(A) 7,50 x 10-2 Ω
(B) 6,00 x 10-2 Ω
(C) 3,75 x 10-2 Ω
(D) 1,25 x 10-2 Ω
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (D)
🛑 A diferença de potencial total da associação das seis células em série é de 9,00 V, podemos obter a diferença de potencial elétrico para uma única célula:
❇️ UTotal = 6 x Ucélula ⇔ Ucélula = 9,00 / 6 = 1,50 V
❇️ 𝑈 = 𝜀 − 𝑟 × 𝐼 ⇒ 1,50 = 2,00 − 𝑟 × 40 ⇔ 𝑟 = 0,0125 Ω
🛑 O valor da resistência interna (𝑟 = 0,0125 Ω) da célula 1 (ou qualquer outra destas células).
- Opção (D) ……………. 10 pontos
3.3. No sistema de refrigeração dos motores de combustão, são, geralmente, usados líquidos de elevada capacidade térmica mássica.
Um professor desafiou os alunos a identificarem, de entre dois líquidos desconhecidos, qual seria o mais adequado para um sistema de refrigeração. Deveriam realizar apenas um ensaio para cada líquido e retirar uma conclusão sem recorrer a cálculos. Disponibilizou amostras de cada um dos líquidos, com massas iguais e à mesma temperatura, uma resistência de imersão, de potência P desconhecida e constante, um cronómetro e um termómetro.
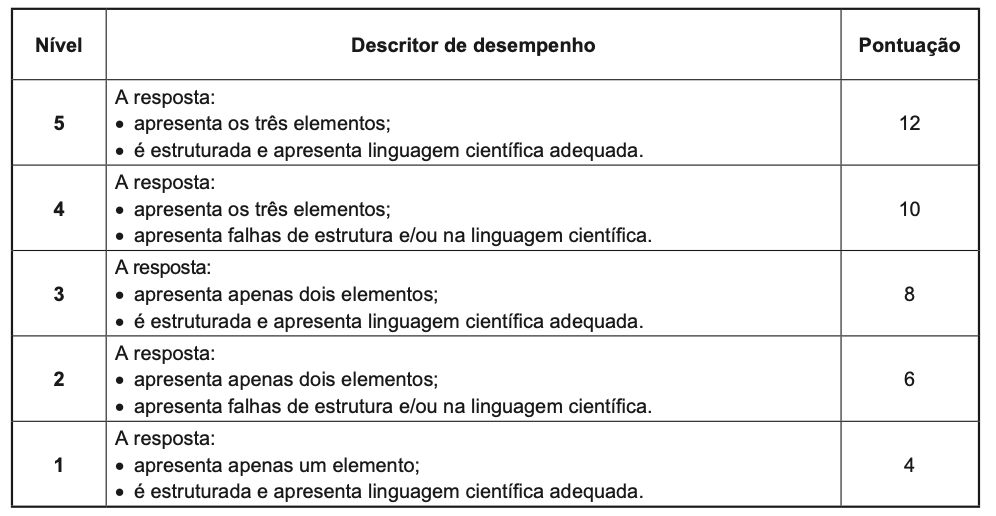
Descreva o modo como os alunos podem dar resposta ao desafio.
Na sua resposta:
– deduza a relação matemática que suporta a atividade experimental;
– apresente o procedimento experimental, identificando as grandezas a medir;
– refira a conclusão a retirar a partir da análise dos resultados.
Apresente um texto bem estruturado e utilize linguagem científica adequada.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 A energia elétrica fornecida pela resistência de imersão, de potência P , a cada um dos líquidos é E = P Δt , que, por sua vez, é responsável pelo aumento da energia térmica de cada um dos líquidos, E = mc Δθ .
- P Δt = mc Δθ
🛑 Para comparar as capacidades térmicas mássicas dos dois líquidos, com a mesma massa e a mesma temperatura inicial, os alunos, utilizando a resistência de imersão, devem aquecer os dois líquidos durante o mesmo intervalo de tempo, Δt , recorrendo a um cronómetro, e medir as respetivas temperaturas, utilizando o termómetro, para determinar as variações de temperatura, Δθ .
❇️ Como P e m são iguais, o líquido mais adequado para o sistema de refrigeração do motor, ou seja, o que apresenta maior capacidade térmica mássica, é o que sofrer menor variação de temperatura para o mesmo intervalo de tempo.
Elementos de resposta:
⇒ [Os alunos] obtêm c = (PΔt)/(mΔθ) (ou equivalente);
⇒ [Os alunos] aquecem cada um dos líquidos durante o mesmo intervalo de tempo e medem as respetivas variações de temperatura (ou equivalente);
⇒ [Os alunos] referem que o líquido mais adequado à refrigeração do motor é o [que tem maior capacidade térmica mássica, o que corresponde ao líquido] que sofre menor variação de temperatura no mesmo intervalo de tempo [,uma vez que P/m é constante] (ou equivalente).
4. Um automóvel, de massa 1000 kg , encontra-se parado junto a um semáforo.
No instante em que o automóvel inicia o seu movimento, é ultrapassado por uma mota, de massa 150 kg , que se move, na mesma direção e no mesmo sentido, com velocidade constante de módulo 10 m s-1, que mantém ao longo de todo o percurso em análise.
Considere que a trajetória descrita por ambos os veículos é retilínea e horizontal e que estes podem ser representados pelo seu centro de massa, segundo o modelo da partícula material.
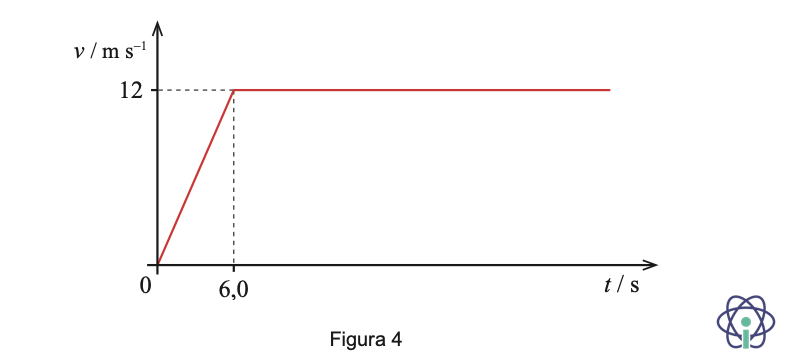
A Figura 4 apresenta o gráfico do módulo da velocidade do automóvel em função do tempo.
4.1. Admita que, nos primeiros 6,0 s de movimento, o automóvel transformou 90% da energia que lhe foi fornecida em energia cinética de translação, dissipando a restante.
Determine a energia que foi fornecida ao automóvel nesse intervalo de tempo.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 A variação da energia cinética do automóvel, durante os primeiros 6,0 s, é:
- ΔEc = Ecf – Eci ⇔ ΔEc = ½ mvf2 – 0 ⇔ ΔEc = ½ x 1000 x 122 ⇔ ΔEc = 7,20 x 104 J
🛑 90% da energia fornecida ao automóvel foi transformada em energia cinética de translação, a energia total fornecida, nesse intervalo de tempo, é:
- Ef = ΔEc / 0,90 ⇔ Ef = 7,20 x 104 / 0,90 ⇔ Ef = 8,0 x 104 J
❇️ A energia fornecida ao automóvel é igual a 8,0 x 104 J
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a variação da energia cinética (7,20 x 104 J) ………. 5 pontos
⇒ Calcula a energia que foi fornecida ao automóvel (8,0 x 104 J) ………. 5 pontos
4.2. Determine a distância percorrida pelos dois veículos até se encontrarem novamente.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 Durante os seis primeiros segundos do movimento, a moto deslocou-se com movimento uniforme e, à taxa de 10 m s-1, percorrerá 60 m (6 s × 10 m s-1 = 60 m).
🛑 No mesmo intervalo de tempo, o automóvel deslocar-se-á com um movimento retilíneo uniformemente acelerado e o valor da distância por ele percorrida pode ser obtido pela área delineada pelo gráfico 𝑣(t) com o eixo das abcissas, 12 × 6,0 / 2 = 36 m.
🛑 A partir dos 6,0 s, instante em que a moto se encontra a 60 m e o carro a 36 m do semáforo, ambos se encontram com movimento retilíneo e uniforme, sendo o automóvel (12 m s-1) mais rápido do que a moto (10 m s-1).
🛑 Quando se cruzarem terão a mesma posição em relação à origem, o que acontecerá num instante t contado a partir dos seis segundos iniciais, que pode ser obtido por:
- 𝑥automóvel = 𝑥moto ⇔ 36 + 12 𝑡 = 60 + 10 𝑡 ⇔ 12 × 𝑡 − 10 × 𝑡 = 60 − 36 ⇔ 2 × 𝑡 = 24 ⇔ 𝑡 = 12 𝑠
🛑 Onde o automóvel e a moto se encontrarão a 180 m do semáforo:
- 𝑥automóvel = 36 + 12 × 12 ⇔ 𝑥automóvel = 180 m
ou
- 𝑥moto = 60 + 10 × 12 ⇔ 𝑥moto = 180 m
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a distância percorrida pelo automóvel nos primeiros 6s de movimento (36,0 m) ………. 3 pontos
⇒ Calcula o instante em que o carro e a mota se voltam a encontrar (18,0 ou 12,0 s após o instante t = 6,0 s) ………. 4 pontos
⇒ Calcula a distância percorrida pelos dois veículos até se encontrarem novamente (1,8 x 102 m) ………. 3 pontos
4.3. O instante em que o automóvel e a mota apresentam igual velocidade ocorre
(A) antes dos 6,0 s, tendo os dois veículos a mesma energia cinética.
(B) após os 6,0 s, tendo os dois veículos a mesma energia cinética.
(C) antes dos 6,0 s, tendo os dois veículos diferente energia cinética.
(D) após os 6,0 s, tendo os dois veículos diferente energia cinética.
- Opção (C)
🛑 Como o automóvel parte do repouso e aumenta uniformemente a sua velocidade em magnitude até atingir os 12 m s-1 (no instante t = 6 s) e a moto se desloca sempre com uma velocidade de magnitude 10 m s-1, os dois veículos encontram-se à mesma velocidade quando ambos estiverem com a velocidade de magnitude 10 m s-1, o que terá de ocorrer necessariamente antes de t = 6 s.
🛑 Nesse instante, apesar de apresentarem velocidade de igual magnitude, a energia cinética do automóvel será maior, dado que as suas energias cinéticas serão, neste caso, diretamente proporcionais às suas massas.
❇️ Os dois veículos terão diferente energia cinética.
- Opção (C) ……………. 10 pontos
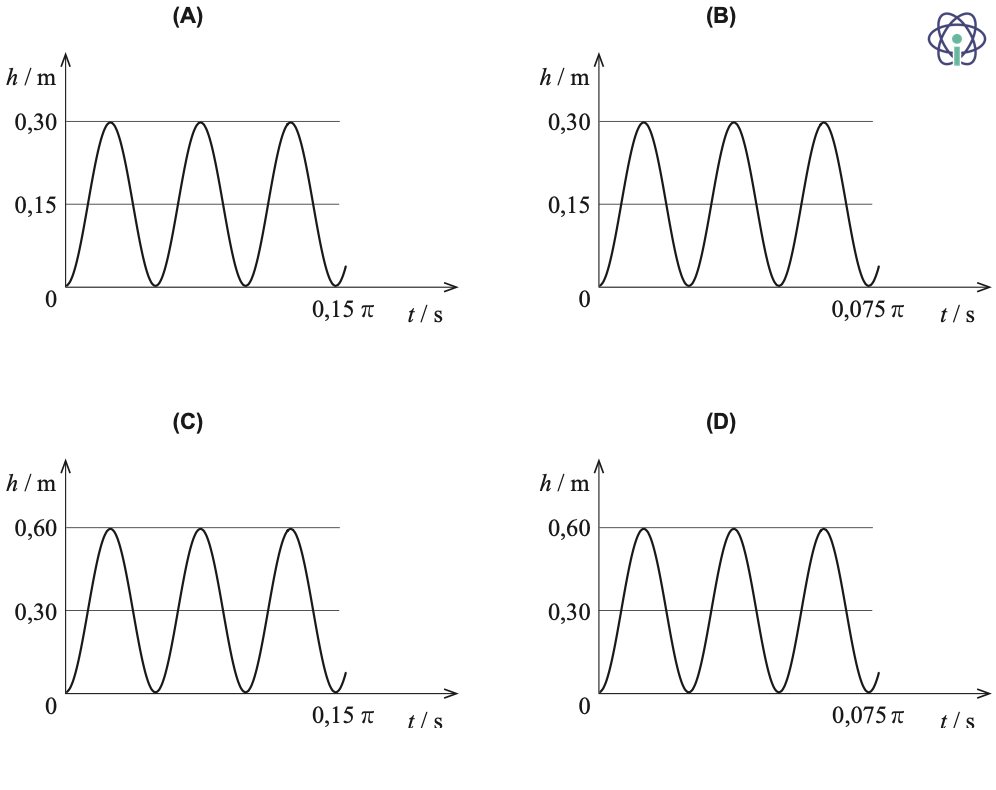
4.4. Considere um ponto X localizado na periferia de uma roda do automóvel, de raio 30 cm, que contacta com o solo, sem deslizar, quando o automóvel se desloca a uma velocidade constante, de módulo 12 m s-1.
Qual é o gráfico que pode representar a altura, h, do ponto X em relação ao solo, em função do tempo, t ?
- Opção (C)
🛑 Estando o ponto X em contacto com o solo, ao fim de um período, T , este ponto, após ter atingido a altura máxima, duas vezes o raio (0,60 m), regressa ao solo (0 m).
❇️ Como nos gráficos estão representados três períodos, o tempo correspondente ao movimento será:
- t = 3 x 0,050 π = 0,15 π s
- Opção (C) ……………. 10 pontos
5. Os óxidos de nitrogénio, essencialmente provenientes da combustão nos motores dos automóveis e nas centrais térmicas, contribuem para a formação de diversas espécies químicas com impacto no ambiente.
5.1. Os óxidos de nitrogénio são constituídos por átomos de nitrogénio e de oxigénio.
5.1.1. A energia de ionização do nitrogénio, isolado e em fase gasosa, é a energia mínima necessária para que, a partir de uma mole de átomos no estado fundamental, se forme uma mole de iões
(A) N+, tendo cada ião dois eletrões desemparelhados.
(B) N–, tendo cada ião dois eletrões desemparelhados.
(C) N+, que não têm eletrões desemparelhados.
(D) N–, que não têm eletrões desemparelhados.
- Opção (A)
🛑 A energia de ionização do nitrogénio (N) isolado e em fase gasosa é a energia mínima necessária para que, a partir de uma mole de átomos no estado fundamental, se forme uma mole de iões positivos (N+).
🛑 Um átomo de nitrogénio no estado fundamental tem a configuração eletrónica 1s2 2s2 2p3, tendo três eletrões desemparelhados na subcamada 2p.
❇️ Removendo um eletrão, forma-se o ião N+, com a configuração 1s2 2s2 2p2, onde possui dois eletrões desemparelhados.
- Opção (A) ……………. 10 pontos
5.1.2. Comparando o átomo de nitrogénio com o de oxigénio, ambos no estado fundamental, verifica-se que a carga nuclear do átomo de nitrogénio é
(A) maior e que o seu raio atómico é maior.
(B) menor e que o seu raio atómico é menor.
(C) maior e que o seu raio atómico é menor.
(D) menor e que o seu raio atómico é maior.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (D)
🛑 O nitrogénio tem número atómico 7, o que significa que possui 7 protões no seu núcleo. O oxigénio tem número atómico 8, o que significa que possui 8 protões no seu núcleo. Portanto, a carga nuclear do nitrogénio é menor do que a do oxigénio.
🛑 Como o nível de valência é o mesmo, devido à carga nuclear menor do nitrogénio (7 protões) em comparação com a do oxigénio (8 protões), a atração dos eletrões de valência pelo núcleo é menor no nitrogénio.
❇️ Com esta consideração, podemos verificar que o raio atómico do nitrogénio é maior do que o do oxigénio.
- Opção (D) ……………. 10 pontos
5.2. Na preparação de uma comunicação sobre o efeito da poluição automóvel na camada de ozono, um grupo de alunos recolheu a informação seguinte:
O gás monóxido de nitrogénio, NO, proveniente do escape dos automóveis, oxida-se facilmente na troposfera, formando o gás dióxido de nitrogénio, NO2 . Ao chegar à estratosfera, o NO2 decompõe-se, por ação da radiação UV, em dois radicais livres, o monóxido de nitrogénio e o oxigénio atómico. Por sua vez, o radical monóxido de nitrogénio pode reagir com o ozono estratosférico, O3 , originando dióxido de nitrogénio e dioxigénio gasosos.
Apresente, num texto bem estruturado e utilizando linguagem científica adequada, uma proposta de comunicação que inclua:
– as três equações químicas que traduzem as reações descritas na informação recolhida pelos alunos;
– a fundamentação para o facto de a decomposição do NO2 ocorrer predominantemente na estratosfera;
– a explicação para o facto de uma única molécula de NO conduzir à destruição de várias moléculas de ozono.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 As três reações descritas na informação recolhida pelos alunos são traduzidas pelas seguintes equações químicas:
- 2 NO (g) + O2 (g) → 2 NO2 (g) ; (na troposfera)
- NO2 (g) → NO. (g) + O. (g) ; (na estratosfera)
- NO. (g) + O3 (g) → NO2 (g) + O2 (g) (na estratosfera)
🛑 A fotodissociação do dióxido de nitrogénio, NO2 (g), (decomposição traduzida pela equação 2), ocorre predominantemente na estratosfera, porque é na estratosfera que a energia da radiação UV (UVB e UVC) é suficiente para provocar a decomposição do NO2 .
A segunda e terceira equações traduzem um processo de destruição do ozono:
- O3 → O2 + O.
🛑 A terceira equação traduz a decomposição da camada do ozono, que ocorre predominantemente na estratosfera, por ação da radiação ultravioleta de média energia (UVB), com recuperação das moléculas de dióxido de nitrogénio, NO2 (g), que podem voltar a reagir, segundo a reação (2), num processo cíclico (em cadeia).
❇️ A partir de uma única molécula de monóxido de nitrogénio proveniente dos escapes dos automóveis e dos aviões, são destruídas muitas moléculas de ozono, devido ao referido processo cíclico (2) + (3) .
Elementos de resposta:
- 2 NO + O2 → 2 NO2 ;
- NO2 → NO. + O. ;
- NO. + O3 → NO2 + O2 (ver nota);
⇒ [é na estratosfera que] a energia da radiação UV é suficiente para provocar a reação de fotodissociação da molécula de NO2 (ou equivalente);
⇒ a segunda e a terceira equações traduzem um processo cíclico de destruição de O3 , em que o NO2 é regenerado [, tendo como precursor uma molécula de NO proveniente dos escapes dos automóveis] (ou equivalente).
OU
⇒ o NO [,proveniente dos escapes dos automóveis,] origina NO2 que, por sua vez, [por ação da radiação UV,] forma o [radical] NO. Este radical reage com o O3 regenerando o NO2 que pode assim repetir o processo [de destruição de O3] (ou equivalente).
Nota: a apresentação de coeficientes estequiométricos incorretos é equiparada a falhas na linguagem científica.
5.3. Na atmosfera, os óxidos de nitrogénio podem originar o ácido nítrico, HNO3 , um ácido forte, e o ácido nitroso, HNO2 , um ácido fraco, que contribuem para a acidificação da água da chuva.
Considere duas soluções aquosas, uma de HNO3 , com pH 1,00, e outra de HNO2 , com pH 2,16, ambas com a mesma concentração e à mesma temperatura.
5.3.1. Determine a constante de acidez, Ka , do HNO2 para a temperatura considerada.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 Informações fornecidas:
⇒ Ka = 5,14 x 10-4
⇒ pH(solução de HNO3) = 1,00
⇒ pH(solução de HNO2) = 1,00
⇒ cHNO2 = cHNO3
⇒ KaHNO2 = ?
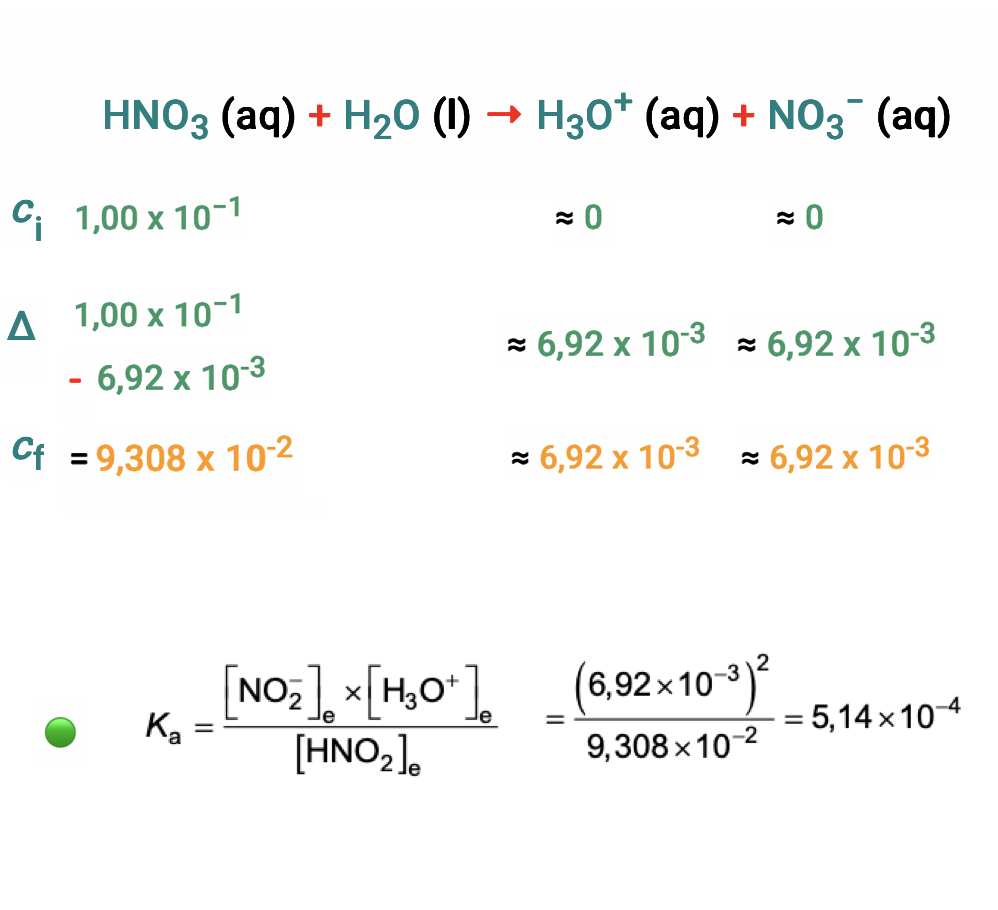
🛑 Cálculo da concentração da solução de ácido nítrico, (HNO3 ):
Como o ácido nítrico, HNO3 , é um ácido forte, a sua ionização é muito extensa em soluções aquosas diluídas, praticamente total:
HNO3 (aq) + H2O (l) → H3O+ (aq) + NO3− (aq)
🛑 De acordo com a estequiometria da reação de ionização deste ácido, c (H Δ NO3)inicial =c (H3O+)final
- pH = – log [H3O+] ⇔ [H3O+] = 10-pH ⇔ [H3O+] = 10-1,00 ⇔ [H3O+] = 1,00 x 10-1 mol dm-3
🛑 Cálculo da constante de acidez, Ka , do ácido nitroso, (HNO2) :
Como as duas soluções aquosas ácidas têm a mesma concentração, a concentração inicial da solução de ácido nitroso, c (HNO2 )inicial = 1,00 x 10−1 mol dm−3 .
- pH = 2,16 ⇔ [H3O+] = 10-2,16 ⇔ [H3O+] = 6,92 x 10-3 mol dm-3
O ácido nitroso, HNO2 , é um ácido fraco, logo a sua ionização não é total e, portanto, a reação de ionização deste ácido em água é expressa pelo equilíbrio traduzido pela equação química:
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula a concentração da solução de HNO3 (1,000 x 10-1 mol dm-3) ………. 4 pontos
⇒ Calcula a concentração de HNO2 no equilíbrio (9,308 x 10-2 mol dm-3) ………. 4 pontos
⇒ Calcula a constante de acidez, Ka , do HNO2 (5,14 x 10-4) ………. 4 pontos
5.3.2. Soluções de HNO3 e de HNO2 , de igual volume, foram tituladas com uma solução aquosa de uma base forte, NaOH, à temperatura de 25 ºC, até se atingir o ponto de equivalência.
O volume de titulante gasto para titular a solução de HNO2 é _______ ao volume de titulante gasto para titular a solução de HNO3 , e o pH no ponto de equivalência para a titulação de HNO2 é _______ a 7.
(A) inferior … superior
(B) inferior … inferior
(C) igual … superior
(D) igual … inferior
- Opção (C)
🛑 A reação de titulação destes ácidos com a solução de hidróxido de sódio pode ser traduzida, em ambos os casos, por
HA (aq) + OH− (aq) → A− (aq) + H2O (l)
🛑 Como as soluções dos dois ácidos têm a mesma concentração e os ácidos são ambos monopróticos, usando volumes iguais destas soluções, as quantidades de cada ácido a titular são iguais.
Como a proporção estequiométrica entre os reagentes na equação química da titulação é 1:1, as quantidades e os volumes de titulante gastos são iguais.
❇️ No ponto de equivalência da titulação da solução de HNO2 , as partículas presentes nesse ponto são todas neutras, à exceção do anião nitrito, NO− (aq), base conjugada do ácido nitroso fraco, pelo que 2 o pH no ponto de equivalência é superior a 7
- Opção (C) ……………. 10 pontos
6. O ácido acetilsalicílico é uma das substâncias mais utilizadas na redução da inflamação, da dor e da febre.
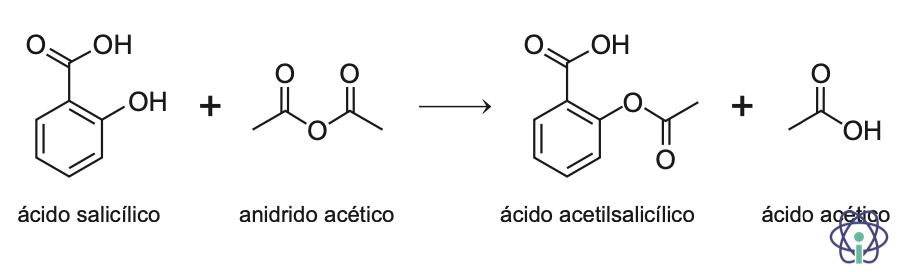
Na síntese desta substância, o ácido salicílico, C7H6O3 (M = 138,13 g mol-1), reage com o anidrido acético, C4H6O3 (M = 102,10 g mol-1 e ρ = 1,08 g cm-3), dando origem ao ácido acetilsalicílico, C9H8O4 (M = 180,17 g mol-1), e ao ácido acético. Esta reação é catalisada por ácido sulfúrico e pode ser traduzida por
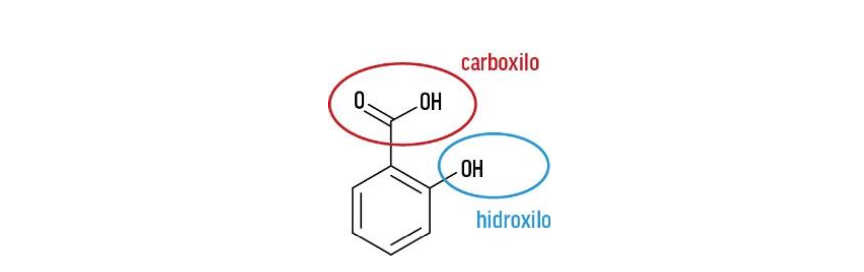
6.1. Os grupos funcionais presentes no ácido salicílico são
(A) carboxilo e hidroxilo.
(B) carboxilo e amina.
(C) carbonilo e hidroxilo.
(D) carbonilo e amina.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
- Opção (A) ……………. 10 pontos
6.2. Ordene as ações identificadas pelas letras de A a E, de modo a reconstituir parte do procedimento que permite determinar experimentalmente o rendimento na síntese do ácido acetilsalicílico.
Escreva, na folha de respostas, a sequência correta das letras.
A. Juntar o anidrido acético ao ácido salicílico.
B. Medir a massa dos cristais de ácido acetilsalicílico.
C. Secar os cristais de ácido acetilsalicílico.
D. Adicionar o catalisador e agitar.
E. Filtrar a vácuo os cristais obtidos.
⇒ A , D , E , C , B ………. 10 pontos
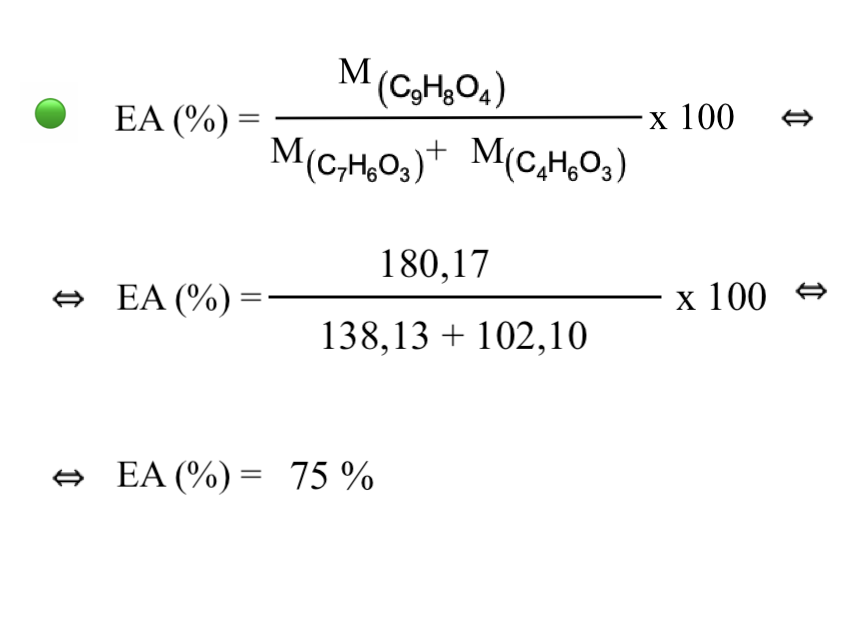
6.3. Na reação de síntese, qual é, aproximadamente, a percentagem, em massa, dos átomos dos reagentes incorporados no ácido acetilsalicílico?
(A) 32%
(B) 75%
(C) 49%
(D) 57%
- Opção (B) ……………. 10 pontos
6.4. Adicionaram-se 5,00 cm3 de anidrido acético a 2,02 g de ácido salicílico e obtiveram-se 1,83 g de ácido acetilsalicílico.
Determine o rendimento da síntese do ácido acetilsalicílico.
Apresente todos os cálculos efetuados.
A pontuação obtida na resposta contribui obrigatoriamente para a classificação final da prova
🛑 Informações fornecidas:
⇒ M(C7H6O3)= 138,13 g mol-1
⇒ M(C4H6O3)= 102,10 g mol-1
⇒ M(C9H8O4)= 180,17 g mol-1
⇒ ρ(C4H6O3)= 1,08 g cm-3
⇒ m(C7H6O3)= 2,02 g
⇒ V(C4H6O3)= 5,00 cm-3
⇒ mobtido (C9H8O4)= 1,83 g
🛑 Cálculo da quantidade de ácido salicílico e de anidrido acético:
⇒ a quantidade de ácido salicílico pode ser calculada pela expressão:
- n (C7H6O3) = m / M ⇔ n (C7H6O3) = 2,02 / 138,13 ⇔ n (C7H6O3) = 1,462 x 10-2 mol
⇒ para calcular a quantidade de anidrido acético é necessário primeiro calcular a sua massa:
- ρ = m / V ⇔ m = ρ x V ⇔ m (C4H6O3) = 1,08 x 5,00 ⇔ m (C4H6O3) = 1,08 x 5,00 g
- n (C4H6O3) = m / M ⇔ n (C4H6O3) = 5,40 / 102,10 ⇔ n (C4H6O3) = 5,289 x 10-2 mol
🛑 Identificação do reagente limitante:
A relação estequiométrica na reação entre o ácido salicílico e o anidrido acético é 1:1.
Comparando as quantidades disponíveis:
- 1,462 x 10-2 mol C7H6O3 < 5,289 x 10-2 mol C4H6O3
Portanto, o ácido salicílico é o reagente limitante.
🛑 Calcular o rendimento da reação de síntese do ácido acetilsalicílico:
A reação produz 1 mol de ácido acetilsalicílico para cada 1 mol de ácido salicílico, a quantidade prevista de ácido acetilsalicílico será 1,462 × 10−2 mol.
Calculando a massa prevista de ácido acetilsalicílico:
- n = m/M ⇔ mprevista = 1,462 x 10-2 x 180,17 ⇔ mprevista = 2,6341 g
❇️ O rendimento da reação de síntese do ácido acetilsalicílico é:
Determina o valor solicitado, percorrendo as etapas seguintes:
⇒ Calcula as quantidades de ácido salicílico (1,462 x 10-2 mol) e de anidrido acético (5,289 x 10-2 mol)
ou
Calcula a massa de anidrido acético necessária para a reação completa do ácido salicílico (1,493 g) ………. 3 pontos
⇒ Identifica o reagente limitante (ácido salicílico) ………. 3 pontos
⇒ Calcula o rendimento da reação de síntese do ácido acetilsalicílico (69,5 %) ………. 4 pontos
FIM