2015 – Época Especial – Prova Escrita de Física e Química A
Voltar a: Física e Química
Prova Escrita de Física e Química A – versão 1
Prova 715: Época especial – 2015
GRUPO I
Se a luz do Sol for analisada com um espectroscópio de baixa resolução, o espectro que se observa é contínuo. No entanto, o espectro da luz emitida por um gás a baixa pressão tem características diferentes. Em vez da imagem contínua e multicolorida do espectro solar, aparecem riscas coloridas sobre um fundo negro. Cada risca corresponde a uma cor ou, na linguagem da teoria ondulatória, a uma frequência.
A. Einstein, L. Infeld, A Evolução da Física, 1.ª ed., Lisboa, Livros do Brasil, p. 237 (adaptado)
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
1. O que se observa num espectro atómico de emissão na região do visível?
⇒ Observam-se riscas coloridas sobre um fundo negro, resultantes da emissão de radiações com certos valores de energia na zona do visível.
⇒ Cada elemento tem um espetro de emissão próprio que permite identificá-lo.
- Riscas coloridas sobre um fundo negro. …………. 5 pontos
2. Os espectros das estrelas são espectros térmicos.
A temperatura superficial de uma estrela de cor azul é
(A) superior à temperatura superficial do Sol, de acordo com a lei de Stefan-Boltzmann.
(B) superior à temperatura superficial do Sol, de acordo com a lei do deslocamento de Wien.
(C) inferior à temperatura superficial do Sol, de acordo com a lei de Stefan-Boltzmann.
(D) inferior à temperatura superficial do Sol, de acordo com a lei do deslocamento de Wien.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
O conteúdo deste item foi excluído do atual Programa e Metas Curriculares da disciplina.
- Opção (B) …………. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
3. A energia dos eletrões num átomo pode ser determinada por técnicas espectroscópicas.
Considere a configuração eletrónica do átomo de néon no estado fundamental. Das orbitais ocupadas, quantas têm a mesma energia?
- 10Ne – 1 s2 2s2 2p6
⇒ Das orbitais ocupadas, há três orbitais com a mesma energia.
⇒ São as três orbitais 2p, (2px, 2py, 2pz).
⇒ Estas orbitais, por terem a mesma energia, designam-se por orbitais degeneradas.
- Três [orbitais] ………….. 5 pontos
- 10ºano – Química – Domínio 1 – subdomínio 2 (Energia dos eletrões nos átomos)
4. Quais são os níveis de energia inicial e final da transição eletrónica no átomo de hidrogénio que origina a emissão de radiação visível de menor frequência?
(A) ninicial = 2 ; nfinal = 1
(B) ninicial = 1 ; nfinal = 2
(C) ninicial = 2 ; nfinal = 3
(D) ninicial = 3 ; nfinal = 2
- Opção (D)
⇒ No átomo de hidrogénio, a série de emissão espetral observada na zona do visível, série de Balmer, corresponde a transições do eletrão de um nível de energia superior para o primeiro estado excitado, isto é, para o nível de energia n = 2.
⇒ A energia do fotão emitido numa desexcitação é igual à diferença de energias dos níveis entre os quais ocorre a transição, a emissão de radiação visível de menor frequência, ou seja, de menor energia, corresponde a uma transição eletrónica do nível n = 3 para o nível n = 2.
- Opção (D) …………. 5 pontos
5. Considere uma radiação monocromática que se propaga inicialmente no ar e que passa, depois, a propagar-se num vidro.
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
5.1. Ao propagar-se no vidro, a radiação terá
(A) menor frequência e menor comprimento de onda.
(B) a mesma frequência e maior comprimento de onda.
(C) a mesma frequência e menor comprimento de onda.
(D) menor frequência e maior comprimento de onda.
- Opção (C)
⇒ A frequência da radiação monocromática é constante, é independente do meio de propagação.
⇒ Para um dado meio de propagação, a relação entre a frequência e o comprimento de onda de uma radiação é:
- v = λ f
⇒ Como a velocidade de propagação no ar é aproximadamente igual à do vácuo (3,00 x 108 m s-1) , em qualquer outro meio apresenta menor valor.
⇒ A velocidade de propagação no vidro é inferior à do ar e a frequência mantém-se, então o comprimento de onda da radiação no vidro é inferior à do ar.
- Opção (C) …………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 3 (Ondas eletromagnéticas)
5.2. A velocidade de propagação da radiação considerada nesse vidro é 2/3 da sua velocidade de propagação no ar.
Qual é o índice de refração desse vidro para a radiação considerada?
Apresente o resultado com dois algarismos significativos.
nar (índice de refração do ar) = 1,00
- vvidro = 2/3 var
⇒ O índice de refração absoluto de um dado meio de propagação é:
- n = c/V ⇔ n x v = c
- nvidro x vvidro = nar x var ⇒ nvidro x 2/3 var ⇔ 2/3 nvidro = nar ⇔nvidro = 3/2 x 1,00 = 1,5
⇒ O índice de refração do vidro para a radiação considerada é igual a 1,5.
- 1,5 …………. 5 pontos
GRUPO II
O ozono, O3, é um gás que, na troposfera, é um poluente, mas que, na estratosfera, é essencial para a vida na Terra. A diminuição da concentração deste gás na estratosfera está, em parte, relacionada com a ação indesejável dos clorofluorocarbonetos (CFC).
- 10ºano – Química – Domínio 2 – subdomínio 2 (Gases e dispersões)
1. O valor estabelecido pela União Europeia como teor máximo de ozono na troposfera, à pressão de 1 atm e à temperatura de 20 ºC, é 1,20 x 10-4 gm-3.
Qual das expressões seguintes permite calcular a quantidade máxima de ozono que poderá existir em 50 dm3 de ar, de acordo com o valor estabelecido pela União Europeia?
- Opção (D)…………. 5 pontos
2. Na estratosfera, ocorrem, simultaneamente, reações que conduzem à formação do ozono e outras que conduzem à sua destruição.
Uma das reações que conduzem à formação do ozono ocorre entre as moléculas de oxigénio e os radicais livres de oxigénio.
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
2.1.Escreva a equação química que traduz essa reação.
- O2 (g) + O (g) → O3 (g)
- O2 (g) + O (g) → O3 (g) …………. 5 pontos
Notas:
A omissão da indicação do(s) estado(s) físico(s) de uma ou mais espécies não implica qualquer desvalorização.
A apresentação de ⇋ (em vez de →) não implica qualquer desvalorização.
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
2.2. Considere que por cada mole de O3 (g) que se forma se libertam cerca de 105 kJ.
A energia, em joule, que se liberta quando, através da reação referida, se forma uma molécula de ozono é
(A) 1,74 x 10-22 J
(B) 6,32 x 1028 J
(C) 1,74 x 10-19 J
(D) 6,32 x 1025 J
- Opção (C)…………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 3 (Transformações químicas)
2.3.Os radicais livres originados pela rutura de ligações nos CFC, por ação da radiação ultravioleta, catalisam algumas das reações que conduzem à destruição do ozono.
Conclua, justificando, qual das ligações, C – Cl ou C – F, sofrerá mais facilmente rutura.
⇒Os elementos flúor e cloro localizam-se no mesmo grupo da Tabela Periódica, grupo 17, e nos períodos 2 e 3, respetivamente, ou seja, o flúor antecede o cloro no mesmo grupo da TP.
⇒Como o raio atómico aumenta ao longo do grupo, o raio atómico do cloro é superior ao raio atómico do flúor.
⇒O comprimento de ligação C-Cl é maior do que o comprimento de ligação C-F.
⇒As diferenças nas energias de ligação resultam fundamentalmente dos diferentes comprimentos de ligação dos átomos ligados.
⇒ Menores comprimentos de ligação conduzem a ligações mais fortes, pelo que a energia de ligação C-Cl é menor que a energia de ligação C-F.
⇒Será necessário mais energia para romper a ligação C-F do que para romper a ligação C-Cl.
- A ligação C-Cl sofre mais facilmente rutura.
- A resposta integra os tópicos de referência seguintes ou outros de conteúdo equivalente:
A)O raio atómico do cloro é superior ao raio atómico do flúor, pelo que o comprimento da ligação C – Cl será maior do que o comprimento da ligação C – F.
B)Assim, será necessária mais energia para romper a ligação C – F do que para romper a ligação C – Cl, pelo que a ligação C – Cl sofrerá mais facilmente rutura.
3.A monitorização da concentração de alguns poluentes pode ser feita por satélites artificiais.
- 11ºano – Física – Domínio 1 – subdomínio 3 (Forças e movimentos)
3.1. Considere um desses satélites, em órbita aproximadamente circular em torno da Terra, a uma altitude aproximada de 705 km.
Determine o número de órbitas completas descritas pelo satélite em 24 horas.
Apresente todas as etapas de resolução.
- mTerra(massa da Terra) = 5,98 × 1024 kg
- rTerra (raio da Terra) = 6,4 × 106 m
- Etapas de resolução:
A) Determinação do módulo da velocidade orbital do satélite (v = 7,50 × 103 m s-1) …….. 5 pontos
B)Determinação do período do movimento do satélite (T = 5,95 × 103 s)
ou
- Determinação da frequência do movimento do satélite ( f = 1,68 × 10-4 Hz) …….. 3 pontos
C) Determinação do número de órbitas completas descritas pelo satélite em 24h (14) (ver nota) ……..2 pontos
Nota – A não indicação do número de órbitas completas descritas pelo satélite implica a pontuação desta etapa com zero pontos.
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
3.2. Os satélites estão geralmente equipados com painéis fotovoltaicos que se orientam segundo uma direção perpendicular à da radiação solar.
Considere que a potência média da radiação solar por unidade de área, ao nível da órbita de um satélite, é 1,3 x 103 W m-2 e que um conjunto de painéis fotovoltaicos, de área 12 m2, instalado no satélite, tem um rendimento médio de 20%.
Qual das expressões seguintes permite calcular, em kW h, a energia fornecida ao satélite por esse conjunto de painéis em 6 horas de funcionamento?
- Opção (A)
- A = 12 m2
- η = 20 %
- Δt = 6 h
- Er = 1,3 x 103 W m-2
Calcular a energia fornecida ao satélite, Eútil:
⇒ Er = P/A ⇔ Pradiação = Er x A = 1,3 x 103 x 12 W
⇒ Pútil = η x Pradiação = 0,20 x 1,3 x 103 x 12 W
⇒ Eútil = Pútil x Δt = 0,20 x 1,3 x 103 x 12 x 6 W = 0,20 x 1,3 x 103 x 12 x 6 x 10-3 kW = 0,20 x 1,3 x 12 x 6 kW
- Opção (A)…………. 5 pontos
GRUPO III
1. O etino, C2H2, pode ser obtido fazendo-se reagir carboneto de cálcio, CaC2(s), com água, de acordo com a equação química
CaC2 (s) + 2 H2O (l) → Ca(OH)2 (aq) + C2H2 (g)
- 11ºano – Química – Domínio 1 – subdomínio 1 (Aspetos quantitativos das reações químicas)
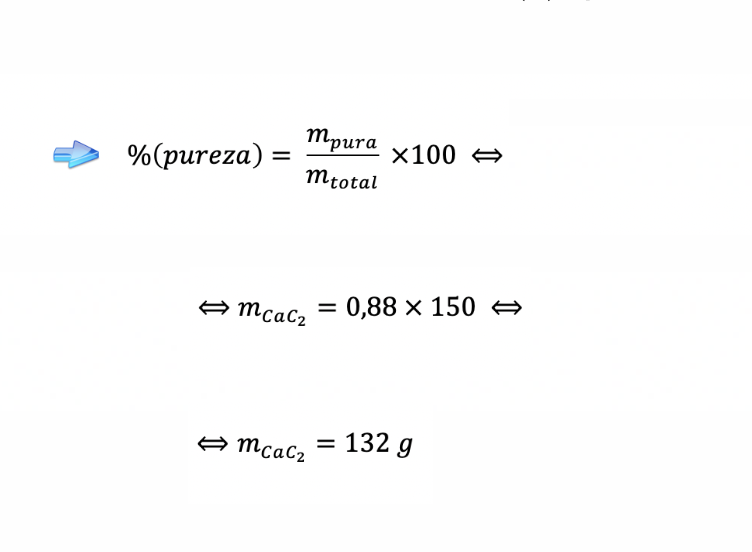
1.1. Considere que se fez reagir, com excesso de água, uma amostra impura de 150 g de carboneto de cálcio contendo 12% de impurezas, tendo-se obtido 30,0 dm3 de etino, em condições normais de pressão e de temperatura (PTN).
Determine o rendimento da reação de síntese do etino realizada.
Apresente todas as etapas de resolução.
⇒ Cálculo da massa de CaC2 (s) que existe na amostra:
⇒ Cálculo do volume de C2H2 (g) que se formaria, em condições PTN, se a reação fosse completa:
- Como a reação ocorreu com excesso de água, o reagente limitante é o CaC2 (s).
- De acordo com a estequiometria da reação, 1 mol de CaC2 (s) origina 1 mol de C2H2 (g).
- A quantidade de C2H2 (g) que se obteria se a reação fosse completa seria igual à quantidade de CaC2 (s) inicial.
⇒ Cálculo do rendimento da reação de síntese do etino:
- Etapas de resolução:
A) Determinação da massa de CaC2 (s) que existe na amostra (m = 132 g) …….. 2 pontos
B) Determinação do volume de C2H2 (g) que se deveria formar, em condições normais de pressão e de temperatura (V = 46,13 dm3) …….. 5 pontos
C)Determinação do rendimento da reação (65% ou 0,65) …….. 3 pontos
- 11ºano – Química – Domínio 2 – subdomínio 3 (Soluções e equilíbrio de solubilidade)
1.2. O produto de solubilidade do hidróxido de cálcio, Ca(OH)2, a 25 ºC, é 8,0 x 10-6.
Qual é a concentração de iões Ca2+(aq) numa solução saturada de hidróxido de cálcio, a 25 ºC ?
(A) 1,3 x 10-2 mol dm-3
(B) 2,0 x 10-2 mol dm-3
(C) 1,4 x 10-3 mol dm-3
(D) 2,0 x 10-3 mol dm-3
- Opção (A) …………. 5 pontos
2. A combustão do etino pode ser traduzida por
2 C2H2 (g) + 5 O2 (g) → 4 CO2 (g) + 2 H2O (l )
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
2.1. A variação de entalpia associada a esta reação é -2,60 x 103 kJ por mole de reação.
A combustão de 1 mol de etino envolverá a
(A) libertação de 2,60 x 103 kJ.
(B) absorção de 2,60 x 103 kJ.
(C) libertação de 1,30 x 103 kJ.
(D) absorção de 1,30 x 103 kJ.
- Opção (C)
- ΔHreação = – 2,60 x 103 kJ mol-1
⇒Como ΔHreação < 0, a combustão do etino envolve libertação de energia.
⇒ A equação química representada indica que a combustão de duas moles de etino envolve a libertação de 2,60 x 103 kJ.
⇒A combustão de 1 mol de etino envolverá a libertação de 1,30 x 103 kJ
- Opção (C)…………. 5 pontos
- 11ºano – Química – Domínio 2 – subdomínio 2 (Reações de oxidação redução)
2.2. Qual é o número de oxidação do carbono na molécula de CO2?
(A) +4
(B) +2
(C) -4
(D) -2
- Opção (A)
⇒ O número de oxidação do carbono em CO2 é + 4, como se mostra:
- x + 2 x (- 2) = 0 ⇒ x = + 4
- Opção (A) …………. 5 pontos
- 10ºano – Química – Domínio 2 – subdomínio 1 (Ligação química)
3. Na molécula de etino, C2H2, a ligação entre os átomos de carbono é covalente tripla. Na molécula de eteno, C2H4, a ligação entre os átomos de carbono é covalente dupla.
Comparando aquelas ligações entre os átomos de carbono, verifica-se que a ligação na molécula de eteno tem ____ energia e ____ comprimento.
(A) menor … menor
(B) menor … maior
(C) maior … maior
(D) maior … menor
- Opção (B)
⇒ A ligação tripla carbono-carbono é mais forte e mais curta que a ligação dupla carbono-carbono.
⇒ A ligação dupla de eteno tem menor energia e maior comprimento do que a ligação tripla de etino.
- Opção (B)…………. 5 pontos
GRUPO IV
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
1. As constantes de acidez, a 25 ºC, do ácido cianídrico, HCN(aq), e do ácido nitroso, HNO2(aq), são 4,9 x 10-10 e 5,1 x 10-4, respetivamente.
Considere, àquela temperatura, uma solução de ácido cianídrico e uma solução de ácido nitroso de igual concentração.
O pH da solução de ácido _____ é maior, uma vez que a ionização deste ácido é ______ extensa.
(A) cianídrico … menos
(B) cianídrico … mais
(C) nitroso … menos
(D) nitroso … mais
- Opção (A)
- Ka (HCN) = 4,9 x 10-10
- Ka(HNO2) = 5,1 x 10-4
⇒Quanto maior for o valor de Ka, mais forte é o ácido, ou seja, mais extensa é a respetiva reação de ionização.
⇒Como Ka (HNO2) > Ka (HCN), a reação de ionização de HCN é menos extensa que a de HNO2.
⇒Como as soluções destes ácidos têm igual concentração, a [H3O+] da solução de HCN será inferior à da solução HNO2.
⇒ Como pH = – log [H3O+], quanto menor for a [H3O+], maior é o respetivo valor de pH.
⇒O pH da solução de ácido cianídrico é maior, uma vez que a ionização deste ácido é menos extensa.
- Opção (A)…………. 5 pontos
2. A reação de ionização do ácido fluorídrico em água pode ser traduzida por
HF(aq) + H2O(l) ⇋ F–(aq) + H3O+(aq)
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2.1. Considere que se dilui 100 vezes uma solução de ácido fluorídrico, HF (aq), de concentração 27,8 mol dm-3.
O pH da solução diluída é 1,87, a 25 ºC.
Calcule a percentagem de ácido não ionizado na solução diluída de ácido fluorídrico.
Apresente todas as etapas de resolução.
- [HF(aq)]inicial = 27,8 mol dm-3
- Fator de diluição, f = 100
⇒Como o fator de diluição é igual a 100, a concentração da solução diluída de ácido fluorídrico é:
- f = ci/cf ⇔ [HF(aq)]diluida = 27,8 mol dm-3/ 100 = 0,278 mol dm-3
pH da solução diluída de HF = 1,87 a 25 ºC.
⇒ De acordo com a definição de pH, pH = – log [H3O+], pH = 1,87 corresponde à seguinte concentração do ião hidrogénio aquoso:
- [H+(aq)] = 10-1,87 = 1,349 x 10-2 mol dm-3
⇒ De acordo com a reação de ionização do ácido fluorídrico, e desprezando a autoprotólise da água, podemos considerar
- [HF(aq)ionizado] = [F–(aq)] = [H3O+(aq)] = 1,349 x 10-2 mol dm-3
- [HF(aq)]não ionizado = 0,278 – 1,349 x 10-2 = 0,265 mol dm-3
⇒A percentagem de ácido não ionizado na solução diluída de ácido fluorídrico é:
- % HF (não ionizado)= (0,265/0,278) x 100 = 95,3%
- Etapas de resolução:
A)Determinação da concentração da solução diluída (c = 0,278 mol dm-3) …….. 2 pontos
B)Determinação da concentração de ácido fluorídrico ionizado ([F–] = 1,349 × 10-2 mol dm-3) …….. 5 pontos
C)Determinação da concentração de ácido fluorídrico não ionizado ([HF] = 0,265 mol dm-3) …….. 5 pontos
D) Determinação da percentagem de ácido não ionizado na solução diluída de ácido fluorídrico (95%) …….. 3 pontos
- 11ºano – Química – Domínio 2 – subdomínio 1 (Reações ácido-base)
2.2.Conclua, justificando, como varia a quantidade de ácido fluorídrico não ionizado se a uma solução deste ácido forem adicionadas, a temperatura constante, algumas gotas de uma solução concentrada de um ácido forte.
⇒Se a uma solução de ácido fluorídrico forem adicionadas algumas gotas de solução concentrada de um ácido forte, a concentração de H3O+ (aq) aumenta.
⇒De acordo com o Princípio de Le Châtelier, o aumento da [H3O+(aq)] provoca uma evolução do sistema no sentido em que ocorra uma diminuição da concentração deste ião, ou seja, no sentido inverso, desfavorecendo a ionização do ácido.
⇒ A quantidade de ácido fluorídrico não ionizado na solução aumenta.
- A resposta integra os tópicos de referência seguintes ou outros de conteúdo equivalente:
A) A adição [a uma solução de ácido fluorídrico] de algumas gotas de uma solução concentrada de um ácido forte provoca um aumento da concentração de H3O+(aq).
B) [De acordo com o Princípio de Le Châtelier,] o aumento da concentração de H3O+(aq) favorece a reação que conduz a uma diminuição da concentração daquele ião que, neste caso, é a reação inversa.
C)Assim, conclui-se que a quantidade de ácido fluorídrico não ionizado na solução aumenta.
GRUPO V
Um grupo de alunos fixou um lançador de projéteis na extremidade de uma mesa, como se representa na Figura 1, e ajustou o ângulo de disparo do lançador, de modo a lançar uma esfera horizontalmente.
Na Figura 1, estão ainda representados um referencial bidimensional, Oxy, com origem no solo, e a distância, d, desde a origem do referencial considerado até ao ponto em que a esfera embateu no solo (alcance).
O ponto de lançamento situa-se a uma altura de 66,0 cm em relação ao solo.
1. Se a altura do ponto de lançamento em relação ao solo for maior e a esfera for lançada com a mesma velocidade,
(A) o tempo de voo da esfera será igual e o alcance será menor.
(B) o tempo de voo da esfera será maior e o alcance será maior.
(C) o tempo de voo da esfera será igual e o alcance será maior.
(D) o tempo de voo da esfera será maior e o alcance será menor.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
O conteúdo deste item foi excluído do atual programa e metas curriculares da disciplina.
- Opção (B) …………. 5 pontos
2. Na tabela seguinte, encontram-se registadas as distâncias, d, obtidas em três ensaios.
Determine o módulo da velocidade de lançamento da esfera, considerando que a resistência do ar é desprezável.
Recorra exclusivamente às equações do movimento, x (t) e y (t).
Apresente todas as etapas de resolução.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
O conteúdo deste item foi excluído do atual programa e metas curriculares da disciplina.
- Etapas de resolução:
A)Determinação do valor mais provável da distância d (d = 1,81 m) (ver nota) …….. 2 pontos
B)Determinação do tempo de voo da esfera (t = 0,363 s) …….. 4 pontos
C) Determinação do módulo da velocidade de lançamento da esfera (v = 5,0 m s-1) …….. 4 pontos
Nota – A apresentação do valor mais provável da distância d com um arredondamento incorreto, ou com um número incorreto de algarismos significativos, implica a pontuação desta etapa com zero pontos.
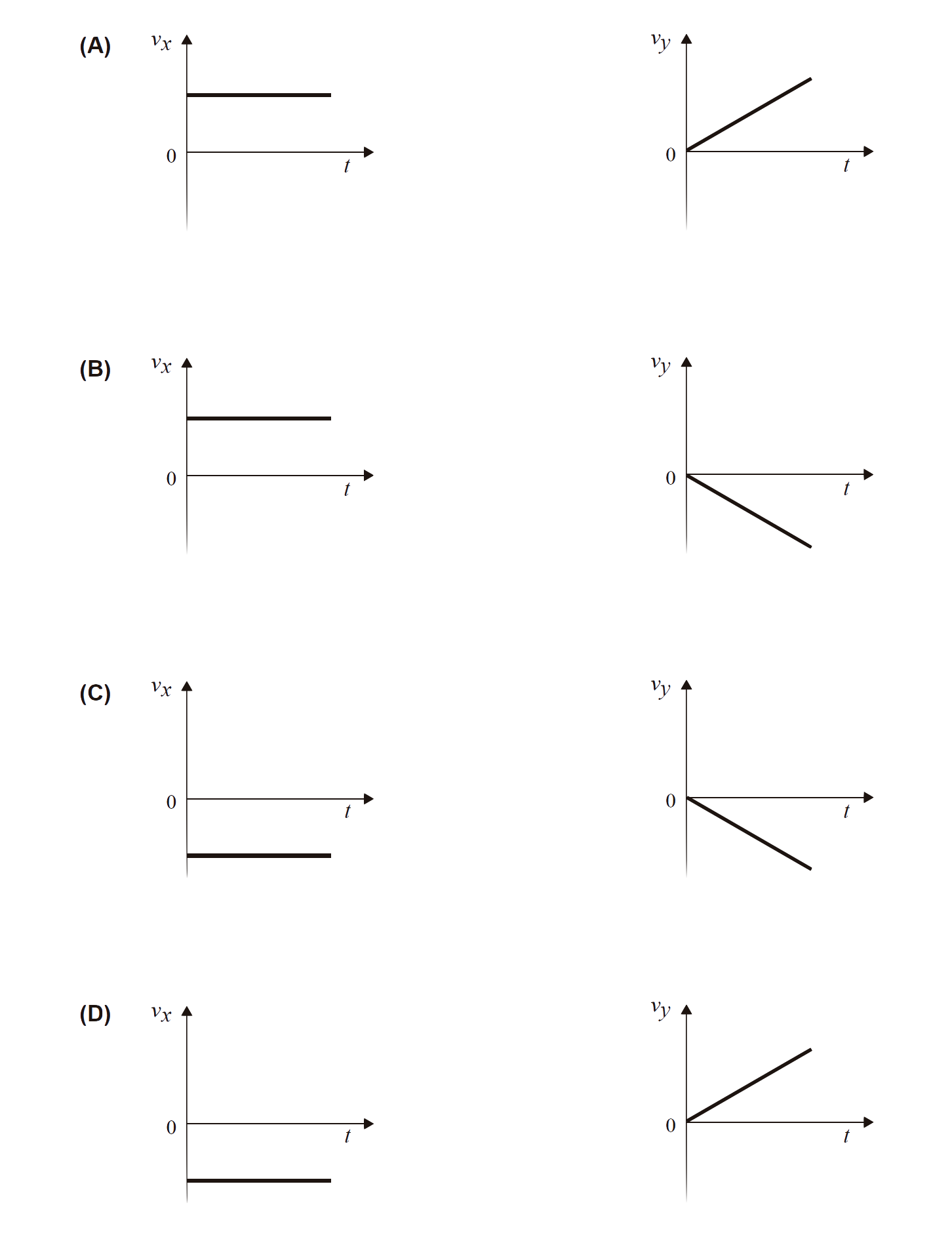
3. Qual das opções apresenta os esboços dos gráficos das componentes escalares, vx e vy, da velocidade da esfera, em relação ao referencial considerado, em função do tempo, t, durante a queda da esfera, se a resistência do ar for desprezável?
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
O conteúdo deste item foi excluído do atual programa e metas curriculares da disciplina.
- Opção (B) …………. 5 pontos
GRUPO VI
Abandonou-se um carrinho no topo de um plano inclinado.
Admita que o carrinho pode ser representado pelo seu centro de massa (modelo da partícula material).
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
1. O trabalho realizado pela força gravítica que atua no carrinho, desde o topo do plano inclinado até à base do plano, é
(A) negativo e igual à variação da energia cinética do carrinho.
(B) positivo e simétrico da variação da energia cinética do carrinho.
(C) negativo e igual à variação da energia potencial gravítica do sistema carrinho + Terra.
(D) positivo e simétrico da variação da energia potencial gravítica do sistema carrinho + Terra.
- Opção (D)
⇒O peso é uma força conservativa, cujo trabalho, durante um dado deslocamento, é igual ao simétrico da variação da energia potencial gravítica do sistema corpo + Terra, para o mesmo deslocamento.
⇒Ao descer o plano inclinado, a variação da energia potencial gravítica do sistema carrinho + Terra é negativa, pois a altura está a diminuir, logo, o trabalho realizado pelo peso é positivo.
- Opção (D) …………. 5 pontos
2. Na tabela seguinte, estão registadas distâncias, d, percorridas pelo carrinho, desde o topo do plano até várias posições, A, B, C e D, sobre este, e a energia cinética, Ec, do carrinho em cada uma dessas posições.
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2.1. Quando o carrinho se encontra na posição A, a energia potencial gravítica do sistema carrinho+Terra é 2,72 x10-1 J e, quando se encontra na posição C, aquela energia é 1,27 x 10-1 J.
Calcule a intensidade da resultante das forças não conservativas que atuam no carrinho na direção do deslocamento, no percurso entre as posições A e C, admitindo que essa resultante se mantém constante.
Apresente todas as etapas de resolução.
EpA = 2,72 x 10-1 J
EcA = 2,73 x 10-2 J
dA = 0,30 m
EpC = 1,27 x 10-1 J
EcC = 9,03 x 10-2 J
dC = 1,10 m
⇒ Calcular a intensidade das forças não conservativas:
- WFNC = ΔEm ⇔ FNC x d x cos 180 = ΔEc + ΔEp ⇔ – FNC x (dC – dA) = ( 9,03 x 10-2 – 2,73 x 10-2) + (1,27 x 10-1 – 2,72 x 10-1) ⇔ – FNC x (1,10 – 0,30) = – 8,02 x 10-2 ⇔ – FNC x 0,80 = – 8,02 x 10-2 ⇔ FNC = – 1,01 x 10-1 N
⇒ A intensidade das forças não conservativas que atuam no carrinho entrea as posições A e C é igual a 1,0 x 10-1 N.
- Etapas de resolução:
A) Determinação da variação de energia mecânica do sistema carrinho + Terra, no percurso considerado (ΔEm = -8,2 × 10-2 J ) …….. 6 pontos
B)Determinação do módulo do deslocamento do carrinho, no percurso considerado (d = 0,80 m) …….. 3 pontos
C) Determinação da intensidade da resultante das forças não conservativas que atuam no carrinho na direção do deslocamento (F = 1,0 × 10-1 N) …….. 6 pontos
- 10ºano – Física – subdomínio 1 (Energia e movimentos)
2.2. Calcule a intensidade da resultante das forças que atuam no carrinho, na situação considerada, admitindo que essa resultante se mantém constante e que tem a direção do deslocamento.
Utilize as potencialidades gráficas da calculadora. Apresente a equação da reta de ajuste obtida, identificando as grandezas físicas representadas.
Apresente todas as etapas de resolução.
⇒ Para determinar a intensidade da resultante das forças que atuam sobre o carrinho, recorre-se ao Teorema da Energia Cinética:
- ΔEc = WFr ⇔ ΔEc = Fr d ⇔ Ec = Ec0 + Fr d (1)
⇒ A equação da reta que se ajusta aos valores tabelados é:
- Ec= 3 x 10-3 + 7,90 x 10-2 d (SI)
⇒ Comparando esta equação com a expressão (1), verifica-se que o declive da reta, 7,90 x 10-2, é igual à intensidade da resultante das forças que atuam sobre o carrinho.
- A intensidade da resultante das forças que atuam sobre o carrinho é igual a 7,90 x 10-2 N.
- Etapas de resolução:
A)Apresentação da equação da reta que melhor se ajusta ao conjunto de valores registados na tabela (Ec = 7,90 × 10-2 d + 3 × 10-3 (SI)) (ver notas 1 e 2) …….. 5 pontos
B)Identificação do declive da reta com a intensidade da resultante das forças que atuam no carrinho, na situação considerada (F = 7,9 × 10-2 N) (ver nota 3) …….. 5 pontos
Notas:
1. A apresentação da equação da reta para o gráfico de d em função de Ec (d = 12,6 Ec – 4 × 10-2) será considerada um erro de tipo 2.
2. A não identificação ou a identificação incorreta de, pelo menos, uma das grandezas físicas consideradas implica a pontuação desta etapa com zero pontos.
3. A apresentação do valor solicitado com um número incorreto de algarismos significativos não implica qualquer desvalorização.
GRUPO VII
- 11ºano – Física – Domínio 2 – subdomínio 2 (Eletromagnetismo)
1. A Figura 2 representa as linhas do campo magnético criado por um íman em barra.
As linhas de campo magnético são, em cada ponto, ____ ao vetor campo magnético e apontam do polo ___ para o polo _____ do íman.
(A) tangentes … norte … sul
(B) perpendiculares … norte … sul
(C) tangentes … sul … norte
(D) perpendiculares … sul … norte
- Opção (A)
⇒ As linhas de campo magnético são, em cada ponto, tangentes ao vetor campo magnético e, por convenção, saem do polo norte e entram no polo sul.
- Opção (A)…………. 5 pontos
- 11ºano – Física – Domínio 2 – subdomínio 2 (Eletromagnetismo)
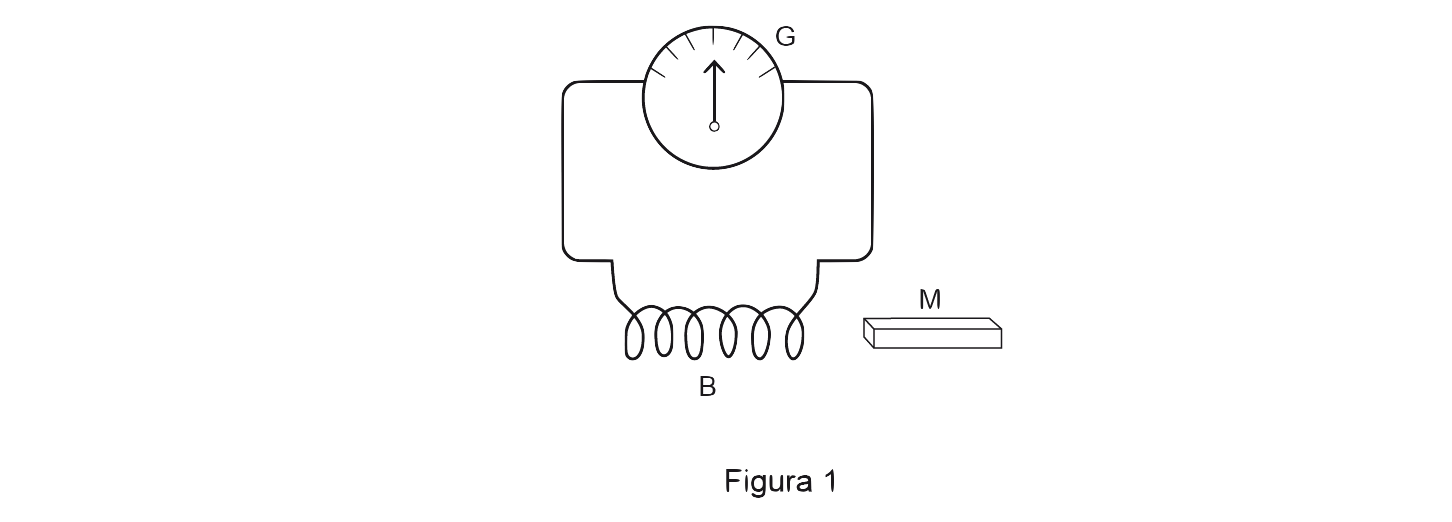
2. Na Figura 3, está representado um íman em barra M, colocado na vizinhança de uma bobina B ligada a um galvanómetro G.
Em qual das seguintes situações o ponteiro do galvanómetro sofre maior desvio?
(A) Quando o íman se move lentamente em relação à bobina.
(B) Quando o íman se move rapidamente em relação à bobina.
(C) Quando o íman e a bobina estão parados um em relação ao outro.
(D) Quando o íman e a bobina se movem com a mesma velocidade.
- Opção (B)
⇒ O ponteiro do galvanómetro sofre um maior desvio quanto maior for a força eletromotriz induzida, ε .
⇒ Para que surja uma corrente induzida é necessário que o fluxo magnético, ϕ , varie no tempo, o que se verifica quando o íman ou a bobina se movimentam um em relação ao outro com velocidades diferentes.
⇒ Como ε = Δϕ /Δt, quanto mais rápido for o movimento do íman, menor será Δt, e, consequentemente, maior será ε .
- Opção (B) …………. 5 pontos
GRUPO VIII
- 10ºano – Física – subdomínio 3 (Energia, fenómenos térmicos e radiação)
1. A capacidade térmica mássica do cobre é 390 J kg-1 K-1.
Que energia, em joule, é necessário fornecer a uma barra de cobre, de massa 400 g, para que a sua temperatura aumente 5,0 ºC ?
⇒ Calcular a energia a fornecer à barra como calor:
- E = m c ΔT ⇒ E = 0,400 x 390 x 5,0 ⇔ E = 7,8 x 102 J
- 7,8 × 102 J ou equivalente. …………. 5 pontos
2. Considere duas barras de cobre, A e B, com a mesma área de secção reta, sendo o comprimento da barra A duplo do comprimento da barra B.
Se a diferença de temperatura entre as extremidades da barra B for o dobro da verificada entre as extremidades da barra A, é de prever que a taxa temporal de transferência de energia, por condução, seja cerca de
(A) duas vezes superior na barra B.
(B) duas vezes superior na barra A.
(C) quatro vezes superior na barra B.
(D) quatro vezes superior na barra A.
*O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)
- O conteúdo deste item já não faz parte dos atuais referenciais programáticos da disciplina.
- Opção (C)…………. 5 pontos
FIM









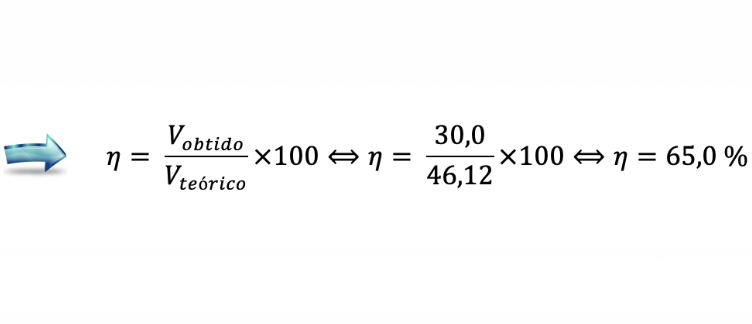







Boa tarde, no exercicio 2.1 do grupo IV, se se determinasse a concentracao inicial a partir da concentracao final e do fator de diluição não seria esse o valor da concentracao do acido não ionizado?
Porque temos de ir pelo valor do ph?
obrigada
O fator de diluição apenas nos faz a relação entre concentração diluída e a concentrada, através do pH conseguimos calcular a concentração de [H3O+] ionizada, ou seja, aquilo que efetivamente reagiu. A partir daí é fácil calcular o grau de ionização. Continuação de bons estudos.